
Ген древних ретровирусов на службе у мозга млекопитающих
14 ноября 2019
Ген древних ретровирусов на службе у мозга млекопитающих
- 1913
- 11
- 4
Известны примеры, когда гены вирусов покидали вирусный мир и были отобраны для выполнения важных функций в организме хозяина. Таков оказался ген Arc, ставший ключевым игроком в обеспечении синаптической пластичности мозга млекопитающих.
коллаж автора статьи с использованием изображения с сайта Miray
-
Автор
-
Редакторы
Статья на конкурс «био/мол/текст»: У большинства людей вирусы ассоциируются исключительно с вызываемыми ими заболеваниями. Действительно, вирусы являются облигатными клеточными паразитами, которые зачастую при размножении убивают организм хозяина. Между хозяином и его паразитом происходит непрерывная эволюционная «гонка вооружений». Однако в процессе эволюции некоторые вирусные гены, закрепившиеся в геномах клеточных форм жизни, включая животных, начали выполнять важные для этих организмов функции. Об одном из таких генов, играющих ключевую роль в обучении и памяти, и пойдет речь.
Конкурс «био/мол/текст»-2019
Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2019.

Генеральный спонсор конкурса и партнер номинации «Сколтех» — Центр наук о жизни Сколтеха.

Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

Спонсором приза зрительских симпатий выступила компания BioVitrum.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Вездесущие убийцы
Вирусы являются самой распространенной формой жизни в окружающей среде.
Стоит отметить, что споры о присуждении вирусам статуса живого ведутся до сих пор. Эти споры происходят в большей степени не от того, что нами не были четко определены основные свойства вирусов, а от того, что существует множество определений живого, часть из которых, как ни парадоксально, лежит за пределами биологической науки как таковой. Одно из наиболее общих и одновременно емких определений жизни предложило Национальное управление по аэронавтике и исследованию космического пространства (National Aeronautics and Space Administration, NASA) в процессе выработки стратегий для поиска внеземных форм жизни: «Жизнь — это самоподдерживающаяся химическая система, способная к дарвиновской эволюции» (life is a self-sustaining chemical system capable of Darwinian evolution) [1]. Как следует из этого определения, вирусы, на первый взгляд, не являются в полном смысле «живыми», поскольку, будучи облигатными паразитами, не удовлетворяют свойству самоподдержания. Однако самоподдержание любой биологической системы необходимо рассматривать в контексте среды ее существования, какой бы она ни была (будь то влажная и теплая среда экваториального пояса, экстремальные условия термальных источников или же высокоупорядоченная внутренняя среда клетки). Поэтому, ниже в тексте автор говорит о вирусах как о формах жизни. Вопрос о статусе вирусов в систематике жизненных форм также затронут в работе «Гигантские вирусы: 4-й домен жизни?» [2].
В океанах вирусы составляют около 90% объектов, содержащих нуклеиновые кислоты [3]. Однако в связи с их размером, который на порядки уступает таковому у клеточных форм жизни, их вклад в биомассу океана оценивается всего пятью процентами. В то время как на прокариот, количественно составляющих около 10% объектов, содержащих нуклеиновые кислоты, приходится более 90% океанической биомассы (рис. 1). По оценкам, только в мировом океане содержится 1030 вирусных частиц, которые непрерывно инфицируют самые разные клеточные формы жизни. Так, свыше 20% инфицированных микроорганизмов ежедневно погибает от вирусов [3].
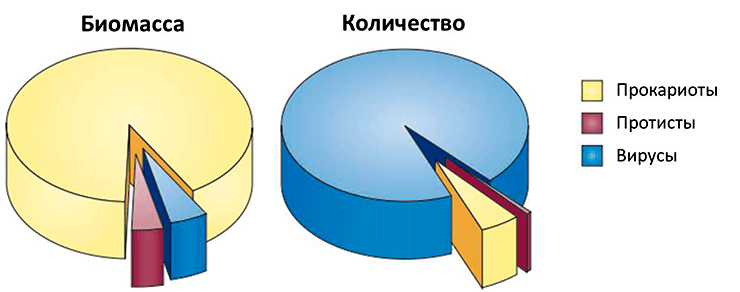
Рисунок 1. Относительные биомасса и количество прокариот, протистов и вирусов в океанах. Приведены усредненные данные по всей толще океанических вод.
[3], рисунок адаптирован
Атмосфера Земли также полна вирусами. Показано, что в нижних слоях тропосферы сквозь квадратный метр проносятся несколько миллиардов вирусных частиц в течение суток (плотность потока колеблется в диапазоне от 0,26×109 до >7×109 шт. в м2 за сутки). В то же время аналогичный показатель для бактерий на два порядка меньше [4]. По оценкам авторов, большинство вирусов и бактерий (~69% и ~97% соответственно) путешествуют в атмосфере, будучи прикрепленными к частицам пыли или органическим агрегатам. Этот способ глобального распространения вирусов через воздух объясняет тот факт, что идентичные или очень схожие последовательности вирусных нуклеиновых кислот были обнаружены в самых различных экосистемах планеты.
Кроме того, что вирусы являются самой распространенной формой жизни на Земле, они также обладают потрясающим генетическим разнообразием и различными механизмами репродукции в клетке хозяина. Жизненный цикл некоторых из них проходит через этап встраивания своих генов в геном клетки-хозяина... И иногда эти гены, передаваясь от поколения к поколению, остаются в нем на многие миллионы лет. Таковы некоторые ретровирусы — РНК-содержащие вирусы, чей жизненный цикл проходит через стадию интеграции своего генетического материала в геном хозяина.
Неупокоенное кладбище вирусных генов
Геномы эукариот, и в особенности многоклеточных организмов, таких как растения и животные, содержат большое количество генов, принадлежащих в прошлом ретровирусам, инфицировавшим зародышевые линии предковых видов и наследуемым вертикально от родителя к потомку. По всей видимости, обнаруженные в геномах эукариот ретротранспозоны, содержащие длинные концевые повторы (long terminal repeats, LTRs), произошли именно таким образом. LTR-ретротранспозоны включают в себя три семейства: Bel/Pao (Belpaoviridae), Ty3/gypsy (Metaviridae) и Ty1/copia (Pseudoviridae). Эти мобильные генетические элементы имеют явное сходство организации генов с таковым у ретровирусов. В общем случае они содержат ген gag, кодирующий белок (group-specific antigen, группоспецифический антиген), сходный с белком капсида ретровирусов; а также гены, необходимые для репликации и последующего встраивания ретротранспозона в новый сайт-мишень. Вдобавок у семейства Ty3/gypsy также обнаружен ген вирусной оболочки (env). Недавно, на основании накопленных филогенетических данных и схожести механизмов репликации Международным комитетом по таксономии вирусов все эти три семейства ретротранспозонов были объединены с семейством Retroviridae в один порядок Ortervirales [5].
Геном кукурузы, к примеру, более чем на 80% состоит из транспозонов, причем бóльшая их часть приходится на LTR-ретротранспозоны Ty3/gypsy и Ty1/copia. Многие из них в процессе эволюции утратили способность «прыгающих» генов, активация же других, ее сохранивших, в значительной мере модулируется внешними условиями, среди которых атака патогенов, ранение и различные экологические стрессы [6]. LTR-ретротранспозоны присутствуют и в геномах млекопитающих, хотя и в значительно меньшем числе копий, и занимают от 4 до 10% генома (рис. 2) [7–9].
О строении и жизненном цикле разных ретротранспозонов подробно рассказано в статье «Мода на ретро. Где встречается обратная транскрипция, и как она эволюционировала» [10].
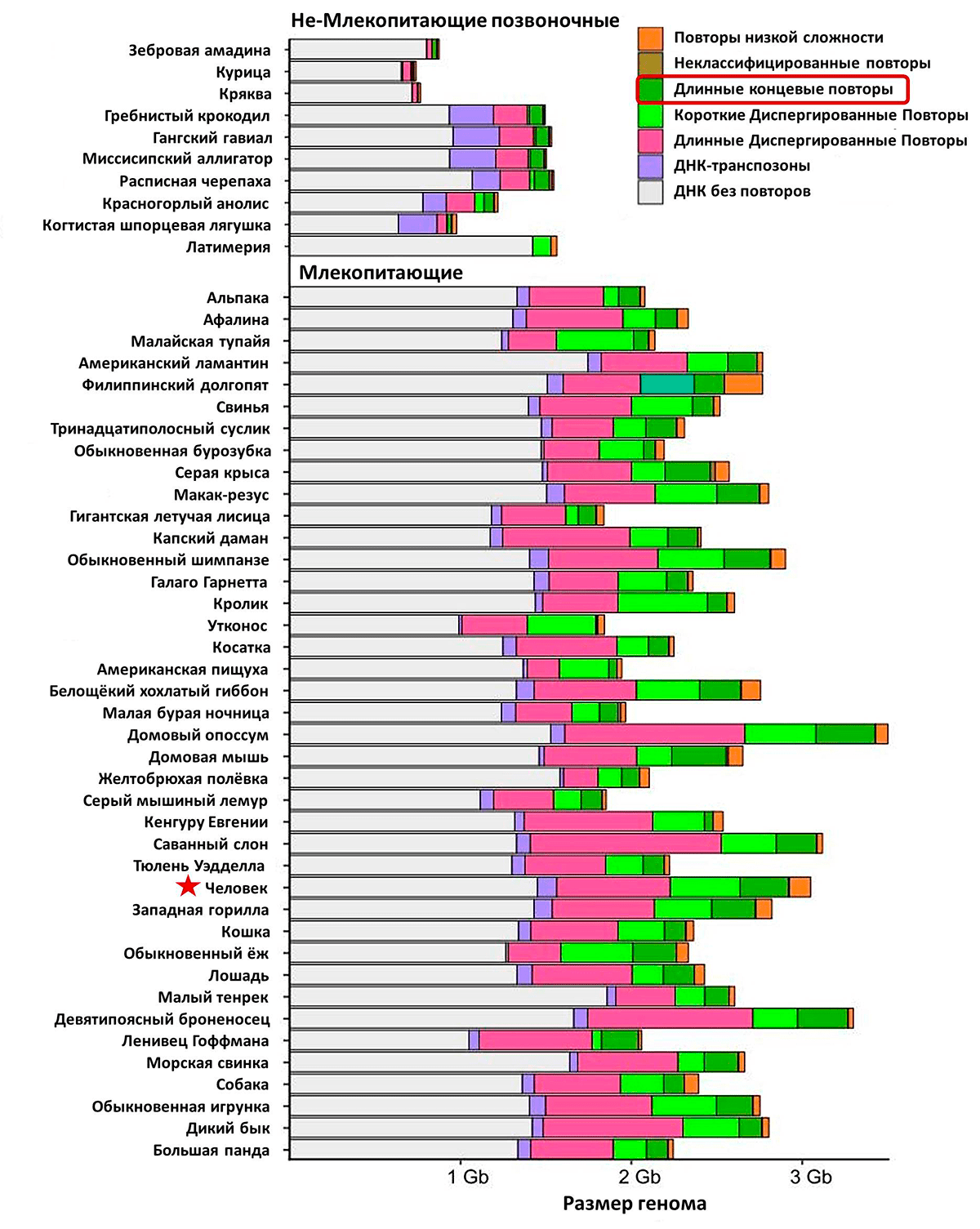
Рисунок 2. Представленность различных мобильных генетических элементов в геномах млекопитающих и других позвоночных животных. По оси ординат указан размер генома в гигабазах (Гб) (109 млрд пар оснований). Красной рамкой в легенде выделены LTR-ретротранспозоны. Звездой обозначен вид Homo sapiens.
[7], рисунок адаптирован
С одной стороны, сохранившие активность ретротранспозоны являются геномными паразитами, которые могут приводить к дестабилизации генома. Поэтому организмы выработали эпигенетические способы сдерживания подобных угроз, включая метилирование ДНК, модификацию гистонов и малые некодирующие РНК [11]. С другой стороны, активность LTR-ретротранспозонов приводит к дополнительной изменчивости в генофонде популяций, обеспечивая новый материал для отбора [12], [13]. Чаще речь идет об изменении регуляторных участков (промоторов и энхансеров, к примеру) эукариотических генов. Однако даже целые гены ретровирусов могут в процессе эволюции организма отбираться для выполнения определенной функции этого организма. Например, гены ретровирусной оболочки (env) способствовали возникновению класса млекопитающих (Mammalia) в том виде, в каком мы наблюдаем его сейчас . Закрепившаяся за ними функция состоит в обеспечении клеточного слияния, приводящего к формированию синцитиотрофобласта в развивающейся плаценте [14].
Подробнее о вкладе вирусов в эволюцию клеточных форм жизни рассказано в статьях «Вирусные геномы в системе эволюции» [15], «Многоликая и уникальная: плацента в лабиринте эволюции» [34] и «Преодолевая барьеры (как объединить необъединимое)» [35].
Другим удивительным примером вирусного гена, вставшего на службу животным, является ген Arc (другое название Arg 3.1). О нем и пойдет речь в статье.
«А master regulator of synaptic plasticity» («Ведущий регулятор синаптической пластичности»)
В название этой главы легла цитата из заголовка обзорной статьи 2011 года, которую опубликовали Джейсон Шеферд и Марк Бэр на основании накопленных данных о роли Arc в обеспечении синаптической пластичности нервной системы млекопитающих [16]. Ген Arc был независимо открыт в середине 90-х годов прошлого века двумя группами ученых, одной из которых руководил Пол Уорли из США, другой — Дитмар Куль из Германии. Они обнаружили, что вскоре после судорожной активности или индукции долговременной потенциации (long-term potentiation (LTP) — устойчивого усиления синаптической передачи между двумя нейронами, возникающего после высокочастотной электрической стимуляции одного из них) происходит быстрое накопление продуктов экспрессии Arc в дендритах активированных нейронов [17], [18].
Авторы проводили свое исследование на гиппокампе, одной из самых «популярных» структур в нейробиологических исследованиях млекопитающих. Показано, что гиппокамп играет важную роль в переходе кратковременной памяти в долговременную, а также пространственной навигации и формировании эмоций. А его часть, зубчатая извилина, является одной из двух областей взрослого мозга млекопитающих, где на протяжении всей жизни животного образуются новые нейроны. Так, в процессе высокочастотной стимуляции одного из проводящих путей гиппокампа, приводящей к индукции LTP, мРНК гена Arc обнаруживалась в дендритах нейронов зубчатой извилины гиппокампа на расстоянии ~300 мкм от их тел (рис. 3) [19].
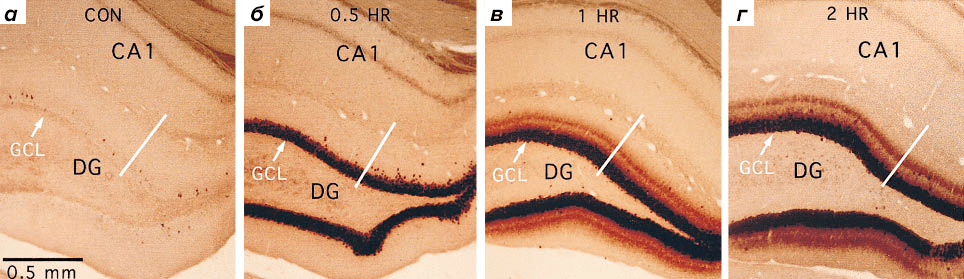
Рисунок 3. Динамика накопления мРНК Arc в активированных дендритах нейронов зубчатой извилины крысы (Rattus norvegicus domestica). а — Животные, не получавшие стимуляции. б — Спустя 30 мин после стимуляции. в — 1 час после стимуляции. г — 2 часа после стимуляции. На рисунке видно, что с течением времени после стимуляции мРНК Arc распространяется от тел нейронов (темно-коричневая полоса) к их удаленным дендритам (светло-коричневая полоса). Условные обозначения: DG — зубчатая извилина; GCL — гранулярный клеточный слой; CA1 — анатомическая область гиппокампа (от лат. Cornu Ammonis 1).
Подобный характер экспрессии Arc позволил отнести его к так называемым немедленным ранним генам. Немедленные ранние гены (immediate early genes, IEGs) — разнородная группа генов, способных быстро и кратковременно активироваться в течение нескольких минут после воздействия различных экстраклеточных агентов, включая факторы роста, нейромедиаторы и деполяризацию клеточной мембраны .
Разные IEGs описаны в статье «Технологии изучения клеточных механизмов памяти» [20].
Позже, на нокаутных по Arc мышам (ген инактивировали во всех клетках организма) было показано нарушение извлечения долговременной памяти в разнообразных поведенческих задачах, среди которых — водный лабиринт Морриса (задача на пространственное обучение и память), условно-рефлекторное замирание на обстановку, условно-рефлекторное замирание на звуковой сигнал, задача на распознавание новых объектов и обусловленная вкусовая аверсия. В последней из перечисленных задач животное учится ассоциировать вкус определенного вещества с последующим наступлением ухудшения самочувствия. Уровень предпочтения этого вещества после нескольких сеансов обучения говорит о сформированной памяти. В то же время, ни в одной из этих задач у нокаутных животных, по сравнению с животными дикого типа, не была нарушена кратковременная память [21]. С помощью введения в миндалевидное тело (структуру лимбической системы мозга, играющюю важную роль в формировании эмоций) антисмысловых олигонуклеотидов к мРНК Arc для ингибирования ее трансляции удалось показать нарушение извлечения долговременной памяти у мышей в задаче условно-рефлекторного замирания на звуковой сигнал. Опять же, кратковременная память нарушена не была [22].
Используя оптогенетическое ингибирование нейронов гиппокампа, экспреcсировавших Arc при обучении условно-рефлекторному замиранию на обстановку, ученые смогли блокировать извлечение сформированной памяти об этой обстановке в тестировании спустя две недели [23]. С другой стороны, локальное увеличение экспрессии Arc в зрительной коре мышей за счет введения Arc-содержащих лентивирусов, восстанавливало пластичность зрительной коры, характерную для ювенильных особей этого вида [24].
Подробнее об оптогенетике, современном и мощном инструменте для и изучения клеточных механизмов памяти, можно прочитать в ранее вышедших на «Биомолекуле» статьях: «Обнаружены управляемые светом анионные каналы» [25], «Светлая голова» [26].
Эти и многие другие результаты с очевидностью говорят о ключевой роли гена Arc в процессе формирования долговременной памяти. А теперь вернемся к его эволюционной истории.
Arc: наследие древних ретровирусов
В 2006 году по результатам широкомасштабного анализа генома человека было выявлено 85 генов, кодирующих 103 белковые изоформы, схожие с ретровирусными белками Gag. К сожалению, на тот момент лишь немногие из этих белков были охарактеризованы и исследованы экспериментально, однако в число тех немногих входил Arc, к тому времени активно исследуемый в связи со своей ролью в синаптической пластичности мозга млекопитающих [27].
Лишь спустя без малого 10 лет это наблюдение привлекло внимание нейробиологов. Научный коллектив под руководством Пола Уорли, одного из первооткрывателей Arc, с помощью рентгеноструктурного анализа установил трехмерную структуру N- и C-доменов (относительно стабильных фрагментов третичной структуры белка, укладка которых проходит независимо от остальных частей этого белка) белка Arc. Выяснилось, что трехмерная структура этих доменов имеет значительное сходство с доменом капсидного белка Gag вируса иммунодефицита человека, принадлежащего к семейству Retroviridae (рис. 4). Ученые предположили, что Arc может происходить от Ty3/gypsy ретротранспозонов [28]. Кроме того, N-домен имеет функциональный сайт связывания субъединицы ɣ2 трансмембранного пептида, регулирующего AMPA-рецепторы (transmembrane AMPAR regulatory protein gamma subunit 2, TARPɣ2, или старгазин). Известно, что AMPA-рецепторы — самый распространенный тип рецепторов, передающих быстрые возбуждающие сигналы в синапсах нервной системы позвоночных. Таким образом, структура N-домена белка Arc может опосредовать его роль в приобретении долговременной памяти, о которой шла речь выше.
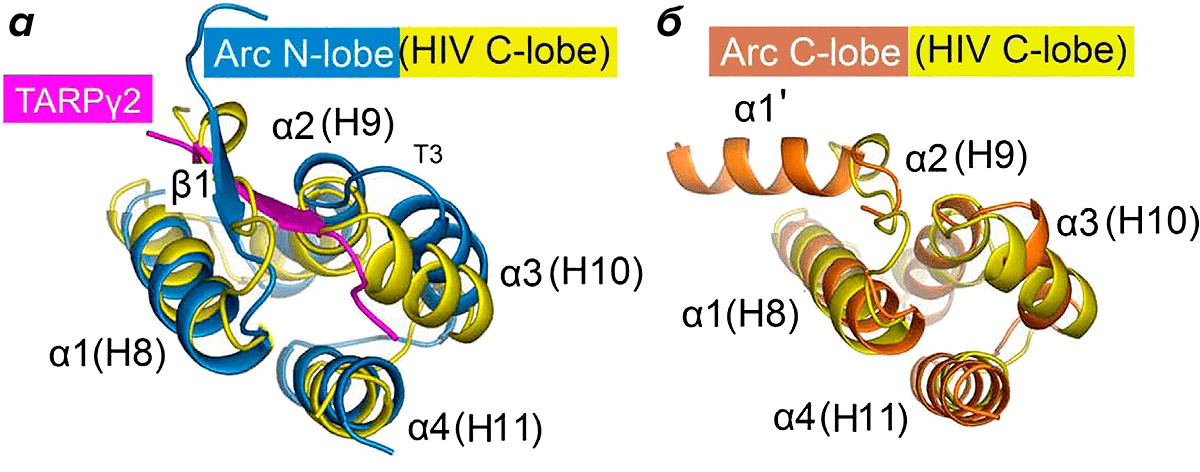
Рисунок 4. Трехмерная структура доменов белка Arc. 3D-совмещение N- и C-доменов (синий (а) и оранжевый (б) соответственно) с соответствующими доменами капсида вируса иммунодефицита человека (HIV). Розовым цветом показана субъединица ɣ2 трансмембранного пептида, регулирующего AMPA-рецепторы.
В том же году появились первые указания на то, что рекомбинантный человеческий белок Arc, как и белки вирусных капсидов, способен к обратимой самоолигомеризации при физиологических условиях [29]. Но самое интересное ждало исследователей впереди. После того, как было открыто вирусное происхождение гена Arc, учитывая его важную роль в обеспечении синаптической пластичности, резонно было задаться вопросом: какими свойствами ретровирусов он может обладать?
В 2018 году группа ученых под руководством Джейсона Шеферда опубликовала исследование в журнале Cell, где продемонстрировала, что белок Arc формирует вирусоподобные «капсиды», способные переносить мРНК Arc от одного нейрона к другому. Более того, мРНК Arc в нейроне-акцепторе начинает транслироваться при деполяризации мембраны его дедритов [30]!
Для начала авторы провели масштабный филогенетический анализ и обнаружили высоко консервативные ортологи мышиного гена Arc у всех исследованных наземных позвоночных, но не у рыб и других вторичноротых. Ортологи и паралоги гена Arc плодовой мушки Drosophila melanogaster, darc1 и darc2, были обнаружены у так называемых настоящих мух (секция Schizophora), но отсутствовали у других исследованных первичноротых (рис. 5) [30].
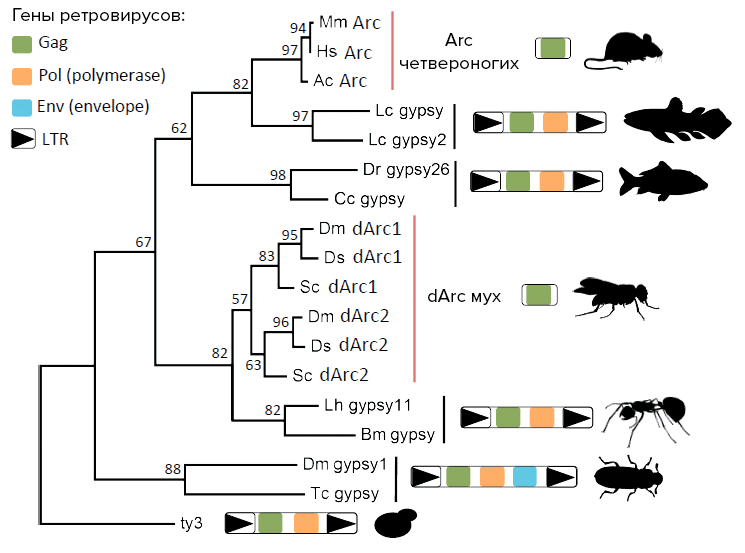
Рисунок 5. Филогененетическое дерево, отражающее эволюционные связи гена Arc наземных позвоночных (четвероногих), darc1 мух и gag, родственных Ty3/gypsy ретротранспозонам. Указаны следующие ретровирусные гены: группоспецифического антигена Gag (обозначен зеленым), белка капсида; полимеразы Pol (обозначен оранжевым), необходимой для репликации и последующего встраивания вирусной ДНК в геном хозяина; белка вирусной оболочки Env (обозначен голубым).
[30], рисунок адаптирован
Интересно, что в этом же номере журнала вышла не менее потрясающая статья, в которой был описан механизм транс-синаптической передачи белка dArc1 и его мРНК в нейро-мышечном контакте у личинок плодовых мушек [31]. По всей видимости, наземные позвоночные, обладающие лишь одной копией гена Arc, приобрели его независимо от генов darc настоящих мух, у которых произошло несколько раундов дупликаций этого гена. Однако и тот, и другой имеют значительную гомологию в ретровирусном Gag-домене [30].
Построив филогененетическое дерево гена Arc, ученые принялись за детальное изучение его «вирусных» свойств. Сперва показали, что очищенный белок Arc (prArc) спонтанно формирует олигомерные двуслойные структуры, подобные вирусным капсидам, средний диаметр которых составляет 32 ± 0,2 нм (рис. 6).
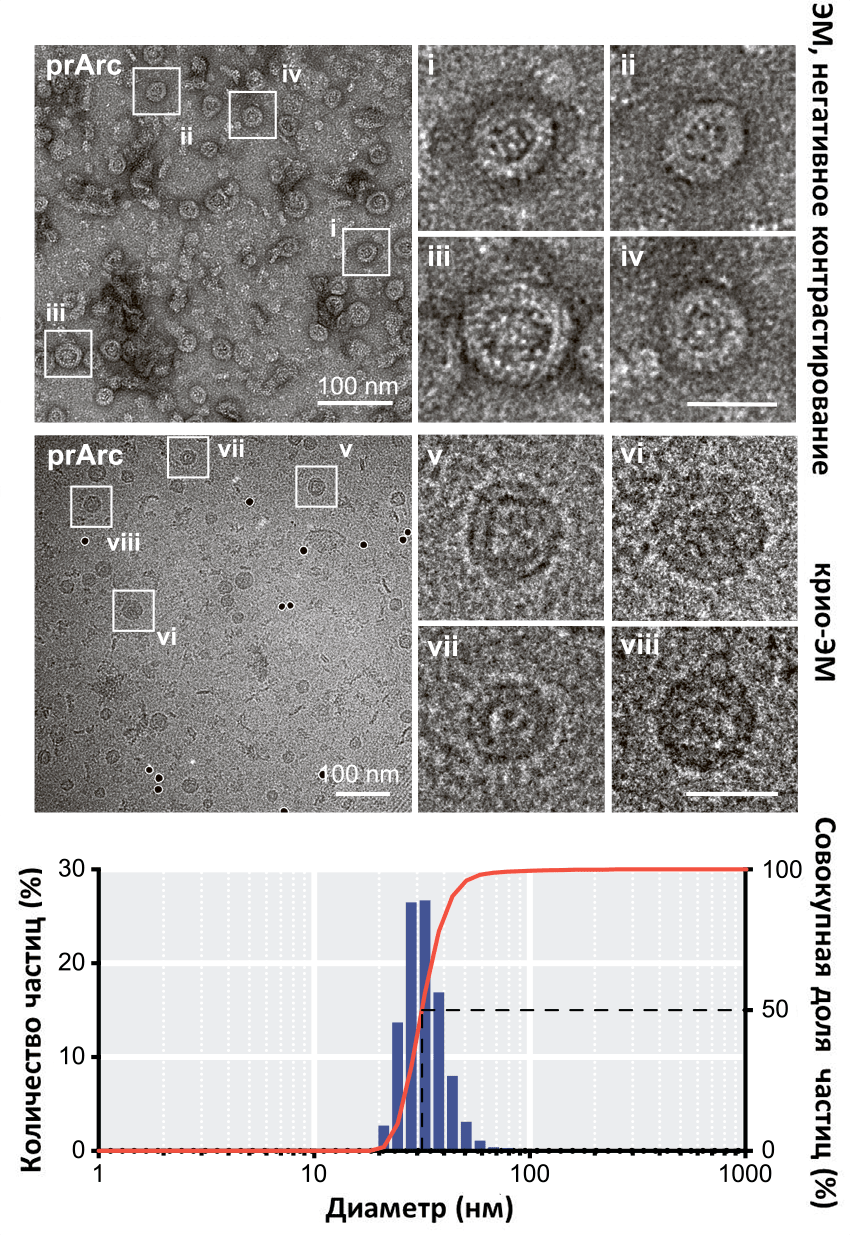
Рисунок 6. Капсидоподобные структуры, формируемые белком Arc. Сверху — микрофотографии (электронная микроскопия, негативное контрастирование) полноразмерного очищенного белка (prArc) крысы (1 мг/мл, увеличение × 42 000); (i–iv), шкала 30 нм. В середине — микрофотографии (криогенная электронная микроскопия) prArc (2 мг/мл, увеличение × 62 000); (v–viii), шкала 30 нм. На снимках видны двуслойные стенки «капсидов». Внизу — распределение размеров частиц «капсидов» prArc (метод светового рассеяния), средний диаметр которых составляет 32 ± 0,2 нм.
[30], рисунок адаптирован
Далее ученые установили, что Arc связывает и инкапсулирует РНК. Более того, для формирования полноценных «капсидов» белку Arc необходимо наличие мРНК Arc в среде. Отсутствие какой-либо РНК в среде приводит к значительно меньшему количеству полностью сформированных «капсидов» Arc. В тоже время даже добавление мРНК зеленого флуоресцентного белка (GFP, green fluorescent protein) способствовало достоверно значимому увеличению количества полноценных «капсидов» Arc (рис. 7).
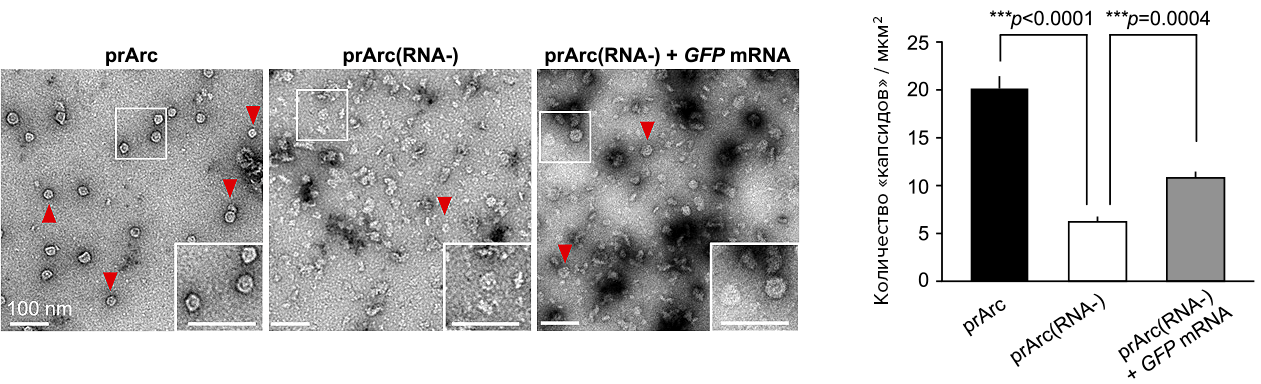
Рисунок 7. Взаимодействие Arc с РНК. Слева — микрофотографии (негативное контрастирование) структур, формируемых белком Arc c его мРНК (prArc), очищенным от нуклеиновых кислот белком Arc (prArc(RNA–) и очищенным от нуклеиновых кислот белком Arc с добавлением мРНК GFP (prArc(RNA–) + GFP mRNA). Красными стрелками отмечены полностью сформированные «капсиды». Справа — плотность «капсидов» Arc в мкм2. Данные представлены как «среднее ± стандартная ошибка среднего».
[30], рисунок адаптирован
Отлично! Но как поведет себя Arc в живых системах? Для ответа на этот вопрос ученые трансфецировали (ввели нуклеиновую кислоту в эукариотические клетки невирусным методом) клеточную линию, полученную из эмбриональных почек человека (HEK293), плазмидами, содержащими ген Arc. После трансфекции они обнаружили, что среда Arc-трансфецированных клеток HEK293 содержит фракцию везикул размером до 100 нм, напоминающих экзосомы. А сами эти везикулы несут мРНК Arc. Arc-содержащие везикулы также были найдены в среде культуры нейронов коры головного мозга мыши спустя 24 часа инкубации. Более того, авторы показали, что везикулы с «капсидами» Arc могут переносить мРНК от клетки к клетке. Для этого спустя 18 часов инкубации от Arc-трансфецированной культуры клеток (исследование проводили на уже упомянутой линии HEK293) авторы отобрали культуральную среду и перенесли ее к нетрансфецированной культуре клеток. Спустя 24 ч ученые обнаружили в клетках второй культуры мРНК и белок Arc, продемонстрировав таким образом, что Arc-содержащие везикулы способны проникать внутрь клеток, высвобождая мРНК Arc. По-видимому, их проникновение в клетку происходит путем эндоцитоза, так как весь процесс блокируется ингибитором эндоцитоза динасором (Dynasore).
В выше описанных экспериментах «вирусные» свойства Arc были продемонстрированы на культуре клеток из эмбриональных почек человека, но in vivo Arc экспрессируется далеко не в клетках почек. Поэтому на заключительном этапе исследования ученые задались вопросом: «Происходит ли нечто подобное в нервных клетках?» Для ответа на него они провели инкубацию культуры нейронов гиппокампа от нокаутных по Arc мышей (KO) со средой, взятой от культуры нейронов коры больших полушарий мозга мышей дикого типа (WT), в которой находились везикулы с Arc (рис. 8). В ходе этого эксперимента было установлено, что эндогенный Arc переносит собственную мРНК в нейроны нокаутных мышей, и, опять же, этот процесс специфически блокировался ингибитором эндоцитоза динасором (Dynasore).
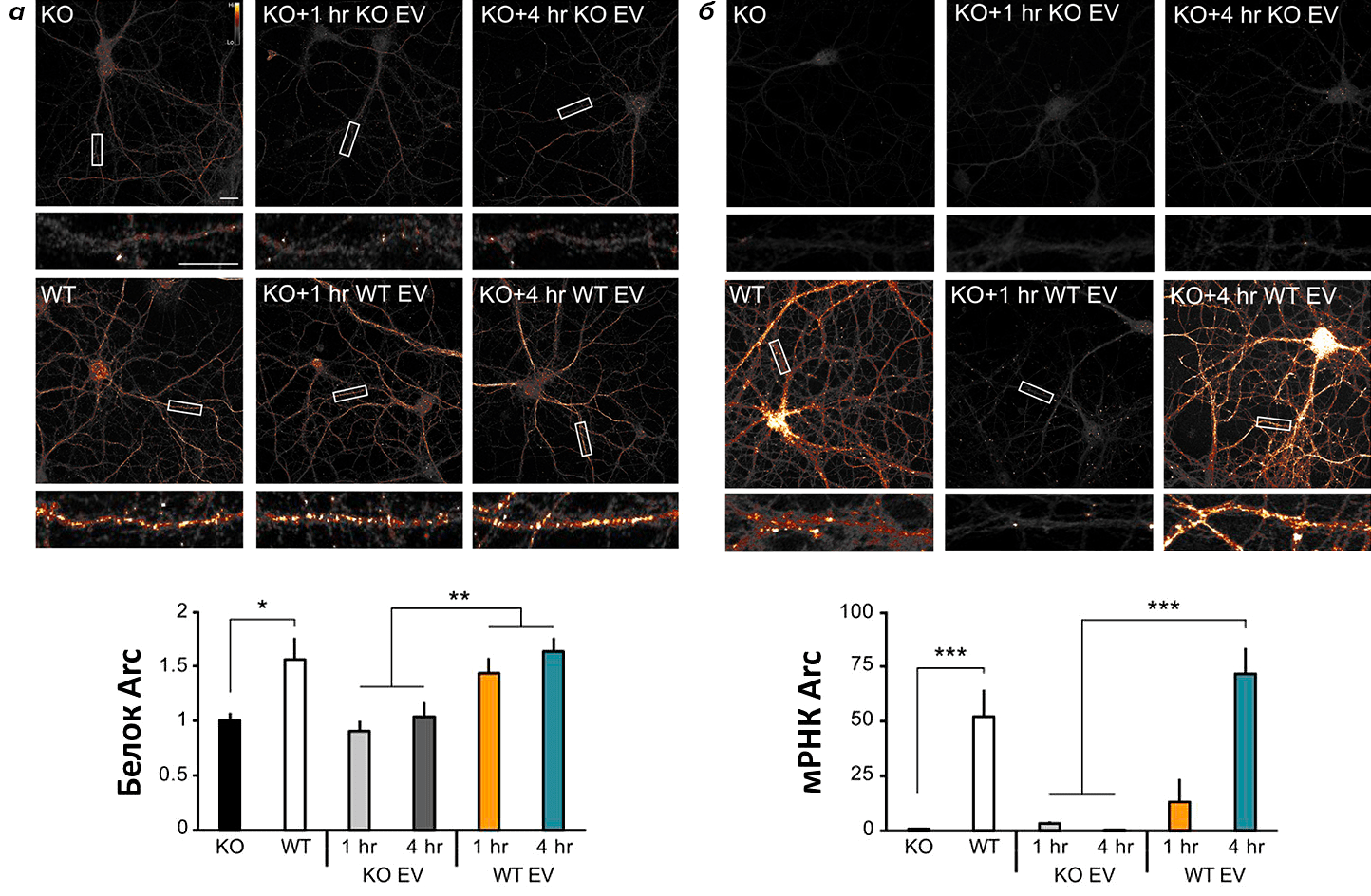
Рисунок 8. Эндогенный Arc способствует переносу мРНК Arc от нейрона к нейрону. а — Микрофотографии иммуноцитохимически окрашенных нейронов гиппокампа от нокаутных по Arc мышей, которые были инкубированы либо с фракцией везикул, полученной от таких же нокаутных мышей (верхний ряд), либо с фракцией везикул, полученной от культуры нейронов коры больших полушарий мозга мышей дикого типа (WT, нижний ряд) в течение 1 или 4 часов. На гистограмме показано достоверно значимое увеличение белка Arc в дендритах нейронов нокаутных мышей уже спустя 1 ч после инкубации с везикулами от нейронов мышей дикого типа. б — Микрофотографии культур нейронов, аналогичных тем, что представлены на рисунке а, но окрашенных с помощью флуоресцентной in situ гибридизации (FISH). На гистограмме показано достоверное увеличение мРНК Arc в дендритах нейронов от нокаутных мышей спустя 4 ч. после инкубации с везикулами от нейронов мышей дикого типа. мРНК Arc и белок Arc нормализован на количества мРНК Arc и белка Arc в дендритах нокаутных животных без инкубации. Данные на гистограммах представлены как «среднее ± стандартная ошибка среднего».
[30], рисунок адаптирован
Однако самым удивительным в этой истории оказалось, что перенесенная мРНК Arc начинает транслироваться в дендритах нейронов при деполяризации их мембраны. Ранее было показано, что мРНК Arc транслируется при активации метаботропных глутаматных рецепторов mGluR1/5 (обеспечивающих медленную, опосредуемую метаболическими путями, реакцию на глутаматергические сигналы), например, их агонистом DHPG (3,5-дигидроксифенилглицином) [32]. Авторы повторили выше описанные эксперименты по переносу мРНК Arc в нейроны гиппокампа нокаутных по Arc мышей, но в этот раз добавили в культуральную среду DHPG, вызвав деполяризацию мембраны их дендритов. В итоге в дендритах этих нейронов количество белка Arc достоверно значимо увеличивалось (рис. 9). В свою очередь ингибитор трансляции циклогексимид (CHX) блокировал эффект увеличения количества белка Arc в дендритах, вызванный добавлением DHPG в культуральную среду.

Рисунок 9. Трансляция экзогенной мРНК Arc при деполяризации мембраны дендритов. Микрофотографии иммуноцитохимически окрашенных культур нейронов гиппокампа от нокаутных по Arc мышей, которые были инкубированы либо с фракцией везикул, полученной от таких же нокаутных мышей (KO, верхний ряд), либо с фракцией везикул, полученной от культуры нейронов коры больших полушарий мозга мышей дикого типа (WT, нижний ряд) в течение четырех часов при добавлении DHPG (3,5-дигидроксифенилглицина). На гистограмме показано достоверно значимое увеличение белка Arc в дендритах нейронов от нокаутных мышей после добавления в среду DHPG. Эффект DHPG блокировался добавлением в среду ингибитора трансляции циклогесимида (CHX). Данные на гистограмме представлены как «среднее ± стандартная ошибка среднего».
[30], рисунок адаптирован
Полученные результаты сложно переоценить: по сути, был открыт новый механизм коммуникации между нейронами, непосредственно связанный с их электрической активностью. И это открытие, как и любое другое в естественных науках, рождает множество новых вопросов, требующих дальнейших исследований.
Например, какие молекулярные механизмы опосредуют выход капсидоподобных структур Arc из нейрона-донора и их проникновение в нейрон-акцептор? Или, учитывая гомологию Arc млекопитающих и darc1 мух, является ли это результатом конвергентной эволюции? Если да, то какие эволюционные требования привели к отбору этих генов для обеспечения функций нервной системы в столь далеких друг от друга таксонах? Вне всяких сомнений в ближайшем будущем нас ждет еще немало удивительных открытий, связанных с геном Arc, потомком древних ретровирусов.
Подробнее эти и другие вопросы, связанные с геном Arc, обсуждаются в обзоре [33].
Литература
- About life detection. NASA Official;
- Гигантские вирусы: 4-й домен жизни?;
- Curtis A. Suttle. (2007). Marine viruses — major players in the global ecosystem. Nat Rev Microbiol. 5, 801-812;
- Isabel Reche, Gaetano D’Orta, Natalie Mladenov, Danielle M. Winget, Curtis A. Suttle. (2018). Deposition rates of viruses and bacteria above the atmospheric boundary layer. ISME J. 12, 1154-1162;
- Mart Krupovic, Jonas Blomberg, John M. Coffin, Indranil Dasgupta, Hung Fan, et. al.. (2018). Ortervirales: New Virus Order Unifying Five Families of Reverse-Transcribing Viruses. J Virol. 92;
- Leonardo Galindo-González, Corinne Mhiri, Michael K. Deyholos, Marie-Angèle Grandbastien. (2017). LTR-retrotransposons in plants: Engines of evolution. Gene. 626, 14-25;
- Roy N. Platt, Michael W. Vandewege, David A. Ray. (2018). Mammalian transposable elements and their impacts on genome evolution. Chromosome Res. 26, 25-43;
- Eric S. Lander, Lauren M. Linton, Bruce Birren, Chad Nusbaum, Michael C. Zody, et. al.. (2001). Initial sequencing and analysis of the human genome. Nature. 409, 860-921;
- Mouse Genome Sequencing Consortium. (2002). Initial sequencing and comparative analysis of the mouse genome. Nature. 420, 520-562;
- Мода на ретро. Где встречается обратная транскрипция, и как она эволюционировала;
- Nathaly Castro-Diaz, Marc Friedli, Didier Trono. (2015). Drawing a fine line on endogenous retroelement activity. Mobile Genetic Elements. 5, 1-6;
- Jonathan Göke, Huck Hui Ng. (2016). CTRL + INSERT : retrotransposons and their contribution to regulation and innovation of the transcriptome. EMBO Rep. 17, 1131-1144;
- Peter J. Thompson, Todd S. Macfarlan, Matthew C. Lorincz. (2016). Long Terminal Repeats: From Parasitic Elements to Building Blocks of the Transcriptional Regulatory Repertoire. Molecular Cell. 62, 766-776;
- Christian Lavialle, Guillaume Cornelis, Anne Dupressoir, Cécile Esnault, Odile Heidmann, et. al.. (2013). Paleovirology of ‘ syncytins ’, retroviral env genes exapted for a role in placentation. Phil. Trans. R. Soc. B. 368, 20120507;
- Вирусные геномы в системе эволюции;
- Jason D Shepherd, Mark F Bear. (2011). New views of Arc, a master regulator of synaptic plasticity. Nat Neurosci. 14, 279-284;
- W. Link, U. Konietzko, G. Kauselmann, M. Krug, B. Schwanke, et. al.. (1995). Somatodendritic expression of an immediate early gene is regulated by synaptic activity.. Proceedings of the National Academy of Sciences. 92, 5734-5738;
- Gregory L Lyford, Kanato Yamagata, Walter E Kaufmann, Carol A Barnes, Laura K Sanders, et. al.. (1995). Arc, a growth factor and activity-regulated gene, encodes a novel cytoskeleton-associated protein that is enriched in neuronal dendrites. Neuron. 14, 433-445;
- Oswald Steward, Christopher S Wallace, Gregory L Lyford, Paul F Worley. (1998). Synaptic Activation Causes the mRNA for the IEG Arc to Localize Selectively near Activated Postsynaptic Sites on Dendrites. Neuron. 21, 741-751;
- Технологии изучения клеточных механизмов памяти;
- Niels Plath, Ora Ohana, Björn Dammermann, Mick L. Errington, Dietmar Schmitz, et. al.. (2006). Arc/Arg3.1 Is Essential for the Consolidation of Synaptic Plasticity and Memories. Neuron. 52, 437-444;
- J. E. Ploski, V. J. Pierre, J. Smucny, K. Park, M. S. Monsey, et. al.. (2008). The Activity-Regulated Cytoskeletal-Associated Protein (Arc/Arg3.1) Is Required for Memory Consolidation of Pavlovian Fear Conditioning in the Lateral Amygdala. Journal of Neuroscience. 28, 12383-12395;
- Christine A. Denny, Mazen A. Kheirbek, Eva L. Alba, Kenji F. Tanaka, Rebecca A. Brachman, et. al.. (2014). Hippocampal Memory Traces Are Differentially Modulated by Experience, Time, and Adult Neurogenesis. Neuron. 83, 189-201;
- Kyle R. Jenks, Taekeun Kim, Elissa D. Pastuzyn, Hiroyuki Okuno, Andrew V. Taibi, et. al.. (2017). Arc restores juvenile plasticity in adult mouse visual cortex. Proc Natl Acad Sci USA. 114, 9182-9187;
- Обнаружены управляемые светом анионные каналы;
- Светлая голова;
- M CAMPILLOS, T DOERKS, P SHAH, P BORK. (2006). Computational characterization of multiple Gag-like human proteins. Trends in Genetics. 22, 585-589;
- Wenchi Zhang, Jing Wu, Matthew D. Ward, Sunggu Yang, Yang-An Chuang, et. al.. (2015). Structural Basis of Arc Binding to Synaptic Proteins: Implications for Cognitive Disease. Neuron. 86, 490-500;
- Craig Myrum, Anne Baumann, Helene J. Bustad, Marte Innselset Flydal, Vincent Mariaule, et. al.. (2015). Arc is a flexible modular protein capable of reversible self-oligomerization. Biochemical Journal. 468, 145-158;
- Elissa D. Pastuzyn, Cameron E. Day, Rachel B. Kearns, Madeleine Kyrke-Smith, Andrew V. Taibi, et. al.. (2018). The Neuronal Gene Arc Encodes a Repurposed Retrotransposon Gag Protein that Mediates Intercellular RNA Transfer. Cell. 172, 275-288.e18;
- James Ashley, Benjamin Cordy, Diandra Lucia, Lee G. Fradkin, Vivian Budnik, Travis Thomson. (2018). Retrovirus-like Gag Protein Arc1 Binds RNA and Traffics across Synaptic Boutons. Cell. 172, 262-274.e11;
- Maggie W. Waung, Brad E. Pfeiffer, Elena D. Nosyreva, Jennifer A. Ronesi, Kimberly M. Huber. (2008). Rapid Translation of Arc/Arg3.1 Selectively Mediates mGluR-Dependent LTD through Persistent Increases in AMPAR Endocytosis Rate. Neuron. 59, 84-97;
- Alexander V. Kedrov, Mikhail Durymanov, Konstantin V. Anokhin. (2019). The Arc gene: Retroviral heritage in cognitive functions. Neuroscience & Biobehavioral Reviews. 99, 275-281;
- Многоликая и уникальная: плацента в лабиринте эволюции;
- Преодолевая барьеры (как объединить необъединимое).
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚





