Геномный минимализм
26 апреля 2019
Геномный минимализм
- 1670
- 0
- 6
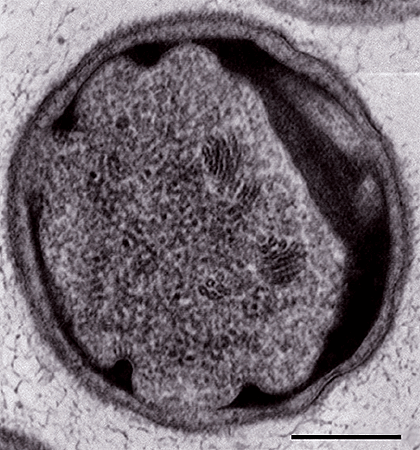
Электронная микрофотография клетки Ca. Carsonella rudii. Шкала — 200 нм.
-
Автор
-
Редактор
Определение минимального набора генов, необходимого для функционирования живого организма, долгое время привлекало внимание исследователей. Особенно интересны в этом отношении организмы с очень небольшим числом генов, а именно, свободноживущие и эндосимбиотические прокариоты, имеющие всего нескольких сотен генов (для сравнения, геном кишечной палочки Escherichia coli содержит около 4200 генов, а в геноме миксобактерии Sorangium cellulosum насчитывается более 11 тысяч генов). Чем отличается метаболизм клеток с такими маленькими геномами? Какие процессы привели к утрате огромного числа генов? Ответам на эти вопросы и посвящен наш обзор.
Геномы с необычно низким количеством генов (или редуцированные геномы) можно найти среди прокариот двух экологических групп: свободноживущих морских бактерий и бактерий-эндосимбионтов. Считается, что в случае свободноживущих микроорганизмов уменьшению числа генов способствует отбор, а у эндосимбиотических бактерий большую роль играют нейтральные процессы, а именно, утрата генов, которые просто-напросто стали ненужными в связи с образом жизни. Действительно, зачем таскать с собой при каждом делении множество генов замысловатых метаболических путей, когда почти все необходимое поставляется или организмом-хозяином, или другим организмом-симбионтом? Особенно любопытно, что среди очень маленьких геномов периодически попадаются такие, которые выбиваются из общего тренда эволюции бактериальных геномов — снижения GC-состава и сохранения порядка следования генов друг за другом (синтении). Кроме того, ученые уже много лет работают над получением бактерий с искусственно уменьшенными геномами и достигли определенных успехов.
В статье мы обсудим, как устроены самые маленькие геномы и как их обладатели приспособились к жизни с таким количеством генов, а также коснемся последних достижений по получению бактерий с искусственно уменьшенными геномами.
Свободноживущие прокариоты с малым числом генов
До появления и широкого распространения современных молекулярно-генетических методов считалось, что свободноживущие прокариоты имеют не менее 1300 генов. Однако в 2013 году с помощью метагеномики в образце воды из Средиземного моря описали актинобактерию Candidatus Actinomaria minuta, геном которой содержит всего лишь 800 генов. Как оказалось впоследствии, эта бактерия и сама по себе весьма миниатюрна: объем ее клеток составляет лишь 0,013 мкм3 [2].
О самых маленьких клетках читайте наш обзор «Маленький, да удаленький: самые маленькие клетки» [1].
Среди свободноживущих архей обладателем мельчайшего генома считается Methanothermus fervidus: в его ДНК насчитывается 1311 белок-кодирующих генов и 50 генов, соответствующих некодирующим РНК [2] (рис. 1).
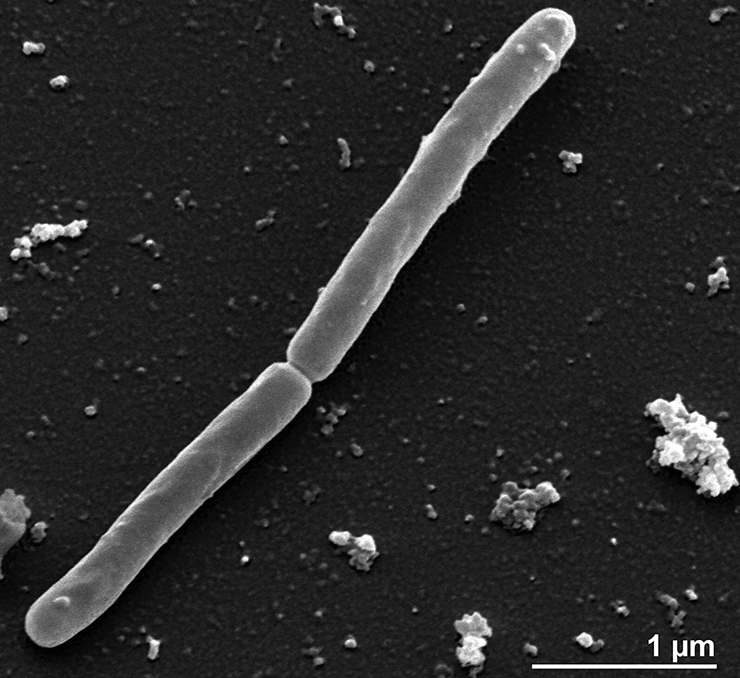
Рисунок 1. Methanothermus fervidus — архея с одним из самых маленьких геномов в своем домене. Фотография получена методом сканирующей электронной микроскопии.
Примерно столько же генов имеется у наиболее разнообразной группы морских гетеротрофных α-протеобактерий, известной как SAR11, и группы β-протеобактерий под названием OM43. Геномы фотосинтезирующих бактерий, как правило, содержат больше генов. Малое число генов имеется и у некоторых неморских прокариот: так, геном сапротрофной бактерии Acholeplasma laidlawii содержит 1380 белок-кодирующих генов, лактобацилла Weissela koreensis имеет 1335 генов, а архея Desulphurococcus mucosus, относящаяся к типу кренархеот и обладающая способностью к серному дыханию, — 1371 ген [2].
Почему столь далекие друг от друга свободноживущие организмы имеют не менее 1300 белок-кодирующих генов? Возможный ответ заключается в том, что с меньшим их числом клетки в «свободном полете» просто не выживают. Впрочем, вероятно, нижний предел количества генов для свободноживущих микроорганизмов еще меньше: бактерия Lactobacillus fermentum CECT 5716, которую можно найти на слизистых оболочках и в грудном молоке человека, обладает лишь 1109 белок-кодирующими генами, а описанная выше Ca. Actinomaria minuta — всего 800. Не исключено, что со временем будет побит и этот рекорд [2].
Что является движущей силой уменьшения числа генов у свободноживущих прокариот? На этот счет существует несколько гипотез.
Согласно гипотезе рационализации (streamlining hypothesis), естественный отбор поддерживает уменьшение генома свободноживущих прокариот, населяющих местообитания, бедные питательными веществами. Когда в геноме клетки происходит делеция, увеличивающая ее приспособленность, она быстро фиксируется в популяции: в условиях нехватки питательных веществ клеткам невыгодно волочить за собой большой геном, на поддержание которого тратится много энергии и других ресурсов.
Гипотезой рационализации можно объяснить и стремление к понижению GC-состава у свободноживущих микроорганизмов, населяющих бедные среды (в их ДНК суммарная доля гуанина и цитозина, как правило, не превышает 36%). Дело в том, что для репликации генома с низким GC-составом требуется меньше фосфора и азота. Кроме того, в скудных условиях клетке выгодно иметь большое соотношение площади поверхности к объему, чтобы более эффективно поглощать питательные вещества, а снижение объема клетки неизбежно ведет к уменьшению ее генома.
Стоит отметить, что уменьшить геном можно не только за счет утраты белок-кодирующих генов. Так, у бактерии Ca. Pelagibacter ubique с геномом в 1308 т.п.н. среднее расстояние между генами составляет лишь три нуклеотида, а псевдогенов, профагов или дуплицированных генов нет совсем [2].
Гипотезу рационализации удалось проверить в лабораторных условиях. Ученые получили штаммы Salmonella enterica, имеющие большие делеции, причем некоторые из них оказались более приспособленными к окружающим условиям, чем бактерии дикого типа [2].
При уменьшении размеров генома зачастую утрачиваются гены, белковые продукты которых задействованы в репарации, поэтому иногда у бактерий с редуцированными геномами (например, у ряда свободноживущих цианобактерий, а также симбиотических организмов) наблюдается повышенная скорость мутирования белок-кодирующих последовательностей. Это в некоторых условиях может быть на руку бактериям, например, при освоении новых местообитаний. Штаммы, отличающиеся повышенной частотой приобретения мутаций, иногда называют мутаторными [2].
Объяснить уменьшение размера геномов свободноживущих прокариот может и гипотеза Черной Королевы (Black Queen hypothesis). Она предлагает рассматривать выгоду от утраты генов не для отдельной клетки, а для популяции в целом. Согласно этой гипотезе, в сообществах микроорганизмов существуют бактерии-«трудоголики», производящие ценные ресурсы, и бактерии-«иждивенцы», которые питаются плодами их работы. Именно у «иждивенцев» часто наблюдается уменьшение геномов: действительно, многие гены им становятся просто не нужны благодаря клеткам-«трудоголикам». Например, цианобактерия Prohlorococcus, отличающаяся малым числом генов, не кодирует собственной каталазы-пероксидазы, поэтому она может существовать лишь вместе с бактериями, которые имеют этот фермент и могут обезвреживать токсины в окружающей среде. Похожие изменения метаболизма можно найти у вышеупомянутой бактерии Ca. Pelagibacter ubique. Исследователям долгое время не удавалось выращивать ее на искусственных средах, пока не выяснили, что эта бактерия питается разнообразными низкомолекулярными метаболитами, которые в небольших количествах, но постоянно производит обитающий рядом с ней фитопланктон. В силу высокой специализированности Ca. Pelagibacter ubique оказалась неспособна расщеплять такие «деликатесы», как широко использующийся микробиологами триптон, а предпочитала гораздо более простые соединения вроде метионина, глицина и пирувата [2].
Нас и здесь неплохо кормят: почему эндосимбиотические бактерии теряют множество генов
Жизнь на всем готовом, как известно, не способствует активной творческой деятельности. То же самое верно и для бактерий-эндосимбионтов, которые живут в эукариотических клетках и питаются их метаболитами. Разумеется, многие гены, особенно отвечающие за сложные метаболические пути, становятся в таких условиях просто-напросто не нужными, и чтобы не волочить за собой многие килобазы бесполезных последовательностей, бактерии-эндосимбионты постепенно их утрачивают. Переход микробов к симбиотическому существованию часто сопровождается инактивацией генов (в том числе генов, кодирующих факторы репарации, что приводит к усиленному накоплению мутаций) и перестройками генома. На изменения в геноме эндосимбиотических бактерий влияют и особенности их хозяина: так, у бактерий, живущих в эндосимбиозе с насекомыми, на ранних этапах приспособления к новой среде происходит бурное размножение мобильных генетических элементов, а у эндосимбионтов протистов подобного не наблюдается. Дело в том, что эндосимбионты насекомых периодически вынуждены преодолевать «бутылочное горлышко», которое снижает давление отбора, что и «развязывает руки» транспозонам. Кстати, именно перемещение транспозонов и вызывает инактивацию многих генов. Стоит, однако, отметить, что у древних эндосимбионтов практически все мобильные генетические элементы утрачены. Кроме того, как и для геномов многих морских свободноживущих бактерий, для геномов эндосимбионтов со стажем характерен низкий GC-состав [2].
Уменьшение размеров генома происходит наиболее стремительно после того, как симбиоз становится облигатным, то есть бактерия оказывается неспособной существовать без своего хозяина. Так, эндосимбионт рисового долгоносика (Sitophilus oryzae), Candidatus Sodalis pierantonius, потерял 55% своих генов в течение всего лишь 28 тысяч лет — невероятно короткий срок по эволюционным меркам. Эта бактерия живет внутри специализированных клеток — бактериоцитов и имеет довольно внушительный геном, содержащий 2309 белок-кодирующих генов и 1771 псевдогенов. Еще более удивительно, что около 18% ее генома приходится на мобильные генетические элементы, на совести которых лежат многочисленные геномные перестройки Ca. Sodalis pierantonius и около 10% случаев инактивации генов. Однако стремительное уменьшение числа активных генов и размеров генома может происходить и без участия транспозонов. Например, бактерия Polynucleobacter necessaries, обитающая в клетках инфузории Euplotes aediculatus, утратила более 40% белок-кодирующих генов, хотя мобильных генетических элементов в ее геноме нет [2].
На завершающих этапах формирования эндосимбиотических отношений геном бактерии становится существенно стабильнее, и постоянство расположения генов на хромосоме (синтения) является одной из отличительных черт облигатных мутуалистических бактерий. Первоначально такую стабильность связывали с утратой эндосимбиотическими бактериями гена recA, продукт которого играет важнейшую роль в гомологичной рекомбинации. Однако впоследствии выяснилось, что у многих таких микробов со стабильными геномами ген recA все-таки есть. Верно и обратное: сокращение числа генов, кодирующих белки рекомбинации и репарации, не гарантирует стабильность генома. Эндосимбионт белокрылки Bemisia tabaci, Candidatus Portiera aleyrodidarum, отличается выраженным геномным полиморфизмом, который наблюдается даже среди бактерий, населяющих одно и то же насекомое, хотя активных генов рекомбинации и репарации у него чрезвычайно мало [2].
Известны две бактерии с крайне редуцированными геномами, которые, тем не менее, имеют необычно высокий для эндосимбионтов GC-состав. Речь идет о двух эндосимбионтах цикады Diceroprocta seminitica — Candidatus Hodgkinia cicadicola и Candidatus Sulcia muelleri. Геном ходжкинии достигает лишь 144 т.п.н. в длину, однако его GC-состав равен 58%. Причины, лежащие в основе повышения GC-состава, неясны. Часто этому могут способствовать ферменты, задействованные в конверсии генов, однако у ходжкинии таких белков нет. Польза от столь высокого GC-состава для эндосимбиотической бактерии также не очевидна [2].
Еще одна особенность, присущая многим эндосимбиотическим бактериям с очень малыми геномами, — использование немного измененного генетического кода. Чаще всего в этих случаях стоп-кодон UGA начинает кодировать триптофан. Согласно одной из гипотез, объясняющих этот феномен, в геномах с низким GC-составом (каковыми, как мы помним, является большинство мельчайших геномов) стоп-кодон UGA часто мутирует в другой стоп-кодон — UAA. Если впоследствии произойдет обратная мутация, то есть UAA вновь превратится в UGA, он с большой вероятностью станет кодировать какую-то аминокислоту, как правило, триптофан. Однако у упоминавшейся выше ходжкинии GC-состав совсем немаленький, хотя UGA все же кодирует триптофан, поэтому описанный механизм «переключения» кодонов вряд ли имел место в ее случае. Существует и альтернативное объяснение: эндосимбионты часто утрачивают фактор терминации трансляции RF2, который распознает стоп-кодон UGA, поэтому UGA становится кодирующим (впрочем, неизвестно, почему именно триптофановым) [2].
У бактерии Candidatus Riesia pediculicola, обитающей в теле вшей Pediculus humanus corporis, есть другая особенность аппарата трансляции: набор ее тРНК сокращен до допустимого минимума. Эта бактерия утратила все ферменты, модифицирующие тРНК, за исключением тех, которые модифицируют антикодоновую шпильку. Именно эта часть молекулы тРНК принимает участие в распознавании комплементарного кодона в мРНК. Некоторые исследователи предположили, что такой скромный набор тРНК у Candidatus Riesia pediculicola похож на набор тРНК самых древних клеток. Действительно, фермент псевдоуридинсинтаза А, ответственный за появление псевдоуридинов в антикодоновой шпильке тРНК, имелся у последнего общего предка всех форм жизни. Однако пока неясно, насколько древними являются те немногие ферменты модификации тРНК, которыми обладает Candidatus Riesia pediculicola [2].
Стоит заметить, что эндосимбиотические бактерии не только теряют гены, но порой и приобретают. Когда в организме одного и того же хозяина обитает несколько бактерий-эндосимбионтов, между ними нередко происходит горизонтальный перенос генов, причем в некоторых случаях в обмене участвуют и гены самого хозяина. В качестве примера можно привести бактерию Ca. Carsonella rudii, которая является облигатным эндосимбионтом листоблошки Pachyphsylla venusta. Она обладает одним из мельчайших известных геномов: он состоит лишь из 160 т.п.н. и содержит 213 генов, среди которых нет ряда генов, необходимых для функционирования любой живой клетки. Однако карсонелла способна жить припеваючи и в отсутствие других эндосимбионтов в организме насекомого. Как показал детальный транскриптомный анализ, биосинтез ряда аминокислот карсонелла осуществляет совместно с бактериоцитом, в котором живет: некоторые реакции катализируют ферменты бактерии, другие — эукариотической клетки. Примечательно, что многие ферменты метаболизма аминокислот в бактериоцитах кодируются генами бактериального происхождения, вероятно, приобретенными от других эндосимбионтов (рис. 2) [2].
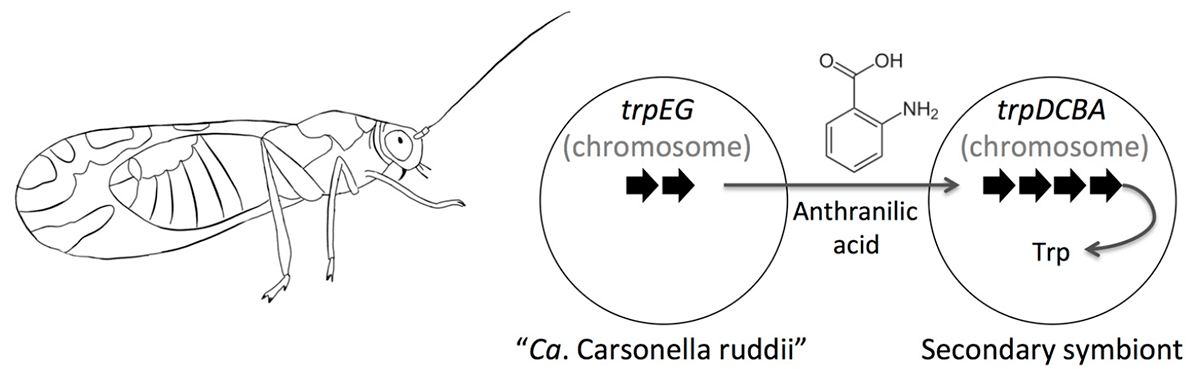
Рисунок 2. Схема синтеза триптофана в симбиотическом союзе листоблошки и Ca. Carsonella rudii. Ca. Carsonella rudii синтезирует антраниловую кислоту, которая превращается в триптофан под действием ферментов другого симбионта или ферментов, которые бактериоцит от него позаимствовал.
В обмен генами с эндосимбиотическими бактериями вступают не только насекомые, но и другие организмы. Например, нематода Brugia malayi более 10% своего генома обязана эндосимбиотической бактерии из рода Wolbachia. А некоторые бактерии приспособились к жизни внутри грибов [2].
Иногда сам хозяин становится зависимым от своих эндосимбионтов. Например, бактерии Buchnera aphidicola и Ca. Serratia symbiotica совместно снабжают своего хозяина, тлю Cinara cedri, триптофаном: часть ферментов его биосинтеза кодируется плазмидой B. aphidicola, а остальные — геномом Ca. Serratia symbiotica [2].
Наконец, эндосимбиотические бактерии иногда сами становятся хозяевами для других бактерий, образуя подобие матрешки. Обладательница одного из самых маленьких геномов Ca. Tremblaya princeps, живет в бактериоцитах войлочника Planococcus citri, но и сама является хозяином бактерии Ca. Moranella endobia. Эти бактерии сами по себе не имеют полного набора генов почти всех жизненно важных метаболических путей, однако взаимно дополняют друг друга, так что в их тандеме имеются все необходимые ферменты. Впрочем, как организован столь запутанный метаболический круг, неясно, поскольку непосредственного перемещения белков между цитоплазмами двух бактерий пока не удалось показать [2].
Синтетическая биология: сделаем мельчайший геном сами
В наше время исследователи располагают внушительным арсеналом методов редактирования геномов и синтеза протяженных последовательностей ДНК, что открывает перспективы создания новых форм жизни с геномами, собранными в лаборатории. Область биологии, занимающаяся созданием искусственных форм жизни и биологических систем, получила название синтетической биологии .
Подробнее о синтетической биологии и создании искусственной жизни читайте в наших статьях [3–5].
Пионером в области искусственных геномов стал известный ученый Крейг Вентер, изобретатель секвенирования методом дробовика и один из ведущих ученых, работавших над секвенированием генома человека. Его группа смогла в лабораторных условиях воссоздать геном бактерии Mycoplasma mycoides, который далее внесли в клетки другой микоплазмы, Mycoplasma capricolum, из которых предварительно удалили ее собственную ДНК. Сенсационные результаты получения нового вида бактерий, названного Mycoplasma laboratorium, были опубликованы в Science в 2010 году [6].
А можно ли собрать геном, которого в природе не существует? Например, искусственно получить самый маленький геном, способный поддерживать функционирование живой клетки? Работы по постепенному уменьшению размеров генома начались снова с микоплазм как одних из самых изученных бактерий с миниатюрными геномами. В 2016 году в Science было объявлено о создании мельчайшего из известных геномов, способных поддерживать жизнь, на основе генома M. mycoides. Ученым удалось сократить исходный бактериальный геном примерно наполовину — с 1079 т.п.н. до 531 т.п.н., а число генов «ужали» до 473 минимально необходимых. К слову, функции 149 из них так и остались неясными, несмотря на их абсолютную необходимость для жизни клетки (рис. 3) [7]. Подробнее об этом исследовании читайте в нашей статье [8].
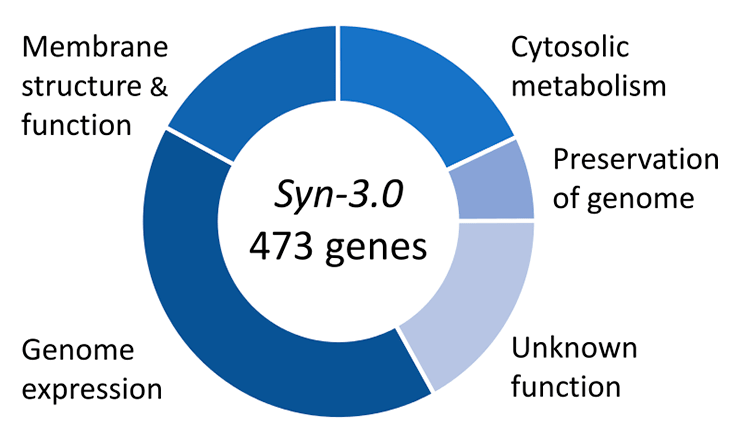
Рисунок 3. Функции генов в минимальном геноме, сконструированном в 2016 году на основе генома M. mycoides.
Стоит заметить, что предпринимались попытки уменьшить геном и других бактерий, правда, не для получения минимально возможного генома, а для других целей: например, клеток, эффективно производящих определенные вещества. Уменьшение генома проводили для кишечной палочки Escherichia coli, еще одной микоплазмы Mycoplasma genitalium, Bacillus subtilis, Corynebacterium glutamicum, Pseudomonas putida, Streptomyces avermitilis и Vibrio natriegens. В этих работах использовали искусственный химический синтез ДНК, а также различные варианты рекомбинации, например, опосредованные системами CRISPR/Cas9 или Cre-loxP (рекомбиназа Cre, распознающая локусы под названием loxP [11]). Ведутся активные работы по созданию оптимизированных геномов цианобактерий и других фотосинтетических бактерий с колоссальным потенциалом для получения биотоплива [7].
Разумеется, собрать абсолютно минимальный геном, «минимальную жизнь», вряд ли возможно: слишком уж разные местообитания населяют разные бактерии и слишком различны их метаболические потребности. Однако искусственная оптимизация геномов многих биотехнологически важных микроорганизмов, вероятно, будет иметь большое прикладное значение.
Литература
- Маленький, да удаленький: самые маленькие клетки;
- David J. MartÃnez-Cano, Mariana Reyes-Prieto, Esperanza MartÃnez-Romero, Laila P. Partida-MartÃnez, Amparo Latorre, et. al.. (2015). Evolution of small prokaryotic genomes. Front. Microbiol.. 5;
- Синтетическая биология: от программирования компьютеров к программированию клеток;
- Синтетическая биология: от наблюдения к вмешательству;
- Синтетическая жизнь;
- D. G. Gibson, J. I. Glass, C. Lartigue, V. N. Noskov, R.-Y. Chuang, et. al.. (2010). Creation of a Bacterial Cell Controlled by a Chemically Synthesized Genome. Science. 329, 52-56;
- Esteban Martínez-García, Víctor de Lorenzo. (2016). The quest for the minimal bacterial genome. Current Opinion in Biotechnology. 42, 216-224;
- С геномом налегке: минимальный размер бактериального генома — это сколько?;
- J. Gijs Kuenen. (2008). Anammox bacteria: from discovery to application. Nat Rev Micro. 6, 320-326;
- Iain Anderson, Olivier Duplex Ngatchou Djao, Monica Misra, Olga Chertkov, Matt Nolan, et. al.. (2010). Complete genome sequence of Methanothermus fervidus type strain (V24ST). Stand. Genomic Sci.. 3, 315-324;
- 12 методов в картинках: генная инженерия. Часть II: инструменты и техники.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚