Гепатит B: запутанная история от динозавров до наших дней
30 мая 2025
Гепатит B: запутанная история от динозавров до наших дней
- 1960
- 0
- 0
Кадр из сериала «Доктор Хаус». Грегори Хаус держит в руках лист бумаги, на котором написано: «результаты анализа». Положительный результат теста на гепатит B — тяжелое испытание. Чтобы таких диагнозов было как можно меньше, в статье подробно рассказано о путях распространения этой болезни и методах ее профилактики.
мем автора статьи
-
Автор
-
Редакторы
-
Иллюстратор
Гепатит — заболевание, поражающее печень. Его причины обширны и разнообразны: от бактерий и вирусов до отравлений (токсический гепатит), а также побочных эффектов от медикаментов (лекарственный гепатит). Вирусные гепатиты занимают второе место в мире среди инфекционных болезней с высокой летальностью: на их долю приходится более 1 млн смертей в год. Уступают они только самой опасной болезни — туберкулезу, борьбе с которым посвящена одна из предыдущих статей цикла «История одной эпидемии». Самый коварный из вирусных гепатитов — гепатит B (83% умерших), с большим отрывом следует «ласковый убийца» — гепатит C (17%). Причем это данные всего за 60 лет наблюдений, потому что долгое время гепатиты были загадочной болезнью, неуловимых возбудителей которой обнаружили только в 1970-х годах! Полной случайностей истории их открытия и работе над методами профилактики посвящена эта статья.
История одной эпидемии
«Забытые» инфекции: оспа, корь, туберкулез, чума, холера, бешенство… Читая или мимолетно слыша о них, мы вряд ли задумываемся, насколько они опасны. Хотя не так давно одно только слово «испанка» или «полиомиелит» заставляло людей в панике бежать друг от друга! При этом упоминание оспы, наоборот, было приглашением в дом больного на «вечеринку». Зачем же тогда понадобилось ее ликвидировать? И, кстати, может быть ужасы о болезнях несколько преувеличены, и нет большой необходимости бороться с ними с помощью вакцинации? Об этом мы рассказывали в партнерском спецпроекте «Вакцинация», а в статьях этого цикла давайте вернемся в прошлое, чтобы узнать, «из какого сора» рождалась современная медицина и профилактика болезней.

Партнер спецпроекта — «Национальная иммунобиологическая компания», фармацевтический холдинг, созданный госкорпорацией Ростех в 2013 году с целью развития производства важных для национальной безопасности иммунобиологических лекарственных препаратов.
Вирус гепатита B относится к семейству гепаднавирусов (Hepadnaviridae). Благодаря останкам древних животных известно, что он существует миллионы лет. Его древние подвиды поражали архозавров (предшественники земноводных) и предков птиц, живших 150–147 млн лет назад. Люди удостоились его «внимания» в эпоху мезолита, то есть 15–20 тыс. лет назад [1]. Этот вирус был обнаружен в геноме древних людей, живших по обе стороны атлантики: это косвенно подтверждает, что контакты между американским и европейским континентами могли происходить задолго до эпохального плавания Христофора Колумба.
Врачи древности выделяли гепатит среди других болезней благодаря тому, что его сопровождала не только лихорадка и расстройство пищеварения, но и характерная желтуха, когда кожа и белки глаз приобретают желтоватый оттенок. Первое описание подобных симптомов встречается в Вавилонском трактате и греко-римском манускрипте De internis affectionibus (V в. до н.э.). В «Эпидемии» Гиппократа указано, что при желтухе также наблюдается увеличение печени, а ее причину «отец медицины» видел в нарушении гармонии четырех основных жидкостей организма из-за преобладания желчи (подробности — во врезке «Великие врачи древности»).
Живший несколькими веками позже древнеримский медик Гален писал про свойственное гепатитам воспаление печени, а также про их «холодную» и «горячую» разновидности. В Х веке великий Авиценна впервые классифицировал разные виды желтух, но термин «гепатит» впервые появился лишь в XVIII веке в книге Жана Бианша Historia hepatica sen theoria ex praxis omnium morborum hepatis et bilis [2].
Первые эпидемии желтухи начались в Средневековье [4], когда «печеночный тиф» стал неотъемлемым спутником крестовых походов и войн (известно письмо римского папы Захария, который в 751 году н.э. предлагал отправлять на карантин людей и лошадей с признаками желтухи [2]). К XVIII столетию это заболевание получило такое массовое распространение, что без него не обходилась ни одна военная кампания: наполеоновские войны, война американского Севера и Юга , франко-прусская, англо-бурская, русско-японская и, конечно же, все войны ХХ века, включая афганскую! Впрочем, сейчас трудно установить, какой именно вирус вызывал их: если судить по невысокой смертности, большая часть случаев была вызвана вирусом гепатита A, который прекрасно передается в условиях скученности через воду и грязные руки [5].
Наравне с гепатитами в армиях бушевали корь и паротит. Ситуация была настолько серьезной, что многие солдаты погибали не на полях сражений, а из-за болезней. О том, какой урон нанесла американским войскам корь во время войны Севера и Юга, читайте в статье «Унесенные корью: корь у взрослых — это опасно?» [6].
Одна болезнь — множество причин
Первое научное описание эпидемии желтухи относится к 1791 году, однако более детальная документация появилась только в XIX веке. Пожалуй, самой известной является вспышка в немецком городе Бремене среди докеров (грузчики в порту), которых в 1855 году привили против оспы: признаки желтухи появились у 14% (191 из 1289 привитых). Когда стали исследовать причины заражения, предположили, что оно могло произойти из-за человеческой лимфы, которая присутствовала в вакцине. Впоследствии этот случай, подкрепленный другими свидетельствами развития желтухи после медицинских манипуляций, навел ученых на мысль о «постпрививочной желтухе» (сывороточном гепатите). Однако до середины 1940-х годов о природе этой болезни шли бесконечные споры [4]:
-
2,5 тысяч лет господствовало предположение Гиппократа о воспалении печени вследствие дисбаланса тканевых жидкостей (дискразическая теория).
-
В 1829 году французский врач Франсуа Бруссе предположил, что гепатит является следствием воспаления желчных путей, затрудняющих отток желчи из печени.
-
В 1830-х годах британский врач Уильям Стокс полагал, что желтуха является следствием воспаления, которое поражает верхние отделы тонкого кишечника и далее распространяется на ткани печени. Его коллега Ричард Брайт, напротив, считал гепатит самостоятельным заболеванием, которое приводит к желтухе (гепатогенная теория).
-
В 1842 году австрийский патологоанатом Карл Рокитанский связал желтуху с усиленным распадом крови в печени (гематогенная теория).
-
В 1865 году Рудолф Вирхов опубликовал катарально-обструкционную теорию, суть которой заключалась в механической закупорке желчных протоков, приводящей к катару (воспалению слизистой оболочки) общего желчного протока и, следовательно, к «катаральной желтухе».
-
В 1888 году Сергей Боткин предложил новый взгляд на происхождение желтух: он считал их инфекционным заболеванием, в некоторых случаях приводящим к циррозу печени, которое возникает из-за загрязненных продуктов и воды [7]. Боткин подробно описал симптоматику, а также разные формы этой болезни, включая безжелтушную.
Первые обоснованные догадки о вирусной природе гепатита появились в 1908 году у шотландского врача Стюарта МакДональда, однако их было невозможно проверить из-за низкой мощности технических средств. К 1917 году врачей, рассуждавших в подобном ключе, стало больше, поэтому появился термин «инфекционная желтуха», чей возбудитель считали «невидимым, как таковой при желтой лихорадке» [4].
Первое серьезное подтверждение вирусного происхождения гепатита было получено в 1930-х годах шотландским ученым Джорджем Финдлеем (рис. 3), который в 1929 году занимался вопросами вакцинации в британских африканских колониях. Вместе с соавторами он опубликовал статью, в которой анализировал случаи возникновения инфекционной желтухи после различных медицинских манипуляций, выделив три ее разновидности:
-
посттранфузионную (вследствии переливаний крови и ее компонентов);
-
поствакцинальную (после прививок);
-
постинокуляционную (из-за случайных повреждений иглами медицинских работников) [8].

Рисунок 3. Ученые, изучавшие острые гепатиты в 1930–1940 годах и получившие первые научные подтверждения его вирусного происхождения. Слева: Фредерик МакКоллум (1909–94) — выдающийся канадско-британский вирусолог, долгие годы занимавшийся вирусными гепатитами. Он вспоминал, что в 1942 году принимал участие в обсуждении вакцинации Уинстона Черчилля против желтой лихорадки перед его поездкой в Москву через Ближний Восток. Учитывая, что риски заразиться гепатитом были высоки, а времени на формирование поствакцинального иммунитета не было, приняли решение отказаться от прививки. Интересно, что региональный начальник королевских ВВС, привитый вакциной из той же серии, которая предполагалась для премьер-министра, через два месяца заболел тяжелой формой гепатита. Справа: Джордж Финдлей (1893–1952) — британский ученый шотландского происхождения, военный врач и доктор философии. Был одним из руководителей медицинской службы британской армии в северной Африке, специализировался на желтой лихорадке [9]. С 1950 года — президент Королевского микроскопического общества.
коллаж автора статьи по [8]
В 1937–38 годах Финдлей вместе с канадским ученым Фредериком МакКоллумом (рис. 3) опубликовал результаты наблюдения за поствакцинальным гепатитом у привитых против желтой лихорадки. Данные указывали на вирусный возбудитель, появившийся в вакцине из-за технологии производства с использованием сыворотки донорской крови. В 1938 году была опубликована аналогичная работа, которая касалась уже противокоревой сыворотки. Похожие результаты получили и советские ученые исследовательской группы П. Г. Сергеева и Е. М. Тареева после расследования вспышки вирусной желтухи в одном из черноморских пунктов иммунизации против лихорадки паппатачи (из 350 человек заболело 92). К сожалению, их работа не получила широкой огласки [5]. Впрочем, так как обнаружить возбудителя не удавалось (а его усиленно искали, в том числе среди бактерий, вызывающих желудочно-кишечные болезни), все эти предположения оставались только теориями.
Поиск длиною в 20 лет
В 1941–42 годах произошло невероятное событие: в американской армии началась поствакцинальная эпидемия желтухи, от которой пострадали 28 тысяч военнослужащих! В армии Великобритании подобные заражения тоже не были редкостью, поэтому две страны объединили усилия по поиску неуловимого возбудителя. МакКоллум и Финдлей были привлечены к исследованиям в первую очередь. Для начала они изучили результаты первых опытов по заражению волонтеров, проведенных в Австрии, и сообщения о случайных заражениях в Японии.
Исследование началось в конце 1942 года и продлилось два года. Ученые собирали биологические материалы больных гепатитом (кровь, моча, фекалии), а потом вводили их волонтерам: внутрь, внутриназально, внутримышечно, подкожно (в ряде случаев материал фильтровали через бактериальные фильтры и нагревали). Кроме этого, они ознакомились с данными наблюдений Уолтера П. Хевенса за эпидемией желтухи на Сицилии.
Благодаря собранной информации ученые смогли установить пути передачи болезни и основные характеристики инфекционного процесса, а также окончательно поставить точку в вопросе о ее вирусном происхождении. Им удалось даже выявить некоторые свойства возбудителя! Но самое главное, появилось предположение, что гепатит — это не одно, а два разных заболевания со своими особенностями [10]. В итоге в 1947 году Фредерик МакКоллум предложил различать вирусные гепатиты, поделив их на виды A и B [11].
В 1950–60 годы вирусы гепатита активно изучали с помощью неэтичных с современной точки зрения экспериментов на заключенных и умственно отсталых детях (об этой нелицеприятной истории читайте в статье «Не дружите дети с гепатитом B» [14]). Их результаты подтвердили предположение МакКоллума о двух разных возбудителях и помогли в создании первой иммунной сыворотки.
Болезнь Боткина: гепатиты в СССР
В царской России врачи не уделяли желтухе большого внимания — в то время были более серьезные проблемы: туберкулез, холера, оспа и дифтерия. Тем не менее в 1888 году именно русский врач и ученый Сергей Петрович Боткин пересмотрел существующие взгляды на «катаральную желтуху», выдвинув гипотезу, что это инфекционная болезнь. Он обратил внимание на периодические вспышки желтухи в виде связанных между собой случаев и писал, что катаральная желтуха «есть болезнь инфекционная, ибо без этого понятия нельзя объяснить даже таких резких симптомов, как увеличение селезенки, встречающееся иногда поражение почек и, наконец, эпидемическое появление болезни» [7].
Несмотря на научные труды Боткина, в первой половине ХХ века в российской науке не было определенной позиции по гепатитам. Считалось, что их наиболее вероятным возбудителем являются бактерии, в частности лептоспиры. Однако исследования В. И. Терских и М. Я. Ясиновского в 1940-х годах опровергли это предположение — ни один из известных в то время бактериальных возбудителей не имел отношения к желтухе. Также, как и за океаном, в СССР наиболее вероятным стали считать вирусный возбудитель [5].
Хуже обстояло дело с хроническими гепатитами — отечественные ученые выделяли их великое множество, включая хронизацию процесса после острой фазы, а также сифилитические, туберкулезные, малярийные и бруцеллезные [5]. По этой причине к началу Великой Отечественной войны теоретические представления о желтухе у большинства медиков сильно устарели — при этом, заболеваемость в армии носила массовый характер (рис. 5):
-
продвижение по разоренными и разрушенным населенным пунктам было сопряжено с идеальными условиями для вспышек гепатита A;
-
с каждым годом войны увеличивалось количество военнослужащих, перенесших переливание крови, а также вакцинацию от разных болезней, благодаря чему возрастало количество носителей вируса гепатита B;
-
продвижение войск на запад было в принципе связано с ростом венерических заболеваний из-за беспорядочных половых контактов.
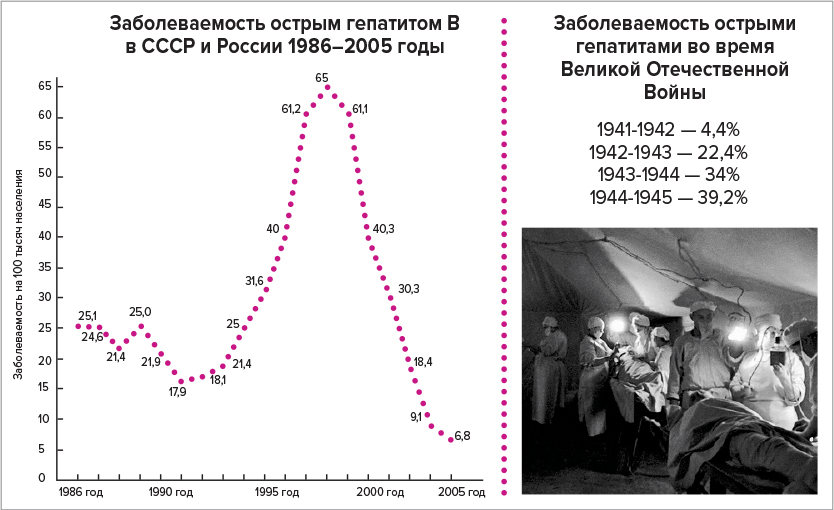
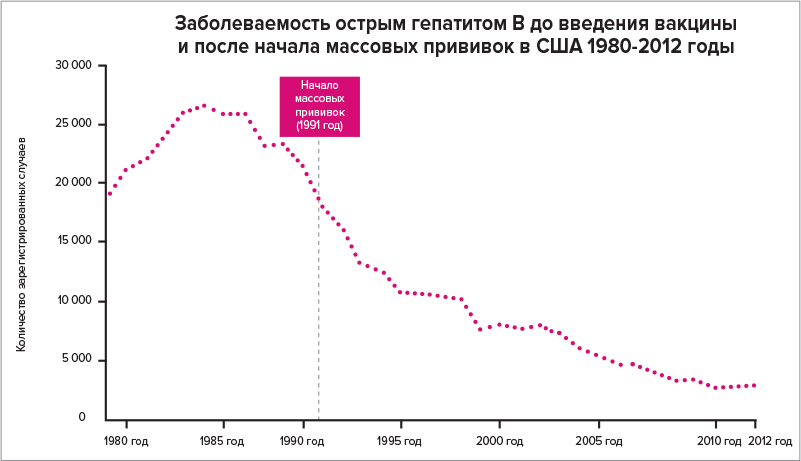
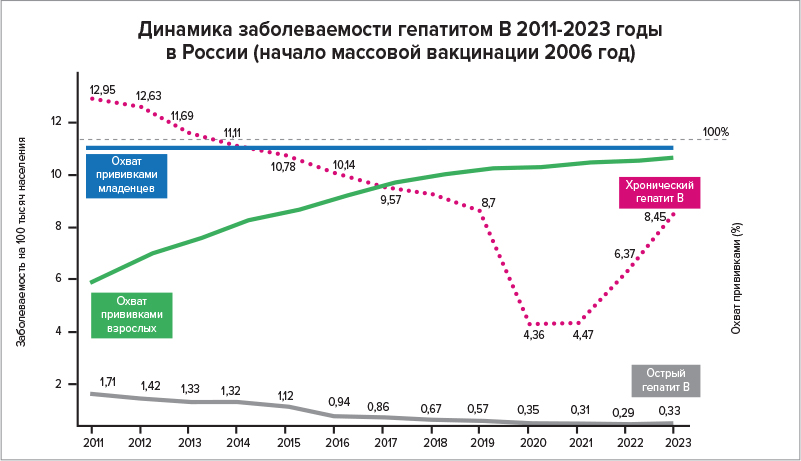
Рисунок 5. Заболеваемость острым гепатитом B в нашей стране 1986–2005 годы (слева) и количество пациентов с острыми гепатитами в Красной армии во время Великой Отечественной Войны (справа). Скорее всего, в первые два года ВОВ в основном были вспышки гепатита А, а во второй половине должна была серьезно возрасти доля гепатита B. Более точных данных нет, так как основная статистика за вирусными гепатитами в нашей стране ведется с 1999 года. Благодаря началу массовой вакцинации в 2006 году уровень заболеваемости острым гепатитом B сократился с 43,7 на 100 000 населения в 1999 году до 0,33 в 2023 году.
В 1949 году, в СССР прошла конференция, организованная Е. М. Тареевым, на которой обсуждались вопросы происхождения желтух: вирусная природа острых гепатитов уже не вызывала сомнений, однако оставались споры вокруг циррозов печени и хронических процессов. Как бы то ни было, начиная с 1950 года больных острыми гепатитами стали лечить в инфекционных больницах [5], благодаря чему появилась статистика заболеваемости (рис. 5).
На конец 1980-х годов среди источников распространения гепатита B лидировали медицинские манипуляции (то есть им заражались преимущественно в больницах из-за использования многоразовых инструментов). Показатель заболеваемости был достаточно высок: 42–43 случая на 100 000 населения. Высокой была и доля зараженных среди подростков 15–19 лет (половой путь передачи, инъекционный прием наркотиков), а также детей первых лет жизни (вертикальная передача инфекции в родах) [15].
Долгожданная удача
Возбудителей вирусных гепатитов удалось обнаружить по чистой случайности. Ведущую роль в этом сыграл банк образцов сыворотки крови, который в 1960-х годах собрал американский врач и биохимик Барух (Барри) Бламберг (рис. 6).

Рисунок 6. Барух Бламберг в лаборатории на фоне банка сывороток, которые он собрал в разных странах мира, чтобы изучить отличия и изменения в крови представителей разных этнических групп. Лауреат Нобелевской премии по медицине 1976 года за открытие австралийского антигена и вклад в исследование вируса гепатита B. С 2005 года был президентом Американского философского общества.
Его целью было изучение генетических маркеров предрасположенности к разным болезням. Для этой цели он собрал образцы крови у представителей разных этнических групп и изучал сывороточные белки. Проводя эксперименты, Бламберг предположил, что у людей, часто получающих препараты донорской крови, должны вырабатываться антитела против чужеродных белков [16]. Он назвал их «полиморфными». Такие белки имеют большое сходство в строении, однако у них есть небольшие генетические различия в аминокислотной последовательности.
Несколько образцов сыворотки австралийских аборигенов привлекли внимание его коллеги Харви Альтера, обнаружившего в них неизвестную структуру, которую позже назвали «австралийским антигеном» (AuAg). Сначала Бламберг предположил, что это один из полиморфных сывороточных белков, но вскоре появились доказательства о его возможной связи с гепатитом, о чем упоминается в научной статье Бламберга 1967 года (впоследствие за вклад в открытие и исследование вируса гепатита B он получил Нобелевскую премию по медицине).
Антигеном называют любое вещество (молекулу, частицу), которое вызывает иммунный ответ (про антигены на «Биомолекуле» есть отличная статья [17]).
В 1968 году эту догадку удалось подтвердить Альфреду Принсу из Нью-Йоркского центра переливания крови, который целенаправленно искал антиген «сывороточного» гепатита у пациентов с гепатитом B. Сравнивая обнаруженные им антигены с австралийским, он понял, что они идентичны. Немного позже другие исследователи обнаружили, что этот антиген маркирует как острый, так и хронический, гепатит B. Еще одним важным открытием стало обнаружение австралийского антигена у здоровых людей (это доказывало существование бессимптомной хронической инфекции у части переболевших). Исследования Бламберга также помогли наладить процедуру тестирования донорской крови. Пусть это не давало 100% эффекта, но помогло значительно снизить риск заражения [16]. Впрочем, открытие австралийского антигена не отвечало на вопрос о возбудителе. Мало того, не было понимания что именно представляет из себя этот антиген: он мог быть как белком, образовавшимся в ответ на инфекцию, так и возбудителем или его частью.
Серия экспериментов, проведенных в 1971 году, позволила предположить, что все-таки речь может идти о патогене: под электронным микроскопом австралийский антиген представлял собой не единое целое, а маленькие круглые частицы разного размера (это отличало его от известных в то время вирусов). Исследовательская группа Бламберга не обнаружила в нем нуклеиновых кислот, поэтому было высказано предположение, что он вызывает инфекцию иным способом — как, например, возбудитель губчатой энцефалопатии (позже выяснилось, что эта болезнь обусловлена прионами — белками с патогенными свойствами, появляющимися из-за изменения их конформации). Но и это было неверно. В 1971–72 годах британский ученый Дэвид С. Дейн обнаружил, что австралийский антиген присутствует в довольно крупных вирусоподобных объектах с хорошо заметным внутренним ядром, а его коллега Джун Алмейда смогла выделить ядерные частицы и с помощью иммунно-электронной микроскопии доказала, что у пациентов с гепатитом B к этим частицам образуются антитела. Проще говоря, австралийский антиген являлся поверхностным белком оболочки вируса (сокращенно HbsAg — hepatitis B surface antigen), который инфицированные вирусом клетки печени (гепатоциты) выделяют в кровоток в виде круглых или нитевидных неинфекционных частиц вместе с полноценным вирусом (рис. 7) [16].
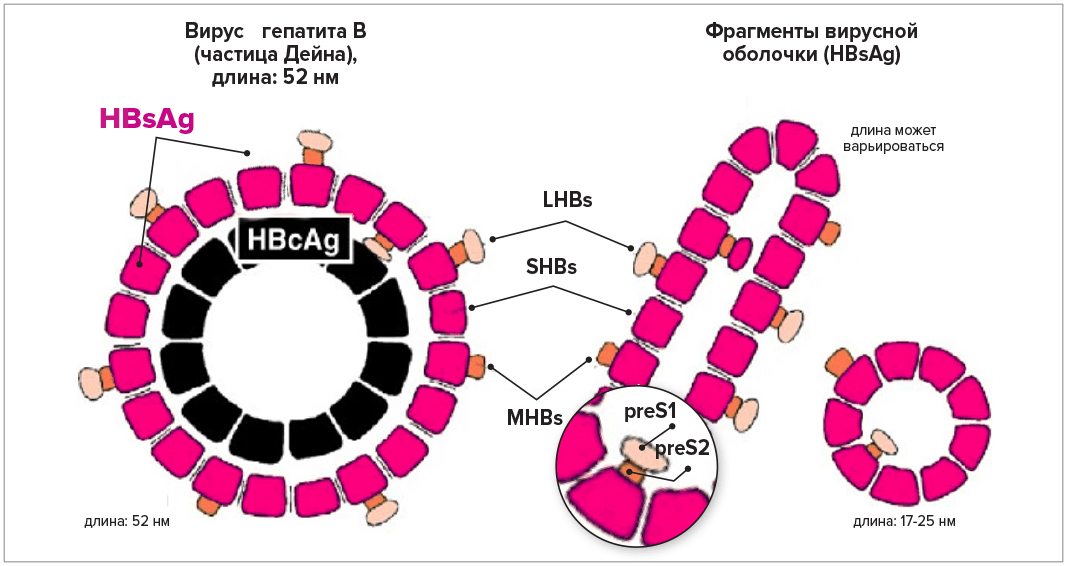
Рисунок 7. Строение вируса гепатита B. Слева: частица Дейна. Справа: нитевидные, а также сферические частицы поверхностного белка HBsAg. Этот белок существует в трех формах: большой (L) с доменами preS1, preS2 и S; средней (M) без домена preS1, а также SHBs без доменов preS1 и preS2. В ходе размножения вируса образуются побочные продукты: пустые оболочки и дефектная линейная ДНК, которая может встраиваться в геном клеток организма.
адаптация автора статьи по [16]
Гепатит B и его антигены
Открытие поверхностного антигена вируса гепатита B (рис. 7) HBsAg не отвечало на два главных вопроса: какова инфекционная нагрузка в данный момент и насколько заразен его носитель. В 1972 году шведский исследователь Ларс Магнус обнаружил в образцах крови пациентов на разных стадиях болезни подтип этого белка, который назвал HBeAg. Буква «е» означает enigma — загадка, так как в течение нескольких лет его природа была головоломкой для ученых. И лишь когда Уильям Руттер и Фолькер Брусс независимо друг от друга доказали, что HBeAg является укороченным производным белка HBcAg (рис. 8), стали понятны его роли [16]. Одна из них заключается в том, чтобы подавлять иммунный ответ (распознавание Т-лимфоцитами зараженных клеток). Иными словами, HBeAg маркирует стадию активной репликации вируса гепатита B (рис. 8).
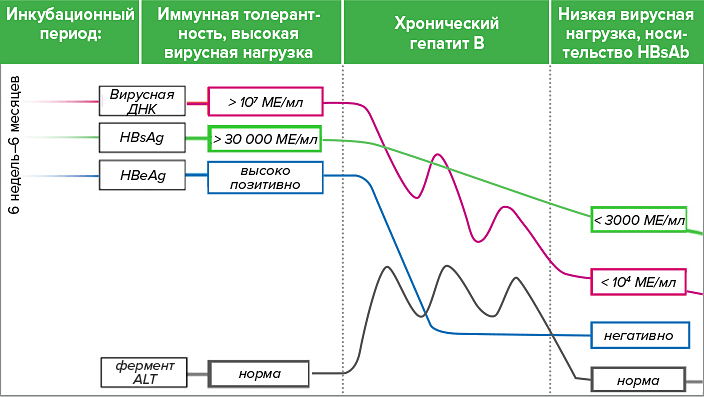
Рисунок 8. Три стадии хронической инфекции гепатита B. Если гепатит B не переходит в хроническую форму, HBsAg циркулирует в крови примерно полгода; в случае когда он присутствует дольше этого срока, говорят о хроническом процессе. При хроническом гепатите B вирусная нагрузка значительно снижается благодаря работе иммунной системы, однако гибель зараженных клеток печени приводит к очагам постоянного воспаления, которое может продолжаться годами, поскольку новые клетки инфицируются вирусами, и процесс идет по замкнутому кругу. Минимальной вирусной нагрузки (виремия <104/мл) удается добиться не каждому пациенту, поэтому хронический гепатит B нередко приводит к циррозу печени.
адаптация графика автора статьи из [16]
Важным моментом является то, что инфекция нарастает постепенно, поэтому в лабораторной диагностике существует шестинедельное «окно», когда вирус еще нельзя обнаружить, но его размножение уже идет. Это наиболее актуально для беременных и сексуальных партнеров зараженных: даже отрицательный результат анализа не гарантирует отсутствия болезни!
Генная инженерия приходит на помощь
Так как вирус, вызывающий гепатит B, был открыт сравнительно недавно, история профилактики этой болезни началась только в 1970-х годах. Первой была получена сыворотка из крови хронических больных, которую инактивировали нагреванием. В 1974 году Пауль Келер доказал, что донорские антитела к поверхностному белку вируса (рис. 8) достоверно снижают развитие инфекции у детей, родившихся у матерей-носителей гепатита B [18]. В начале 1980-х годов на Тайване было проведено исследование, показавшее, что 71% таких младенцев будут защищены от болезни, если сразу же после родов им ввести антитела [16]. Тем не менее подобная защита является пассивной и длится менее месяца, поэтому не является решением проблемы распространения гепатита B.
Донорские антитела или иммуноглобулины — это очищенные и концентрированные сыворотки; в них содержится высокая доля антител.
Понимая важность профилактики гепатита B, НПО «Микроген» разработало новый специфический иммуноглобулин против этой инфекции. В основу разработки легла собственная запатентованная технология компании по получению высокоочищенных и вирусобезопасных иммуноглобулинов класса G. Это ноу-хау позволяет создавать препараты из плазмы крови с характеристиками, соответствующими последнему поколению иммунобиологических средств.
В процесс производства включены дополнительные стадии очистки, в том числе хроматография. Это обеспечивает высокую степень безопасности в отношении вирусов, которые могут находиться в плазме донорской крови, и снижает вероятность развития нежелательных реакций у пациентов. В отличие от препаратов предыдущего поколения, новый иммуноглобулин вводится внутривенно, что обеспечивает более выраженный терапевтический эффект.
Этот препарат рекомендован в первую очередь младенцам, рожденным от матерей-носителей вируса гепатита B, для профилактики передачи инфекции. Также он показан пациентам с повышенным риском заражения этой болезнью: перед хирургическими операциями, при повторных гемотрансфузиях, гемодиализе, а также при органной и клеточной трансплантации.
Благодаря сыворотке появились и первые вакцины: выделенные из нее неинфекционные частицы, содержащие поверхностный белок HBsAg (рис. 8), стали использовать для производства плазменных вакцин, которыми в общей сложности привили около 5 млн человек из групп риска [16], [18]. Они показали высокую эффективность (95–98%) у детей и молодых взрослых, но вызывали ряд редких побочных эффектов и имели меньшую эффективность у пожилых людей и младенцев. К тому же они были дороги в производстве, ведь для них требовались большие запасы высокоочищенной сыворотки больных, количество которых, благодаря профилактике, стало снижаться. Использование продуктов крови также внушало опасения, что они могут быть онкогенными, вызывать аутоиммунные реакции или содержать цельные вирусные частицы (чтобы избежать этого, сыворотку обрабатывали ферментами, разрезающими белки: формальдегидом и мочевиной, однако этого могло быть недостаточно). Подобные подозрения стали наиболее актуальны, когда началась эпидемия ВИЧ, поэтому в начале 1980-х годов с помощью недавно появившейся технологии генной инженерии началась разработка вакцин следующего поколения.
Крупные фармацевтические компании MSD и Smith Kline Beecham (сейчас GSK) «заставили» клетки пекарских дрожжей синтезировать HBsAg. С помощью векторов (об этой технологии читайте в моей статье «Гонка во спасение: безопасны ли вакцины против коронавируса?» [19]) они вводили в дрожжи ген, кодирующий образование этого белка. Полученный HBsAg не был на 100% идентичен натуральному, однако в экспериментах на животных, а потом и среди тайских младенцев от матерей-носителей вируса такая вакцина показала высокую эффективность (графики вакцинации, принятые в нашей стране, см. на рис. 9).

Рисунок 9. Рекомендованный график вакцинации против гепатита B календаря прививок РФ.
инфографика автора статьи
Таким образом в 1986 году появилась первая рекомбинантная вакцина против гепатита B Engerix B. Она была настолько эффективной и безопасной, что к 2004 году в мире было привито более 700 млн доз [18]! Количество больных в развитых странах стало стремительно уменьшаться (рис. 10).
Факты о гепатите B, которые надо знать
Вирус гепатита B очень заразен: он может передаваться через любые биологические жидкости (кровь, слюну и т.д.), а также предметы обихода (бритвы, зубные щетки). Сами вирусные частицы не вредят организму — последствия болезни возникают из-за иммунного ответа на их размножение в клетках печени.
Среди всех возрастных групп гепатит B наиболее опасен для детей, особенно для младенцев, у которых он переходит в хроническую инфекцию приблизительно в 90% случаев. Хронический гепатит B — это пожизненное носительство вируса, опасность для окружающих, высокий риск развития цирроза и в некоторых случаях рака печени.
Существуют три основных антигена этого вируса: HbeAg (маркер стадии активной репликации), HbsAg (основной антиген вирусной оболочки) и HbcAg (ядерный белок). Наиболее известный из них — HbsAg, анализ на который сдают перед операцией или во время беременности. Риск передачи инфекции ребенку значительно возрастает у матерей с острой инфекцией (носители HbeAg), поэтому во время беременности им назначают противовирусные препараты, а младенцев не только прививают, но и вводят им иммуноглобулин.
Борьба с гепатитом B — задача не из легких. Согласно статистике ВОЗ, из 400 млн зараженных этим вирусом о своем статусе знает только каждый 20-й. По этой причине в нашей стране постоянно расширяют программы скрининга взрослых. Благодаря младенческой вакцинации заболеваемость гепатитом B снизилась в 16,5 раз по сравнению с 2007 годом. Дети до 17 лет им уже практически не болеют (данные Роспотребнадзора), а острый гепатит B у детей на сегодняшний день полностью ликвидирован. Впрочем, он запросто снова «восстанет», если начнутся массовые отказы от прививок.
Литература
- Выживший. Вирус гепатита, пришедший к нам через великие массовые вымирания;
- Мамедов М.К., & Михайлов М.И. (2003). Эволюция взглядов на этиологию гепатита: от дискразической теории к вирусной. Биомедицина (Баку). 4, 38–43;
- Оспа — забытая победа (небольшой эпидемиологический детектив);
- Бондарев Л.С. (2009). О проблеме вирусных гепатитов в историческом аспекте. Инфекционные болезни, гепатология. 281;
- Хазанов А.И. (2005). Острые вирусные гепатиты в Великую Отечественную войну. Мир вирусных гепатитов. 5, 2–5;
- Унесенные корью: корь у взрослых — это опасно?;
- Beliaeva V.S. (2013). S.P. Botkin and his works in gastroenterology (on the occasion of the 180th anniversary of his birth). Therapeutic Archive. 85, 96–98;
- Мамедов М.К. (2019). Фpедеpик Мак-Кэллум и его вклад в pазвитие виpусологии. Биомедицина (Баку). 4, 4–9;
- Мир до и после изобретения вакцин;
- F. O. MacCallum. (1946). Homologous Serum Hepatitis. Proceedings of the Royal Society of Medicine. 39, 655–657;
- Homologous Serum Hepatitis. (1947). The Lancet;
- «Ласковый убийца» под прицелом Миравирсена;
- Гепатит C. (2024). Всемирная организация здравоохранения;
- Не дружите, дети, с гепатитом B;
- Беляева Н.М. (2002). Вирусные гепатиты – прошлое и будущее. РМЖ. 2;
- Wolfram H Gerlich. (2013). Medical Virology of Hepatitis B: how it began and where we are now. Virol J. 10;
- Антиген — невидимка;
- Мамедов М.К. (2006). Успехи, проблемы и перспективы иммунопрофилактики вирусного гепатита В. Биомедицина (Баку). 2, 34–39;
- Гонка во спасение: безопасны ли вакцины против коронавируса?;
- Sina Ogholikhan, Kathleen Schwarz. (2016). Hepatitis Vaccines. Vaccines. 4, 6;
- Michael M. McNeil, Frank DeStefano. (2018). Vaccine-associated hypersensitivity. Journal of Allergy and Clinical Immunology. 141, 463–472;
- Hepatitis B. (2025). Immunize.org;
- Hepatitis B: What Hospitals Need to Do to Protect Newborns. (2016). Immunize.org;
- K Van Herck, E Leuridan, P Van Damme. (2007). Schedules for hepatitis B vaccination of risk groups: balancing immunogenicity and compliance. Sexually Transmitted Infections. 83, 426–432;
- Гепатит B. (2024). Всемирная организация здравоохранения;
- Jalal Poorolajal, Mahmood Mahmoodi, Reza Majdzadeh, Siavosh Nasseri-Moghaddam, AliAkbar Haghdoost, Akbar Fotouhi. (2010). Long-term protection provided by hepatitis B vaccine and need for booster dose: A meta-analysis. Vaccine. 28, 623–631;
- Susan L. Stramer, Ulrike Wend, Daniel Candotti, Gregory A. Foster, F. Blaine Hollinger, et. al.. (2011). Nucleic Acid Testing to Detect HBV Infection in Blood Donors. N Engl J Med. 364, 236–247;
- Зайцев И.А., Новак И.Н., Зайцева О.Е., & Кириенко В.Т. (2019).Значение генотипов вируса гепатита В в клинической практике. Актуальная инфектология, 7, 63–70;
- Neil Rajoriya, Christophe Combet, Fabien Zoulim, Harry L.A. Janssen. (2017). How viral genetic variants and genotypes influence disease and treatment outcome of chronic hepatitis B. Time for an individualised approach?. Journal of Hepatology. 67, 1281–1297.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚