
Инмазеб. Новая страница в истории лечения Эболы
08 февраля 2022
Инмазеб. Новая страница в истории лечения Эболы
- 938
- 0
- 1
Фотография жизнерадостного молотоголового крылана, потенциального переносчика вируса Эбола.
Рисунок в полном размере.
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Лихорадка Эбола, уже дважды взбудоражившая весь мир вспышками в Западной Африке, казалось бы, побеждена — во многих странах уже разработана вакцина, однако лечение уже заболевших людей все так же остается малоэффективным. Группе исследователей из «Регенерон Фармасьютикалс» удалось создать препарат, включение которого в терапию значительно снижает летальность заболевания. Каким же образом он работает? И почему разработка лекарства была такой трудной?
Конкурс «Био/Мол/Текст»-2021/2022
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2021/2022.

Партнер номинации — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

Генеральный партнер конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Что такое «Эбола»?
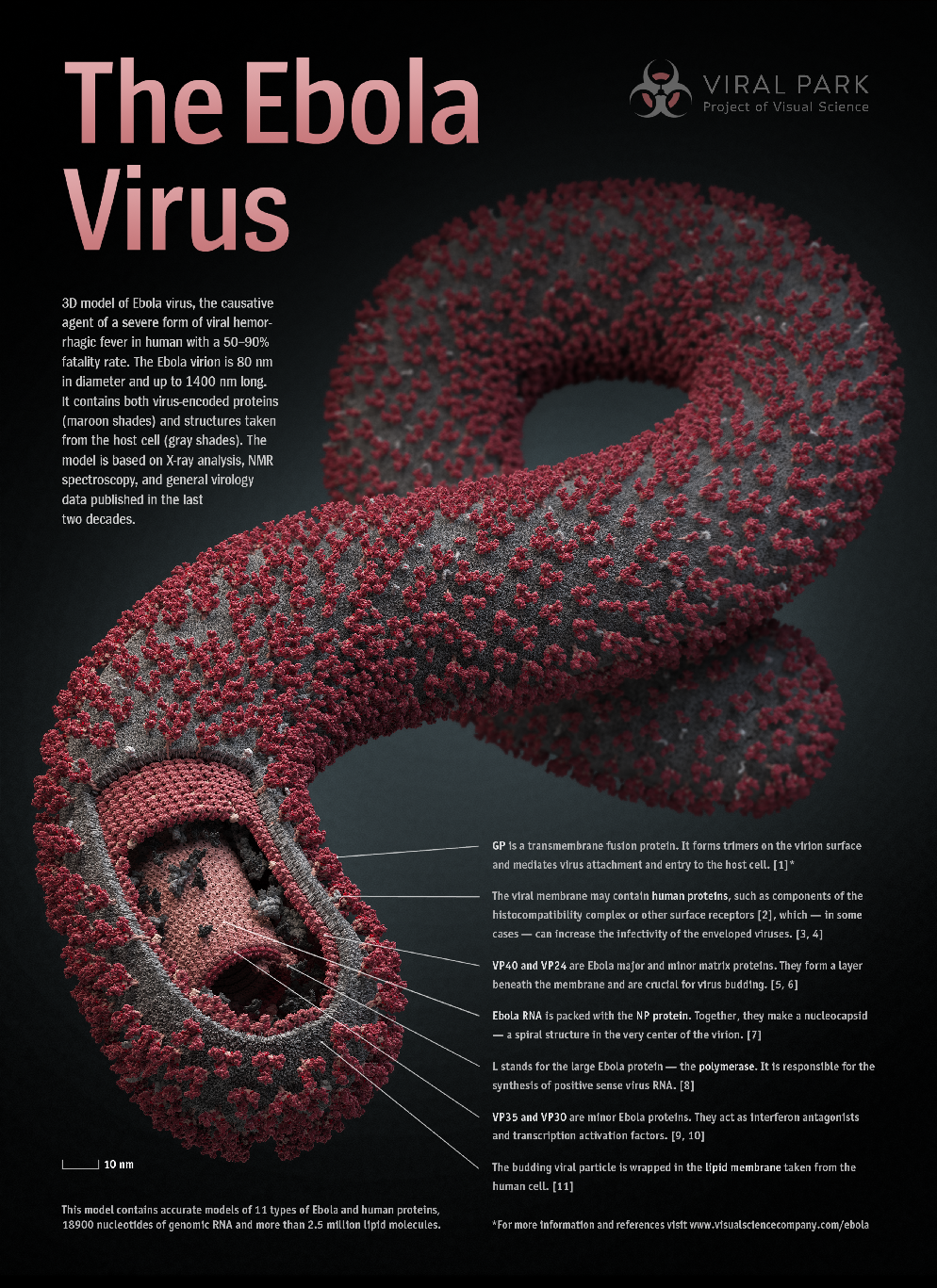
Рисунок 1. Информационный плакат о вирусе Эбола.
Геморрагическая лихорадка Эбола — острая вирусная болезнь с высокой заразностью, которая характеризуется развитием тромбогеморрагического синдрома. Он выражается в снижении числа лейкоцитов (белых кровяных тел, частично отвечающих за иммунитет) у больного и, как следствие, — в уменьшении сопротивляемости организма инфекции; а затем и в снижении количества тромбоцитов, что приводит к нарушению свертываемости крови и, нередко, нарушению целостности сосудистой стенки и кровоизлияниям.
Вирус Эболы (рис. 1, 2) вызывает тяжелое заболевание с острым течением, которое обладает близкой к абсолютной летальностью в отсутствие лечения и средней — порядка 60% от всех заболевших — для пациентов, получающих симптоматическое лечение [1]. Распространяясь через физиологические жидкости больных или умерших людей и животных, а также через загрязненные биологическим материалом предметы, болезнь быстро поражает членов одной семьи или деревни после проявления симптомов инфекции. Низкая плотность населения в Африке — один из немногих естественных барьеров для передачи болезни, но представьте только потенциальную активность этого потрясающего патогена в городских условиях развитых стран! Вирус также разносится естественными носителями, обитателями влажных тропических лесов — крыланами (рис. 3), очаровательными летучими мышами, употребляемыми местными жителями в пищу.
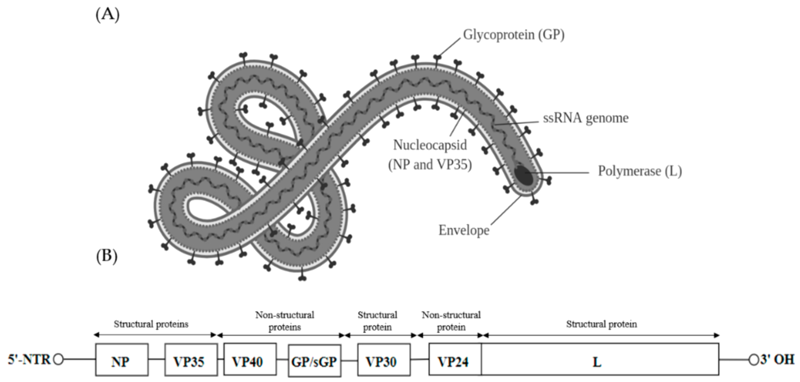
Рисунок 2. Схема структуры вируса Эбола с изображением вирусной РНК и относительным расположением участков, кодирующих его элементы.
«Никак вы не научитесь» — именно такой фразой могли отреагировать люди, которым в 2019 году стали известны возможные истоки пандемии коронавируса, цитируя персонажа Сапковского.

Рисунок 3. Крылан молотоголовый, естественный носитель вируса Эболы.
На первом этапе, наступающем через 6–10 дней после контакта с зараженным материалом [2], заболевшие (рис. 4) испытывают симптомы, схожие с другими распространенными в тропических странах заболеваниями, такими как малярия, тифоидная лихорадка (брюшной тиф) и менингит. А именно, у больного наблюдаются повышенная утомляемость, слабость, лихорадка с повышением температуры свыше 38 оС и боли в теле. Спустя еще некоторое время проявляются симптомы обыкновенных кишечных инфекций — тошнота, боли в животе, рвота и диарея.
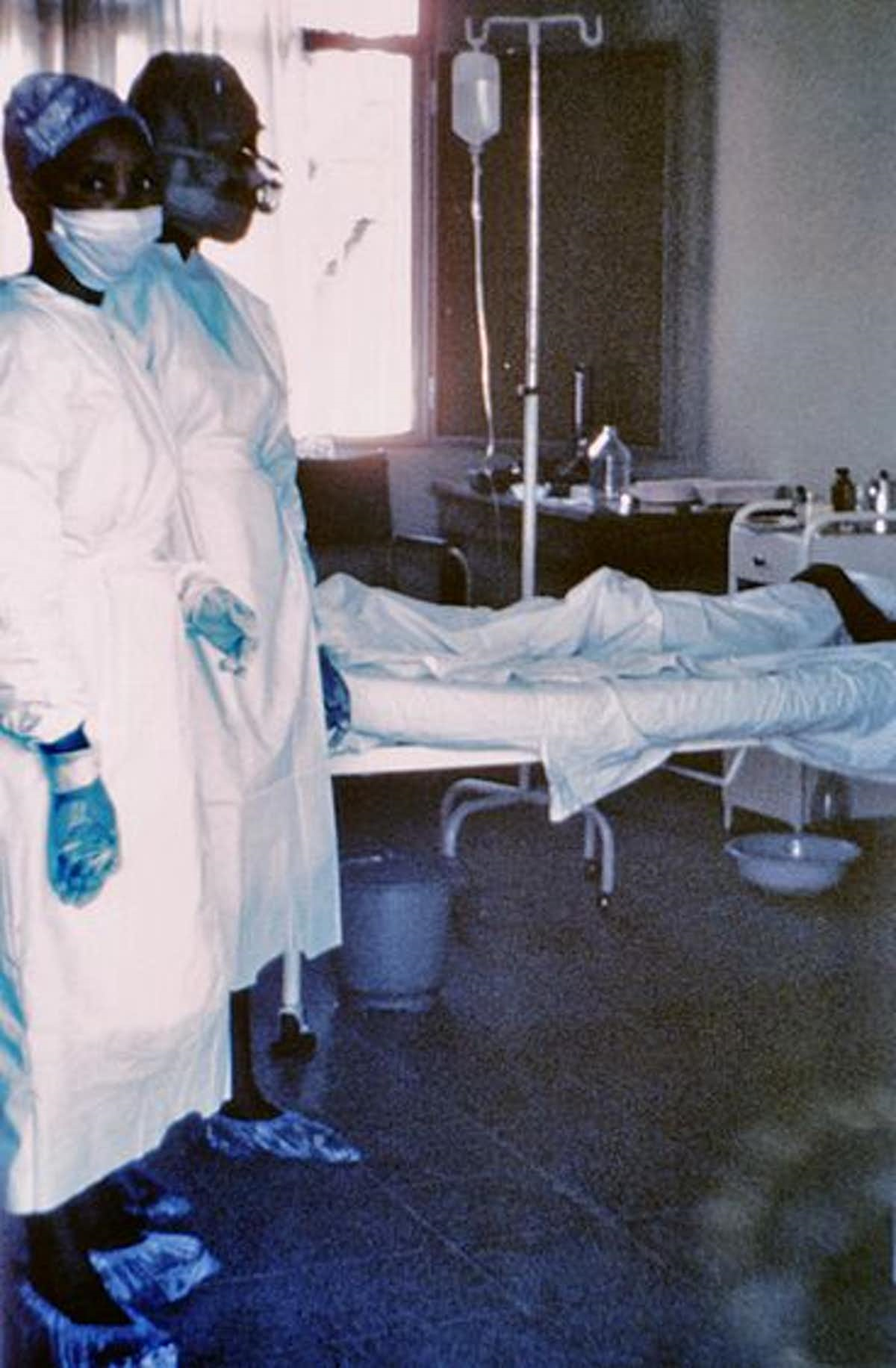
Рисунок 4. Две медсестры около кровати с больным лихорадкой Эбола. Позднее пациент скончался.
Настоящий ад для заболевших начинается примерно через неделю после проявления первых характерных симптомов. До этого момента, без возможности сделать ПЦР-тест, геморрагическую лихорадку Эбола невозможно обнаружить.
Q-ПЦР (или количественная полимеразная цепная реакция ) — метод молекулярной биологии, позволяющий создать копии определенного фрагмента ДНК из исходного образца, повысив его содержание в пробе на несколько порядков. Он применяется с целью увеличения количества РНК вирусных частиц в пробе и их последующего детектирования посредством взаимодействия с флуоресцентным красителем и регистрации излучения оптическими системами.
Подробнее об истории метода, его принципах и основных разновидностях читайте в статье «12 методов в картинках: полимеразная цепная реакция» [3].
Через неделю после проявления первых симптомов лихорадки у больных начинается стадия обильных кровотечений. Вирус Эбола вызывает некоторое снижение свертываемости крови, что в условиях жизни африканских народов в естественном ареале распространения инфекции может провоцировать сильные кровотечения в желудочно-кишечном тракте из-за особенностей слизистых оболочек тонкого и толстого кишечника в десяти процентах случаев, а обильное кровотечение из прочих слизистых — практически в каждом втором. Это приводит к наличию крови в рвоте, кашле и стуле, что многократно повышает заразность заболевания [4].
Как же трактовать частоту появления кровоизлияний? С точки зрения чистой статистики, одна десятая численности — небольшое количество, однако это потенциальные три сотни человек при многотысячной вспышке, подобной той, что была последней в ДРК на текущий момент, которые могут истекать кровью на улице, загрязнять предметы зараженной кровью и разносить инфекцию по округе. Слоняясь в умирающих деревнях, они могут неумышленно распространить вирус на людей, остановившихся с целью помочь и облегчить страдания кажущегося раненным измученного африканца. Инкубационный период болезни вполне может позволить таким туристам покинуть очаг эпидемии...
Как известно эпидемиологам и постоянным читателям «Биомолекулы», болезнь была впервые обнаружена и задокументирована в 1976 году в Южном Судане и Демократической Республике Конго. Первая же крупная вспышка заболевания в Западной Африке, которая охватила Гвинею, Сьерра-Леону и Либерию, произошла в 2013–2016 годах (рис. 4) и оказалась наиболее сложной и масштабной с момента описания заболевания. Согласно данным из «Исторического обзора вспышек лихорадки Эбола» [5], во время этой эпидемии погибло более одиннадцати тысяч человек только из-за невозможности введения своевременного карантина и отсутствия лекарственной терапии. С избранными переведенными главами этой работы и объединенной историей эпидемий эболавируса также можно познакомиться в исторической части статьи «Смертельная зараза: за что мы благодарны лихорадке Эбола и при чем тут „Спутник V“», также опубликованной на конкурсе «Био/мол/текст» в этом году [6].
Именно этот обзор привлек внимание и вызвал оправданное беспокойство нескольких групп эпидемиологов, в том числе американских, к опасности заболевания, возбудитель которого был быстро отнесен к первой группе патогенности.
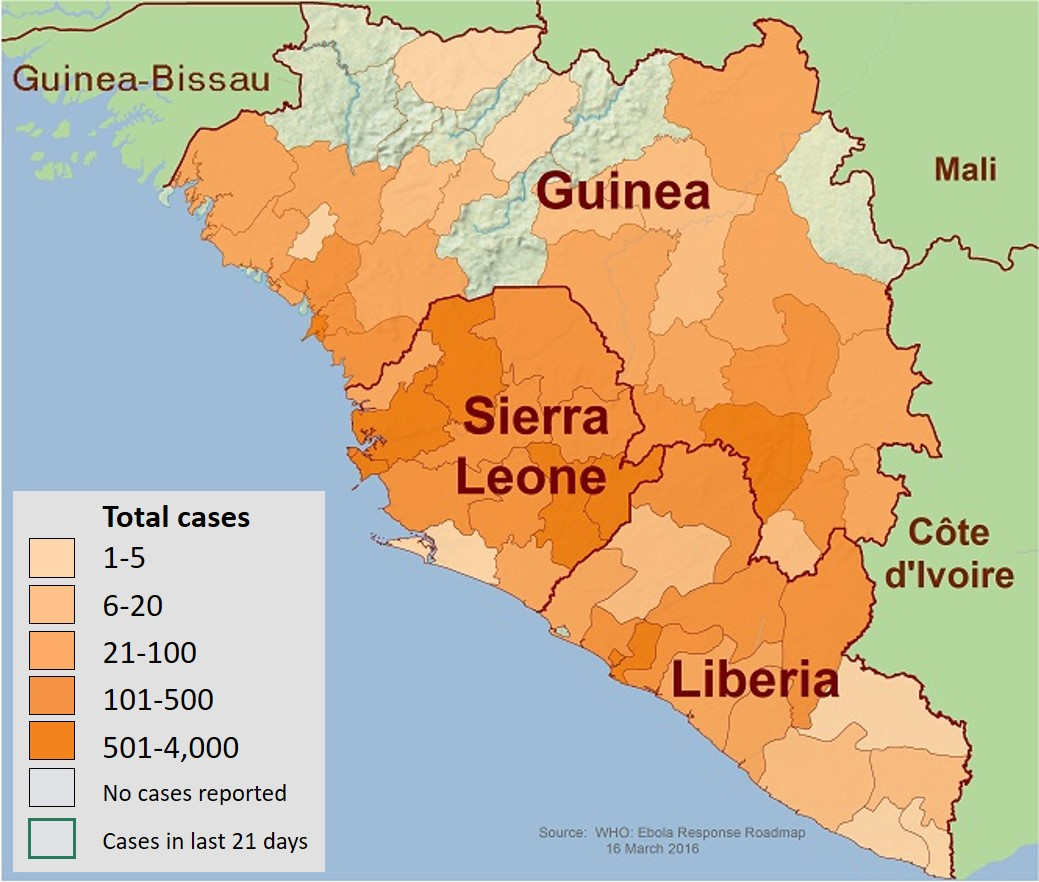
Рисунок 5. Карта распространения вируса Эбола во время вспышки в 2013–2016 годах.
Текущая обстановка в регионах распространения заболевания остается напряженной: вспышка 2018–2019 годов окончилась при поддержке экспериментальных вакцин как на основе модифицированной ДНК, содержащей гены нуклеопротеинов и гликопротеинов вируса Эболы, так и посредством наиболее свежих на тот момент разработок — векторных вакцин на основе рекомбинантных вирусов .
Подробнее о вакцинах от вируса Эболы, их принципах действия, истории создания и последних успехах ученых читайте в статье «Смертельная зараза: за что мы благодарны лихорадке Эбола и при чем тут „Спутник V“» [6]. Выборочно ознакомиться с принципом получения и механизмом действия векторных рекомбинантных вакцин можно в другой статье — «Уколы от Эболы» [7].
Параллельно с этим больным оказывалась симптоматическая медицинская помощь в полевых госпиталях и предоставление гуманитарной помощи для находящихся на карантине пострадавших стран. К несчастью, испытания и лечение больных сопровождались вооруженными нападениями на госпитали из-за продолжающейся гражданской войны в ДРК, что неоднократно подрывало миссию медиков и поиск эффективного лечения заболевания и тестирования противовирусных препаратов [8].
Что же такое Инмазеб?
«Инмазеб, также известный как REGN-EB3, представляет собой препарат из трех групп стабилизированных моноклональных антител человека, разработанный компанией „Регенерон Фармасьютикалс“ (США) для лечения геморрагической лихорадки Эбола», — сообщает Энтони Маркхэм, ведущий научный сотрудник Adis International Limited по направлению моноклональных антител, в своем отчете о получении разрешения на применение Инмазеба в терапевтическом лечении лихорадки Эбола от FDA [9].
Данный трехкомпонентный препарат состоит из натуральных человеческих специфических антител, которые взаимодействует с гликопротеинами вируса Эбола и блокируют его внедрение в клетки человека, что способствует снижению скорости репликации вирусных частиц и уменьшает тяжесть течения заболевания [10]. В сочетании с имеющимися протоколами лечения болезни, вызываемой вирусом Эбола, это значительно увеличивает эффективность терапии.
О потенциально успешном применении моноклональных антител сообщалось во время ранних клинических препарата ZMapp для лечения лихорадки Эбола [16], и хотя его эффективность не была полностью подтверждена, именно усилия создателей данного лекарственного средства и несколько спасенных жизней показали один из возможных путей борьбы с данной инфекцией. Так начались поиски эффективного типа антител для подавления или ослабления вируса с целью облегчения течения болезни и ее лечения.
Впервые препарат REGN-EB3 был применен в качестве экспериментального лечения во время вспышки заирского эболавируса в 2018 году как на взрослых пациентах, так и на детях параллельно с проведением третьей части клинических испытаний препарата [17]. Согласно данным предварительных исследований, рекомендуемая дозировка для каждого компонента препарата составила 50 мг/кг, однако по завершении вспышки и сбора данных рекомендуемая дозировка была поднята до 100 мг/кг. Препарат разводят перед применением и однократно вводят пациенту внутривенно [18].
Научная сторона исследований
Препарат REGN-EB3, состоящий из антител атолтивимаб (REGN3470), мафтивимаб (REGN3479) и одесивимаб (REGN3471), показал высокое сродство к гликопротеинам вируса Эболы как in silico — при моделировании его активности путем молекулярного докинга, — так и in vivo — при испытании на животных и на людях. Данные электронной микроскопии показали, что при одновременном применении трех типов антител, их связывание с гликопротеином происходит на различных участках, что полностью изменяет свойства белка [18].
В ходе клинических испытаний препарата, проведенных во время вспышки 2018–2019 годов в ДРК, было обнаружено снижение средней летальности с 50 до 27% и уменьшение общей вирулентности патогена в ходе мутаций в естественной среде обитания, что, несомненно, показывает эффективность препарата в лечении заболевания, однако все еще предполагает комбинированную терапию для достижения наилучшего результата с минимальным количеством летальных исходов.
Обнаруженные во время клинических испытаний побочные эффекты от применения препарата REGN-EB3 включали в себя лихорадку, озноб, тахикардию, учащенное дыхание и другие симптомы (рис. 6), характерные для геморрагической лихорадки Эбола средней тяжести. Полное описание свойств и особенностей представлено на странице 177 опубликованного отчета [9].
Дальнейшие планы
Согласно данным Национальной библиотеки медицины США, протокол клинических испытаний NCT03576690 был одобрен к проведению 14 октября 2020 года, и по настоящее время проводится проверка препарата для лечения болезни, вызываемой заирским эболавирусом, в рамках расширенных клинических испытаний. К исследованиям допускаются люди всех возрастов и полов, которые имеют положительный результат ПЦР-теста и не обладают противопоказаниями к применению представленного протокола лечения геморрагической лихорадки Эбола. Также стоит отметить разрешение от Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США на включение в перечень допущенных до тестирования субъектов беременных женщин, инфицированных вирусом Эбола.
Несмотря на наличие вакцины от болезни, вызываемой вирусом Эбола у многих стран мира, считается, что ей необходимы дополнительные клинические испытания на людях. Параллельно с этим проводятся расширенные клинические исследования препарата моноклональных антител для терапии больных людей. Всё вместе это отражает стремление ученых к созданию не только средств для предотвращения поражения людей этим смертельно опасным вирусом, но и способов лечения для лиц в зоне риска, а именно — жителей Западной Африки, находящихся далеко от пунктов медицинской помощи. Создание единого комплекса мер по противодействию лихорадке Эбола может стать одним из ключей, необходимых жителям африканских республик для дальнейшего развития в неблагоприятных условиях жизни.
Литература
- Mandary, Masomian, Poh. (2019). Impact of RNA Virus Evolution on Quasispecies Formation and Virulence. IJMS. 20, 4657;
- Charles N. Haas. (2014). On the Quarantine Period for Ebola Virus. PLoS Curr;
- 12 методов в картинках: полимеразная цепная реакция;
- Derek Gatherer. (2014). The 2014 Ebola virus disease outbreak in West Africa. Journal of General Virology. 95, 1619-1624;
- Kasangye Kangoy Aurelie, Mutangala Muloye Guy, Ngoyi Fuamba Bona, Kaya Mulumbati Charles, Avevor Patrick Mawupemor, Li Shixue. (2018). A Historical Review of Ebola Outbreaks. Advances in Ebola Control;
- Смертельная зараза: за что мы благодарны лихорадке Эбола и при чем тут «Спутник V»;
- Уколы от Эболы;
- Amy Maxmen. (2019). Science under fire: Ebola researchers fight to test drugs and vaccines in a war zone. Nature. 572, 16-17;
- Anthony Markham. (2021). REGN-EB3: First Approval. Drugs. 81, 175-178;
- Kristen E Pascal, Drew Dudgeon, John C Trefry, Manu Anantpadma, Yasuteru Sakurai, et. al.. (2018). Development of Clinical-Stage Human Monoclonal Antibodies That Treat Advanced Ebola Virus Disease in Nonhuman Primates. The Journal of Infectious Diseases. 218, S612-S626;
- Моноклональные антитела;
- Открытие моноклональных антител;
- Murphy K., Travers P., Walport M. Appendix 1: Immunologists’ Toolbox. In.: Janeway’s Immunobiology, 7th edition. Garland Science, 2008. — P. 735;
- Антитело: лучший способ распознать чужого;
- Краткая история открытия и применения антител;
- Вирус Эбола и макака резус: получено новое эффективное лекарство;
- Возвращение домой: вирус Эбола снова атакует ДРК;
- Sumathi Sivapalasingam, Mohamed Kamal, Rabih Slim, Romana Hosain, Weiping Shao, et. al.. (2018). Safety, pharmacokinetics, and immunogenicity of a co-formulated cocktail of three human monoclonal antibodies targeting Ebola virus glycoprotein in healthy adults: a randomised, first-in-human phase 1 study. The Lancet Infectious Diseases. 18, 884-893;
- Sabue Mulangu, Lori E. Dodd, Richard T. Davey, Olivier Tshiani Mbaya, Michael Proschan, et. al.. (2019). A Randomized, Controlled Trial of Ebola Virus Disease Therapeutics. N Engl J Med. 381, 2293-2303.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚





