
История болезни Паркинсона: от дрожи к дофамину
01 апреля 2026
История болезни Паркинсона: от дрожи к дофамину
- 298
- 0
- 2
Рисунок в полном размере.
рисунок авторов
-
Авторы
-
Редакторы
Комикс на конкурс «Био/Мол/Текст»: Болезнь Паркинсона — нейродегенеративное заболевание, находящееся на втором месте по распространенности после болезни Альцгеймера. Болезнь Паркинсона в первую очередь характеризуется двигательными нарушениями, в частности, тремором рук. Развитие и прогрессирование болезни связано с гибелью дофаминовых нейронов в черной субстанции. В этом комиксе описана история изучения этого заболевания, а также современные представления о его патогенезе.
Конкурс «Био/Мол/Текст»-2025/2026
Эта работа опубликована в номинации «Наглядно о ненаглядном» конкурса «Био/Мол/Текст»-2025/2026.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Болезнь Паркинсона (БП) была впервые описана как неврологический синдром в 1817 году английским врачом Джеймсом Паркинсоном в работе «эссе о дрожательном параличе» (An essay on the shaking palsy) [1], [2]. Хотя упоминания об этом заболевании встречаются еще раньше: например, Франциск Сильвий писал о треморе покоя (непроизвольное дрожание конечностей в покое, чаще всего рук), а Франсуа Босье де Лакруа описал изменение походки, что тоже является яркой чертой БП [3]. Однако именно Джеймс Паркинсон впервые дал описание проявлений БП как синдрому с рядом отличительных признаков, вследствие чего ввел название «дрожательный паралич» (Paralysis agitans на латинском). Уже в то время Паркинсон хорошо осознавал неполноту своего трактата, в связи с чем в предисловии он указывал на замену аналогией анатомического исследования, «единственного надежного основания для патологических знаний» [2].

Рисунок 1. Джеймс Паркинсон (11.04.1755–1824) и Жан-Мартен Шарко (29.11.1825–16.08.1893). Изображение различных видов тремора, выполненное Шарко (1887). Отрезок AB обозначает состояние покоя, BC — состояние активности. Верхняя схема иллюстрирует тремор при рассеянном склерозе; средняя и нижняя — при болезни Паркинсона [5].
рисунок авторов
Важный вклад в исследование БП внес французский врач-психиатр и невролог Жан-Мартен Шарко, который описал спектр клинических проявлений этого заболевания. Он также был первым, кто предложил использовать термин «болезнь Паркинсона», отказавшись от более раннего «дрожательного паралича», поскольку признал, что у пациентов с БП не всегда заметна слабость, а также необязательно присутствует выраженный тремор [4]. Кроме того, Шарко привел отличия БП от рассеянного склероза, так как у подобных пациентов тремор развивается при движениях и усугубляется при приложении усилий, а у людей с БП тремор наблюдается в покое и во время движений, но он не становится сильнее в период активности (то есть при приложении усилий) [4], [5].
Шарко изучил эссе Джеймса Паркинсона, описав выделенные последним особенности, и проанализировал 4 ключевых симптома БП: тремор, гипокинезию, нарушение осанки и походки. Несмотря на признание Шарко тремора как одного из основных проявлений БП, он настаивал на необязательности его проявления для постановки диагноза. Он признал, что у большинства пациентов наблюдаются как ригидность, так и тремор, и разделил варианты паркинсонизма на две основные категории: случаи с тремором без ригидности (треморная форма) и случаи с ригидностью без тремора (ригидная/акинетическая) [4], [5].
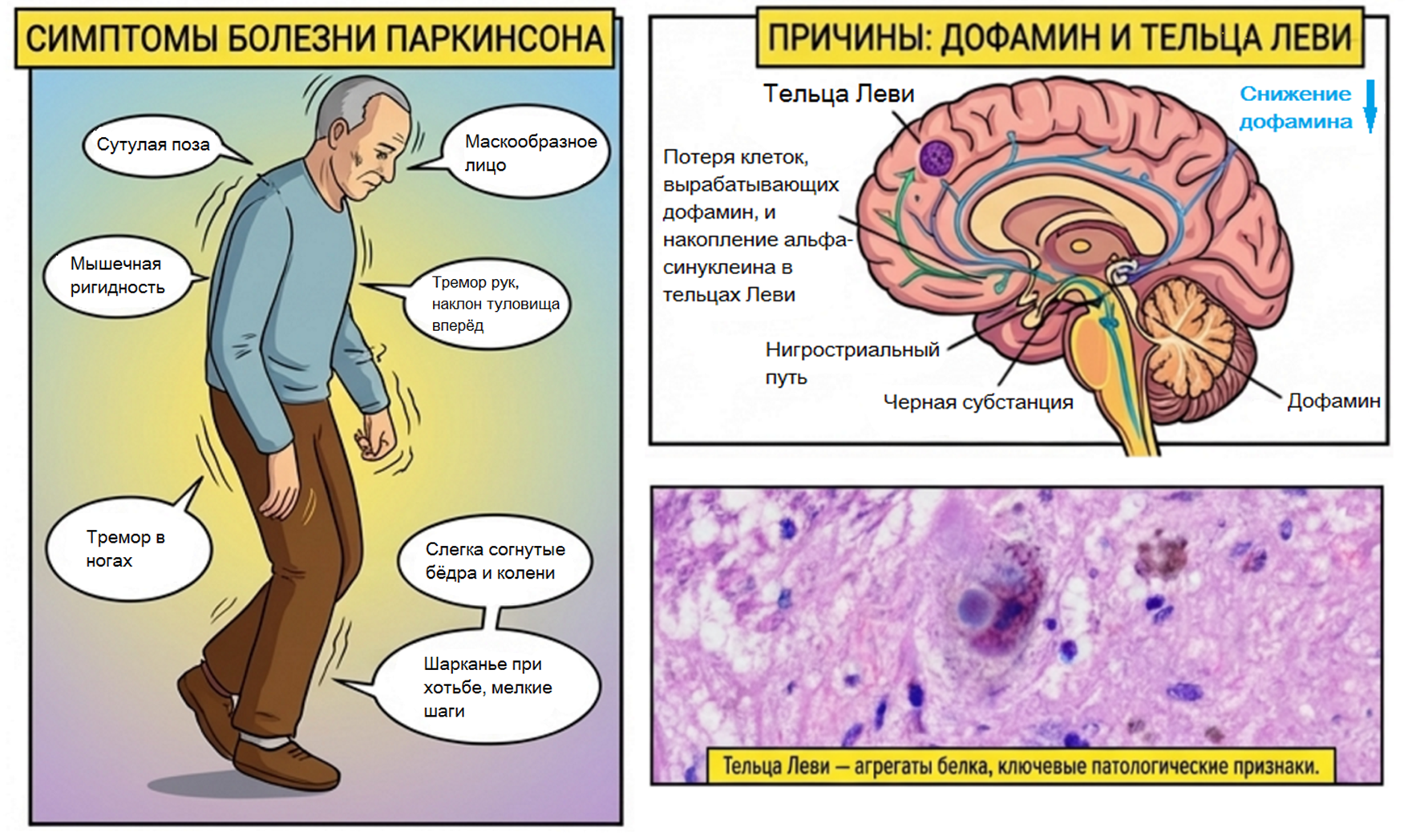
Рисунок 2. Двигательные симптомы болезни Паркинсона, дофаминовые пути и проекции в головном мозге, изображение телец Леви.
рисунок авторов
Причины возникновения БП и патологические процессы, лежащие в основе заболевания, оставались непонятными до первой половины ХХ века. В 1912 году Фридрих Леви описывал характерные включения в головном мозге у пациентов с БП. Далее Константин Третьяков опубликовал в 1919 году работу, в которой он изучил мозг девяти пациентов с БП: он первым заявил о поражении структуры головного мозга под названием черная субстанция (substantia nigra). Третьяков связывал уменьшение количества пигментированных клеток в черной субстанции с нарушением мышечного тонуса при БП (рис. 2, панель справа) [6]. Позже, в 1923 году, Леви обнаружил, что в большинстве атрофированных клеток наблюдались скопления фибрилл, а также была замечена обширная гибель клеток в бледном шаре и дорсальном ядре блуждающего нерва [6]. В настоящее время благодаря исследованиям Третьякова и Леви данные включения признаны одним из основных патоморфологических признаков БП и носят название тельца Леви [7] (рисунок 2, панель снизу).
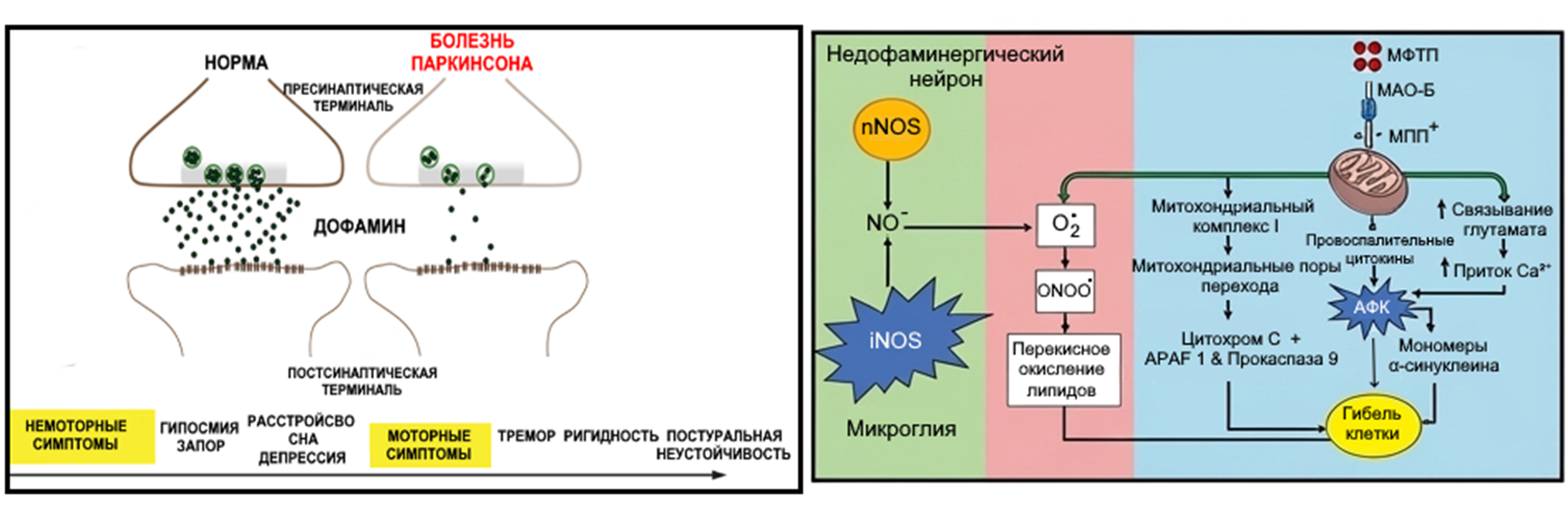
Рисунок 3. Снижение количества дофамина коррелирует с развитием немоторных и моторных нарушений, этиологические факторы развития болезни Паркинсона (в качестве примера триггера гибели клеток приведен нейротоксин 1-метил-4-фенил-1,2,3,6-тетрагидропиридин (МФТП).
рисунок авторов
Другим эпохальным открытием в понимании патогенеза БП, сделанного в 60-е годы 20 века Олегом Хорникевичем и Гербертом Эрингером, стало обнаружение значительно низких уровней дофамина в стриатуме (структура головного мозга, также известная как полосатое тело) у пациентов с БП и постэнцефалическим паркинсонизмом [8]. Позднее, в 1973 году, этими же учеными было проведено посмертное исследование пациентов с БП, показавшее серьезное истощение дофамина в стриатуме (более 80%) и демонстрирующее корреляцию между уровнем дофамина и количеством клеток черной субстанции [9]. На основании этих данных была предположена теория экспоненциально прогрессирующего развития БП с коротким доклиническим периодом. При этом характерные симптомы БП проявлялись при снижении количества дофаминергических нейронов в черной субстанции на 68% и более от нормы [10].
Несмотря на открытие дофаминового дефицита при БП и нарушениях в работе базальных ганглиев, все еще мало было известно об этиопатогенезе БП. Однако вещество 1-метил-фенил-1,2,3,6-тетрагидропиридин (МФТП) дало много информации о паркинсонизме, потенциальной патогенной роли токсинов и окислительного стресса, а также заложило начало моделирования БП на животных. В 1979 году Дэвис и его коллеги [11] описали клинические и патологические особенности первоначального случая БП, обусловленной МФТП у 23-летнего мужчины, злоупотреблявшего психоактивными веществами (МФТП был побочным продуктом их синтеза). Сейчас этот нейротоксин широко используется в экспериментах по моделированию БП у животных [12].
Механизм действия нейротоксина МФТП можно кратко представить следующим образом [13] (рисунок 3, панель справа): в мозге фермент МАО Б (моноаминоксидаза-B) превращает неактивный МФТП в его активный метаболит — МПП⁺ (1-метил-4-фенилпиридин). МПП⁺ имеет сходную с дофамином структуру, поэтому он проходит через DAT (транспортер дофамина) и избирательно накапливается именно в дофаминовых нейронах. Внутри нейрона МПП⁺ попадает в митохондрии — «энергетические станции» клетки. Его главная мишень — митохондриальный комплекс I (первый комплекс дыхательной цепи). В результате блокируется производство молекул АТФ, и клетки начинают «голодать». Ингибирование комплекса II приводит к резкому увеличению активных форм кислорода (АФК, O₂•). Одновременно активируются клетки микроглии (иммунные клетки мозга). Они производят провоспалительные цитокины (сигналы «тревоги») и iNOS (индуцибельную синтазу оксида азота), которая генерирует много NO. NO и O₂• вступают в реакцию, образуя мощный окислитель — пероксинитрит (ONOO•). ONOO• вызывает перекисное окисление липидов (разрушение мембран клетки). Далее запускается апоптоз (клеточное самоубийство). Повреждение митохондрий приводит к открытию митохондриальных пор перехода. Через эти поры из митохондрий выходит цитохром C, который связывается с белком APAF-1 и формой прокаспазы-9, образуя «апоптосом». Активированная каспаза-9 запускает каскад других каспаз — ферментов, которые «разрезают» клетку изнутри, приводя к ее гибели. Избыток глутамата приводит к притоку ионов кальция (Ca²⁺), что еще сильнее перегружает митохондрии. Образовавшийся окислительный стресс способствует агрегации токсичного белка α-синуклеина в токсичные олигомеры, которые сами по себе повреждают клетку.
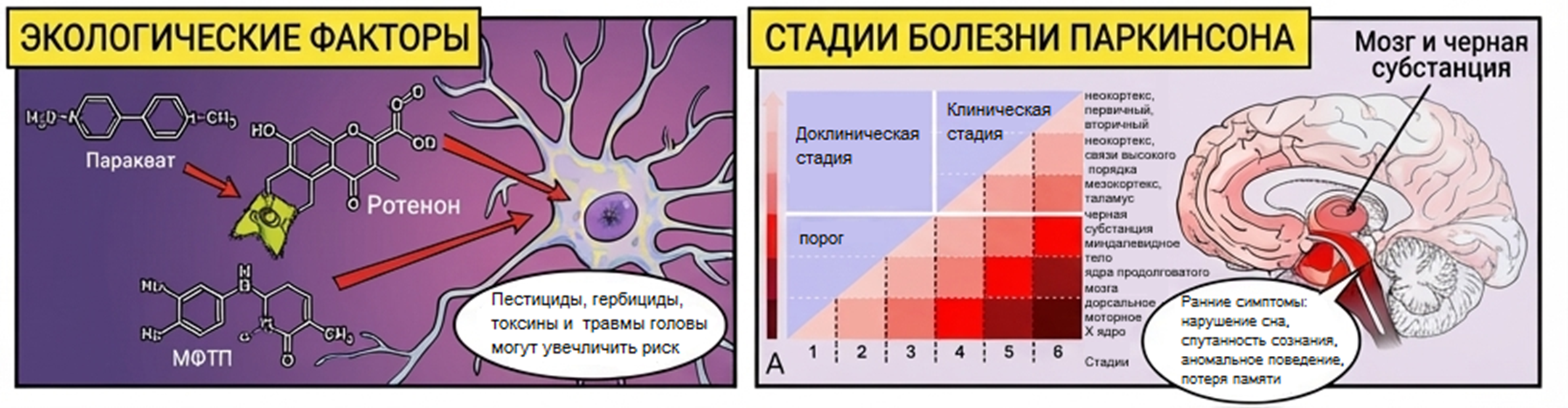
Рисунок 4. Экологические факторы риска развития и ее стадии болезни Паркинсона (по Брааку).
рисунок авторов
В 90-х годах 20 века несколько исследователей из разных географических регионов (Швеция, Италия и Тайвань) сообщили о повышенном риске развития БП в результате воздействия пестицидов и гербицидов [14], [15]. В настоящее время хорошо известно два вещества из этой сферы использования, а именно — паракват и ротененон, которые обладают общими с МФТП свойствами: они селективно ингибируют комплекс I дыхательной цепи митохондрий (рис. 4, панель слева), что приводит к окислительному стрессу и гибели нейронов. Кроме того, еще в 19 веке были описаны неврологические проявления при воздействии марганца.
Немецким исследователем Брааком была выдвинута гипотеза [16], согласно которой ранние патологические изменения при БП происходят в продолговатом мозге и обонятельной луковице (стадии 1 и 2), прежде чем перейти на вышележащие структуры головного мозга — к черной субстанции и среднему мозгу (стадии 3 и 4), причем на этих стадиях, уже наиболее вероятно проявляются клинические симптомы и классические признаки БП, а на более поздних стадиях (5 и 6), поражаются корковые области головного мозга. Вышеописанная концепция позволила выделить домоторную форму БП, проявляющуюся прежде всего немоторными нарушениями (депрессия, нарушение сна, диспептические расстройства и др.) (рис. 4, панель справа).
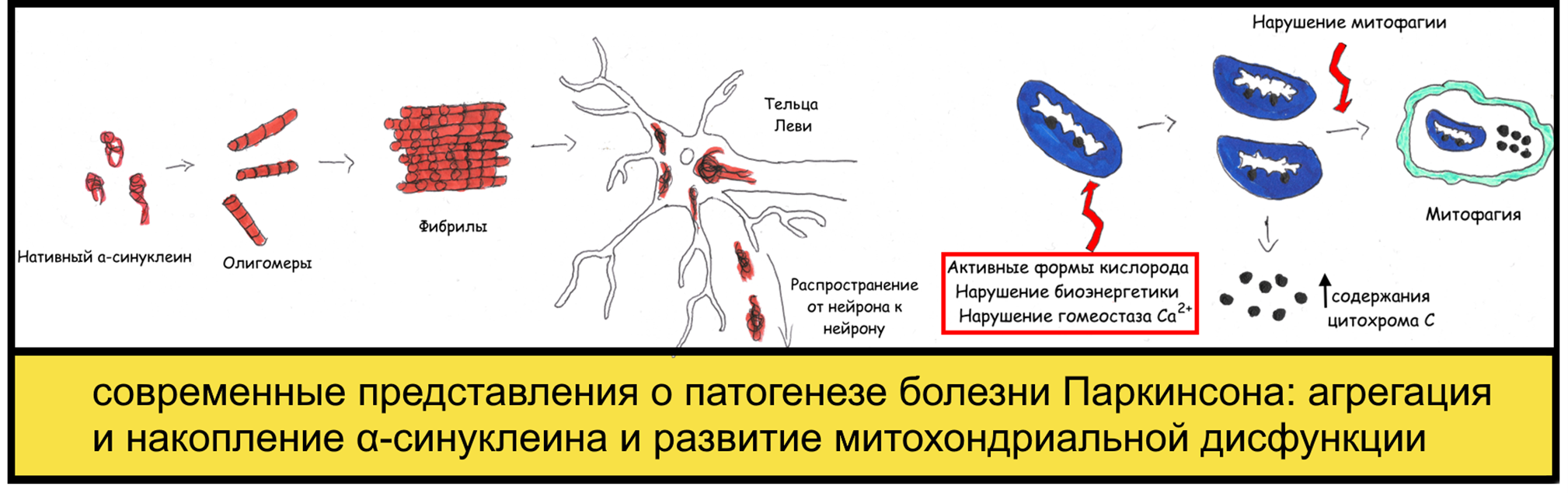
Рисунок 5. Современные представления о патогенезе болезни Паркинсона: показан процесс агрегации и накопления токсичного белка α-синуклеина с его дальнейшим распространением между нейронами, а также процесс развития митохондриальной дисфукнции, выражающейся в нарушении процесса митофагии и энергетическом дисбалансе.
рисунок авторов
В современной медицине имеется более глубокое представление о патогенезе БП, расширившееся за счет многочисленных исследований в период с 70-х годов 20 века по нынешнее время. Независимо от лежащей в основе этиологии (экологические, генетические или другие факторы риска), последовательно сообщалось о нескольких ключевых явлениях и отличительных признаках, обнаруженных на молекулярном уровне при исследовании биопсийных материалов пациентов с БП, а также при проведении экспериментов с линиями клеток млекопитающих in vitro, органоидами человеческого мозга и животными моделями. К подобным явлениям относятся: неправильное сворачивание и агрегация токсичного белка α-синуклеина (более подробно о нем и его роли при БП можно прочитать в статье «Биомолекулы» [17]) c последующим распространением его агрегатов к другим нейронам (рис. 5, панель слева), нарушение работы митохондрий (рис. 5, панель справа) и клиренса белка (с участием ключевых убиквитин-протеасомных и аутофагия-лизосомальных систем; об этом также можно более подробно прочитать в статье «Биомолекулы» [18]). Эти основные молекулярные и клеточные признаки часто связаны со многими другими взаимосвязанными явлениями, включающими в себя нарушение везикулярного транспорта, потерю целостности микротрубочек, нейрональную эксайтотоксичность, нарушение трофических факторов, нарушение регуляции метаболических путей железа и нарушение функционирования эндоплазматического ретикулума. По существу, все эти механизмы потенциально способствуют запрограммированной гибели клеток (апоптозу) или некрозу. Поскольку клеточные процессы динамичны, а нейродегенерация происходит в течение длительного периода повреждений/стрессовых воздействий и при задействовании различных компенсаторных механизмов, невозможно с какой-либо уверенностью определить, работают ли эти пути независимо или сходятся к единому пути к гибели нейронов. Более вероятно, что различные патофизиологические процессы пересекаются друг с другом, что приводит к затяжному каскаду различных нарушений и, в конечном счете, необратимому повреждению клеток.
Литература
- Kai Yang, Zhengqi Wu, Jie Long, Wenxin Li, Xi Wang, et. al.. (2023). White matter changes in Parkinson’s disease. npj Parkinsons Dis.. 9;
- IM Donaldson. (2015). James Parkinson’s Essay on the Shaking Palsy. J R Coll Physicians Edinb. 45, 84-86;
- C. G. Goetz. (2011). The History of Parkinson's Disease: Early Clinical Descriptions and Neurological Therapies. Cold Spring Harbor Perspectives in Medicine. 1, a008862-a008862;
- O. Walusinski. (2018). Jean-Martin Charcot and Parkinson's disease: Teaching and teaching materials. Revue Neurologique. 174, 491-505;
- Factor S. A., Weiner W. J. Parkinson's disease: diagnosis and clinical management. Demos Medical Publishing, 2007. — 1024 p.;
- J M S PEARCE. (2001). The Lewy body. Journal of Neurology, Neurosurgery & Psychiatry. 71, 214-214;
- Воронков Д., Сальков В., Ануфриев П., Худоерков Р. (2018). Тельца Леви при болезни Паркинсона (гистологическое, иммуногистохимическое и интерферометрическое исследование). Архив патологии. 80, 9–13;
- H. Ehringer, O. Hornykiewicz. (1960). Verteilung Von Noradrenalin Und Dopamin (3-Hydroxytyramin) Im Gehirn Des Menschen Und Ihr Verhalten Bei Erkrankungen Des Extrapyramidalen Systems. Klin Wochenschr. 38, 1236-1239;
- H. Bernheimer, W. Birkmayer, O. Hornykiewicz, K. Jellinger, F. Seitelberger. (1973). Brain dopamine and the syndromes of Parkinson and Huntington Clinical, morphological and neurochemical correlations. Journal of the Neurological Sciences. 20, 415-455;
- JULIAN M. FEARNLEY, ANDREW J. LEES. (1991). AGEING AND PARKINSON'S DISEASE: SUBSTANTIA NIGRA REGIONAL SELECTIVITY. Brain. 114, 2283-2301;
- Glenn C. Davis, Adrian C. Williams, Sanford P. Markey, Michael H. Ebert, Eric D. Caine, et. al.. (1979). Chronic parkinsonism secondary to intravenous injection of meperidine analogues. Psychiatry Research. 1, 249-254;
- K. Tieu. (2011). A Guide to Neurotoxic Animal Models of Parkinson's Disease. Cold Spring Harbor Perspectives in Medicine. 1, a009316-a009316;
- Wasim Akram, Vishal Kumar, Swamita Arora, Sanjar Alam, Rohit Kumar. (2022). Neurotoxin models and treatments of Parkinson’s disease. ijhs. 10316-10341;
- H. H. Liou, M. C. Tsai, C. J. Chen, J. S. Jeng, Y. C. Chang, et. al.. (1997). Environmental risk factors and Parkinson's disease. Neurology. 48, 1583-1588;
- Smargiassi A., Mutti A., De Rosa A., De Palma G., Negrotti A., Calzetti S. (1998). A case-control study of occupational and environmental risk factors for Parkinson's disease in the Emilia-Romagna region of Italy. Neurotoxicology. 19, 709–712;
- Heiko Braak, Estifanos Ghebremedhin, Udo Rüb, Hansjürgen Bratzke, Kelly Del Tredici. (2004). Stages in the development of Parkinson’s disease-related pathology. Cell Tissue Res. 318, 121-134;
- Белок альфа-синуклеин — важный участник проявления болезни Паркинсона?;
- Болезнь Паркинсона: что изучать? как изучать?.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚





