Кошачий Альцгеймер — как кошкам изменяет память
14 февраля 2023
Кошачий Альцгеймер — как кошкам изменяет память
- 5086
- 0
- 6
Синдром когнитивной дисфункции — нарушение работы центральной нервной системы кошек.
Рисунок в полном размере.
сайты pikpng, cdn.vanderbilt
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Только ли людей донимают нейродегенеративные заболевания? Оказывается, нет. У всякого животного к старости нервная система все хуже и хуже выполняет свои функции. Это касается и домашних животных. В этой статье мы рассмотрим синдром когнитивной дисфункции у кошек.
Конкурс «Био/Мол/Текст»-2022/2023
 Эта статья опубликована в номинации «Нейробиология» конкурса «Био/Мол/Текст»-2022/2023 и заслужила приз зрительских симпатий.
Эта статья опубликована в номинации «Нейробиология» конкурса «Био/Мол/Текст»-2022/2023 и заслужила приз зрительских симпатий.
Партнер номинации — компания «Сесана»: — один из ведущих поставщиков оборудования и реагентов для полного цикла научного исследования.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Мой добрый кот, мой кот ученый
Печальный подавляет вздох
И лапкой белой и точеной,
Сердясь, вычесывает блох.
Николай Гумилев, «Маркиз де Карабас»
Прогрессирующая гибель нервных клеток — нейродегенерация — общая черта нейродегенеративных заболеваний. К таким заболеваниям относятся болезнь Альцгеймера, болезнь Паркинсона и др. Нейродегенерация может приводить к деменции — приобретенному слабоумию. Нейродегенеративные заболевания могут настигнуть человека в любом возрасте, но чаще всего ими страдают пожилые люди.
На первых этапах развития эти заболевания почти не проявляют себя. Заметными они становятся уже на поздних стадиях. При деменции происходит прогрессирующее снижение когнитивных функций (внимания, памяти, интеллекта). При таком раскладе больные утрачивают социально-бытовые навыки. Многих из них, в конечном счете, приковывает к кровати [1].
Люди — млекопитающие. Значит, и у остальных представителей этого класса встречаются подобные нарушения нервной системы. В качестве примеров таких животных можно привести обезьян, белого медведя, собаку и кошку [2].
По опросам, кошка — самое популярное домашнее животное в России. Не зря говорят, что домашние животные похожи на своих хозяев. У людей и их питомцев многие болезни протекают схожим образом. Например, с возрастом коты и кошки также страдают деменцией. В это статье я постарался пролить свет на тему нейродегенеративных отклонений у кошек.
Не всё коту масленица — и у кошек бывает деменция
Некоторые домашние кошки могут дожить до 20 лет. Продолжительность кошачьей жизни зависит от диеты, здравоохранения и окружающей среды. Кастрированные коты и стерилизованные кошки, как правило, живут дольше, потому что кастрация и стерилизация предотвращают репродуктивные заболевания, и такие коты и кошки менее склонны к бродяжничеству. Чем старше животные, тем выше риск нейродегенеративных заболеваний у них. Практически как у человека, тем более нервная система у кошек и людей устроена аналогично (рис. 1).
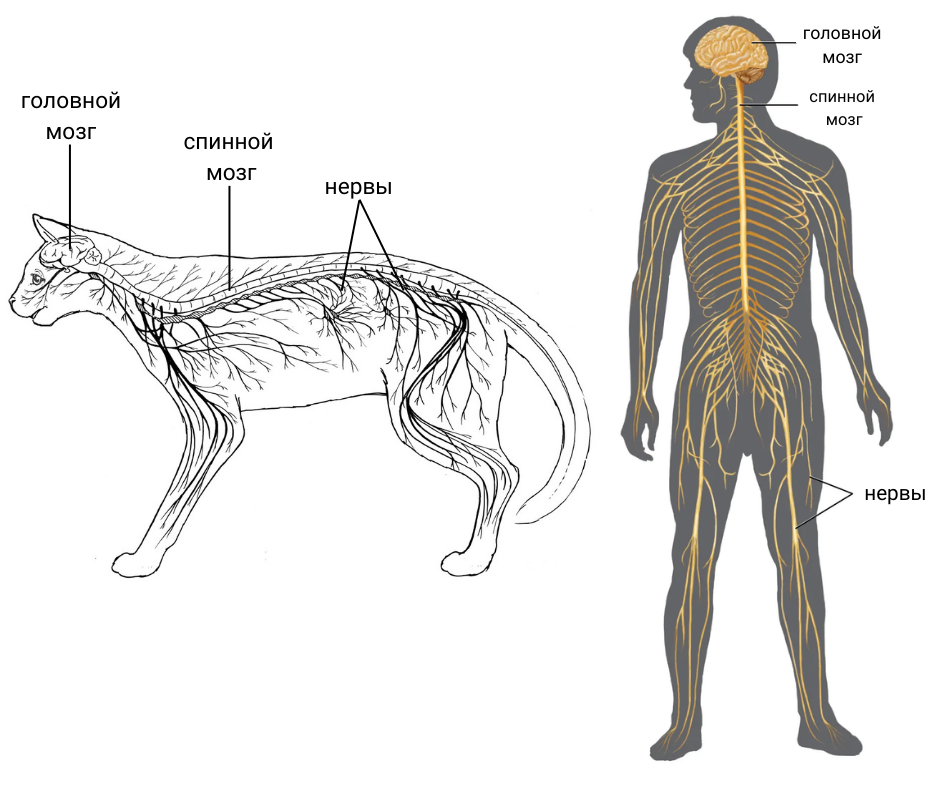
Рисунок 1. Общий план нервной системы кошки и человека.
Похожее на болезнь Альцгеймера нарушение центральной нервной системы у кошек (и других животных) носит название «синдрома когнитивной дисфункции» (СКД). У страдающих СКД кошек проявляются поведенческие аномалии. Животные чрезмерно мяукают. У них меняется взаимодействие с хозяевами: они могут показывать повышенную привязанность и внимание. Изменения затрагивают также циклы сна и бодрствования. Заметна пространственная дезориентация таких животных — кошки бродят кругами (см. видео). Естественно, болезнь влияет и на активность кошек, у них появляется тревожность, страдает память и теряется способность к обучению [3].
Видео 1. Кот с деменцией ходит кругами — признак дезориентации в пространстве при синдроме когнитивной дисфункции.
Болезнь Альцгеймера у человека характеризуется накоплением β-амилоидных бляшек и нейрофибриллярных клубков из гиперфосфорилированного тау-белка в коре головного мозга [4]. Похожая ситуация наблюдается и при синдроме когнитивной дисфункции у кошек [3], [5].
У 28% домашних кошек в возрасте от 11 до 14 лет развивается по крайней мере одна поведенческая проблема, связанная с СКД. А после 15 лет такие изменения наблюдаются более чем у половины кошек [6].
Основные признаки СКД обобщает английская аббревиатура DISHAAL (рис. 2):
- Disorientation — дезориентация (кошка застревает, не может обойти объекты, бессмысленно смотрит на пол или стены, с трудом узнает знакомых людей или других домашних животных, бросает и не может найти еду, у кошки проявляется ослабленная или, наоборот, слишком бурная реакция на раздражители);
- alterations in Interactions — изменения во взаимодействии между домашним животным и его хозяином или другими домашними животными (кошка менее общительная, чем прежде, избегает контактов с людьми и другими животными);
- alterations in the Sleep-wake cycle — изменения в цикле сна—бодрствования (кошка долго спит днем, плохо спит ночью);
- House-soiling — беспорядок в доме из-за кошки (кошка справляют нужду в местах, не предназначенных для этого, хотя она была приучена к лотку);
- alterations in Activity levels — изменение уровня активности (кошка бесцельно бродит, облизывает хозяев или предметы обихода, не хочет больше играть, заботиться о себе, имеет пониженный или, наоборот, повышенный аппетит);
- Anxiety — Беспокойство (кошка тревожна, мяукает часто и своеобразно);
- Learning and memory — проблемы с обучением и памятью (кошка с трудом обучается и выполняет команды, — хотя кошачьи и без особых когнитивных нарушений слабо обучаются командам) [7].
Другие ученые предлагают другую аббревиатуру — VISHDAAL. Они выделяют вокализацию (Vocalisation) как отдельный признак синдрома когнитивной дисфункции у домашних животных [3].
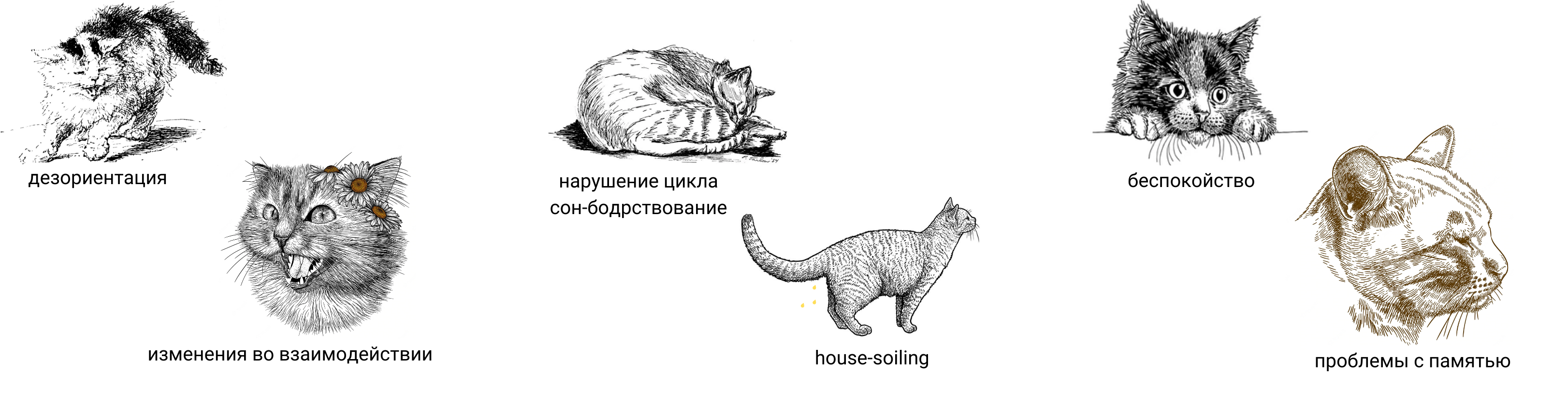
Рисунок 2. Основные признаки синдрома когнитивной дисфункции у кошек.
коллаж на основе gutenberg.org, freepik.com, etsystatic.com, dreamstime.com, shutterstock.com, freepik.com
С возрастом мозг претерпевает ряд анатомических и физиологических изменений. Эти изменения включают постепенную атрофию коры головного мозга и базальных ганглиев, локальную потерю нейронов, увеличенный размер желудочков, сосудистые и периваскулярные изменения (изменения вокруг кровеносных сосудов), накопление липофусцина, β-амилоида и гиперфосфорилирование тау-белка.
От каждого по способностям, каждому по потребностям — когнитивная дисфункция охватывает многие районы мозга
Анатомические и физиологические изменения затрагивают разные части головного мозга кошки (рис. 3). Посмотрим, что именно меняется при СКД у кошек и к каким проблемам это приводит. Сначала рассмотрим изменения, касающиеся конкретных анатомических структур головного мозга.
Мозжечок — основная структура заднего мозга позвоночных, отвечающая за координацию движений и регуляцию равновесия и мышечного тонуса. Возрастные изменения больше всего затрагивают молекулярный слой мозжечка животных. У старых кошек в мозжечке клеток Пуркинье и других нейронов меньше, чем в мозжечке здоровых. Это приводит к дезориентации животных, потере координации движений [3].
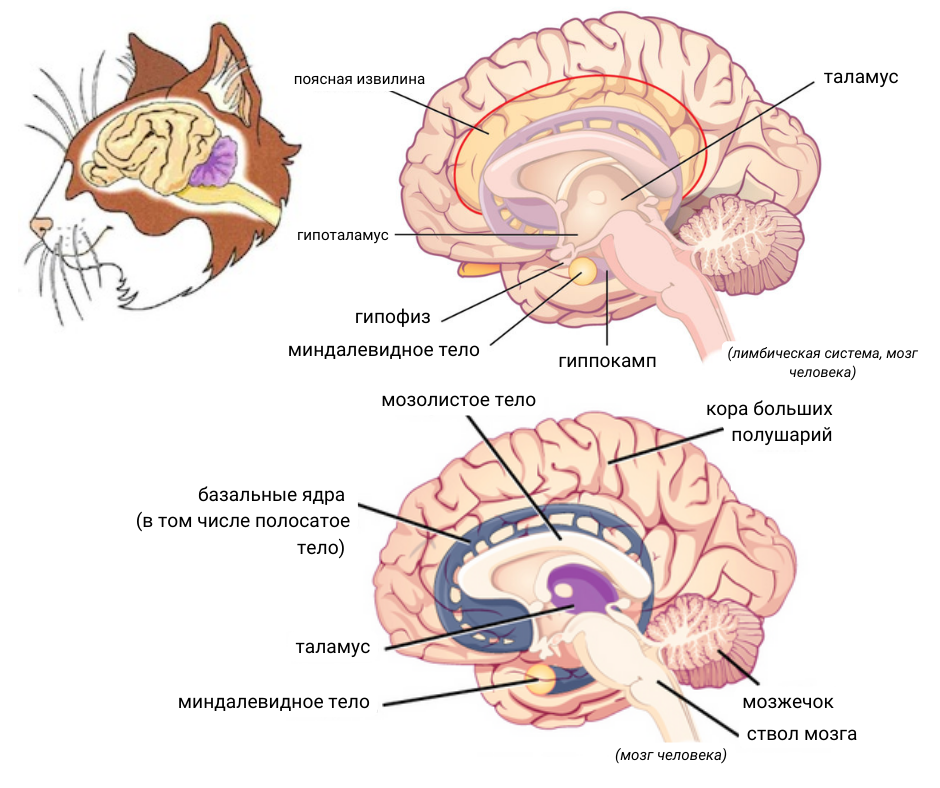
Рисунок 3. Головной мозг кошки и человека. Здесь приведен разрез головного мозга человека, чтобы показать расположение структур мозга, имеющихся у кошки. Кошки и люди — млекопитающие, их головной мозг устроен практически одинаково.
Хвостатое ядро, входящее в состав полосатого тела, выполняет моторные функции, отвечает за процедурное и ассоциативное обучение и ингибиторный контроль (самоконтроль). У кошек в возрасте 6–7 лет появляются изменения в хвостатом ядре. Происходит потеря нейронов и снижение количества синапсов. Считается, что это вызывает нарушения двигательной функции и неспособность привыкнуть к повторяющимся раздражителям у старых кошек, из-за чего они могут пугаться обычных шумов [3].
Гиппокамп, отвечающий за консолидацию памяти, также страдает при СКД. У кошек старше 14 лет наблюдается тяжелая потеря нейронов гиппокампа. В пораженных нервных клетках присутствуют β-амилоидные бляшки и нейрофибриллярные клубки из гиперфосфорилированного тау-белка [3].
СКД затрагивает также различные системы нейромедиаторов, работающие в головном мозге. Голубое пятно, многие из нейронов которого используют норадреналин в качестве нейромедиатора, отвечает за физиологическую реакцию на напряжение и тревогу. У кошек в возрасте 15–18 лет наблюдается разрушение миелиновых оболочек аксонов, уменьшение размера холинергических нейронов и длины дендритов в голубом пятне. Эти аномалии могут вызывать изменения в цикле сон—бодрствование у старых кошек [3].
Другая система нейромедиаторов, страдающая при СКД, — ацетилхолиновая. Совокупность нейронов, секретирующих ацетилхолин в качестве нейромедиатора, называется холинергической системой. Холинергическая система регулирует различные аспекты работы головного мозга, включая сенсорную обработку, внимание, сон и возбуждение, путем модуляции нервной активности через ацетилхолиновые рецепторы [8]. Ацетилхолин участвует в передаче импульсов в разных отделах мозга. Изменения в обмене ацетилхолина приводят к серьезному нарушению функций мозга. Недостаток этого нейромедиатора во многом определяет клиническую картину болезни Альцгеймера.
Перейдем к рассмотрению признаков патологии, не привязанных к конкретной структуре или системе, а проявляющихся повсеместно в головном мозге при СКД.
Бляшки, которые обнаруживают при нейродегенеративных заболеваниях, сформированы преимущественно β-амилоидом. Этот пептид образуется в ходе особого ферментативного расщепления белка-предшественника β-амилоида [9]. Благодаря правильной пространственной структуре, белки могут выполнять свою специфическую функцию. Когда пространственная укладка белков нарушается, могут образоваться жесткие агрегаты — амилоиды. Амилоидогенез — нарушение белкового обмена, которое сопровождается образованием и отложением в тканях амилоида. Для образования амилоидов уложенный белок должен денатурировать и начать компактно укладываться в β-складки, образуя олигомеры (переходную форму от нормальной укладки белка к амилоидной), которые агрегируют между собой либо в аморфные агрегаты, либо в амилоидные фибриллы. Такая пространственная форма белков устойчива к протеазам (ферментам, расщепляющим белки) и растворителям, поэтому они могут накапливаться в клетках и тканях организма [10]. Нерастворимые жесткие фибриллы обладают токсическим действием, усиливают образование активных форм кислорода [11] и разрушают мозг [12].
Считается, что олигомеры β-амилоидного белка представляют собой наиболее токсичную конформацию, приводящую к синаптической дисфункции при болезни Альцгеймера у человека. Эти олигомеры были обнаружены и в мозге кошек старше года. Однако связь между этими олигомерами и поведенческими аномалиями остается неясной.
У кошек старше 10 лет происходит агрегация β-амилоида. Эти скопления имеют более диффузное распределение, чем у человека. В мозжечке кошек обнаружены только внутриклеточные бляшки, а внеклеточные бляшки, которые наблюдаются у человека, отсутствуют [3]. В других областях мозга кошек встречаются как внутриклеточные, так и внеклеточные амилоидные бляшки [5].
Несмотря на то, что между отложениями β-амилоида, наблюдаемыми у кошек и людей, есть сходство, β-амилоидные бляшки у кошек менее выраженные, чем у людей с болезнью Альцегеймера. Характер распределения β-амилоидных бляшек у кошек с СКД, возможно, больше похож на то, что наблюдаются в мозге здоровых, не страдающих деменцией, пожилых людей. Тем не менее, кошки с отложениями β-амилоида могут демонстрировать ненормальное поведение. Они проявляют спутанность сознания, чрезмерную вокализацию и блуждание. Однако тяжесть такого поведения, по-видимому, не коррелирует со степенью отложений β-амилоида [3].
Тау-белок (τ-белок), или microtubule-associated protein tau (MAPT), стабилизирует микротрубочки нейронов и клеток глии головного мозга и обеспечивает нормальный транспорт веществ внутри них. При посттрансляционной модификации тау-белок фосфорилируется. Иногда тау-белок может оказаться гиперфосфорилированным, тогда он прекращает выполнять свою функцию, и микротрубочки разбираются на части. Сам тау-белок является внутренне неупорядоченным и обретает определенную структуру только в связанном с микротрубочками виде. Он образует патологические агрегаты — парные спиральные филаменты и сложенные из них более крупные нейрофибриллярные клубки [1], [11]. У кошек вырабатывается ряд различных изоформ тау-белка, сходных с таковыми у людей с болезнью Альцгеймера. Хотя некоторые исследования не нашли нейрофибриллярные клубки из гиперфосфорилированного тау-белка в мозге старых кошек, другие обнаружили там следы тау-белка. Было высказано предположение, что вместо нейрофибриллярных клубков у кошек наблюдается образование «предпузырьков». Поскольку ученые обнаружили клубки гиперфосфорилированного тау-белка только у небольшого числа кошек, связь между нейрофибриллярными клубками и СКД пока не может быть установлена. Интересно, что гиперфосфорилированный тау-белок также обнаруживается внутри нервных клеток у самых маленьких котят, а также у взрослых кошек при ишемии и судорогах [3].
На развитие СКД у кошек влияют также изменения, происходящие в сосудах и периваскулярном пространстве головного мозга животных. К ним относятся микрокровоизлияния, инфаркты, артериосклероз и накопление β-амилоида в бляшках вокруг кровеносных сосудов в мозге [3].
Иногда β-амилоид накапливается в сосудах головного мозга. При таком сценарии возникают нарушения кровообращения, происходит воспаление и развивается церебральная амилоидная ангиопатия [11]. Считается, что она является основной причиной сосудистой дисфункции и когнитивного спада у людей. Однако ее можно обнаружить и в мозге здоровых людей, не страдающих слабоумием, что позволяет предположить, что эта патология не является специфической для болезни Альцгеймера. Существуют разногласия по поводу существования церебральной амилоидной ангиопатии у кошек. В некоторых исследованиях она была обнаружена в мозге пожилых кошек, а в других — нет [3].
Болен — лечись, а здоров — берегись. Диагностика и лечение синдрома когнитивной дисфункции
Диагностика СКД представляет собой сложную задачу. Изменения в поведении могут быть вызваны не только СКД, но и другими заболеваниями. К ним относятся гипертония, хронические, эндокринные, инфекционные и другие заболевания. Поведение также может меняться из-за обычных болей в желудке, мышцах, зубах и т.д. Прежде чем поставить диагноз СКД, необходимо исключить другие потенциальные причины изменений поведения. Некоторые из вышеперечисленных состояний могут усугублять клинические признаки СКД, а поскольку пожилые кошки часто имеют букет сопутствующих заболеваний, это осложняет как диагностику, так и лечение.
Ветеринары должны провести полное обследование кошки, изучить ее историю болезни и поведенческие проблемы, провести полный физический осмотр, сделать необходимые анализы. Только после этого ветеринарный врач может выявить основную причину (или причины) изменений в поведении животного. Необходимо обнаружить все сопутствующие заболевания, чтобы обеспечить возможность точного вмешательства. Владельцы кошек могут научиться тому, как распознавать и отслеживать изменения в поведении домашнего животного, и своевременно обращать внимание на изменения в поведении. Также хозяева могут наблюдать за изменениями в массе тела кошки, потреблении пищи, воды и выделении мочи и кала [3].
Вылечить СКД у кошек не получится, можно только замедлить развитие заболевания у животного. Мы вновь видим, что кошачий СКД и человеческая болезнь Альцгеймера похожи. Хотя СКД невозможно вылечить, терапия может уменьшить его клинические проявления и улучшить качество жизни кошек. Потенциальные меры вмешательства включают изменение окружающей среды животного, диетические добавки, специальные диеты и медикаменты. Все меры должны быть адаптированы к каждой конкретной кошке, изменениям в ее поведении и учитывать сопутствующие заболевания. Но пока у нас еще мало информации о том, какие вмешательства с наибольшей вероятностью могут помочь конкретным кошкам [3].
Литература
- На руинах памяти: настоящее и будущее болезни Альцгеймера;
- Maria Neus Bosch, Marco Pugliese, Javier Gimeno-Bayon, Manuel Jose Rodriguez, Nicole Mahy. (2012). Dogs with Cognitive Dysfunction Syndrome: A Natural Model of Alzheimer’s Disease. CAR. 9, 298-314;
- Lorena Sordo, Danièlle A. Gunn‐Moore. (2021). Cognitive Dysfunction in Cats: Update on Neuropathological and Behavioural Changes Plus Clinical Management. Veterinary Record. 188;
- На руинах памяти: настоящее и будущее болезни Альцгеймера;
- Sordo L. Neuropathology, diagnosis, and potential treatment of feline cognitive dysfunction syndrome and its similarities to Alzheimer's disease. PhD Thesis. — The University of Edinburgh, 2021. — 346 p.;
- D. Gunn-Moore, K. Moffat, L.-A. Christie, E. Head. (2007). Cognitive dysfunction and the neurobiology of ageing in cats. J Small Animal Practice. 48, 546-553;
- Gary M. Landsberg, Jeff Nichol, Joseph A. Araujo. (2012). Cognitive Dysfunction Syndrome. Veterinary Clinics of North America: Small Animal Practice. 42, 749-768;
- Xiangning Li, Bin Yu, Qingtao Sun, Yalun Zhang, Miao Ren, et. al.. (2018). Generation of a whole-brain atlas for the cholinergic system and mesoscopic projectome analysis of basal forebrain cholinergic neurons. Proc. Natl. Acad. Sci. U.S.A.. 115, 415-420;
- β-амилоид: невидимый враг или тайный защитник? Запутанная тропка болезни Альцгеймера;
- Агрегация белков – смерть или выживание?;
- Заговор с целью нейродегенерации: бета-амилоид и тау-белок;
- Возможно, β-амилоид болезни Альцгеймера — часть врождённого иммунитета.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚