Микрофлюидика и «лаборатория-на-чипе»: маленький мир больших возможностей
10 марта 2026
Микрофлюидика и «лаборатория-на-чипе»: маленький мир больших возможностей
- 307
- 0
- 2
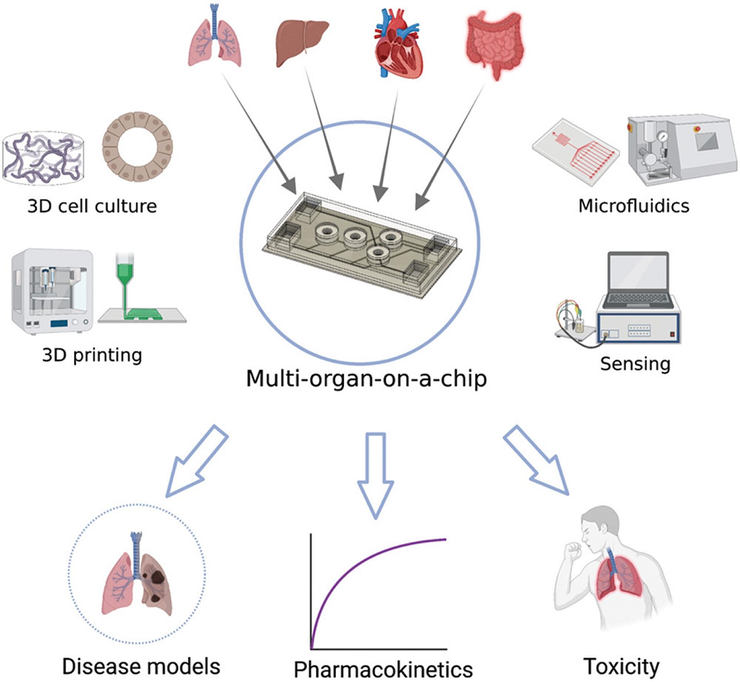
Схема концепции мультиоргана-на-чипе с техническими компонентами и потенциальными приложениями.
Рисунок в полном размере.
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Микрофлюидика, наука о движении жидкостей в микроканалах, за последние десятилетия превратилась из академического эксперимента в одну из самых перспективных технологий современной биомедицины. «Лаборатория-на-чипе» позволяет объединять сложные процессы — от получения образца до обработки результата — на миниатюрных платформах, помещающихся на ладони. В данном обзоре рассматривается эволюция микрофлюидных систем от первых устройств 1970-х годов до современных моделей «орган-на-чипе», а также новые области применения в контексте 3D-печати и тканевой инженерии. Отдельное внимание уделено диагностическому направлению — микрофлюидные чипы уже используются для секвенирования, молекулярной детекции и экспресс-анализов. Микрофлюидика демонстрирует, как на стыке физики, химии и биологии рождается новая логика лабораторных исследований: от массивных приборов к автономным системам, где миллионы реакций могут происходить в капле жидкости одновременно.
Конкурс «Био/Мол/Текст»-2025/2026
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2025/2026.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

Партнер номинации — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Как микрофлюидика меняет биологические исследования
Представьте себе фармаколога, которому нужно протестировать тысячу новых химических соединений. В традиционной лаборатории это потребует недели работы, литры дорогих реактивов и сотни чашек Петри. Или биолога, наблюдающего за тем, как раковая клетка покидает кровеносный сосуд — это редкое событие требует часов «караула». А создание живой модели, например, человеческого легкого для тестирования лекарств и вовсе кажется фантастикой.
Проблема в том, что классические методы часто работают с усредненными, статичными и слишком большими объемами, что мешает нам увидеть тонкие детали динамических биологических процессов. Микрофлюидика меняет правила игры.
Что, если не просто уменьшить пробирку, а создать для клеток и молекул их собственный «микромир», управляемый с высочайшей точностью? Именно эту задачу решает микрофлюидика — технология, основанная на управлении малыми объемами жидкостей в микроскопических устройствах (микрофлюидных чипах). Это позволяет создавать физические и химические условия, близкие к физиологическим, для моделирования биологических процессов. Ее ключевое воплощение — «лаборатория-на-чипе», миниатюрная платформа, где на площади в несколько квадратных сантиметров размещена целая сеть микроканалов и камер. Внутри этой системы кипит жизнь: по искусственным артериям-каналам текут растворы, в специальных камерах растут, взаимодействуют и реагируют на стимулирующие факторы живые клетки, а биохимические реакции происходят в объемах в тысячи раз меньше капли.
Чем же этот подход так привлекателен?
- Не просто экономия, а новые горизонты. Уменьшение объемов образцов и реагентов до нано- и микролитров, в первую очередь, необходимо не ради бережливости. Это шанс изучать редкие образцы, например, биопсии, которые в обычных условиях быстро расходуются. Микрофлюидика позволяет проводить тысячи параллельных экспериментов на одном чипе, что кардинально ускоряет скрининг лекарств по сравнению с классическими методами [1].
- Не просто быстро, а динамично. В микроскопических масштабах силу поверхностного натяжения и диффузию нельзя игнорировать — они доминируют в поведении жидкостей. Это позволяет не только ускорять уже известные реакции, но и воспроизводить физиологически релевантную динамику, например, градиенты концентраций и потоки, аналогичные кровотоку в капиллярах [2].
- Не статичная картинка, а живая физиология. Ключевой прорыв — возможность поместить клетки в среду, механически и химически близкую к их естественному окружению. Именно на этом принципе основаны «органы-на-чипе» [3], микрофлюидные устройства, в которых модели органов функционируют, как в живом организме, обеспечивая перфузию, обмен веществ и межклеточные взаимодействия. Такие модели используются для изучения развития тканей, физиологии органов и этиологии заболеваний, а также для оценки эффективности и токсичности медикаментов [4].
Микрофлюидика — это гораздо больше, чем миниатюризация. Это смена парадигмы в биологических исследованиях, переход от пассивного наблюдения за биологией в пробирке к созданию и контролю целых микромиров, где ставятся вопросы, на которые ранее у науки не было ответов.
Зарождение и эволюция технологии
Хотя история микрофлюидики как самостоятельной области начинается в 1990-е годы, ее технологические корни уходят гораздо глубже, в фундаментальные достижения микроэлектроники и микроэлектромеханических систем. С момента изобретения методов создания сложных микросхем на кремниевых пластинах в 1950-х годах ученые начали задумываться: если мы уже умеем миниатюризировать электронные схемы, получится ли осуществить нечто похожее с химическим и биологическими лабораториями? Это позволило бы ускорить биохимические реакции в тысячи раз. Фундаментальные технологии, такие как фотолитография и химическое травление, позволили переносить методы микроэлектроники в мир жидкостей.
Одним из первых реальных шагов в этом направлении стал миниатюрный газовый хроматограф, разработанный Стивеном Терри в Стэнфордском университете в конце 1970-х годов [5]. Это устройство содержало целый набор функций газовой хроматографии на маленьком кремниевом чипе — от инжекции пробы до детектора. Несмотря на свою простоту по современным меркам, оно продемонстрировало жизнеспособность идеи «лаборатории-на-чипе» еще за несколько десятилетий до того, как это стало массовым трендом.
Тем не менее, именно конец 1980-х — начало 1990-х стали поворотным моментом. В 1990 году аналитик Андреас Манц и его коллеги впервые формализовали концепцию µTAS (micro Total Analysis System) — устройства, которое могло бы интегрировать все этапы химического анализа (подготовка пробы, разделение, детекция) на одном миниатюрном чипе. Эта концепция стала идеологической основой современной микрофлюидики. В 1993 году группа Манца и соавторов продемонстрировала первый рабочий прибор µTAS, способный выполнять капиллярный электрофоретический анализ аминокислот на стеклянном чипе всего за несколько секунд, что стало важным шагом к практическим приложениям технологии [6].
Ключевой технологической вехой стало и появление «мягкой литографии» в середине 1990-х, метода производства микрофлюидных устройств из полидиметилсилоксана (PDMS) [7]. Этот эластичный, прозрачный и биосовместимый полимер оказался гораздо более удобным для быстрой и недорогой разработки прототипов, чем традиционные кремний и стекло. Именно с его помощью микрофлюидные системы получили широкое распространение в биологии и медицине.
С конца 1990-х и особенно в 2000-е годы микрофлюидика стала биологически ориентированной [8]. Масштаб микроканалов (десятки микрометров) удивительным образом совпадал с размерами самих клеток, что открыло новые горизонты — теперь можно было манипулировать отдельными клетками, моделировать градиенты химических сигналов и создавать динамическое микроокружение, повторяющее физиологические условия в живых тканях.
На рубеже 2000-х гг. сформировалось новое направление — «органы-на-чипе». В отличие от классических μTAS, которые автоматизировали аналитические процессы, устройства «орган-на-чипе» стремились имитировать работу целых биологических органов (легких, печени, кишечника и др.) в миниатюре. Эти системы объединяют микрофлюидный поток с живыми клеточными культурами, механическими движениями и физиологическими сигналами [9].
Следующее десятилетие стало временем материальной и функциональной диверсификации. Традиционный PDMS дополнили термопласты, бумажные микрофлюидные устройства и новые методы изготовления, адаптированные под массовое производство и высокую воспроизводимость. Применение технологий, таких как литье под давлением термопластов, 3D-печать и гибридные материалы, расширило спектр возможных приложений [10–13]. Сегодня микрофлюидика — это уже не просто лабораторный инструмент, а полноценная инженерная дисциплина.
Диагностика на чипе: когда вся лаборатория умещается на ладони
Диагностика — один из самых быстрорастущих и практичных секторов применения микрофлюидики. Перенос классической лабораторной диагностики, такой как ПЦР (полимеразная цепная реакция), и подготовка образцов, в миниатюрные микрофлюидные устройства позволяет добиться быстрой, недорогой и высокочувствительной диагностики с малыми объемами реактивов и биологических образцов, что ранее было недоступно на традиционных платформах. Благодаря малым объемам и улучшенному теплообмену такие системы ускоряют температурные циклы и повышают эффективность реакции, сохраняя при этом чувствительность и специфичность. Это делает микрофлюидные ПЦР-чипы идеальными для экспресс-диагностики инфекций и генетических маркеров в местах оказания медицинской помощи. Так, например, компания ELVESYS разработала самую быструю в мире систему количественной ПЦР — FASTGENE (рис. 1) [14].
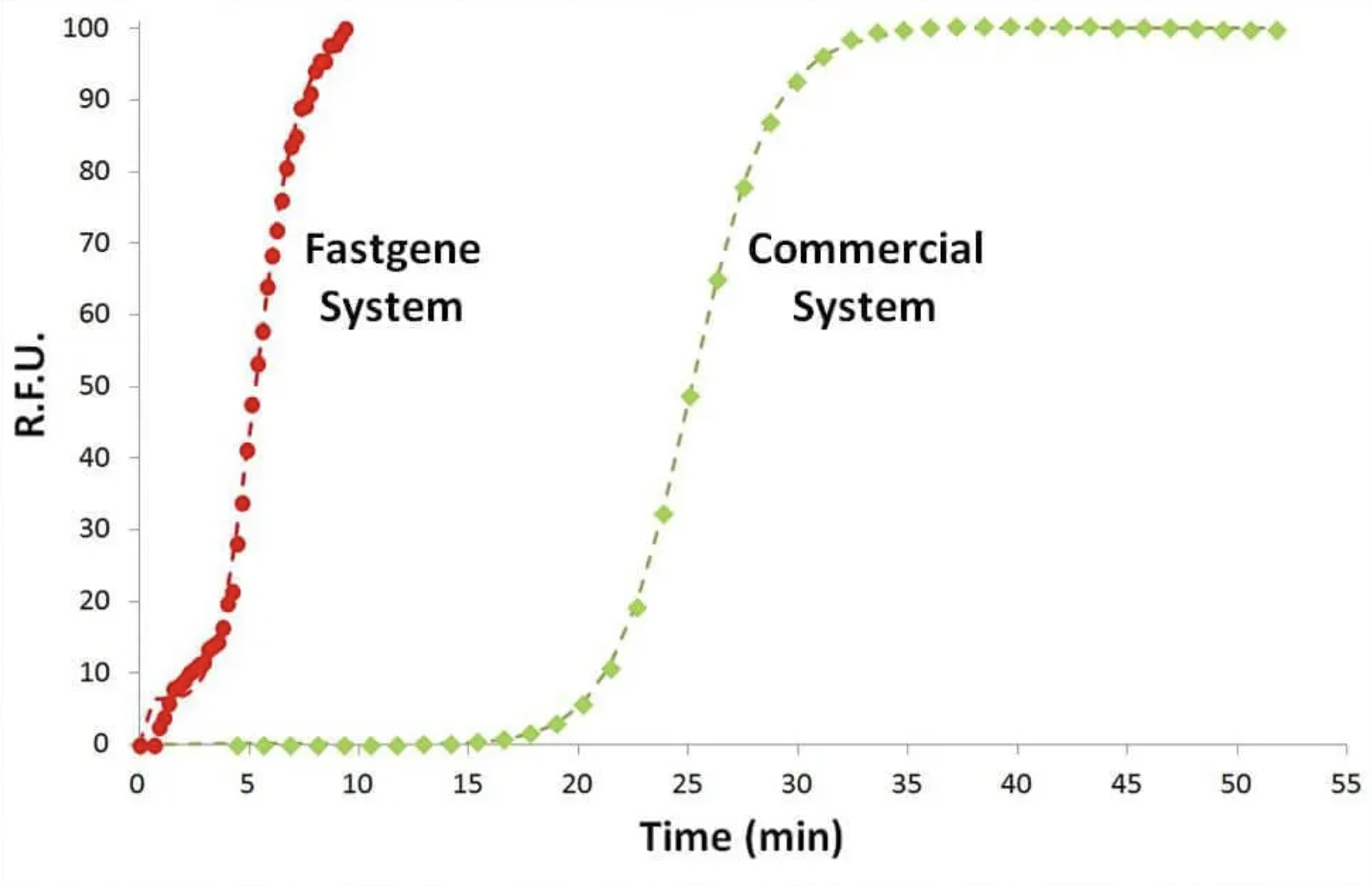
Рисунок 1. Молекулярная детекция Fastgene по сравнению с современной коммерческой системой: система Fastgene позволяет проводить детекцию в 6 раз быстрее.
Другой важный аспект — чтение генома. Еще несколько десятилетий назад секвенирование ДНК, например, в рамках проекта «Геном человека», требовало огромных машин, централизованных лабораторий, множества реакций и затрат в миллиарды долларов. Сегодня методы секвенирования эволюционировали: от классических методов Сэнгера до высокопроизводительных технологий следующего поколения (NGS) и нанопорового секвенирования, которые позволяют читать миллионы—миллиарды нуклеотидов за часы или даже минуты.
Современные микрофлюидные системы не заменяют эти технологии, но интегрируют ключевые этапы подготовки образца и сам процесс чтения в компактные устройства. Например, микрофлюидные платформы позволяют автоматически выполнять на одном чипе такие стадии, как лизис клеток, выделение ДНК, очистка, фрагментация, подготовка библиотек и даже детекция. Все это уменьшает ручной труд, снижает риск контаминации и ускоряет процесс в несколько раз по сравнению с традиционным лабораторным протоколом [15].
В таких системах микроканалы действуют как миниатюрные лабораторные «авто-конвейеры»: молекулы ДНК поступают из пробирки прямо в сеть каналов, где они проходят стадию выделения и очистки, затем фрагментируются и метятся адаптерами, а подготовленные фрагменты передаются в интерфейс для секвенирования на внешнем модуле (например, NGS [16] или нанопоровом сенсоре [17]). Прототипы таких интегрированных систем уже разработаны:
- Системы sample-to-library, предназначенные для микрофлюидной подготовки библиотек для Illumina-секвенирования, работают с минимальным вмешательством человека [18].
- Устройства, похожие на Oxford Nanopore VolTRAX, используют микрофлюидные методы для автоматической подготовки образцов к нанопоровому чтению, сокращая подготовку с нескольких дней до нескольких часов [19].
- Отдельные исследования демонстрируют, как микрофлюидные платформы используют магнитные частицы для извлечения ДНК внутри чипа, что существенно упрощает пробоподготовку для последующего анализа [19].
Такие технологии уже находят применение в клинической диагностике. Например, «лаборатории на чипе» для обнаружения однонуклеотидных полиморфизмов (SNP) (рис. 2) широко используется в биохимических областях, включая геномику, протеомику, разработку лекарств и диагностику инфекционных заболеваний. Эта платформа продемонстрировала много преимуществ, включая высокое соотношение поверхности к объему, малые объемы реагентов, низкий фоновый шум и короткое время реакции [20]. Так, комбинация микрофлюидики с современными технологиями секвенирования стала важной частью биотехнологической революции, дав возможность перевести сложные биохимические процессы на уровень компактных, автоматизированных чипов-устройств.
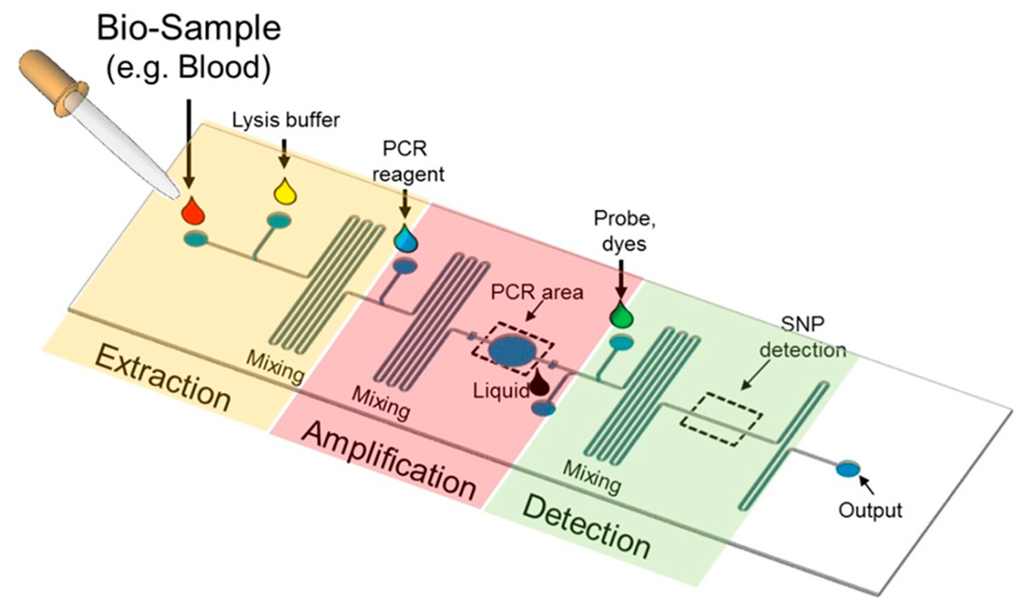
Рисунок 2. Типичная «лаборатория-на-чипе» для обнаружения SNP. Биологические образцы, содержащие ДНК, вводятся во входное отверстие для экстракции ДНК. Клетки крови подвергаются лизису. ДНК поступает в зону ПЦР для амплификации. Реагенты для ПЦР, включая праймер, dNTP и ДНК-полимеразу, вводятся в канал для смешивания с ДНК. Затем продукт ПЦР детектируется на предмет распознавания SNP в области обнаружения.
Но микрофлюидика идет дальше. Биомолекулярные процессы, протекающие в микрофлюидном чипе, превращаются в инструмент сверхбыстрого обнаружения вирусов и бактерий. Там, где раньше требовались часы инкубации, теперь достаточно десятков секунд. Иммуноанализы, те самые реакции «антиген-антитело», благодаря микроканалам и нанолитрам реагентов становятся почти мгновенными. Вместо томительного ожидания результат анализа становится доступен, пока не остыл кофе. И это только начало.
Недавно технологии редактирования генома CRISPR/Cas [21], [22] нашли себя и в микрофлюидной диагностике. Суть разработанного метода диагностики заключается в прямом обнаружении РНК вируса SARS-CoV-2 с использованием технологии CRISPR-Cas13a. При этом исключается этап предварительной амплификации, который является обязательным для «золотого стандарта» — ПЦР. Представьте: миниатюрный чип из PDMS, соединенный со смартфоном, способен засечь всего сотню копий РНК SARS-CoV-2 в миллилитре образца всего за полчаса (рис. 3) [23]. Образцы РНК пациентов с клинически значимой вирусной нагрузкой были точно идентифицированы как положительные менее чем за 5 минут измерения на устройстве. А компактный микроскоп, использующий камеру мобильного телефона, оказался более чувствительным, чем лабораторный планшетный ридер, что позволяет использовать его для диагностики в месте оказания медицинской помощи.
Такой подход, основанный на CRISPR/Cas13a, открывает путь к тестам нового поколения, чувствительным, быстрым и автономным. Однако, для полномасштабного перехода к широкодоступному диагностическому устройству необходима дополнительная работа. Требуется разработать протокол подготовки образца без экстракции, чтобы минимизировать общее время выполнения анализа. Также для массового производства, возможно, понадобятся встроенные датчики с беспроводным подключением к телефону. Так или иначе, метод имеет большой потенциал для частого и быстрого скрининга в условиях пандемии.
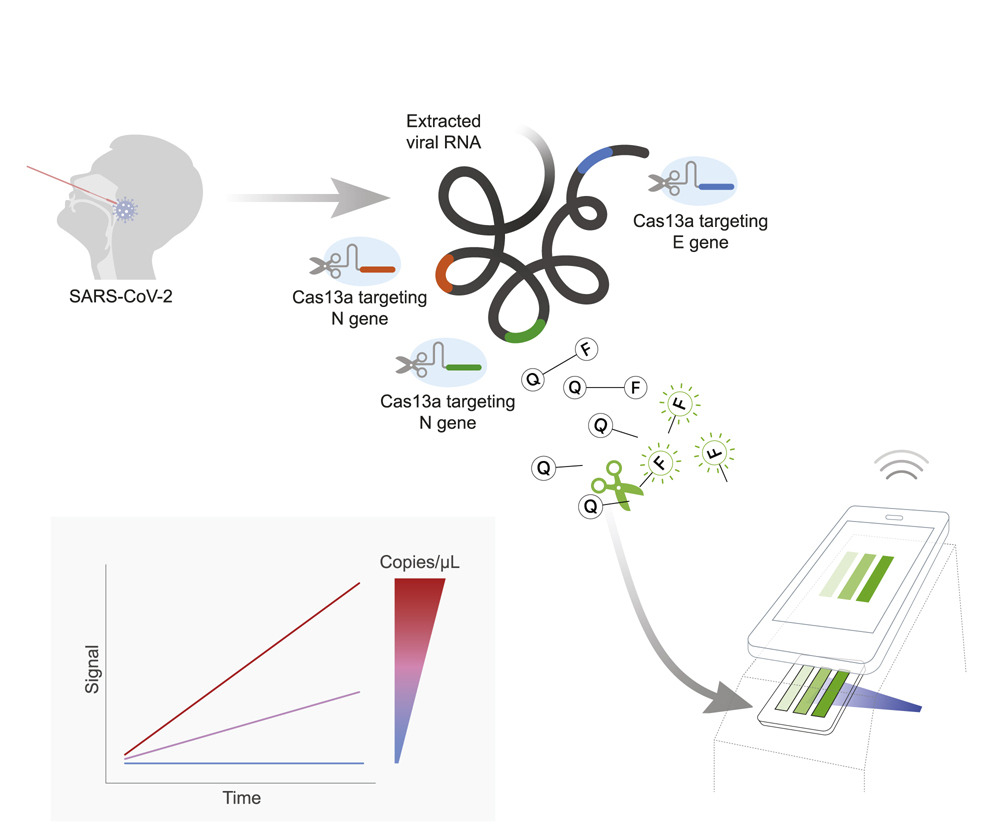
Рисунок 3. Схематическое представление технологии детекции вирусной РНК с помощью системы CRISPR/Cas13a.
Как уже было сказано ранее, подобные полимерные микрофлюидные устройства, изготовленные из полидиметилсилоксана (PDMS) или полиметилметакрилата (PMMA), часто используются, благодаря их низкой стоимости, хорошей биосовместимости и простоте изготовления. Однако на сегодняшний день уже изобрели большое количество различных типов микрофлюидных детекторов (рис. 4) [24]. Так, например, бумажные микрофлюидные устройства (Paper-based) особенно привлекательны для использования в условиях ограниченных ресурсов, поскольку они дешевы, портативны, просты в изготовлении и работают автономно за счет капиллярного действия.
Существуют также электронные микрофлюидные устройства, которые совмещают CRISPR-диагностику с электрохимическим считыванием. Эти устройства преобразуют биохимический сигнал расщепления Cas-белками в электрический, что позволяет проводить быстрый анализ, осуществлять мониторинг в реальном времени и обеспечивать высокую селективность. Еще один тип — цифровые микрофлюидные системы, которые разделяют реагенты на множество микрореакторов (Droplet/Digital chip), что позволяет достигать высокой эффективности и чувствительности, а также точной количественной оценки на уровне одиночных молекул. Одно из таких устройств — CARMEN — использовалось для обнаружения 169 вирусов, а также для субтипирования штаммов гриппа [25].
Пожалуй, самыми необычными из микрофлюидных устройств можно считать носимые микрофлюидные устройства (Wearable), которые предназначены для неинвазивного, долговременного мониторинга и сбора данных в режиме реального времени, что имеет решающее значение для персонализированной медицины и эпидемиологического надзора. Так, например, специальные сенсоры, интегрированные в маски, позволяли мониторить SARS-CoV-2 во вдыхаемом воздухе [26].
Невозможно отрицать, что появляется все больше новых возможностей для быстрой, чувствительной, специфичной и применимой в полевых условиях диагностики инфекционных заболеваний.
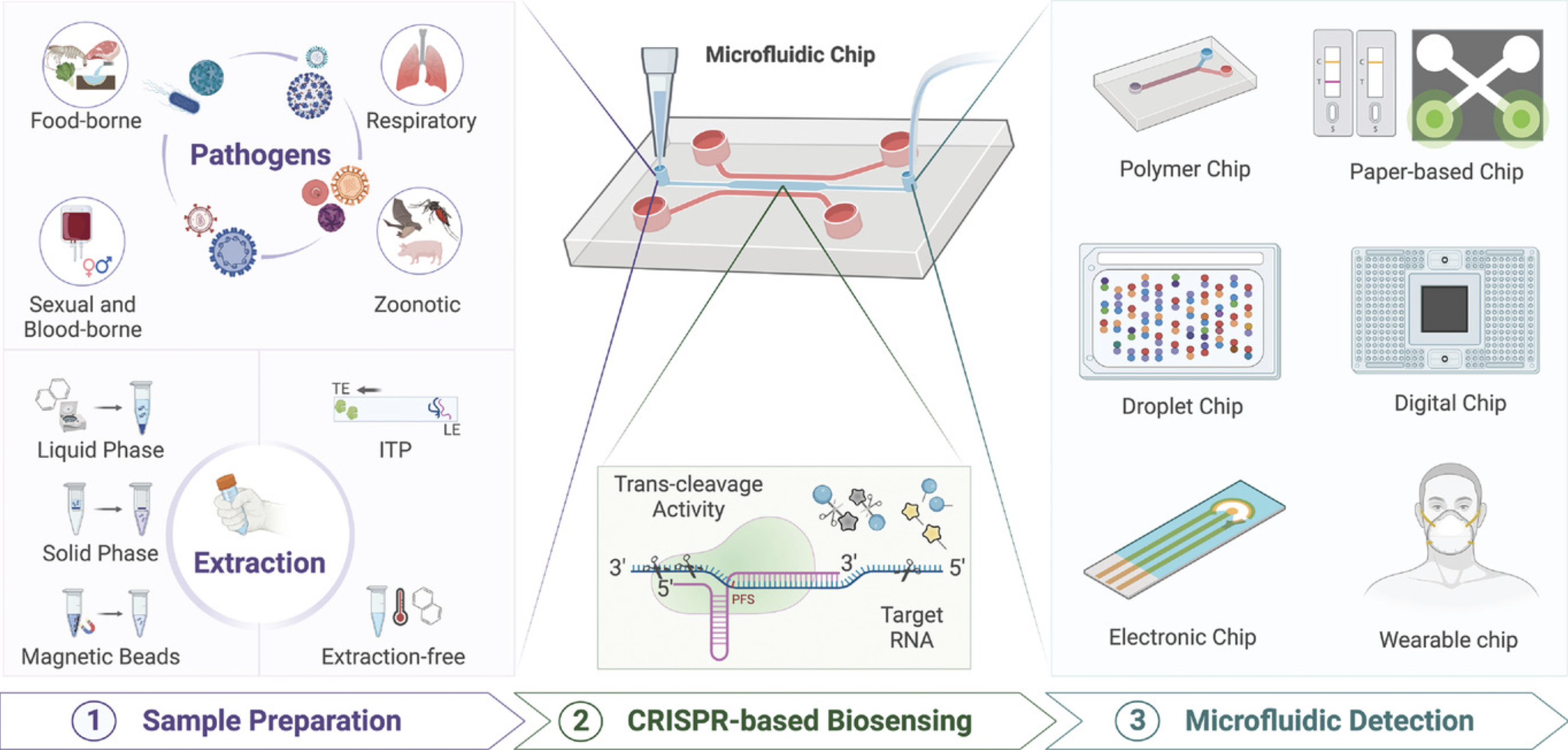
Рисунок 4. Обзор микрофлюидных систем на основе CRISPR в диагностике инфекционных заболеваний.
От клеток к органам: когда микроканалы становятся кровеносной системой
Один из самых интересных поворотов — когда микрофлюидика начинает работать с клетками и тканями. В последнее время также активно развиваются и органоиды. Органоиды представляют собой мини-тканевые самоорганизующиеся трехмерные органоподобные кластеры, состоящие из способных к дифференцировке клеток, которые позволяют точно моделировать исходные функции органов [27]. В настоящий момент исследования на органоидах активно ведутся, однако их сочетание с микрофлюидными платформами дает абсолютно новую категорию: «органоиды-на-чипе» и мультиорганные системы [28].
Зачем вообще это нужно, ведь переносить клеточные культуры в микромир чипа — это очень сложно, а в лаборатории всегда найдется проверенная временем чашка Петри? Интеграция органоидов в микрофлюидные чипы критически необходима для преодоления ограничений традиционных статических 3D-культур. В обычной культуре, когда органоиды достигают размера более 400 мкм, пассивная диффузия не может обеспечить достаточный обмен питательными веществами и кислородом, что приводит к некрозу в их ядре [29].
Микрофлюидика решает эти проблемы путем:
- обеспечения перфузии (имитации кровотока), поскольку чипы создают непрерывный и контролируемый поток среды, улучшая массоперенос. Это способствует пролонгированному культивированию, росту и созреванию органоидов [30];
- моделирования биомеханики, поскольку микрофлюидные платформы позволяют воспроизводить физические силы (например, напряжение сдвига или растяжение). Механические стимулы необходимы для правильного развития и созревания тканей, чего невозможно достичь в статических условиях [31];
- стандартизации, поскольку микрофлюидика позволяет более точно контролировать геометрию органоидов и их микроокружение. Это помогает снизить внутреннюю вариабельность органоидов и улучшить воспроизводимость экспериментов [30].
Применение органоидов в контексте микрофлюидики позволяет создавать мощные человеческие модели для изучения развития органов, заболеваний и тестирования лекарственных препаратов. На данный момент уже успешно реализованы некоторые модели органов, в том числе:
- органоиды мозга для моделирования неврологических расстройств. Сложность архитектуры мозга требует высокоточного контроля. Органоиды «мозга-на-чипе» (cerebral organoids) позволили исследовать физические механизмы формирования извилин, которые критически важны для развития коры. В микрофлюидном чипе имитировались ядерное растяжение и цитоскелетное сокращение, которые необходимы для поверхностного образования складок [30]. Культивирование под контролируемым потоком привело к уменьшению некротического ядра в церебральных органоидах и усилению дифференциации нейронов [31]. Такие модели успешно использовались для изучения пренатального воздействия никотина, демонстрируя преждевременную нейронную дифференциацию [32], а также нарушение кортикальной организации. Также были разработаны модели для изучения нейровоспаления, опосредованного микроглией [33], при воздействии опиоидных рецепторов;
- кишечные органоиды, требующие воспроизведения движения (перистальтики) и обеспечения потока по просвету (люмену), чего статическая культура обеспечить не может. Так, были разработаны чипы, имитирующие перистальтические движения кишечника с помощью циклического вакуума (растяжения эластичной мембраны) [34]. Это привело к формированию ворсинчатых структур и характерной архитектуры, что способствовало пролонгированному культивированию кишечного эпителия. Подобные платформы использовались для изучения накопления слизистого слоя и физиологии толстой кишки, а также для моделирования взаимодействий клетки хозяина — клетки микроорганизмов, включая культивирование комплексного микробиома в анаэробных условиях [33];
- почечные органоиды. Было показано, что в условиях потока (динамического культивирования в чипе) в органоидах наблюдалось повышенное созревание популяций эндотелиальных клеток и формирование перфузируемой сети [31]. Модель использовалась для изучения поликистоза почек, демонстрируя, что абсорбция глюкозы приводит к образованию кист, и позволяя тестировать фармакологические ингибиторы [34];
- органоиды поджелудочной железы. Перфузируемые средой органоиды, имитирующие островки Лангерганса, в микрофлюидном чипе позволили улучшить жизнеспособность клеток и воспроизвести специфическую функцию островков, поскольку органоиды в динамических условиях секретировали инсулин в ответ на стимуляцию глюкозой и регулировали внутриклеточный поток ионов кальция (Ca2+) [35]. Аналогичные платформы также использовались для создания гетерогенных островковых органоидов из hiPSCs (человеческих индуцированных плюрипотентных стволовых клеток) с целью моделирования муковисцидоза (кистозного фиброза) [36].
Наиболее замечательное достижение «органов-на-чипе» — это возможность объединять модели различных органов для имитации системных процессов, таких как метаболизм или токсичность (рис. 5). Так, например, модель, соединяющая органоиды печени и сердца, позволила оценить кардиотоксичность антидепрессанта кломипрамина после его метаболизма в печени [37]. Другой пример — двухорганная модель печени и поджелудочной железы, с помощью которой изучали диабет 2 типа. В совместной культуре наблюдалось усиление снижения уровня глюкозы по сравнению с монокультурой, что подтверждает важность межорганной коммуникации [38]. Другая группа исследователей пошла еще дальше и объединила в одной системе целых три органа — сердце, легкое и печень. Исследования показали, что системная токсичность противоопухолевого препарата блеомицина приводила к прекращению биения сердечных органоидов в мультиорганной системе, тогда как в модели, содержащей только сердце, этот эффект отсутствовал [39].
Но и это еще не все. Были созданы сложные платформы, соединяющие до восьми различных васкуляризованных органных чипов (включая кишечник, печень, почку, сердце, легкое, мозг), что позволило прогнозировать фармакокинетические реакции человека на препараты (например, никотин и цисплатин) [40].
Таким образом, микрофлюидика не просто «сажает» клетки на чип, она привносит контроль, динамику и физиологическую релевантность, которые необходимы для перевода органоидных моделей из фундаментальных исследований в прикладную область тестирования лекарств и персонализированной медицины.
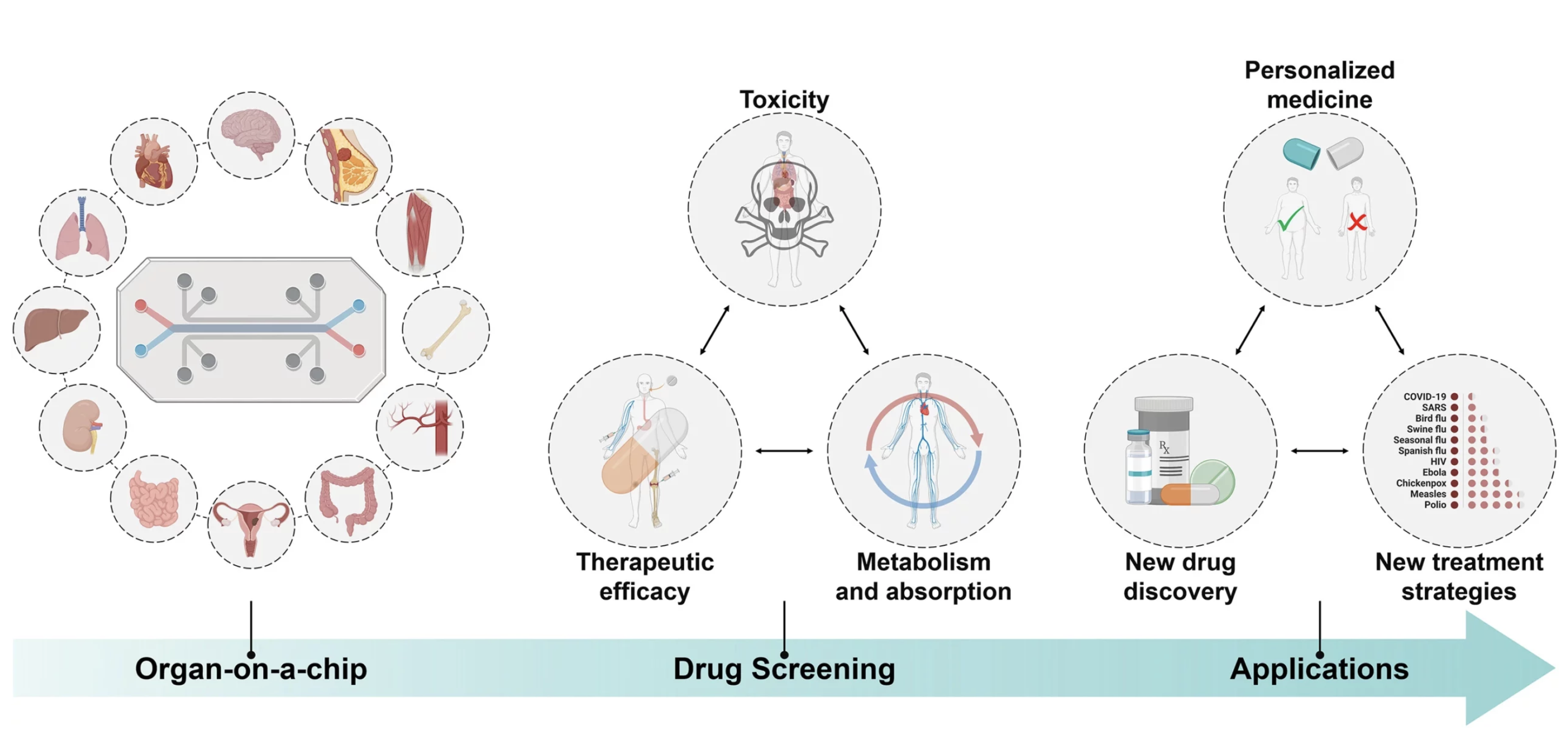
Рисунок 5. «Орган-на-чипе» для скрининга и тестирования лекарственных препаратов.
Однако следует отметить, что такие платформы все-таки представляют собой упрощенные модели человеческих тканей или органов. Одним из основных ограничений является неполный клеточный состав. Часто органоиды не включают все необходимые клеточные типы, присутствующие в настоящем органе. Например, в моделях часто отсутствует строма, иммунные клетки или форменные элементы крови. Другая проблема, возникающая при объединении нескольких органоидов в единую систему, заключается в подборе питательной среды, поскольку каждый тип органоидов требует различного состава среды для оптимального роста и функционирования [28]. Кроме того, на сегодняшний день подобные технологии с использованием органоидов обладают ограниченной воспроизводимостью, что проявляется в вариациях размера, формы и расположения клеток друг относительно друга [30].
Так, несмотря на значительный прогресс, системы «орган-на-чипе» все еще далеки от достижения полной функциональности настоящих человеческих органов. Пока современным технологиям удалось создать лишь модели органов, а не их точные копии. И тем не менее, это является мощным инструментом для исследований.
Распечатать ткань на принтере — неужели это возможно?
Еще один интересный аспект — 3D-биопринтинг в сочетании с микрофлюидикой, направленный на создание функциональных живых тканей и искусственных органов со сложной структурой. Основная идея состоит в том, чтобы создать трехмерные ткани с сетью микроканалов, которые работают как кровеносные сосуды, то есть проводят питательные вещества, кислород и удаляют отходы жизнедеятельности клеток [41]. Без такой сети напечатанные ткани не могут «жить» и развиваться.
pКомбинация 3D-биопечати и микрофлюидики позволяет преодолеть существенные различия между напечатанными конструкциями и реальными тканями, особенно в отношении таких структур, как сосудистые сети [41]. Благодаря этому подходу были успешно предприняты попытки создания сложных функциональных моделей органов, что имеет огромное значение для биомедицинских исследований, скрининга лекарств и персонализированной медицины. Давайте более подробно их рассмотрим.
Создание сосудистых сетей (васкуляризация)
Васкуляризация остается критическим лимитирующим фактором для масштабирования бионапечатанных тканей [42]. Методы, сочетающие биопечать и микрофлюидику, позволили добиться значительного прогресса в этой области.
Во-первых, использование микрофлюидных печатающих головок позволило создать полые гидрогелевые волокна, которые могут имитировать кровеносные сосуды, обеспечивая транспорт жидкости в трехмерной клеточной среде [41]. Во-вторых, были созданы перфузируемые сосудистые конструкции, которые позволили существенно повысить жизнеспособность инкапсулированных клеток (например, фибробластов) по сравнению с неваскуляризованными системами [43]. Примечательно, что такие сосудистые сети демонстрировали физиологические реакции сужения и расширения сосудов, что критически важно для исследований сосудистых анастомозов и заболеваний [44].
Разработка моделей органов-на-чипе
Интеграция микрофлюидики и биопечати оказалась революционной для улучшения систем «орган-на-чипе», которые стали более точно имитировать функции и физиологию человеческих органов. Например, был создан функциональный «мини-орган» печени из hiPSCs с гексагональной дольковой структурой [45]. Еще одним интересным достижением биопечати стало создание извитых проксимальных почечных канальцев, встроенных в перфузируемые чипы. Эта модель обладала характерной морфологией эпителия и функциональными свойствами, а также сохраняла жизнеспособность в перфузируемой культуре в течение двух месяцев [46].
Еще одно интересное исследование продемонстрировало, как с помощью биопечати можно создать сосудистые волокна, а затем высеять на них кардиомиоциты. Такой подход приводил к формированию структур, способных к синхронному сокращению в течение длительного времени [43]. Создаются также и модели опухолевого микроокружения. В данном случае биопечать с микрофлюидикой используется для создания гетерогенных моделей опухолей (например, «глиобластомы-на-чипе»), которые включают опухолевые клетки, васкуляризованные сети и компоненты внеклеточного матрикса, что необходимо для точного скрининга лекарств и изучения метастазирования [44].
Так, микрофлюидные системы в сочетании с 3D-биопечатью предоставляют огромный потенциал для создания тканей, моделирования заболеваний и разработки персонализированных лекарственных средств, поскольку они позволяют создавать более функциональные и точные модели, преодолевая ограничения традиционных методов.
Барьеры и рынок: почему чипы еще не стоят в каждой лаборатории
Если технология так привлекательна, почему она еще не повсеместно используется? Помимо фундаментальных преимуществ микрофлюидных систем, есть ряд практических технических и рыночных барьеров, которые сдерживают их широкое распространение.
Во-первых, в масштабе микрометров поведение жидкостей и взаимодействие с поверхностями существенно отличаются от привычной макроскопической химии: адсорбция молекул на стенках каналов, изменение свойств смачивания каналов, непредсказуемая кинетика переноса массы и диффузии могут приводить к неравномерным искажениям сигналов, потере чувствительности анализов или некорректным данным, особенно при работе с белками, клетками и другими биологическими объектами. Эти эффекты возникают потому, что соотношение поверхность/объем в микроканалах очень велико, и поверхностные процессы начинают доминировать над потоковыми [47].
Во-вторых, массовое производство требует строгой стандартизации и контроля качества, которые обеспечивают стабильность работы устройств независимо от места изготовления. Без стандартов компании вынуждены заново разрабатывать и оптимизировать каждый элемент под конкретное применение, поскольку тонкие различия в материалах, конфигурации чипов или способах их сборки могут приводить к значительным различиям в результатах анализа. Это особенно критично для биомедицинских применений, где воспроизводимость данных — ключевой фактор для внедрения в клиническую практику. Стандарты помогают убедиться, что устройства, произведенные разными организациями, работают сопоставимо и надежно, но их разработка требует времени, согласования экспертов и затрат на валидацию протоколов [48]. Кроме того, стандартизация обычно связана с увеличением стоимости разработки и производства на ранних этапах: компании вынуждены инвестировать в сертификацию, обеспечение качества и масштабируемые производственные линии прежде, чем технологии станут коммерчески выгодными. Это делает такие чипы дороже по сравнению с традиционными лабораторными методами для рутинных задач, особенно в условиях, когда рынку еще не требуется массовое использование.
В-третьих, для работы «лаборатории-на-чипе» необходимы насосы, клапаны, сенсоры, электроника. Даже если чип сам по себе миниатюрный, внешняя система может быть громоздкой. К тому же, существует сложность объединения различных компонентов, включая вспомогательное оборудование (например, источники давления и модули культивирования клеток), компоненты детектирования (например, оптика и инженерные интерфейсы) и модули подготовки образцов (например, смесители и концентраторы) в единую платформу [49].
Наконец, если клиника может использовать проверенный, недорогой метод, она выберет его. Поэтому чип-решения должны быть конкурентоспособны по цене, удобству, качеству и надежности.
Эти проблемы во многом объясняют, почему концепция «лаборатории-на-чипе», знакомая ученым уже десятки лет, так и не превратилась в массово применяемую технологию в повседневной лабораторной практике. Ее внедрение зависит не только от научной ценности, но и от решения сложных инженерных, организационных и экономических задач. И хотя путь к массовому применению требует стандартизации, масштабирования, совершенствования материалов и интерфейсов, потенциал очевиден, «лаборатория-на-чипе» — не просто компактная альтернатива классическим приборам, а новая логика работы с биологическими материалами. Это переход от лаборатории с огромным количеством приборов к интеллектуальной системе, где на площади в несколько сантиметров может развернуться целая вселенная живых процессов.
Литература
- Chiara Leal-Alves, Zhiyang Deng, Natalia Kermeci, Steve C. C. Shih. (2024). Integrating microfluidics and synthetic biology: advancements and diverse applications across organisms. Lab Chip. 24, 2834-2860;
- Grigor Simitian, María Virumbrales-Muñoz, Cristina Sánchez-de-Diego, David J. Beebe, David Kosoff. (2022). Microfluidics in vascular biology research: a critical review for engineers, biologists, and clinicians. Lab Chip. 22, 3618-3636;
- Органы-на-чипе: когда технология сплетается с жизнью;
- Sangeeta N Bhatia, Donald E Ingber. (2014). Microfluidic organs-on-chips. Nat Biotechnol. 32, 760-772;
- S.C. Terry, J.H. Jerman, J.B. Angell. (1979). A gas chromatographic air analyzer fabricated on a silicon wafer. IEEE Trans. Electron Devices. 26, 1880-1886;
- D. Jed Harrison, Karl Fluri, Kurt Seiler, Zhonghui Fan, Carlo S. Effenhauser, Andreas Manz. (1993). Micromachining a Miniaturized Capillary Electrophoresis-Based Chemical Analysis System on a Chip. Science. 261, 895-897;
- Lee A. (2013). The third decade of microfluidics. Lab. Chip. Royal Society of Chemistry. 13, 1660–1661;
- Pamela N. Nge, Chad I. Rogers, Adam T. Woolley. (2013). Advances in Microfluidic Materials, Functions, Integration, and Applications. Chem. Rev.. 113, 2550-2583;
- Chak Ming Leung, Pim de Haan, Kacey Ronaldson-Bouchard, Ge-Ah Kim, Jihoon Ko, et. al.. (2022). A guide to the organ-on-a-chip. Nat Rev Methods Primers. 2;
- Dan S. Tawfik, Andrew D. Griffiths. (1998). Man-made cell-like compartments for molecular evolution. Nat Biotechnol. 16, 652-656;
- Amelia L. Markey, Stephan Mohr, Philip J.R. Day. (2010). High-throughput droplet PCR. Methods. 50, 277-281;
- Andres W. Martinez, Scott T. Phillips, Manish J. Butte, George M. Whitesides. (2007). Patterned Paper as a Platform for Inexpensive, Low‐Volume, Portable Bioassays. Angew Chem Int Ed. 46, 1318-1320;
- M Heckele, W K Schomburg. (2004). Review on micro molding of thermoplastic polymers. J. Micromech. Microeng.. 14, R1-R14;
- Nidhi Verma, Alok Pandya. (2022). Challenges and opportunities in micro/nanofluidic and lab-on-a-chip. Progress in Molecular Biology and Translational Science. 289-302;
- Adam Snider, Michael Nilsson, Mark Dupal, Masoud Toloue, Anubhav Tripathi. (2019). A Microfluidics Workflow for Sample Preparation for Next-Generation DNA Sequencing. SLAS Technology. 24, 196-208;
- 12 методов в картинках: секвенирование нуклеиновых кислот;
- Нанопоровое секвенирование: на пороге третьей геномной революции;
- Hanyoup Kim, Mais J. Jebrail, Anupama Sinha, Zachary W. Bent, Owen D. Solberg, et. al.. (2013). A Microfluidic DNA Library Preparation Platform for Next-Generation Sequencing. PLoS ONE. 8, e68988;
- Gorachand Dutta, Joshua Rainbow, Uros Zupancic, Sotirios Papamatthaiou, Pedro Estrela, Despina Moschou. (2018). Microfluidic Devices for Label-Free DNA Detection. Chemosensors. 6, 43;
- Chao-Wei Huang, Yu-Tsung Lin, Shih-Torng Ding, Ling-Ling Lo, Pei-Hwa Wang, et. al.. (2015). Efficient SNP Discovery by Combining Microarray and Lab-on-a-Chip Data for Animal Breeding and Selection. Microarrays. 4, 570-595;
- CRISPR-эпопея и ее герои;
- Просто о сложном: CRISPR/Cas;
- Parinaz Fozouni, Sungmin Son, María Díaz de León Derby, Gavin J. Knott, Carley N. Gray, et. al.. (2021). Amplification-free detection of SARS-CoV-2 with CRISPR-Cas13a and mobile phone microscopy. Cell. 184, 323-333.e9;
- Yi Xie, Huimin Li, Fumin Chen, Srisruthi Udayakumar, Khyati Arora, et. al.. (2022). Clustered Regularly Interspaced short palindromic repeats‐Based Microfluidic System in Infectious Diseases Diagnosis: Current Status, Challenges, and Perspectives. Advanced Science. 9;
- Cheri M. Ackerman, Cameron Myhrvold, Sri Gowtham Thakku, Catherine A. Freije, Hayden C. Metsky, et. al.. (2020). Massively multiplexed nucleic acid detection with Cas13. Nature. 582, 277-282;
- Peter Q. Nguyen, Luis R. Soenksen, Nina M. Donghia, Nicolaas M. Angenent-Mari, Helena de Puig, et. al.. (2021). Wearable materials with embedded synthetic biology sensors for biomolecule detection. Nat Biotechnol. 39, 1366-1374;
- От эксперимента до индустрии: как органоиды строят мост между наукой и бизнесом;
- Guocheng Fang, Yu‐Cheng Chen, Hongxu Lu, Dayong Jin. (2023). Advances in Spheroids and Organoids on a Chip. Adv Funct Materials. 33;
- Sunghee Estelle Park, Andrei Georgescu, Dongeun Huh. (2019). Organoids-on-a-chip. Science. 364, 960-965;
- Fang Yu, Walter Hunziker, Deepak Choudhury. (2019). Engineering Microfluidic Organoid-on-a-Chip Platforms. Micromachines. 10, 165;
- Lito Papamichail, Lena S. Koch, Devin Veerman, Kerensa Broersen, Andries D. van der Meer. (2025). Organoids-on-a-chip: microfluidic technology enables culture of organoids with enhanced tissue function and potential for disease modeling. Front. Bioeng. Biotechnol.. 13;
- Zheng Ao, Hongwei Cai, Daniel J. Havert, Zhuhao Wu, Zhiyi Gong, et. al.. (2020). One-Stop Microfluidic Assembly of Human Brain Organoids To Model Prenatal Cannabis Exposure. Anal. Chem.. 92, 4630-4638;
- Sasan Jalili-Firoozinezhad, Francesca S. Gazzaniga, Elizabeth L. Calamari, Diogo M. Camacho, Cicely W. Fadel, et. al.. (2019). A complex human gut microbiome cultured in an anaerobic intestine-on-a-chip. Nat Biomed Eng. 3, 520-531;
- Sienna R. Li, Ramila E. Gulieva, Louisa Helms, Nelly M. Cruz, Thomas Vincent, et. al.. (2022). Glucose absorption drives cystogenesis in a human organoid-on-chip model of polycystic kidney disease. Nat Commun. 13;
- Tingting Tao, Yaqing Wang, Wenwen Chen, Zhongyu Li, Wentao Su, et. al.. (2019). Engineering human islet organoids from iPSCs using an organ-on-chip platform. Lab Chip. 19, 948-958;
- Kyu Shik Mun, Kavisha Arora, Yunjie Huang, Fanmuyi Yang, Sunitha Yarlagadda, et. al.. (2019). Patient-derived pancreas-on-a-chip to model cystic fibrosis-related disorders. Nat Commun. 10;
- Fangchao Yin, Xu Zhang, Li Wang, Yaqing Wang, Yujuan Zhu, et. al.. (2021). HiPSC-derived multi-organoids-on-chip system for safety assessment of antidepressant drugs. Lab Chip. 21, 571-581;
- Sophie Bauer, Charlotte Wennberg Huldt, Kajsa P. Kanebratt, Isabell Durieux, Daniela Gunne, et. al.. (2017). Functional coupling of human pancreatic islets and liver spheroids on-a-chip: Towards a novel human ex vivo type 2 diabetes model. Sci Rep. 7;
- Aleksander Skardal, Sean V. Murphy, Mahesh Devarasetty, Ivy Mead, Hyun-Wook Kang, et. al.. (2017). Multi-tissue interactions in an integrated three-tissue organ-on-a-chip platform. Sci Rep. 7;
- Richard Novak, Miles Ingram, Susan Marquez, Debarun Das, Aaron Delahanty, et. al.. (2020). Robotic fluidic coupling and interrogation of multiple vascularized organ chips. Nat Biomed Eng. 4, 407-420;
- Jingyun Ma, Yachen Wang, Jing Liu. (2018). Bioprinting of 3D tissues/organs combined with microfluidics. RSC Adv.. 8, 21712-21727;
- Jafarkhani M. (2019). Bioprinting in vascularization strategies. Iran. Biomed. J. 23, 9;
- Elham Davoodi, Einollah Sarikhani, Hossein Montazerian, Samad Ahadian, Marco Costantini, et. al.. (2020). Extrusion and Microfluidic‐Based Bioprinting to Fabricate Biomimetic Tissues and Organs. Adv Materials Technologies. 5;
- Rashik Chand, Ken-ichiro Kamei, Sanjairaj Vijayavenkataraman. (2025). Advances in Microfluidic Bioprinting for Multi-Material Multi-Cellular Tissue Constructs. Cell Therapy & Engineering Connect. 1, 1;
- Xuanyi Ma, Xin Qu, Wei Zhu, Yi-Shuan Li, Suli Yuan, et. al.. (2016). Deterministically patterned biomimetic human iPSC-derived hepatic model via rapid 3D bioprinting. Proc. Natl. Acad. Sci. U.S.A.. 113, 2206-2211;
- Kimberly A. Homan, David B. Kolesky, Mark A. Skylar-Scott, Jessica Herrmann, Humphrey Obuobi, et. al.. (2016). Bioprinting of 3D Convoluted Renal Proximal Tubules on Perfusable Chips. Sci Rep. 6;
- Skarphedinn Halldorsson, Edinson Lucumi, Rafael Gómez-Sjöberg, Ronan M.T. Fleming. (2015). Advantages and challenges of microfluidic cell culture in polydimethylsiloxane devices. Biosensors and Bioelectronics. 63, 218-231;
- Prapti Pattanayak, Sachin Kumar Singh, Monica Gulati, Sukriti Vishwas, Bhupinder Kapoor, et. al.. (2021). Microfluidic chips: recent advances, critical strategies in design, applications and future perspectives. Microfluid Nanofluid. 25;
- Raymond Mariella. (2008). Sample preparation: the weak link in microfluidics-based biodetection. Biomed Microdevices. 10, 777-784.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚