Наука дает шанс: молекулярная биология в медицине
26 октября 2016
Наука дает шанс: молекулярная биология в медицине
- 1917
- 4
- 4
Мутации, происходящие в ДНК, — «горячие точки», ведущие к непредсказуемым последствиям.
рисунок автора статьи
-
Автор
-
Редакторы
Статья на конкурс «био/мол/текст»: Полвека назад возникла и начала стремительно развиваться молекулярная биология. Биологи и физики (обычный для середины двадцатого века союз) открыли важнейшие клеточные процессы, изобрели основные методы, без которых сегодня немыслима работа любой биологической лаборатории. Сейчас у нас есть громадный потенциал для решения всевозможных задач: прояснения аспектов происхождения жизни, изучения взаимодействий компонентов в живой клетке и сложных биохимических каскадов. Мы знаем и умеем то, что еще лет 60 назад казалось фантастикой. И одна из задач, на решение которой уже могут покуситься ученые, — это борьба с наследственными заболеваниями человека. Некоторые из них, такие как фенилкетонурия, успешно корректируются, подходы к терапии множества других еще не найдены. В этой статье пойдет речь об одном из таких заболеваний — синдроме ломкой X-хромосомы — и о сложностях его изучения.
«Био/мол/текст»-2016
Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2016.
Генеральным спонсором конкурса, согласно нашему краудфандингу, стал предприниматель Константин Синюшин, за что ему огромный человеческий респект!
Спонсором приза зрительских симпатий выступила фирма «Атлас».
Спонсор публикации этой статьи — Андрей Владимирович Марахонов.
Экспансия повторов. Новый тип мутаций — причина давно известных заболеваний
В начале 20 века ученые заметили, что умственная отсталость чаще поражает мужчин. В 1934 году ирландский врач Джеймс Мартин и английский генетик Джулия Белл впервые описали семью, где умственная отсталость наследовалась сцепленно с полом. В этой семье было 11 мужчин-олигофренов и две женщины с легкой степенью умственной отсталости. Обнаруженную семейную форму заболевания назвали синдромом Мартина-Белл. Через 35 лет Герберт Лабс, проводя цитогенетическое исследование, выявил в кариотипе четырех слабоумных мужчин и трех нормальных женщин (из трех поколений одной семьи) странную Х-хромосому, которую он назвал маркерной: ближе к концу длинного плеча у нее была вторичная перетяжка. Лабс предложил отслеживать маркерную хромосому у эмбрионов мужского пола в неблагополучных по синдрому Мартина-Белл семьях, поскольку она может сигнализировать о высоком риске рождения олигофренов (рис. 1) [1]. Так медики обрели первый пренатальный маркер синдрома, а их пациенты — возможность принятия взвешенного решения о сохранении беременности. Маркерную перетяжку локализовали на участке Xq27.3.
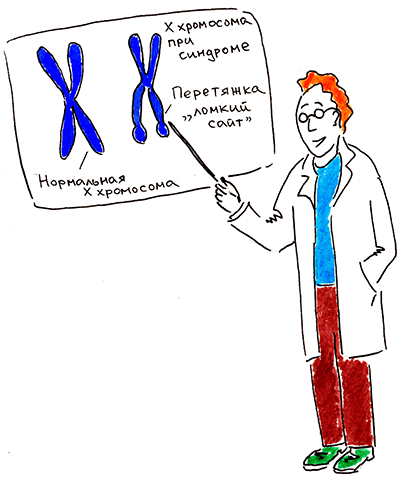
Рисунок 1. Герберт Лабс рассказывает коллегам о перетяжке на X-хромосоме при синдроме Мартина-Белл.
рисунок автора статьи
Позже многие исследователи наблюдали под микроскопом Х-хромосомы не просто с перетяжкой, а как бы поломанными — с «оторванными» кончиками длинных плеч. Место перетяжки/поломки стали называть ломким сайтом (fragile site). Поэтому заболевание получило другое название — синдром ломкой X-хромосомы (fragile X syndrome).
Еще одна интересная особенность этого заболевания — усугубление болезни в каждом последующем поколении (генетическая антиципация). Этот феномен объяснили только в последнем десятилетии 20 века, после открытия особого типа мутаций — экспансии тринуклеотидных повторов.
Если классифицировать заболевания по патогенетическим механизмам, то довольно большую группу составят болезни, обусловленные экспансией повторов [2]. Суть мутации заключается в следующем: в человеческом геноме встречаются короткие участки (например, триплеты нуклеотидов), в норме повторенные несколько раз, но по каким-то причинам их количество начинает резко расти — в десятки и сотни раз, — и общая длина «заикающегося» (содержащего повторы) фрагмента может увеличиться до нескольких тысяч пар нуклеотидов (рис. 2).
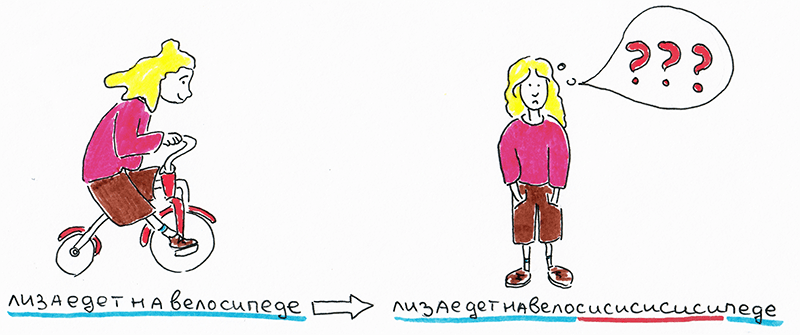
Рисунок 2. Представим, что наш геном — очень длинный текст, а происходящая экспансия превращает его в полную бессмыслицу.
рисунок автора статьи
Позже выяснилось, что экспансия лежит в основе патогенеза не только синдрома ломкой X-хромосомы, но и миотонической дистрофии I и II типов, а также ряда нейродегенеративных заболеваний человека — например, бокового амиотрофического склероза и болезни Гентингтона. В общей сложности известно около 30 заболеваний, для которых характерна такая мутация. Многие из этих патологий связаны с увеличением количества повторов (ЦГГ)n, (ЦАГ)n, (ГАА)n и других [3].
Причины и патогенез синдрома ломкой X-хромосомы
Синдром ломкой X-хромосомы, пожалуй, самая распространенная причина наследственной умственной отсталости после синдрома Дауна. Клинических проявлений синдрома довольно много и наблюдаются из них не все и не всегда, но основные — низкий уровень интеллекта и эмоционального развития вкупе с рядом физических отклонений, —— присутствуют чаще всего. Эти особенности заметны уже в раннем детстве.
Причина заболевания кроется в увеличении числа повторов триплета ЦГГ в области промотора (стартовой площадки для начала синтеза мРНК) гена FMR1 (рис. 3). Продуктом этого гена является белок FMRP (fragile X mental retardation protein), который взаимодействует с РНК и направляет сложные молекулярные каскады, необходимые для нормального формирования нейронов, их синаптической пластичности [4]. У здорового человека количество повторов варьирует в пределах от 5 до 54. При увеличении числа повторов до 55–200 возникает аллель, называемый премутантным. В популяции он встречается достаточно часто: у одного из 200–250 человек. Хотя уровень мРНК гена оказывается выше нормы, содержание FMRP остается неизменным или даже немного снижается. Почему это происходит — пока неизвестно. Можно предположить, что в этом участвует РНК-интерференция — процесс подавления экспрессии гена (какого-то этапа пути от нуклеотидной последовательности до конечного продукта, в данном случае — FMRP) с помощью малых РНК [5].
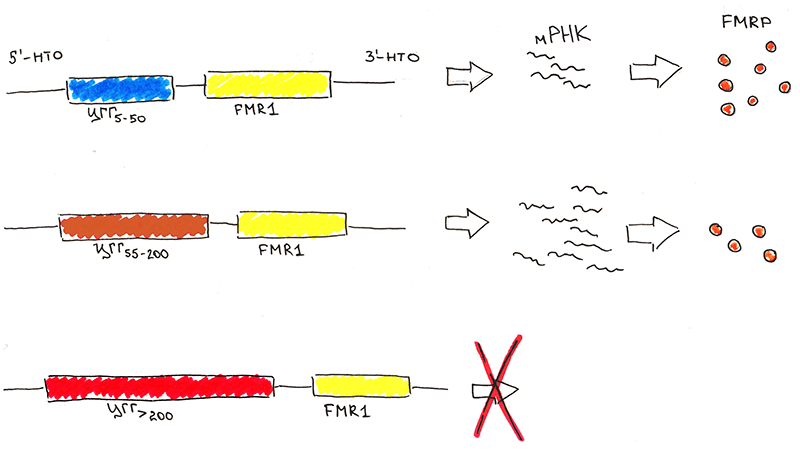
Рисунок 3. Структура гена FMR1 и схема его экспрессии. 5′-НТО и 3′-НТО — 5′- и 3′-нетранслируемые области гена.
рисунок автора статьи
При чуть более выраженной экспансии ЦГГ-повторов у пациентов можно обнаружить особые внутриклеточные включения, состоящие из мРНК FMR1 и РНК-связывающих белков. Это свидетельство того, что мРНК становится токсичной для клетки [6]. Интересно, что «нормальная» мРНК не оказывает токсического эффекта даже в очень высоких концентрациях. У большинства женщин — носительниц премутации, в отличие от мужчин, нет внешних проявлений патологии. В этом заслуга второй X-хромосомы, которая в большей или меньшей доле клеток компенсирует дефект. Более того, есть данные о преимущественной инактивации («выключении») именно дефектной хромосомы . Но зачастую таким женщинам свойственны эмоциональные проблемы, депрессии и фобии.
И разумеется, даже при отсутствии внешних признаков заболевания премутантный аллель передается потомству. При этом происходит «амплификация» повтора — с каждым овогенезом всё больше и больше, вплоть до нескольких тысяч «копий». А это ведет к тому, что премутантный аллель превращается в самый что ни на есть мутантный [2], [7]. В этом случае мы говорим уже о синдроме ломкой Х-хромосомы. Его частота в популяции составляет около 1:3600–6000. Это довольно много! При таком значительном увеличении количества повторов ЦГГ происходят эпигенетические изменения: присоединение метильных групп к цитозину ЦГГ-триплетов в области промотора FMR1 и модификации белков, связанных с ДНК, — гистонов. Всё это ведет к локальному изменению плотности укладки ДНК — формированию конденсированного, неактивного хроматина, называемого гетерохроматин. Экспрессия генов, находящихся в такой зоне, подавляется. Поэтому в случае синдрома Мартина-Белл резко сокращается продукция белка FMRP. Более того, модификации хроматина вызывают визуальную «ломкость» хромосомы в районе Xq27 — ту самую, которую наблюдали ученые еще в середине 20 века. Правда, справедливости ради надо отметить, что у пары процентов больных синдром обусловлен не экспансией ЦГГ-повторов, а другими мутациями гена FMR1.
Инактивация одной из Х-хромосом — жизненно важный процесс дозовой компенсации генов, препятствующий удваиванию экспрессии всех Х-хромосомных генов у самок по сравнению с самцами. То есть в каждой клетке особи любого пола, несмотря на диплоидный набор хромосом, активна только какая-то одна X-хромосома — доставшаяся либо от отца, либо от матери. О захватывающих подробностях «выключения» половых хромосом у человека и червя рассказывают статьи «Загадочное путешествие некодирующей РНК Xist по X-хромосоме» [8] и «Истории из жизни Х-хромосомы круглого червя-гермафродита» [9]. — Ред.
Итак, судя по всему, патогенетические механизмы у синдрома ломкой X-хромосомы и других «экспансивных» заболеваний общие: для всех них характерно какое-то критическое количество триплетов, при котором ген еще функционирует нормально. Причины самόй экспансии до конца не ясны. На сегодняшний день предложено множество гипотез и моделей, пытающихся ее объяснить, например, нарушениями при репликации, проблемами с системами репарации, и т.д. Однако пока ни одна из них не нашла экспериментального подтверждения.
Почему сложно диагностировать экспансию и как эту проблему решают?
Как уже упоминалось, синдром ломкой X-хромосомы далеко не единственное заболевание, проявляющееся умственной отсталостью. Но накопленные знания помогли разработать достаточно подробную методику диагностики именно этого синдрома. Есть возможность выявить даже премутацию у людей с нормальным фенотипом (с нормальным уровнем IQ и без аномалий развития) [10]. Это очень важно, поскольку у женщин-носительниц высок риск появления детей с выраженным синдромом. Правда, эта методика не лишена недостатков и, к сожалению, не применяется широко, поэтому разработке методов молекулярной диагностики до сих пор отводится особое место.
Первоначально проводили исследование хромосомного набора пациента — кариотипирование, — и при обнаружении повреждений в участке Xq27.3 ставили диагноз. Это и сегодня является первым, что делают врачи-генетики — по крайней мере, в России. Проблема кариотипирования заключается в том, что этот метод недостаточно чувствителен, а значит, не слишком надежен. Поэтому всё чаще для постановки диагноза применяют более современные методы. Существуют тест-системы для ДНК-диагностики, основанные на ключевых методах молекулярной биологии: ПЦР (рис. 4), Саузерн-блоте, иммунопреципитации и др. Они позволяют оценить количество белка FMRP и его мРНК, определить число ЦГГ-повторов и уровень метилирования цитозина в промоторе гена FMR1. Это, в свою очередь, помогает лучше понять патофизиологию синдрома, потому что можно соотнести результаты анализа с фенотипом пациентов и носителей премутации.
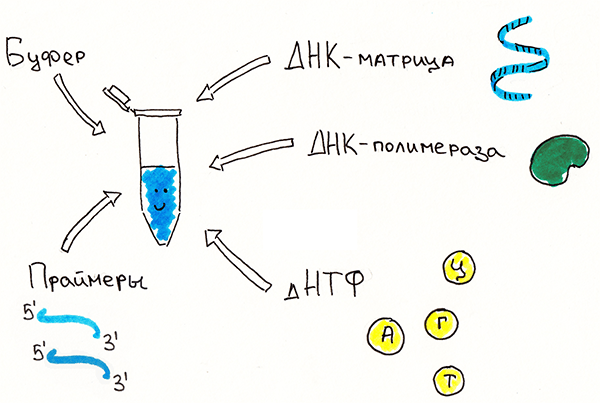
Рисунок 4. ПЦР — полимеразная цепная реакция, один из стандартных методов молекулярной биологии, применяемых в диагностике. Показаны основные компоненты, без которых реакция не пойдет. ДНК-матрица — молекула ДНК, участок которой нужно многократно размножить (амплифицировать). Праймеры — олигонуклеотиды, комплементарные концам (на разных цепях) интересующего участка ДНК-матрицы, как бы ограничивающие его, — выполняют функцию затравки для фермента, копирующего ДНК (ДНК-полимеразы). дНТФ — дезоксирибонуклеозидтрифосфаты — строительный материал для новой молекулы ДНК. Буфер — раствор солей, обеспечивающий необходимые условия (pH, ионную силу); он обязательно содержит соль магния, потому что только в присутствии ионов Mg2+ работает ДНК-полимераза. Если все компоненты смешать, поместить в прибор под названием амплификатор (циклер) и запустить нужную программу циклического повышения-снижения температуры, на матрице исходных единичных молекул ДНК синтезируются тысячи копий интересующего участка, который в итоге будет легко изучать. Если же из-за каких-то мутаций изменятся последовательности, в норме комплементарные праймерам, либо радикально увеличится расстояние между ними, ПЦР-продукта просто не будет.
рисунок автора статьи
ПЦР — основной метод диагностики. Он позволяет наработать область, содержащую (ЦГГ)n. Проведя такой анализ, можно установить точный размер этой области, а значит, и число повторов, и таким способом обнаружить у пациентов премутантные или мутантные аллели. Но нужно сказать, что достичь этого непросто. Исследователи сталкиваются с рядом сложностей при амплификации этих фрагментов. У ДНК, которая будет выступать матрицей для синтеза новых молекул, есть такая характеристика, как ГЦ-состав, отражающая, насколько матрица богата пáрами гуанин-цитозин (богатая матрица содержит примерно 60% ГЦ-пар). Если процент ГЦ-пар высокий, то молекула будет тугоплавкой, и на некоторых этапах ПЦР нужно будет проводить более длительную денатурацию. (ЦГГ)n-область на 100% состоит из пар ГЦ, и ясно, что это очень трудная матрица.
Всё еще более усложняется тем, что такая последовательность без особых усилий образует различные вторичные структуры, очень устойчивые термодинамически: всевозможные шпильки, G-квадруплексы (четыре цепи, связанные между собой гуанинами и поддерживающиеся одновалентным катионом, например K+), i-мотивы (структуры, состоящие из четырех цепей ДНК, богатых цитозином, стабильные в кислой среде) [11]. Изучение подобных структур — очень красивая и интригующая задача для биохимиков и биофизиков, но для установления размера (ЦГГ)n-областей — это серьезное препятствие. Ну и ко всему прочему праймеры (олигонуклеотидные затравки для ДНК-полимеразы) могут образовывать с такими последовательностями димеры, и смесь молекул превращается в один термостабильный нераспутываемый клубок! Ясно, что с такой матрицей просто так не поработаешь. Но! На протяжении нескольких лет ученые активно придумывают всё новые и новые модификации обычной ПЦР, существенно улучшающие результат.
Поскольку ГЦ-богатая матрица нуждается в более длительной и высокотемпературной денатурации, раньше пытались прогревать матрицу дополнительно, перед ПЦР. Однако, как можно догадаться, проблему это не решило. Еще в конце 90-х выяснили, что синтез ДНК прерывается на протяженных участках ЦГГ-повторов в присутствии K+, а чуть позже поняли, что виной тому те самые квадруплексы [12]. Поскольку в наиболее распространенный буфер для ПЦР как раз входит KCl, то самым очевидным решением было исключить его из состава буфера; это дало определенные результаты, но хотелось большего. Поэтому начали активно придумывать альтернативные буферы.
Сейчас часто проводят ПЦР с добавлением чистого Tris-HCl в качестве буфера. Tris —стандартный компонент для получения растворов нуклеиновых кислот: он дешев, и его буферные свойства высоки при рН 7–9 — значениях, физиологичных для живых организмов. В Tris обязательно добавляют хлорид магния в концентрациях, не ингибирующих ДНК-полимеразу и потому не уменьшающих выход специфического продукта. Очень часто смесь «улучшают» разными веществами, изменяющими свойства всей сложной системы ПЦР: ДМСО, бетаин, формамид, — они стабилизируют денатурированную ДНК, помогают снизить температуру плавления. Некоторые используют модифицированные дНТФ, в частности 7-деаза-дГТФ, и отмечают его эффективность (рис. 5); этот модифицированный нуклеотид препятствует формированию сложных дуплексов.
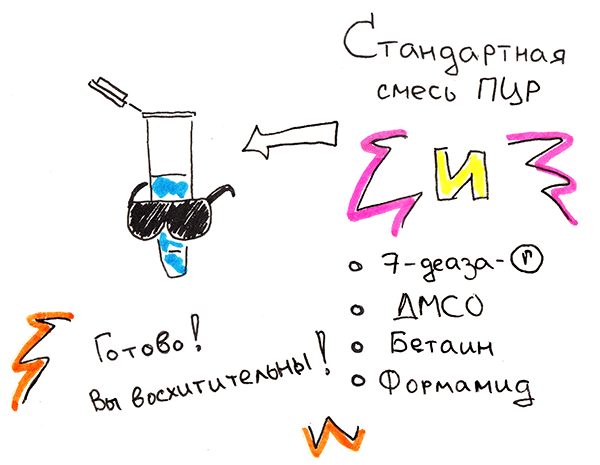
Рисунок 5. Усовершенствованная смесь для ПЦР — первое, что необходимо для амплификации (ЦГГ)n-области.
рисунок автора статьи
Кроме компонентов смеси, существуют интересные варианты температурных циклов. Самый простой вариант, часто использующийся для амплификации не самых «труднопроходимых» последовательностей, — ПЦР с горячим стартом (hot-start PCR). Отличие этой модификации от стандартной ПЦР заключается в использовании специальных антител, предотвращающих активацию полимеразы до достижения нужной температуры, что позволяет избежать неспецифического синтеза. Для работы с экстремально ГЦ-богатыми матрицами (>83%) предложен вариант ПЦР под названием Slowdown (модификация Touchdown): медленные скорости нагрева и охлаждения, ступенчатое снижение температуры отжига через определенное количество циклов, добавление 7-деаза-дГТФ — всё это приводит к повышению выхода целевого продукта ПЦР.
Однако нельзя сказать, что проблема получения необходимых для дальнейшего анализа количеств ГЦ-богатых фрагментов (типа промоторной области FMR1) решена полностью: статьи на эту тему появляются часто, но опубликованные результаты противоречат друг другу; коммерческие компании соревнуются в разработке «волшебных» наборов, но стоить они могут настолько дорого, что их не в состоянии себе позволить даже успешные зарубежные лаборатории.
Определение размера (ЦГГ)n-области — это самый первый и очень важный этап в изучении синдрома ломкой X-хромосомы, который, однако, всё еще нуждается в оптимизации. Если мы научимся считать повторы быстро и качественно, то диагностика станет простой и относительно дешевой. Появится возможность проводить ее массово, а значит, отличать синдром ломкой X-хромосомы от множества других заболеваний, сопровождающихся умственной отсталостью, что крайне важно подбора терапевтических подходов.
Литература
- Lubs H.A. (1969). A marker X chromosome. Am. J. Hum. Genet. 21 (3), 231–244;
- Budworth H. and McMurrey C.T. (2013). A brief history of triplet repeat diseases. Methods Mol. Biol. 1010, 3–17;
- Mirkin S.M. (2007). Expandable DNA repeats and human disease. Nature. 447, 932–940;
- Verkerk A.J., Pieretti M., Sutcliffe J.S., Fu Y.H., Kuhl D.P., Pizzuti A. et al. (1991). Identification of a gene (FMR1) containing a CGG repeat coincident with a breakpoint cluster region exhibiting length variation in fragile X syndrome. Cell. 65, 905–914;
- Lin S.L. (2015). microRNAs and fragile X syndrome. Adv. Exp. Med. Biol. 888, 107–121;
- Hoem G., Raske C.R., Garcia-Arocena D., Tassone F., Sanchez E., Ludwig A.L. et al. (2011). CGG-repeat length threshold for FMR1 RNA pathogenesis in a cellular model for FXTAS. Hum. Mol. Genet. 20, 2161–2170;
- Zhao X. and Usdin K. (2015). The repeat expansion diseases: the dark side of DNA repair. DNA repair (Amst.). 32, 96–105;
- Загадочное путешествие некодирующей РНК Xist по X-хромосоме;
- Истории из жизни Х-хромосомы круглого червя-гермафродита;
- Saldarriaga W., Tassone F., González-Teshima L.Y., Forero-Forero J.V., Ayala-Zapata S., Hagerman R. (2014). Fragile X syndrome. Colomb. Med. (Cali.). 45, 190–198;
- Реалии ДНК-«аномалии»;
- Usdin K. and Woodford K. (1995). CGG repeats associated with DNA instability and chromosome fragility form structures that block DNA synthesis in vitro. Nucleic Acids Res. 23, 4202–4209.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚