Нобелевская премия по физиологии и медицине (2012): индуцированные стволовые клетки
08 октября 2012
Нобелевская премия по физиологии и медицине (2012): индуцированные стволовые клетки
- 15187
- 1
- 14
Колонии человеческих индуцированных плюрипотентных стволовых клеток (ИПСК) человека, полученные из клеток кожи
William Collins, Gladstone Institutes
-
Автор
-
Редакторы
Эмбриологи в первой половине XX века считали, что клетка — она как человек: в «детстве» (недифференцированном состоянии) все дороги открыты, а «взрослой» специализированной клетке обратного пути уже нет. В 2012 году Нобелевская премия по физиологии и медицине вручена за опровержение этой догмы: Джон Гардон и Шинья Яманака награждены «за открытие факта, что зрелые клетки могут быть „перепрограммированы“ обратно в плюрипотентное состояние».
Нобелевскую премию по физиологии и медицине в 2012 году получили Джон Гардон (John B. Gurdon) и Шинья Яманака (Shinya Yamanaka) «за открытие факта, что зрелые клетки могут быть „перепрограммированы“ обратно в плюрипотентное состояние». Их открытие продолжает ряд исследований, опровергающих догмы: ранее считалось, что процесс клеточной дифференциации — это «билет в один конец», и клетки, обретшие специализацию, уже никогда не могут вернуться в первичное состояние, когда все пути к дифференциации в различные клеточные линии еще открыты. (Такое состояние называют плюрипотентным.) В 1962 году британский биолог развития Гардон заложил первый камень в фундамент нового здания, показав, что пересадка ядра эпителиальной клетки взрослой лягушки в икринку, лишенную клеточного ядра, успешно дает начало нормальному головастику, в свою очередь развивающемуся во взрослую лягушку. Это исследование стало предтечей более поздних экспериментов по клонированию животных.
Однако все еще было непонятно, можно ли целую клетку также заставить «де-дифференцироваться», а потом — превратиться в любую из множества других специализированных клеток. В 2006 году положительный ответ на этот вопрос дал японец Шинья Яманака, использовавший небольшой набор транскрипционных факторов для такого «перепрограммирования». Полученные им клетки получили название индуцированных плюрипотентных стволовых клеток (ИПСК).
Оба этих открытия показали, что казавшееся незыблемым состояние дифференциации при «умелом» воздействии вполне можно отменить и полностью изменить тот путь, по которому предстоит развиваться клетке. Работы этих ученых открыли баснословные перспективы в биологии и медицине.
Предыстория
В процессе нормального развития каждая клетка проходит путь от изначального недифференцированного состояния, характерного для оплодотворенной яйцеклетки (зиготы) и клеток раннего эмбриона, до специализированных клеточных форм, медленно делящихся и служащих для выполнения всего спектра клеточных функций (рис. 1а). Наиболее «многофункциональную» клетку — зиготу — называют тотипотентной, то есть, дающей начало абсолютно всем другим типам клеток.
По мере развития, клетки становятся все более специализированными и все менее подверженными «неожиданным» превращениям. Во взрослом организме число стволовых клеток невелико, и они располагаются в строго определенных местах (например, костном мозге), играя роль источника для пополнения популяции дифференцированных клеток. Эта закономерность и сформировала представление, что развитие клеток возможно лишь в одном направлении, и никогда дифференциация не обернется вспять. Конрад Уэддингтон (Conrad Hal Waddington) использовал метафору горного ландшафта, в которой плюрипотентная клетка находится на вершине горы, а специализированные клетки лежат в долинах, «скатываясь» каждая по своей траектории (изображающей путь дифференциации) (рис. 1б). Эта метафора подчеркивает сложность или невозможность обратного пути «в гору» и, значит, превращения одних клеток в другие.
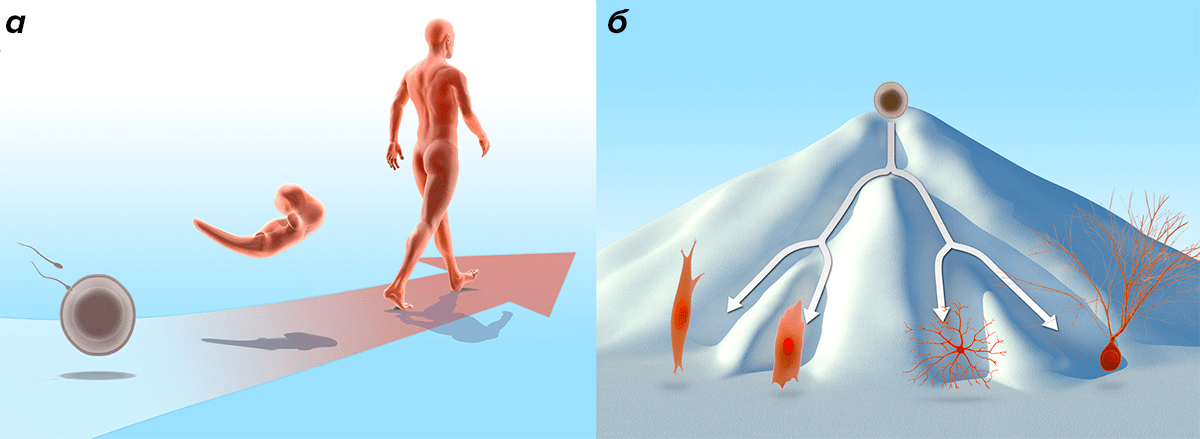
Рисунок 1. Развитие организма и дифференциация клетки. а — Нормальное развитие человека из оплодотворенной яйцеклетки до взрослого организма иллюстрирует идею однонаправленного процесса развития. б — Иллюстрация Уэддингтона [1] для процесса клеточной дифференциации. «Эпигенетический ландшафт» задает путь, который проходит каждая клетка в процессе обретения специализации. Эти картина призвана подчеркнуть, что путь «обратно» невозможен или сильно затруднен.
Однако теоретическая возможность «перепрограммирования» не исключалась полностью; Ханс Шпеман, нобелевский лауреат по физиологии и медицине 1935 года, первым предложил идею «пересадки» ядер дифференцированных клеток в цитоплазму яйцеклетки, чтобы изучить способность к дифференциации.
Перепрограммирование с помощью ядра соматической клетки
Первые попытки пересадки ядер были сделаны не Гардоном; еще в 1952 году Бриггс (Robert Briggs) и Кинг (Thomas King) разработали технологию «пересадки» ядра соматической клетки лягушки Rana pipiens в оплодотворенную икринку, ядро которой предварительно разрушали [2]. Амфибии хорошо подходят для таких экспериментов, потому что их икра крупная и развивается не внутриутробно. В этой работе было показано, что пересадка ядра из эмбриональных клеток действительно может дать начало нормальному головастику, но аналогичный опыт с более дифференцированными клетками к успеху не привел. Поэтому, хотя фактически они проделали ту же работу, что и Гардон несколькими годами позже, им пришлось сделать вывод, что дифференцированные клетки необратимы в своем развитии [3].
Джон Гардон, эмбриолог, закончивший Оксфорд, выбрал для своих опытов другую лягушку — «ветерана» лабораторных исследований Xenopus laevis. Он уничтожал ядро яйцеклетки ультрафиолетовым светом и пересаживал в цитоплазму ядро от дифференцированной клетки эпителия, и в части опытов ему удалось получить нормально плавающих и развивающихся головастиков (рис. 2; [4]). Так что Гардону, в противоположность своим предшественникам, удалось показать именно то, что пересадка ядра от дифференцированных клеток способна вернуть генетическую программу к состоянию плюрипотентности. Однако много лет прошло, прежде чем научное сообщество восприняло эти революционные работы всерьез.
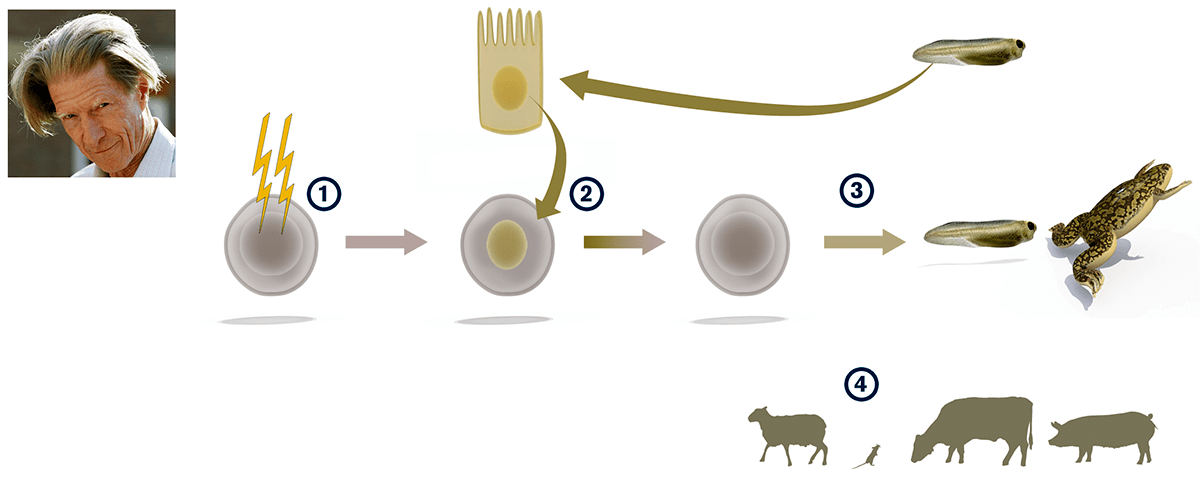
Рисунок 2. Перепрограммирование ядра клетки эпителия лягушки. Гардон использовал ультрафиолет, чтобы разрушить ядро икринки лягушки (1), а потом пересаживал туда другое ядро, полученное из эпителия головастика (2). В большинстве случаев клетки погибли, однако несколько из них развились в головастиков и затем — во взрослых лягушек (3). Этот опыт подтвердил, что генетическая информация сохраняется неизменной на протяжении всего срока жизни клетки, и может в подходящих условиях быть задействована вновь. Более поздние исследования, основанные на том же принципе, привели к клонированию млекопитающих (4).
Исследования Гардона подвели подкоп под парадигму необратимости развития, впервые наглядно продемонстрировав, что ядро дифференцированной клетки вполне может быть возвращено на плюрипотентный этап и дать начало всем типам соматических и половых клеток, — если его поместить в цитоплазму яйцеклетки, «настроенной» на этот режим.
Атака клонов
Работы Гардона положили начало технологии, называемой терапевтическим клонированием (somatic cell nuclear transfer). В 1997 году с помощью этого метода (конечно, с существенными изменениями) появилась на свет знаменитая овечка Долли [5]. Важным дополнением стало то, что ядро перед пересадкой ввергали в покоящееся состояние, что позволяло лучше «синхронизовать» ядро с клеткой, его лишенной. С тех пор уже удалось клонировать довольно много млекопитающих — не только овцу, но и мышь, корову, свинью, волка и степного кота. Метод пересадки ядер также позволил совершить ряд важных открытий в иммунологии.
Эра перепрограммированных клеток
Гардон наглядно доказал, что перенос ядра в окружение раннего эмбрионального развития способен «перезапустить» программу развития. Однако можно ли такое сделать, не извлекая ядро из клетки? Многие ученые продолжали считать это невозможным, полагая эпигенетические изменения, произошедшие в дифференцированной клетке, слишком далеко зашедшими, чтобы можно было их обратить вспять. Наверное, так считал и Яманака, когда он начал заниматься эмбриональными стволовыми клетками (ЭСК) [6], впервые выделенными и культивированными Мартином Эвансом (лауреатом Нобелевской премии по физиологии и медицине 2008 года [7]).
Лаборатория Яманаки работала над поиском факторов, поддерживающих в ЭСК программу плюрипотентности. Было найдено несколько десятков генов, активность которых в ЭСК была намного выше, чем в дифференцированных клетках, и, кроме того, уже открыли, что слияние ЭСК и специализированной клетки может дать две плюрипотентные клетки [8].
Вооруженная этим знанием, группа Яманаки внедрила в клетку (выбрали фибробласт) вектор с 24 генами, заставившими часть клеток дать колонии, подобные стволовым клеткам, и принялась по одному удалять гены из этого набора. В результате был установлен список из всего четырех генов, необходимых для «перепрограммирования» клетки: Myc, Oct3/4, Sox2 и Klf4 (рис. 3) [9]. Полученные клетки, названные Яманакой индуцированными плюрипотентными стволовыми клетками (ИПСК), получались в результате изобретенной процедуры с крайне низким выходом, но применяемые технологии селекции позволяют обнаружить даже одну перепрограммированную клетку на сотни тысяч. Далее последовала серия работ этой и других лабораторий, в которых исследователи оптимизировали состав перепрограммирующих факторов и способ введения вектора в клетку, чтобы повысить эффективность перепрограммирования и снизить вероятность образования опухолевых клеток в результате вызываемой метаморфозы [10].
Об этих и других работах в новой и новейшей истории исследований стволовых клеток «биомолекула» рассказывала в двух больших обзорах: «Была клетка простая, стала стволовая» [10] и «Ствол и ветки: стволовые клетки» [11].

Рисунок 3. Способ перепрограммирования специализированной клетки в стволовую. Начиная с набора 24 транскрипционных факторов и постепенно сужая этот перечень (1), Такахаши и Яманака установили, что всего четыре гена (Myc, Oct3/4, Sox2 и Klf4) могут преобразить фибробласт, вернув его в состояние плюрипотентности (2) [9]. Полученные ИПСК (3) могут давать начало тератомам, что используется как маркер плюрипотентной клетки, а также использоваться в технологии получения химерных мышей (традиционно, для этого использовали ЭСК [7]).
Открытие Яманаки — важнейшее фундаментальное открытие в биологии, поскольку именно оно впервые продемонстрировало, что дифференцированная клетка может снова вернуться в «детство» и стать плюрипотентной. Весьма простая технология получения ИПСК мгновенно была взята на вооружение сотнями лабораторий по всему миру.
Перспективы использования стволовых клеток в медицине
С момента появления технология получения ИПСК была существенно усовершенствована. В частности, теперь не нужно использовать векторы на основе ретровирусов, которые встраиваются в произвольное место генома и могут повредить его или даже запустить программу онкологической трансформации. Теперь используют аденовирусы или другие вирусные векторы, не встраивающиеся в хромосомы, а также РНК, белковые транскрипционные факторы и эписомальные плазмиды. В некоторых случаях число перепрограммирующих факторов можно снизить до одного — например, нейрональные стволовые клетки мыши превращаются в ИПСК введением одного только фактора Oct4 [12].
Открытие Яманаки также сообщило новый импульс поиску способов трансдифференцировки — то есть, превращению одного типа клеток в другой, минуя стадию стволовых клеток. Это возвращает нас в 1960–80-е годы, к работам по имагинальному диску дрозофилы и к таким генам как Antennapedia, MyoD, GATA1 и Pax5. В частности, уже тогда удалось превратить фибробласты в миобласты активацией гена MyoD [13]. Под впечатлением от работ Яманаки быстро нашли способ превратить экзокринные клетки поджелудочной железы в эндокринные [14], а фибробласты — в кардиомиоциты [15]. Есть даже пример превращения друг в друга клеток разных зародышевых листков — мезодермальных фибробластов в эктодермальные нейроны (на что потребовалось три транскрипционных фактора) [16].
Наиболее трепетные ожидания, связанные со стволовыми клетками, заключаются в возможности замещать больные или утраченные клетки прямо в ткани, восстанавливая организм буквально по клеточкам. В самом общем виде такая формула подходит для лечения практически любой болезни — хоть Альцгеймера, хоть Паркинсона, хоть диабета, хоть последствий инфаркта. Конечно, это все находится в туманной дымке светлого будущего, но некоторые реальные перспективы тоже есть. В частности, клеточная терапия с применением ИПСК обещает освободить врачей от проблемы иммунной несовместимости. Конечно, особое внимание нужно уделить безопасности — ведь, как уже было сказано, ИПСК могут иметь как привнесенные при перепрограммировании мутации, так и быть онкогенными сами по себе. В общем, несмотря на то, что ИПСК сулят совершенно баснословные преимущества для медицины, пока что имеется «снежный ком» проблем, связанных с ними [17].
Другая перспектива, уже ставшая твердой действительностью, — возможность получать линии бессмертных клеток (ИПСК), соответствующих различным редким генетическим заболеваниям, и изучать как саму болезнь, так и действие на нее разрабатываемых лекарственных средств (рис. 4) [18]. ИПСК уже получены для таких заболеваний как амиотрофический латеральный склероз (болезнь Шарко), синдром Ретта, спинальная мышечная атрофия (СМА), недостаточность антитрипсина α1, семейная гиперхолестеринемия, а также для различных кардиологических заболеваний. В некоторых из этих клеточных моделей удается связать наблюдаемый фенотип с болезнью: в частности, в случае клеток из СМА, это затухание функций моторных нейронов. Некоторый прогресс есть даже в изучении заболеваний со сложной генетикой, таких как шизофрения.
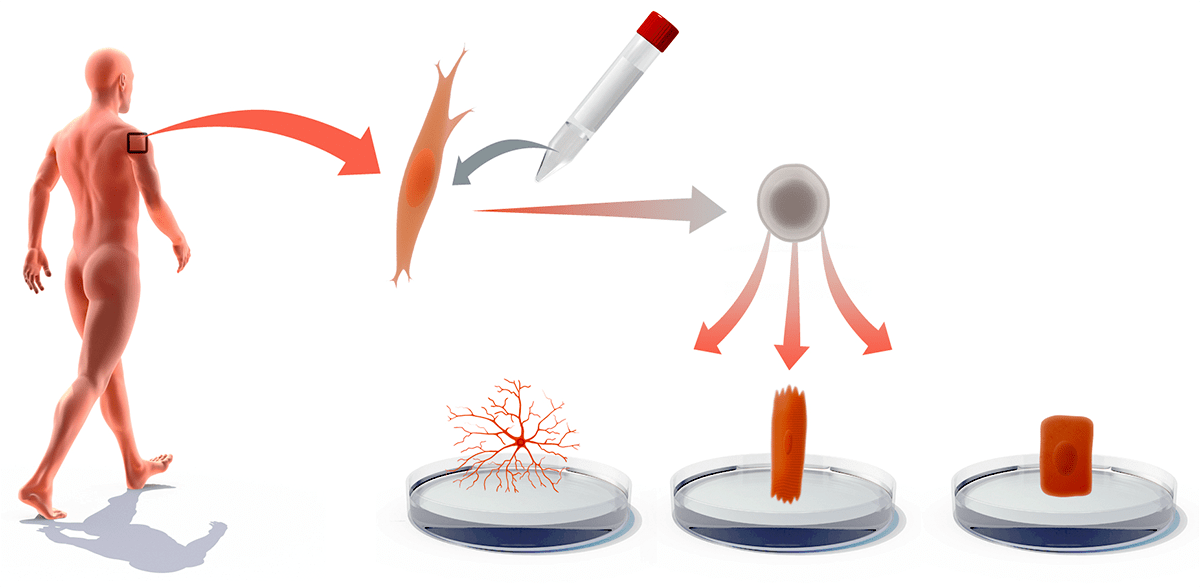
Рисунок 4. ИПСК в медицине. Из тканей пациентов, страдающих различными заболеваниями, можно выделить соответствующие клетки и превратить их в ИПСК. Колонии этих клеток можно дифференцировать в другие типы клеток и использовать их в лечении, или же изучать на них болезнь и действие лекарств.
Исследуют на культурах специфичных для конкретных болезней ИПСК и действие разрабатываемых лекарств. В частности, на модели наследственной вегетативной дистонии проведен скрининг базы химических веществ и найден прототип лекарства кинетин, который способен частично обратить последствия нарушенного сплайсинга гена IKBKAP, вызывающего эту болезнь [19]. Аналогично, показано лекарственное действие бета-блокаторов и блокаторов ионных каналов на ИПСК из модели синдрома удлинения QT интервала [20]. Так ИПСК уже вошли если не в клиническую, то в лабораторную практику и служат «испытательными стендами» для изучения различных болезней и действия на них разрабатываемых лекарств.
Открытие того, что зрелые дифференцированные клетки можно вернуть в плюрипотентное состояние или даже, минуя его, превратить один тип клеток в другой, стало поворотным в эмбриологии, биологии развития и всей молекулярной биологии. Это знание уже осветило все уголки физиологии и медицины, и практические применения в виде новых видов лечения наверняка не заставят себя ждать.
По материалам пресс-релиза Нобелевского комитета.
Литература
- Waddington C.H. The Strategy of the Genes. A Discussion of Some Aspects of Theoretical Biology. London: George Allen & Unwin, Ltd., 1957. — 262 p.;
- R. Briggs, T. J. King. (1952). Transplantation of living nuclei from blastula cells into enucleated frogs' eggs. Proceedings of the National Academy of Sciences. 38, 455-463;
- T. J. King, R. Briggs. (1955). CHANGES IN THE NUCLEI OF DIFFERENTIATING GASTRULA CELLS, AS DEMONSTRATED BY NUCLEAR TRANSPLANTATION. Proceedings of the National Academy of Sciences. 41, 321-325;
- Gurdon J.B. (1962). The developmental capacity of nuclei taken from intestinal epithelium cells of feeding tadpoles. J. Embryol. Exp. Morphol. 10, 622–640;
- I. Wilmut, A. E. Schnieke, J. McWhir, A. J. Kind, K. H. S. Campbell. (1997). Viable offspring derived from fetal and adult mammalian cells. Nature. 385, 810-813;
- Щадящие стволовые клетки;
- Нобелевскую премию по физиологии или медицине вручили за технологию нокаутирования мышей;
- Masako Tada, Yousuke Takahama, Kuniya Abe, Norio Nakatsuji, Takashi Tada. (2001). Nuclear reprogramming of somatic cells by in vitro hybridization with ES cells. Current Biology. 11, 1553-1558;
- Kazutoshi Takahashi, Shinya Yamanaka. (2006). Induction of Pluripotent Stem Cells from Mouse Embryonic and Adult Fibroblast Cultures by Defined Factors. Cell. 126, 663-676;
- Была клетка простая, стала стволовая;
- Ствол и ветки: стволовые клетки;
- Jeong Beom Kim, Boris Greber, Marcos J. Araúzo-Bravo, Johann Meyer, Kook In Park, et. al.. (2009). Direct reprogramming of human neural stem cells by OCT4. Nature. 461, 649-653;
- Robert L. Davis, Harold Weintraub, Andrew B. Lassar. (1987). Expression of a single transfected cDNA converts fibroblasts to myoblasts. Cell. 51, 987-1000;
- Qiao Zhou, Juliana Brown, Andrew Kanarek, Jayaraj Rajagopal, Douglas A. Melton. (2008). In vivo reprogramming of adult pancreatic exocrine cells to β-cells. Nature. 455, 627-632;
- Masaki Ieda, Ji-Dong Fu, Paul Delgado-Olguin, Vasanth Vedantham, Yohei Hayashi, et. al.. (2010). Direct Reprogramming of Fibroblasts into Functional Cardiomyocytes by Defined Factors. Cell. 142, 375-386;
- Zhiping P. Pang, Nan Yang, Thomas Vierbuchen, Austin Ostermeier, Daniel R. Fuentes, et. al.. (2011). Induction of human neuronal cells by defined transcription factors. Nature. 476, 220-223;
- Снежный ком проблем с плюрипотентностью;
- Tamer T Onder, George Q Daley. (2012). New lessons learned from disease modeling with induced pluripotent stem cells. Current Opinion in Genetics & Development. 22, 500-508;
- Gabsang Lee, Eirini P. Papapetrou, Hyesoo Kim, Stuart M. Chambers, Mark J. Tomishima, et. al.. (2009). Modelling pathogenesis and treatment of familial dysautonomia using patient-specific iPSCs. Nature. 461, 402-406;
- Ilanit Itzhaki, Leonid Maizels, Irit Huber, Limor Zwi-Dantsis, Oren Caspi, et. al.. (2011). Modelling the long QT syndrome with induced pluripotent stem cells. Nature. 471, 225-229.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚