Таблетка от травмы: обзор экспериментальных методов лечения мышечных патологий
16 апреля 2026
Таблетка от травмы: обзор экспериментальных методов лечения мышечных патологий
- 366
- 0
- 2
Рисунок в полном размере.
сгенерировано Fusion Brain
-
Авторы
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Современные подходы к лечению спортивных мышечных травм часто направлены на подавление симптомов, но не обеспечивают полноценного восстановления ткани. В обзоре рассматриваются перспективные методы, направленные на прямую стимуляцию регенеративных процессов. Среди них — целевая доставка факторов роста с помощью биосовместимых наночастиц, избирательное удаление стареющих клеток сенолитиками для улучшения среды регенерации и оптимизация режима приема глюкокортикоидов, позволяющая использовать их репаративный потенциал со сниженными побочными эффектами. Анализ показывает, что будущее терапии мышечных повреждений лежит в создании комбинированных и персонализированных стратегий, которые не подавляют, а регулируют естественные механизмы восстановления.
Конкурс «Био/Мол/Текст»-2025/2026
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2025/2026.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

Партнер номинации — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Мышечная ткань — это динамичная и высокоорганизованная система, находящаяся в состоянии постоянного баланса. На ее здоровье влияет множество факторов: физическая активность, питание [1], возраст и наличие патологий наподобие рака [2]. Фундаментом же ее феноменальной способности к регенерации служат клетки-сателлиты (или миосателлиты) — стволовые клетки мышц, которые в спящем состоянии дожидаются сигнала к действию [3].
Пример сложности мышечной ткани — ее белковый баланс. В здоровой мышце существует равновесие между синтезом новых белков и удалением старых или поврежденных. Однако этот хрупкий гомеостаз легко нарушается. Причины могут быть разными: острая травма, хроническое перенапряжение, дегенеративные или наследственные заболевания вроде мышечной дистрофии. Интересно, что даже нарушения в метаболизме (к примеру, ожирение) накладывают свой отпечаток — например, изменяя функцию мышечных митохондрий и их реакцию на физические нагрузки [4].
Парадоксально, но при такой сложности системы в современных принципах лечения мышечных повреждений зачастую отсутствует прочная научная основа. Именно это противоречие подчеркивает острую необходимость в создании принципиально новых, высокоточных терапевтических стратегий. Понимание сложной взаимосвязи всех факторов, влияющих на мышцу, — ключ к разработке эффективных методов профилактики и лечения. Сегодня научный фронт смещается в сторону подходов, которые не просто подавляют симптомы, а целенаправленно стимулируют и усиливают врожденные механизмы заживления, обеспечивая полноценное структурное и функциональное восстановление [5].
Мы рассмотрим некоторые новаторские способы терапии травм и болезней мышц — от липосомных систем доставки лекарств до глюкокортикоидов. Все эти решения пока не дошли до применения на практике наравне с физической реабилитацией, но в будущем могут стать аналогами зелий лечения и аптечек в видеоиграх — быстрым и эффективным способом восстановления мышц.
Наноматериалы на основе липосом
Липосомы — это маленькие сферические везикулы, образованные из одного и более билипидных слоев.
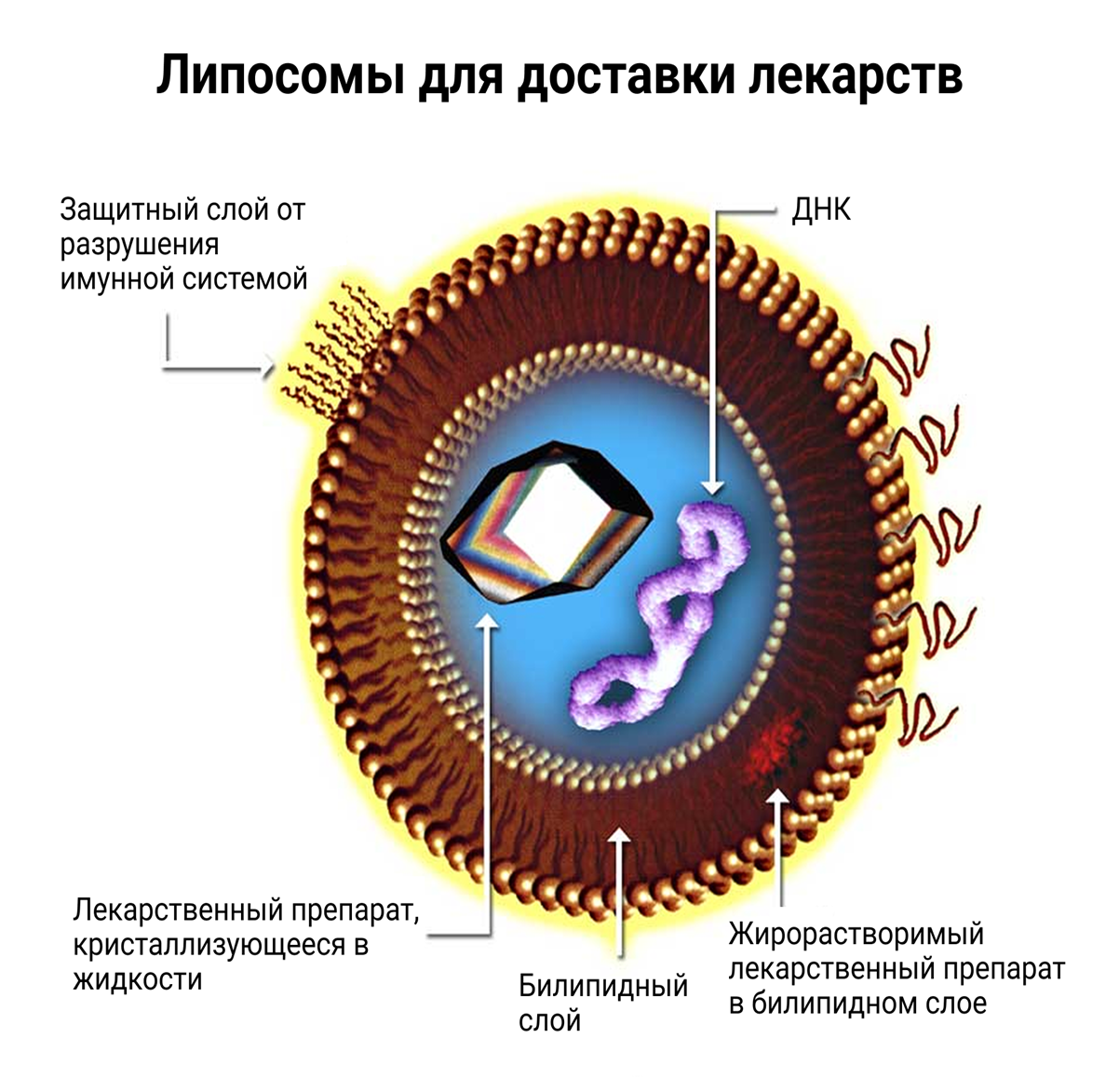
Рисунок 1. Строение липосомы, доработанной для доставки лекарств.
адаптировано из «Википедии»
Малоизвестный, но немаловажный вклад в фармакологию и в применение искусственных фосфолипидных мембран внес ученый Владимир Торчилин. Именно он был одним из руководителей международной группы, в девяностые годы разрабатывавшей ПЭГ-оболочку (оболочку из полиэтиленгликоля), благодаря которой вещества могут дольше циркулировать в крови, а следовательно, с большей вероятностью доходить до мишени [6].
Когда речь заходит о точечной доставке, липосомы (рис. 1) становятся настоящими «интеллектуальными курьерами». Их можно настраивать для целевой доставки в конкретные типы тканей — это применяют, к примеру, для терапии опухолей. Для этого на их поверхность помещают специфические молекулы-лиганды (антитела [7], аптамеры [8] или пептиды [9]), которые, как ключ к замку, подходят к рецепторам на клетках. Липосомы точно так же можно использовать для повышения усвояемости и стабильности препаратов и снижения действия побочных эффектов [10]. Такой подход позволяет минимизировать побочные эффекты и значительно повысить концентрацию лекарства именно в очаге повреждения, будь то противовоспалительное средство или фактор роста.
Липосомы способны переносить не только базовые препараты, но и более сложно действующие молекулы. Например, с их помощью можно доставлять малую интерферирующую РНК (миРНК) [11], чтобы уничтожать мРНК-транскрипты генов. Липосомы позволяют миРНК дольше находиться в кровотоке (по сравнению с 15 минутами без липосом), эффективнее проникать в ткани и лучше абсорбироваться клетками [12]. Благодаря миРНК мы можем снижать экспрессию белков, мешающих регенерации, к примеру, миостатина [13].
Функции миРНК уже применяются в некоторых лекарствах. Onpattro [14] — это первый препарат с малым интерферирующим РНК для лечения наследственного транстиретин-опосредованного амилоидоза [15]. При этом миРНК переносится как раз липосомными наноносителями, нацеленными на гепатоциты.
Несмотря на успехи, у липосомальной терапии есть свои недостатки. Главные из них — это стабильность частиц при хранении, сложность масштабирования производства и необходимость дальнейшего повышения точности доставки. Будущие исследования направлены на создание «умных» липосом нового поколения. Их будут делать еще более «незаметными» для иммунитета и научат реагировать на специфические сигналы в поврежденной мышце, например, на изменение pH или наличие определенных ферментов. Это позволит им высвобождать лекарство строго в нужном месте и в нужное время, открывая путь для персонализированной терапии мышечных травм.
Они показали себя с хорошей стороны в доставке лекарств не только для лечения мышц. Липосомы обладают высокой биосовместимостью и биоразлагаемостью, а также высвобождают лекарства с постоянной скоростью, что дает долгий терапевтический эффект. Кроме того, их структуры продолжают совершенствоваться, что открывает перспективы в уменьшении иммунного ответа и улучшения специфичности.
Сокращение штата. Удаление SA β‐Gal+ клеток с помощью сенолитиков улучшает регенерацию мышц у старых мышей
Активация уже упомянутых нами миосателлитов улучшает регенерацию мышц [16] — однако есть клетки, накопление которых мешает восстановлению.
Старые клетки в мышцах несут как положительную, так и отрицательную роль в регенерации. Их полное отсутствие замедляет регенерацию, однако избыток старых клеток также ей мешает. Согласно закону толерантности Шелфорда, организмам для существования нужны не минимальные или максимальные, а оптимальные для их вида условия — точно так же и в мышцах должно быть определенное количество старых клеток. Американская научная статья 2021 года изучает попытку влиять на здоровье мышцы через уменьшение числа постаревших клеток.
SA beta-Gal+ клетки (рис. 2), то есть имеющие повышенный уровень экспрессии бета-галактозидазы (фермента, катализирующего гидролиз лактозы), своим накоплением предположительно мешают регенерации мышц [17]. С избытком таких клеток можно бороться препратами-сенолитиками. Авторы статьи предлагают применять сенолитический коктейль (видит Бог, лечимся!) — смесь из дазатибина и кверцетина. Сенолитики избирательно активируют апоптотические пути в старых клетках. В своем эксперименте они вводили его как молодым, так и старым мышам, и сравнивали их физические показатели, уровень регенерации, число миосателлитов и некоторые другие показатели.
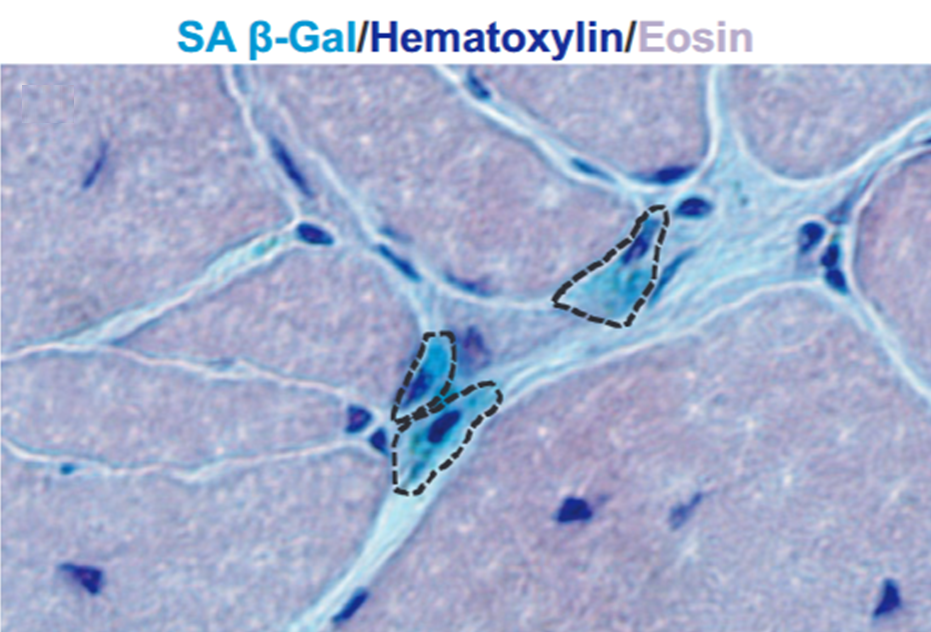
Рисунок 2. Срез мышцы с SA β-Gal клетками, выделенными пунктирной линией.
адаптировано из [7]
В итоге сокращение числа старых клеток в мышцах возрастных мышей способствовало ускорению регенерации и увеличению числа миосателлитов, повлияло на экспрессию генов в энергетических метаболических путях. При этом введение сенолитического коктейля молодым мышам оказало слегка негативный эффект — уменьшенный размер мышечных волокон, хотя исследования in vitro предполагают повышенную пролиферацию миосателлитов.
Такой результат объясняется тем, что у молодых мышей возрастных клеток не так много, как у старых мышей. Возрастные клетки у молодых мышей синтезируют метаболиты, регулирующие регенерацию мышцы и деление миосателлитных клеток. Удаление старых клеток нарушает естественные механизмы поддержания мышечного гомеостаза, что приводит к снижению размера волокон. Однако у старых мышей возрастные клетки находятся в избытке и больше вредят регенерации мышц, нежели способствуют ей. Удаление этого вредного пула клеток снимает тормоз с регенеративных процессов — но только у возрастных мышей; применение сенолитиков для улучшения регенерации молодых мышц, скорее всего, не будет иметь смысла.
Нанотерапия для восстановления мышц: целевая доставка ростовых факторов
В основе этого подхода лежит использование синтетических наночастиц (ПЛГА-ПЭГ), которые работают как высокоточные курьеры. Их задача — доставить прямо в поврежденную мышцу фактор роста фибробластов-2 (FGF-2) — ключевой белок, запускающий процессы регенерации [18].
ПЛГА-ПЭГ — это не одно вещество, а конструктор для создания умных нанокурьеров. Расшифруем:
- ПЛГА (полилактид-гликолид) — это биоразлагаемый полимер, который образует «ядро» наночастицы. В него, как в контейнер, и помещается лекарство (в нашем случае — FGF-2). Его главное свойство — он медленно и безопасно распадается в организме, постепенно высвобождая свое содержимое. Это обеспечивает пролонгированный лечебный эффект [19].
- ПЭГ (полиэтиленгликоль) — его наносят на поверхность ПЛГА-ядра. Это покрытие делает частицу «невидимой» для иммунной системы, позволяя ей дольше циркулировать в крови. Без ПЭГ оболочки частицы быстро захватываются и выводятся из организма, не успев добраться до цели [20].
Я был невидим и еще только начинал сознавать, какие преимущества это давало мне
FGF-2 — это сигнальная молекула, которую наш организм производит сам при повреждениях. Его ключевые задачи:
- Активирует клетки-сателлиты, заставляя их просыпаться, делиться и превращаться в новые мышечные волокна [21].
- Запускает ангиогенез (процесс образования новых капилляров), обеспечивая поврежденный участок кислородом и питательными веществами для успешного заживления [22].
- Помогает управлять воспалительной реакцией, чтобы она была эффективной, но не чрезмерной [23].
Проблема в том, что при серьезной микротравме собственного FGF-2 может не хватать, а введенный извне будет быстро разрушаться.
Наночастицы решают эту проблему, доставляя фактор роста в очаг повреждения и сохраняя его там. Целевая нанодоставка препаратов (к примеру, ростовых факторов) — это мощная стратегия для лечения мышечных травм. Она открывает путь к созданию высокоэффективных терапевтических средств, которые не просто снимают симптомы, а активно и направленно стимулируют естественные механизмы заживления микротравм, обеспечивая полноценное структурное и функциональное восстановление мышцы [24].
Нестероидные противовоспалительные препараты (НПВП)
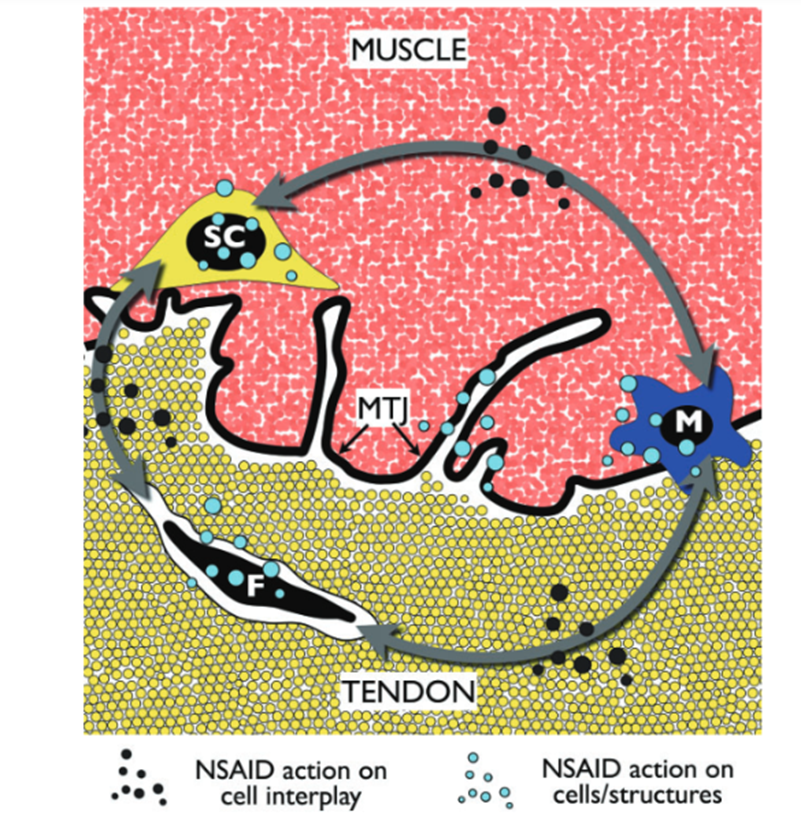
Рисунок 3. Возможные места воздействия НПВП для восстановления поврежденных мышц, сухожилий при растяжении. Миотендионозное соединение (MTJ) пока что мало изучено. Вероятно, мишенями на клеточном уровне являются клетки-сателлиты (SC), макрофаги (M) и фибробласты (F), а также передача сигналов между ними.
В отличие от целевой нанотерапии, нестероидные противовоспалительные препараты (НПВП), такие как ибупрофен, — это действующая без разбора тяжелая артиллерия (рис. 3). Это один из самых распространенных в спорте классов анальгетиков, которые часто применяются при первых признаках мышечной травмы или даже профилактически, несмотря на отсутствие убедительных клинических данных об их эффективности для ускорения восстановления [25].
НПВП работают как мощные ингибиторы циклооксигеназ (ЦОГ) — ферментов, запускающих синтез простагландинов, ключевых медиаторов боли и воспаления [26]. Их задача — быстро заглушить воспалительный ответ и снять болевые ощущения. Однако воспаление — это не только боль и отек. Это сложный, запрограммированный процесс, который критически важен для последующей регенерации. Подавляя его, НПВП могут нарушить естественную последовательность восстановления тканей.
Исследования показывают неоднозначную картину: кратковременно НПВП действительно могут уменьшать боль и воспаление, создавая иллюзию быстрого улучшения. В долгосрочной перспективе картина меняется. Данные, в том числе полученные на животных моделях, свидетельствуют, что первоначальный положительный эффект может нивелироваться или даже сменяться замедленным восстановлением; при применении ингибитора Cox-2 NS-398 мышиные мышцы росли на 75% хуже, чем без него [27]. Это выражается в:
- снижении количества клеток-сателлитов и макрофагов — ключевых игроков в регенерации мышц. НПВП могут подавлять их пролиферацию и активность, нарушая процесс «ремонта» [28];
- негативном влиянии на восстановление соединительной ткани, включая сухожилия и связки. Это особенно критично для лечения растяжений, где повреждение происходит как раз в области контакта мышцы и сухожилия (миотендинозное соединение) [29].
Таким образом, несмотря на широко распространенное использование НПВП при мышечных травмах, их целесообразность находится под сомнением. В то время как нанотерапия направлена на усиление и оптимизацию естественных механизмов заживления, НПВП, по сути, их подавляют. Это заставляет пересмотреть их роль: они могут быть эффективны для ситуативного контроля боли, но их применение требует осторожности, так как может непреднамеренно затормозить полноценное структурное и функциональное восстановление мышцы.
Глюкокортикоиды
Глюкокортикоиды (ГК), такие как преднизон и дефлазакорт, — это мощные противовоспалительные средства, которые уже десятилетиями используются для лечения мышечных заболеваний, в частности, мышечной дистрофии Дюшенна. Несмотря на их доказанную способность замедлять прогрессирование болезни, применение глюкокортикоидов связано со стероидной миопатией, ведущей к мышечной слабости и атрофии. Этот парадокс — способность одновременно лечить и повреждать мышцу — долгое время оставался загадкой. Новые исследования раскрывают механизм этого двойного действия и предлагают стратегию для его контроля.
Оказалось, что ГК воздействуют на фундаментальную характеристику — целостность клеточной мембраны мышечного волокна (сарколеммы). При травме или в результате дистрофического процесса сарколемма повреждается. ГК, как было обнаружено, напрямую ускоряют ее репарацию. Согласно американскому исследованию 2017 года, всего одна инъекция преднизона или дефлазакорта, введенная мышам, значительно улучшает восстановление их мембраны после лазерного повреждения [30]. Этот эффект обеспечивается за счет усиленной выработки ключевых репаративных белков — аннексинов A1 и A6, которые мгновенно устремляются к месту повреждения, формируя «заплатку».
Однако при хроническом применении проявляется вторая, разрушительная сторона ГК. Длительный ежедневный прием запускает в мышцах атрофическую программу: активируется ген Fbxo32 (кодирующий белок атрогин-1) и подавляется транскрипционный фактор Klf15, критический для мышечного метаболизма и выносливости. Это приводит к уменьшению мышечной массы и силы.
Решение лежит на поверхности — изменить режим дозирования. Ежедневный прием для мышей все в том же исследовании действительно усиливает репарацию и снижает фиброз, но эти положительные эффекты полностью перекрываются развивающейся атрофией; еженедельный (импульсный) прием оказывает столь же мощное положительное действие на заживление мембран и борьбу с воспалением, но при этом не запускает механизмы атрофии. Более того, такой режим способствует улучшению мышечной функции, силы и выносливости как при острой травме, так и при хронической дистрофии.
Итак, глюкокортикоиды представляют собой двоякое решение проблемы. Они отлично стимулируют естественные механизмы репарации ран, однако ключ к успешной терапии лежит в выборе правильного режима дозирования. Это позволит извлечь максимальную пользу от усиления регенерации, избежав при этом разрушительных последствий для мышечной массы.
Шаг в сторону от травм. Кахексия и GLP-1R агонисты
Кахексией называют синдром потери мышечной массы, не связанной с недостатком питания и требующей самостоятельной терапии [31]. Некоторые компании уже тестируют препараты для лечения кахексии как осложнения рака. К примеру, Pfizer протестировала на пациентах с кахексией понсегромаб — гуманизированное моноклональное антитело, ингибирующее часто экспрессирующийся при кахексии фактор роста GDF-15. Спустя 12 недель пациенты, принимавшие 400 мг препарата, в среднем имели вес на 2,81 кг больше и были физически активнее, чем контрольная группа (принимавшая плацебо) [32].
Мышцы требуют много энергии, получение которой из кровотока регулирует множество рецепторов — среди них интерес для терапии, в частности, представляет GLP-1R («рецепторы глюкагон-подобного пептида») [33]. Современные работы исследуют влияние этого рецептора на массу и метаболизм мышц [34]. Агонисты этого рецептора применяются для лечения ожирения, но вместе с потерей веса происходит и потеря мышечной массы. Компания Scholar Rock исследует вещества, позволяющие сохранять мышцы во время GLP-1R терапии, в частности, антитело антимиостатина SRK-439 (успешный пример сохранения мышц через ингибирование миостатина), которое позволило увеличить безжировую массу в 2 раза у молодых мышей и в 50 раз у старых и сохранить силу хвата [35]. Проведение дальнейших исследований в этой сфере позволит применять разработанные вещества для терапии или предотвращения кахексии.
Проблемы разработки мышечных препаратов
Современная фармакология сталкивается с рядом фундаментальных вызовов при создании терапий, направленных на истинное восстановление мышечной ткани, а не просто на подавление симптомов.
- Как мы видели на примере глюкокортикоидов и стареющих клеток, ключевые механизмы заживления часто имеют две стороны. Воспаление необходимо для очистки раны, ангиогенеза в месте травмы и пролиферации новых клеток [35], но его избыток ведет к фиброзу. Старые клетки (SA β‐Gal+) в норме помогают регенерации, но их накопление с возрастом ее подавляет. Создать препарат, который точечно усиливает хорошую сторону процесса и подавляет плохую, — крайне сложная задача.
- Проблема доставки. Многие потенциально эффективные вещества — пептиды (как FGF-2), факторы роста или генетический материал — либо быстро разрушаются в кровотоке, либо не могут достичь своей мишени в достаточной концентрации. Системное введение часто требует высоких доз, что повышает риск побочных эффектов, как в случае с тестостероном.
- Мышечная ткань — это не просто скопление волокон. Это сложный орган, включающий нервы, сосуды, соединительную ткань, иммунные и сателлитные клетки. Эффективный препарат должен действовать не на одну, а на несколько мишеней в этой экосистеме, чтобы обеспечить структурное и функциональное восстановление.
- Подход «выключи боль и воспаление», воплощенный в НПВП, оказался тупиковым для полноценной регенерации. Подавляя естественные сигналы, такие препараты нарушают сложную хореографию восстановления, где боль и воспаление — ее неотъемлемые части. Это заставляет пересмотреть сам принцип симптоматической терапии при лечении травм.
Перспективы разработки лекарств от мышечных травм
Вышеуказанные проблемы подчеркивают, что будущее — за прецизионными методами лечения, которые не глушат процессы в организме, а тонко их перенастраивают.
Мы увидели, что регенерацию можно стимулировать, не только добавляя недостающее (клетки-сателлиты, тестостерон, FGF-2), но и убирая лишнее (стареющие клетки с помощью сенолитиков). Третий путь — усилить естественные механизмы, как это делают глюкокортикоиды в импульсном режиме, ускоряя репарацию мембран. Будущее — в комбинированных терапиях, которые будут одновременно активировать стволовые клетки, очищать микроокружение от мешающих факторов и усиливать внутренние восстановительные программы. Нанотехнологии, в частности, липосомы и полимерные наночастицы (ПЛГА-ПЭГ), открывают эру целевой доставки.
Развитие идет в сторону персонализации лечения. Становится ясно, что не существует универсального подхода. Терапия должна учитывать возраст пациента (как в случае с сенолитиками), тип травмы (острая, хроническая, дистрофия) и его генетический профиль. Например, для одного пациента оптимальной будет комбинация нанодоставки ростовых факторов, а для другого — периодический курс сенолитиков для омоложения мышечной ниши.
Восстановление мышц — это симфония, а не какофония случайных процессов. Современная наука учится не заглушать ее громкими, но грубыми аккордами НПВП, а дирижировать ею, тонко регулируя работу каждого инструмента — от клеток-сателлитов до стареющих клеток и факторов роста. Новые терапевтические стратегии, основанные на глубоком понимании биологии и использовании высокоточных средств доставки, открывают путь к настоящей регенеративной медицине, где целью является не просто отсутствие боли, а полное возвращение силы и функции.
Литература
- B. K. Pedersen, B. Saltin. (2015). Exercise as medicine - evidence for prescribing exercise as therapy in 26 different chronic diseases. Scand J Med Sci Sports. 25, 1-72;
- Michael Tieland, Inez Trouwborst, Brian C. Clark. (2018). Skeletal muscle performance and ageing. J cachexia sarcopenia muscle. 9, 3-19;
- Hang Yin, Feodor Price, Michael A. Rudnicki. (2013). Satellite Cells and the Muscle Stem Cell Niche. Physiological Reviews. 93, 23-67;
- Nigel Turner, Clinton R. Bruce, Susan M. Beale, Kyle L. Hoehn, Trina So, et. al.. (2007). Excess Lipid Availability Increases Mitochondrial Fatty Acid Oxidative Capacity in Muscle. Diabetes. 56, 2085-2092;
- Zirui Zhang, Pengfei Yao, Shuai Fan. (2024). Advances in regenerative rehabilitation in the rehabilitation of musculoskeletal injuries. Regenerative Medicine. 19, 345-354;
- Vladimir P. Torchilin. (2005). Recent advances with liposomes as pharmaceutical carriers. Nat Rev Drug Discov. 4, 145-160;
- Vladimir P. Torchilin. (2010). Passive and Active Drug Targeting: Drug Delivery to Tumors as an Example. Handbook of Experimental Pharmacology. 3-53;
- Aman P. Mann, Rohan C. Bhavane, Anoma Somasunderam, Brenda Liz Montalvo-Ortiz, Ketan B. Ghaghada, et. al.. (2011). Thioaptamer Conjugated Liposomes for Tumor Vasculature Targeting. Oncotarget. 2, 298-304;
- Madhumitha Ravikumar, Christa L. Modery, Timothy L. Wong, Anirban Sen Gupta. (2012). Peptide-Decorated Liposomes Promote Arrest and Aggregation of Activated Platelets under Flow on Vascular Injury Relevant Protein Surfaces in Vitro. Biomacromolecules. 13, 1495-1502;
- Shuang Wu, Jianqin Lu. (2025). Liposome‐Enabled Nanomaterials for Muscle Regeneration. Small Methods. 9;
- РНК-терапия: новая глава в истории медицины;
- A. S. Nosova, O. O. Koloskova, A. A. Nikonova, V. A. Simonova, V. V. Smirnov, et. al.. (2019). Diversity of PEGylation methods of liposomes and their influence on RNA delivery. Med. Chem. Commun.. 10, 369-377;
- NaJung Kim, James J. Yoo, Anthony Atala, Sang Jin Lee. (2016). Combination of small RNAs for skeletal muscle regeneration. The FASEB Journal. 30, 1198-1206;
- Первый препарат на основе РНК-интерференции: смерть мРНК — жизнь пациенту!;
- Руку, ногу и сердце: редкий АТТR-амилоидоз;
- Bert Blaauw, Carlo Reggiani. (2014). The role of satellite cells in muscle hypertrophy. J Muscle Res Cell Motil. 35, 3-10;
- Cory M. Dungan, Kevin A. Murach, Christopher J. Zdunek, Zuo Jian Tang, Georgia L. Nolt, et. al.. (2022). Deletion of SA β‐Gal+ cells using senolytics improves muscle regeneration in old mice. Aging Cell. 21;
- Abha Sahni, Sanjeev K. Sahni. (2026). Fibrinogen and Fibrin as Growth Factor Regulators: Pathological Implications, and Translational Opportunities. Biomolecules. 16, 335;
- Yue Su, Bolun Zhang, Ruowei Sun, Wenfang Liu, Qubo Zhu, et. al.. (2021). PLGA-based biodegradable microspheres in drug delivery: recent advances in research and application. Drug Delivery. 28, 1397-1418;
- Anisha A. D’souza, Ranjita Shegokar. (2016). Polyethylene glycol (PEG): a versatile polymer for pharmaceutical applications. Expert Opinion on Drug Delivery. 13, 1257-1275;
- Yewei Liu, Martin F. Schneider. (2014). FGF2 activates TRPC and Ca2+ signaling leading to satellite cell activation. Front. Physiol.. 5;
- Natalina Quarto, Siddharth Menon, Jason L Guo, Ankit Salhotra, Michael T Longaker. (2026). FGF2 alters the calvarial suture niche homeostasis shifting skeletal stem cell/progenitors toward an osteo-angiogenic coupling fate. Stem Cells Translational Medicine. 15;
- Kübra Özdemir, Yeliz Demir. (2026). Biochemical markers of muscle damage and recovery: Insights from exercise physiology and molecular biology. Tissue and Cell. 101, 103406;
- Gun-Jae Jeong, Hannah Castels, Innie Kang, Berna Aliya, Young C. Jang. (2022). Nanomaterial for Skeletal Muscle Regeneration. Tissue Eng Regen Med. 19, 253-261;
- A. L. Mackey, U. R. Mikkelsen, S. P. Magnusson, M. Kjaer. (2012). Rehabilitation of muscle after injury – the role of anti‐inflammatory drugs. Scandinavian Med Sci Sports. 22;
- Praveen Rao, Edward E. Knaus. (2008). Evolution of Nonsteroidal Anti-Inflammatory Drugs (NSAIDs): Cyclooxygenase (COX) Inhibition and Beyond. J Pharm Pharm Sci. 11, 81;
- Margaret L Novak, William Billich, Sierra M. Smith, Kunal B. Sukhija, Thomas J. McLoughlin, et. al.. (2009). COX-2 inhibitor reduces skeletal muscle hypertrophy in mice. American Journal of Physiology-Regulatory, Integrative and Comparative Physiology. 296, R1132-R1139;
- U. R. Mikkelsen, H. Langberg, I. C. Helmark, D. Skovgaard, L. L. Andersen, et. al.. (2009). Local NSAID infusion inhibits satellite cell proliferation in human skeletal muscle after eccentric exercise. Journal of Applied Physiology. 107, 1600-1611;
- Ippokratis Pountos, Peter V. Giannoudis, Elena Jones, Anne English, Sarah Churchman, et. al.. (2011). NSAIDS inhibit in vitro MSC chondrogenesis but not osteogenesis: implications for mechanism of bone formation inhibition in man. Journal of Cellular and Molecular Medicine. 15, 525-534;
- Mattia Quattrocelli, David Y. Barefield, James L. Warner, Andy H. Vo, Michele Hadhazy, et. al.. (2017). Intermittent glucocorticoid steroid dosing enhances muscle repair without eliciting muscle atrophy. Journal of Clinical Investigation. 127, 2418-2432;
- Michael J. Tisdale. (2009). Mechanisms of Cancer Cachexia. Physiological Reviews. 89, 381-410;
- John D. Groarke, Jeffrey Crawford, Susie M. Collins, Shannon Lubaczewski, Eric J. Roeland, et. al.. (2024). Ponsegromab for the Treatment of Cancer Cachexia. N Engl J Med. 391, 2291-2303;
- Две стороны инкретинов: спасение от ожирения и новые угрозы;
- Zhikai Zheng, Yao Zong, Yiyang Ma, Yucheng Tian, Yidan Pang, et. al.. (2024). Glucagon-like peptide-1 receptor: mechanisms and advances in therapy. Sig Transduct Target Ther. 9;
- Helen Weavers, Will Wood, Paul Martin. (2019). Injury Activates a Dynamic Cytoprotective Network to Confer Stress Resilience and Drive Repair. Current Biology. 29, 3851-3862.e4.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚