Эпигенетические часы: сколько лет вашему метилому?
19 июня 2014
Эпигенетические часы: сколько лет вашему метилому?
- 4056
- 0
- 5
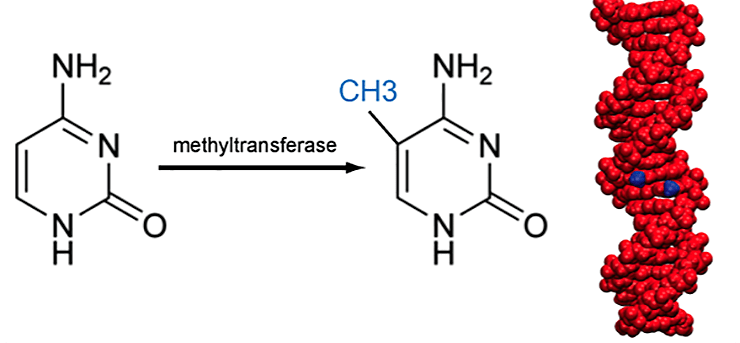
Иллюстрация процесса метилирования цитозина и его положения в молекуле ДНК
лаборатория теоретической и компьютерной биофизики Университета Иллинойса
-
Автор
-
Редакторы
Геном постоянно накапливает изменения. И если пару десятков лет назад представления об этих изменениях навевали мысли об эволюционных масштабах времени, то сейчас мы всё больше узнаем о том, как наш генетический материал меняется прямо на глазах. Молекулярные часы — методика оценки времени эволюционного расхождения видов по анализу замен в ДНК, — уже стали привычной темой для научно-популярной литературы и журналистики, а вот оценка возраста отдельных клеток и тканей организма привлекла внимание совсем недавно. И выясняется, что поиск молекулярных маркеров, позволяющих сказать, сколько лет вам и вашим клеткам, не заглядывая в паспорт, может быть интересен с очень многих точек зрения: от диагностики болезней до поиска преступников и изучения самого процесса старения.
Метилирование ДНК — это один из механизмов регуляции активности генов. Чаще всего метилированию подвергаются остатки цитозина в составе динуклеотида CpG. Причем метилируются цитозины обеих комплементарных цепей ДНК. С этими структурами в геноме потом могут связываться белки, привлекающие ферменты, способные переводить хроматин в неактивное состояние, отчего уровень экспрессии генов в этих областях снижается. Распределение таких сайтов по геному, а также сам процесс метилирования и его снятия, важно изучать сразу по многим причинам. Показано, что механизм метилирования задействован в геномном импринтинге, инактивации Х-хромосомы, подавлении активности мобильных генетических элементов и канцерогенезе [1]. Также уже какое-то время ясно, что профиль метилирования ДНК меняется с возрастом [2]. Однако пока что нет полной ясности относительно того, как и почему в определенных ситуациях метилируются те или иные CpG-сайты, хотя существуют методы полногеномного анализа распределения метилированных нуклеотидов (наиболее популярные технологии и киты разрабатывает компания Illumina).
Несмотря на наличие связи между паттерном метилирования и возрастом человека, до недавнего времени не удавалось по первому точно определить второе. И вот в прошлом году была опубликована прорывная работа в этой области [3]. Ее автор Стив Хорват (Steve Horvath) — специалист в области математики и биологической статистики из Калифорнийского университета в Лос-Анджелесе. Для того, чтобы получить алгоритм, способный оценивать возраст ткани по метилированию, Хорват использовал методику машинного обучения. Для этого он взял ранее опубликованные данные анализа метилирования геномов здоровых людей разных возрастов. Всего было проанализировано 82 набора данных, в которые входило 7844 образца тканей и клеток 51 типа. При этом для «тренировки» алгоритма было взято 39 наборов данных из всего массива. В ходе тренировки программе задаются как сайты метилирования, так и данные о возрасте, в результате чего алгоритм выявляет универсальные для всех наборов CpG-сайты, которые со статистической точки зрения вероятнее всего коррелируют с возрастом. На втором этапе Хорват использовал еще 32 набора для того, чтобы алгоритм уже сам оценивал возраст, а ученый мог оценить эффективность его работы. Последние 11 наборов были нужны для оценки возраста эмбриональных стволовых и индуцированных плюрипотентных клеток.
В результате проведенной работы алгоритм Хорвата выявил 353 сайта метилирования, которые в итоге легли в основу «эпигенетических часов». Анализ профиля метилирования в этих сайтах позволяет оценивать возраст тканей с погрешностью, не превышающей три года. Такой результат оказался во много раз лучше того, что могли дать ранее существовавшие биомаркеры старения (например, длина теломер). Оказалось, что для эмбриональных стволовых клеток и ИПК алгоритм Хорвата выдает значения, близкие к нулю; при этом была выявлена корреляция между определяемым возрастом и количеством пассажей клеток.
Важность наличия точных биомаркеров возраста тканей сложно переоценить. Во-первых, это может пролить свет на саму природу старения, поскольку указывает область, в которой можно искать процессы, к нему приводящие. Так, среди этих сайтов 193 имели положительную корреляцию со старением и со временем приобретали метилирование, а 160 — наоборот, со временем метилирование теряли. Среди генов, которые соседствуют с сайтами «эпигенетических часов», преобладают гены регуляторных белков, участвующих в регуляции клеточной гибели, пролиферации, дифференцировки, а также связанные с канцерогенезом.

Рисунок 1. Стив Хорват
Также, как показано в работе Хорвата, возраст некоторых тканей имел тенденцию отличаться от возраста самого индивида. Оказалось, что клетки груди у женщин, согласно метилированию, стареют на несколько лет быстрее, чем остальные ткани. Клетки раковых опухолей демонстрировали гораздо большее ускорение: на основе исследованных Хорватом образцов, средняя опухоль была «старше» владельца на 36 с небольшим лет. Поэтому анализ возраста метилома различных тканей может быть полезен с диагностической точки зрения. Вполне возможно, что удастся связать аномалии эпигенетического возраста с какими-то другими заболеваниями.
Еще одной областью, в которой может быть важно изучение паттернов метилирования эпигенетических часов, может стать криминалистика, поскольку благодаря этой методике можно будет определять возраст подозреваемого по оставленным на месте преступления образцам биологических тканей.
После выхода публикации Стива Хорвата методику стали проверять в других лабораториях. Коллективу компании Zymo Research в Калифорнии удалось даже показать, что программа Хорвата работает на генетическом материале клеток, выделенных из образцов мочи. Такие ткани не были представлены в исходной выборке, на которой разрабатывался метод. Вслед за публикацией Хорвата стали появляться работы, в которых эпигенетический возраст оценивается даже по меньшему числу сайтов метилирования [7], [8]. Сам доктор Хорват предоставил временный открытый доступ к своему алгоритму, разместив необходимые данные и ссылки для скачивания на сайте лаборатории.
По материалам Nature News [9].
Литература
- Peter A. Jones. (2012). Functions of DNA methylation: islands, start sites, gene bodies and beyond. Nat Rev Genet. 13, 484-492;
- Bruce Richardson. (2003). Impact of aging on DNA methylation. Ageing Research Reviews. 2, 245-261;
- Steve Horvath. (2013). DNA methylation age of human tissues and cell types. Genome Biology. 14, R115;
- Была клетка простая, стала стволовая;
- Ствол и ветки: стволовые клетки;
- Shinya Yamanaka. (2012). The Nobel Prize;
- Gregory Hannum, Justin Guinney, Ling Zhao, Li Zhang, Guy Hughes, et. al.. (2013). Genome-wide Methylation Profiles Reveal Quantitative Views of Human Aging Rates. Molecular Cell. 49, 359-367;
- Carola Weidner, Qiong Lin, Carmen Koch, Lewin Eisele, Fabian Beier, et. al.. (2014). Aging of blood can be tracked by DNA methylation changes at just three CpG sites. Genome Biol. 15, R24;
- W. Wayt Gibbs. (2014). Biomarkers and ageing: The clock-watcher. Nature. 508, 168-170;
- Сверим часы;
- Прообраз биологических часов;
- Найдена связь между обменом веществ и циркадным ритмом;
- Пилюли для эпигенома.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚