ИПСК для ЭКО: как клетки помогают мечтам о родительстве сбыться
24 февраля 2026
ИПСК для ЭКО: как клетки помогают мечтам о родительстве сбыться
- 207
- 0
- 1
Ладонь, держащая маленькую пробирку с подписью Fertilo, на самом деле держит возможность родительства для тех, кому судьба долго отказывала.
Рисунок в полном размере.
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Процедуры экстракорпорального оплодотворения и криоконсервации яйцеклеток уже давно требуют значительной модернизации. Патологии яичников остаются одной из наименее изученных областей, а одобренных методов лечения симптомов менопаузы до сих пор не существует. До 1993 года участие женщин в клинических исследованиях даже не было обязательным, что существенно ограничило понимание женской физиологии и специфики заболеваний. Все эти тезисы являются локомотивом для компании Gameto, которая стремится изменить подход к женскому здоровью с помощью новейших технологий. В основе ее исследований лежит использование индуцированных плюрипотентных стволовых клеток ─ инструмента, открывающего новые возможности в репродуктивной биологии и терапии возрастных изменений.
Конкурс «Био/Мол/Текст»-2025/2026
 Эта работа заняла второе место в номинации «Академия & Бизнес» конкурса «Био/Мол/Текст»-2025/2026.
Эта работа заняла второе место в номинации «Академия & Бизнес» конкурса «Био/Мол/Текст»-2025/2026.

Генеральный партнер конкурса и партнер номинации — международная инновационная биотехнологическая компания BIOCAD.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Биотехнологическая компания Gameto пока очень молодая, она была образована в 2021 году в США. Ее основатели — это Дина Раденкович и Мартин Варсавски, уже опытный на то время «серийный предприниматель» в сфере репродуктивного здоровья. За его плечами — создание сети клиник репродуктивной медицины Prelude Fertility, крупнейшей сети в Северной Америке, а также компании Overture Life, занимающейся автоматизацией эмбриологических лабораторий. Что касается Дины Раденкович, в 2023 году она была включена в список Forbes «30 до 30», и не просто так.
Уроженка Сербии, она получила двойную степень по медицине и физиологии в Университетском колледже Лондона. Уже работая в генетической лаборатории Гарварда, она сузила область своих исследований до проблем женского здоровья и долголетия. Как она сама отмечает, именно тогда к ней пришло понимание, что «яичники стареют быстрее всех органов», и именно они определяют скорость старения женщины в целом. Однако эффективных способов вмешательства в течение менопаузы до сих пор не изобретено.
До основания интересующей нас компании Дина была соучредителем и главным научным сотрудником Hooke London, элитной исследовательской клиники персонализированного долголетия в Лондоне. Она также занимала должность старшего научного сотрудника в Институте исследования старения имени Бака, где участвовала в разработке платформы Buck Institute Artificial Intelligence для поиска биомаркеров старения. Мало того, она свободно владеет восемью языками, три из которых — языки программирования. Похоже, афоризм о том, что талантливый человек талантлив во всем, в ее случае ─ не преувеличение, а факт.
Но давайте вернемся к Gameto. Основной фронт работы этой компании направлен на усовершенствование технологии так называемого созревания ооцитов (незрелых половых клеток женщины) in vitro для процедуры экстракорпорального оплодотворения (ЭКО). Более того, такая технология под названием Fertilo сейчас проходит III фазу клинических испытаний для подтверждения эффективности и безопасности. Про существующие фазы клинических, а также предшествующих им доклинических испытаний и их целей подробнее можно почитать в статье «Путь к тысячам аптек начинается с одной молекулы» [1] из спецпроекта о Клинических исследованиях.
В настоящее время компания активно сотрудничает с репродуктивными клиниками США, Перу, Австралии и Мексики с двумя целями: оценить ту самую эффективность и безопасность своего подхода, а также помочь людям получить долгожданный статус родителей. И в 2024 году с помощью Fertilo уже родился первый ребенок — девочка из Перу.
Изменения назревали давно
Статистические данные указывают на то, что каждая шестая женщина во многих европейских странах страдает от бесплодия. Многие не готовы смириться с таким диагнозом, и тогда вся надежда ложится на научные разработки. И такие разработки известны. Главная из них ─ это процедура экстракорпорального оплодотворения. В свое время данная технология действительно обеспечила грандиозный прорыв в лечении бесплодия, и ее изобретение и внедрение в клиническую практику даже отмечено Нобелевской премией, о чем вы можете почитать на «Биомолекуле» [2]. Однако, как известно, ЭКО далеко не всегда приводит к успешной беременности, и каждая попытка этой процедуры связана с определенными рисками для здоровья женщины.
Все дело в том, что в естественном менструальном цикле обычно созревает только одна готовая к оплодотворению яйцеклетка. Для процедуры ЭКО этого количества недостаточно. Поэтому, чтобы повысить шансы на успешное оплодотворение и последующую беременность, врачи проводят гормональную стимуляцию: в течение недели или двух недель пациентке назначают высокие дозы гормонов гонадотропинов. Эти гормоны запускают рост сразу нескольких фолликулов, позволяя получить несколько яйцеклеток за один цикл и тем самым многократно увеличить вероятность успеха процедуры (рис. 2).
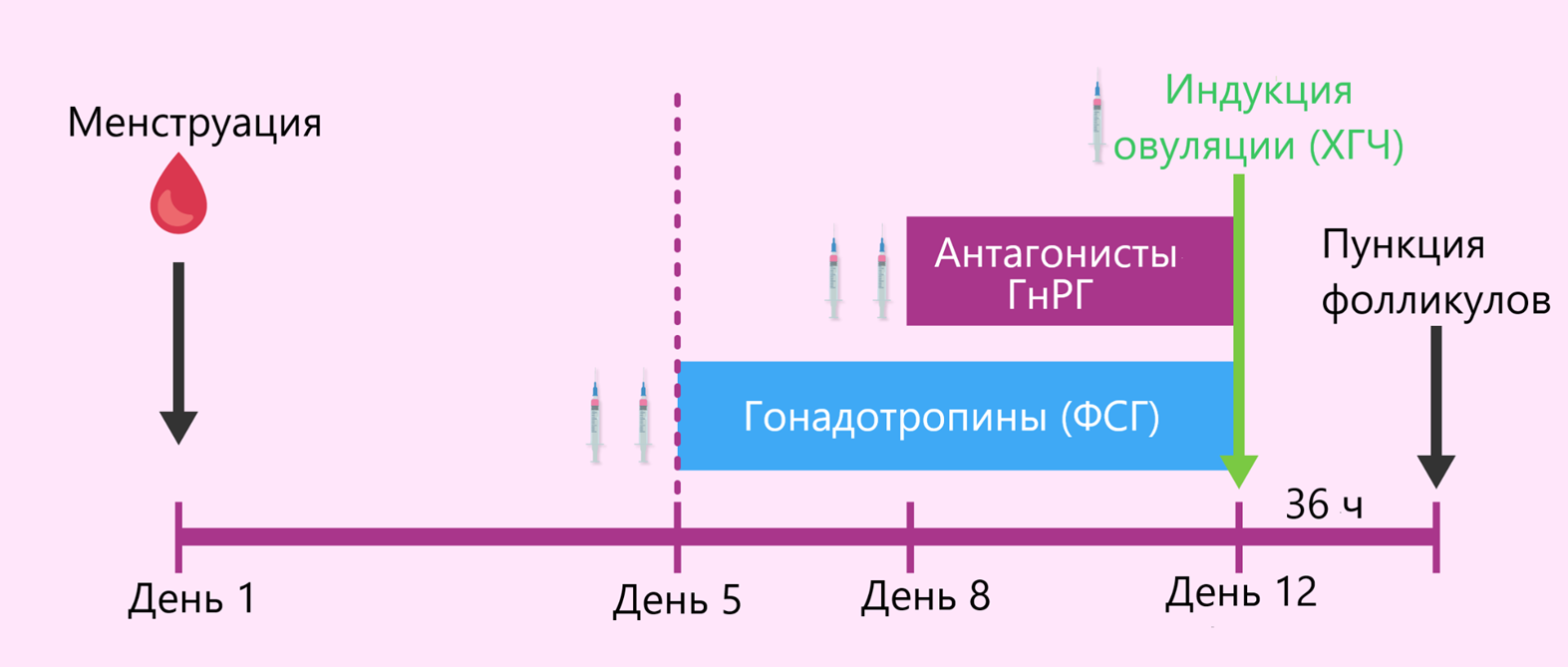
Рисунок 2. Процедура экстракорпорального оплодотворения. Пациентке вводят препараты фолликулостимулирующего гормона (ФСГ) для роста нескольких фолликулов (5–12-й день цикла). С 8-го по 12-й день дополнительно назначают антагонист гонадотропин-рилизинг-гормона (ГнРГ), чтобы предотвратить преждевременную овуляцию. На 12-й день вводят хорионический гонадотропин человека (ХГЧ), который запускает финальное созревание яйцеклеток перед их забором. Врач может назначать и более длительные приемы гонадотропинов. Это зависит от гормонального фона пациентки, запаса ее яйцеклеток и реакции яичников на препараты.
Такое вмешательство, конечно, вряд ли останется незамеченным для организма, и вместе с созреванием яйцеклеток может развиться синдром гиперстимуляции яичников (СГЯ). Он встречается примерно у 20–30% женщин, прошедших процедуру ЭКО, и сопровождается болями в области живота, вздутием и тошнотой. К сожалению, у 2–3% пациенток манифестируется тяжелая форма СГЯ ─ с массивным выходом жидкости в брюшную полость, нарушением водно-электролитного баланса и риском тромбоэмболий или дыхательной недостаточности [3].
В норме стенки сосудов действуют как селективные фильтры для воды и растворенных в ней веществ, поддерживая водно-электролитный баланс и предотвращая выход плазмы за пределы сосудистого русла. При ЭКО этот механизм дает сбой: препараты, используемые для стимуляции овуляции, запускают каскад изменений в яичниках. Ключевую роль играет экзогенный хорионический гонадотропин (ХГЧ), который используется для финального созревания ооцитов. ХГЧ действует как аналог эндогенного лютеинизирующего гормона (ЛГ) и стимулирует клетки яичников к очень активной выработке VEGF — фактора роста эндотелия сосудов, который и становится тем самым камнем преткновения. Его избыточные уровни повышают проницаемость сосудистой стенки: формируются межклеточные пространства, щели и микропоры. Нарушается барьерная функция сосудов, и жидкость начинает скапливаться в так называемом «третьем пространстве» — в брюшной, плевральной, а в очень тяжелых случаях и в перикардиальной полости [4].
К счастью, тяжелая форма синдрома встречается крайне редко, во многом благодаря совершенствованию протоколов стимуляции и внедрению принципов персонализированного лечения. В частности, до начала стимуляции оцениваются возможные риски, связанные с возрастом, уровнем антимюллерова гормона (показатель запаса яйцеклеток) и числом антральных фолликулов — в грубом приближении их можно назвать резервуарами, в каждом из которых зреет по одной потенциальной яйцеклетке. Для пациенток с синдромом поликистозных яичников — гормональным расстройством, которое сопровождается нерегулярными менструациями, повышенным уровнем «мужских» гормонов андрогенов и наличием множества мелких фолликулов в яичниках — характерен избыточный ответ на гормональную стимуляцию, поэтому для них применяют минимально эффективные дозы гонадотропинов. Это позволяет получить нужное количество яйцеклеток с низким риском осложнений [5].
Как видно из рисунка 2, часто протоколы ЭКО дополняют препаратами-антагонистами гонадотропин-рилизинг-гормона (ГнРГ) — они блокируют рецепторы гипофиза и предотвращают преждевременный всплеск лютеинизирующего гормона. Поскольку именно резкий и продолжительный ЛГ-пик способствует образованию факторов, повышающих сосудистую проницаемость, подавление этого всплеска уменьшает вероятность развития СГЯ. Опциональным компонентом протокола служит агонист ГнРГ — гормональный препарат, который запускает финальный этап созревания ооцитов. В отличие от традиционного введения ХГЧ, агонист ГнРГ вызывает короткий и близкий к естественному всплеск ЛГ. Этого достаточно для созревания яйцеклетки, но при этом риск развития СГЯ заметно снижается [6].
И все же риск СГЯ остается. Значит, у врачей еще много работы. Даже легкая форма синдрома вызывает физиологический дискомфорт и минимизирует результативность привычного распорядка женщин, а в отдельных случаях состояние пациенток и вовсе требует госпитализации [9]. Именно поэтому поиск методов, позволяющих полностью исключить риск СГЯ, не прекращается.
Одним из таких решений стала технология созревания in vitro (IVM, или in vitro maturation) — созревание ооцита «в пробирке». А зрелый ооцит — это и есть яйцеклетка, способная к оплодотворению. Так вот, стандартная технология IVM не предполагает гормональной стимуляции, а базируется на извлечении незрелых ооцитов в специальную среду с точно выверенным составом гормонов и факторов роста, где они дозревают в контролируемых лабораторных условиях. После созревания яйцеклетку оплодотворяют по стандартной процедуре ЭКО, культивируют до стадии эмбриона, а затем переносят эмбрион в полость матки. Следует оговориться, что такая стандартная IVM обладает очень низкой результативностью, поэтому в клинической практике минимальная гормональная поддержка все же используется. Она предназначена для повышения количества и качества незрелых ооцитов, которые можно получить из мелких антральных фолликулов. Такие фолликулы содержат рецепторы к ФСГ и реагируют на кратковременное повышение его концентрации, что делает их более структурированными и организованными. Поэтому в ряде клиник практикуют короткие режимы низкодозного ФСГ, однократное введение ХГЧ или их комбинацию [10]. И все же с помощью этого метода удается значительно сократить объем гормональной стимуляции яичников. Вместо этого создаются подходящие условия для созревания ооцитов в питательной среде, что практически сводит на нет риск развития даже легкой формы СГЯ, минимизирует возникновение других побочных эффектов и удешевляет технологию ЭКО ввиду минимизации введения высоких доз гонадотропинов (рис. 4) [11], [12].
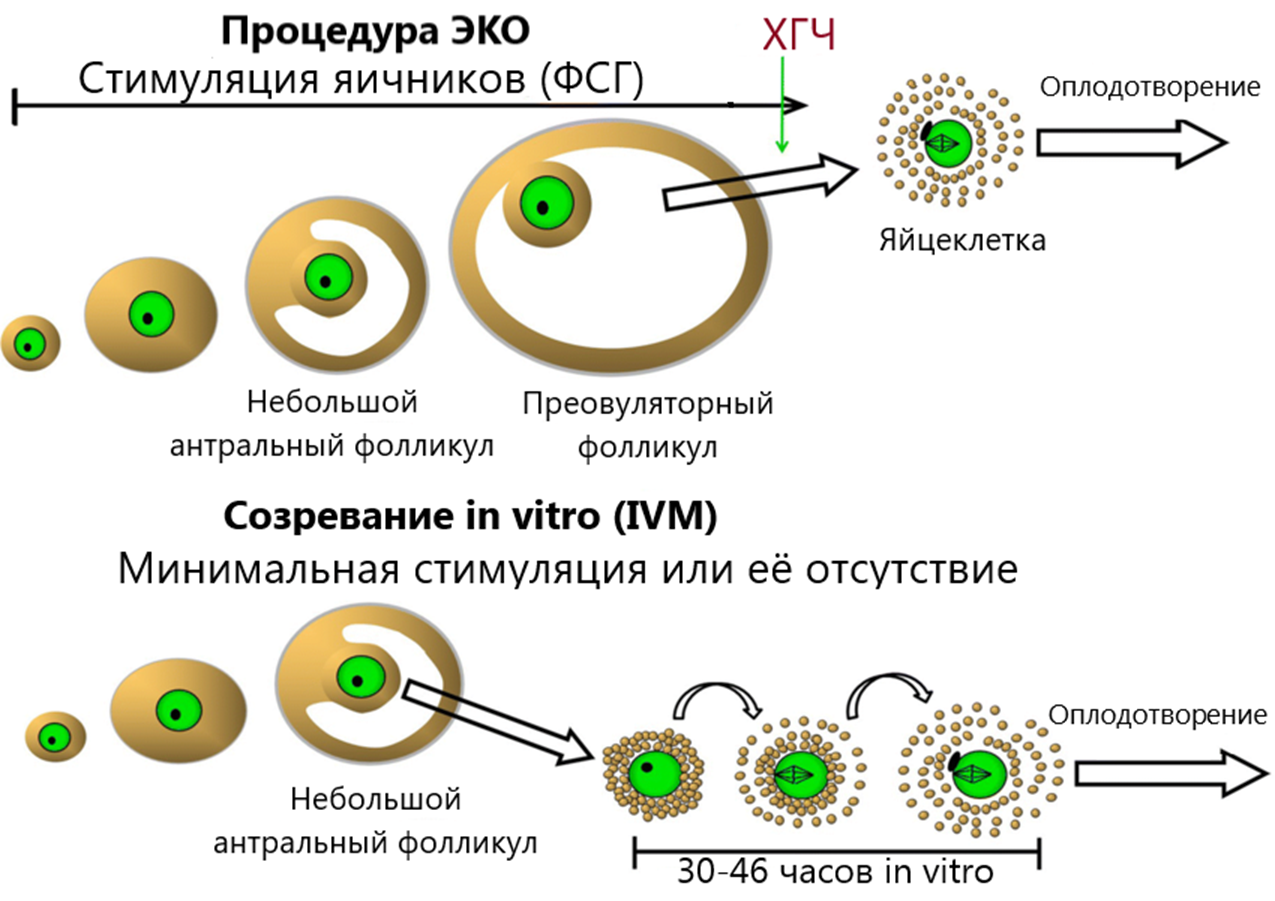
Рисунок 4. Сравнение традиционных протоколов ЭКО и IVM. В традиционных протоколах ЭКО созревание яйцеклеток происходит in vivo и требует длительной гормональной стимуляции яичников гонадотропинами. В результате к моменту пункции получают яйцеклетки, готовые к оплодотворению. Такой подход повышает эффективность процедуры, но сопровождается значительной гормональной нагрузкой на организм. IVM принципиально отличается: ооциты извлекают на более ранней стадии — из небольших антральных фолликулов — с минимальной гормональной стимуляцией или совсем без нее. Финальные этапы созревания ооцитов до яйцеклетки происходят уже в лабораторных условиях. Это снижает риск синдрома гиперстимуляции яичников и делает процедуру более щадящей, хотя эффективность IVM пока в среднем уступает классическому ЭКО.
Тем не менее, и здесь нужны модификации
Концепция IVM далеко не новая. Первые связанные с этой технологией исследовательские работы были опубликованы американскими учеными Грегори Пинкусом и Барбарой Сондерс еще в 1930-х годах. Они извлекали антральные фолликулы сначала у кроликов, а потом у человека, и выявили, что яйцеклетка вполне хорошо созревает in vitro — она достигает второго деления мейоза без дополнительной гормональной стимуляции [13]. Позже, однако, Пинкус столкнулся с серьезной критикой со стороны научного сообщества и общественности в целом. В ряде газетных публикаций его работу интерпретировали так, будто он намерен продолжать эксперименты до получения человеческого потомства «в пробирке». Сам Пинкус публично опроверг эти утверждения, подчеркнув, что его исследования ограничиваются изучением возможности созревания ооцитов в лабораторных условиях и что он не собирается продолжать их в направлении получения эмбрионов. Тем не менее, сама возможность экспериментировать с человеческими половыми клетками оказалась крайне чувствительной темой для общества, что привело к усилению давления на исследователя и фактически вынудило его прекратить дальнейшие работы [14].
Лишь в 1960-х годах к концепции вернулись. В том числе о ней вспомнил прародитель ЭКО — британец Роберт Эдвардс. В попытке получить больше ооцитов для оплодотворения, он изучал способность незрелых ооцитов различных млекопитающих (мышь, овца, свинья, корова, резус-макаки, человек) к созреванию in vitro. Его работа на тот момент была скорее фундаментальная, но ее результаты доказывали, что созревание ооцитов в лаборатории действительно возможно. Причем для большей убедительности он разделил выборку на две категории — с добавлением хорионического гонадотропина, то есть с дополнительной гормональной стимуляцией, и без. И, конечно, заметной разницы он не обнаружил: ооциты прекрасно созревали и без гормона [15]. Именно его фундаментальные эксперименты подтвердили осуществимость созревания ооцитов in vitro и открыли путь последующим работам в этой области. И спустя почти 30 лет, в 1991 году, уже на основе дальнейших научных разработок, родились здоровые девочки-тройняшки, зачатые с применением технологии IVM [16].
Казалось бы, технология созревания in vitro должна была стать новым стандартом вспомогательных репродуктивных технологий: она не предполагает введения высоких доз гормонов, устраняет риск синдрома гиперстимуляции яичников, не требует длительных наблюдений за состоянием пациентки и введения множества уколов. Да и классическое ЭКО сложно назвать идеальным решением: помимо риска СГЯ, оно не гарантирует стопроцентной эффективности и нередко требует нескольких циклов стимуляции, что увеличивает физическую и эмоциональную нагрузку на пациентку. Однако подводные камни для IVM, как всегда, имеются. Даже несмотря на то, что методика созревания «в пробирке» известна уже не одно десятилетие, мировые клиники до сих пор отдают предпочтение классическому ЭКО как более предсказуемому и отработанному стандарту. Почему?
Во-первых, играет роль неубедительность доказательной базы: рандомизированные клинические испытания малочисленны, а их результаты зависят от опыта конкретной клиники. В настоящее время эффективность IVM только лишь в лучших клиниках может достигать 30–40%, что ниже показателей традиционного ЭКО, где частота наступления беременности достигает 40–55% в зависимости от протокола [17].
Второе ограничение касается технических возможностей. Извлечение ооцитов из мелких антральных фолликулов (2–3 мм) требует особой точности, ловкости и опыта, хотя сегодня эти ограничения постепенно нивелируются благодаря специализированным обучающим центрам и новым типам игл. Не менее важным остается и фактор отбора пациенток. IVM показывает наилучшие результаты у женщин с высоким запасом яйцеклеток (по-другому — овариальным резервом) и уровнем антимюллерова гормона (АМГ). Однако при умеренных уровнях АМГ эффективность метода все еще уступает традиционным циклам ЭКО. Для женщин с низким овариальным резервом или старше 38 лет IVM пока не дает убедительных результатов ─ созревание ооцитов замедлено, а их развитие после оплодотворения часто останавливается на стадии дробления [18]. И все-таки, несмотря на это, в 2021 году Американское общество репродуктивной медицины признало IVM «неэкспериментальной» технологией. До этого момента она была не запрещена, но и не рекомендована [17]. Но все же пока всем очевидно, что эта технология нуждается в доработке.
Как же? Как же сделать еще лучше?
Текущие протоколы IVM основаны преимущественно на добавлении в культуральную среду отдельных факторов роста, сигнальных молекул и гормонов, которые руководят созреванием ооцитов. Однако такие протоколы маловоспроизводимы, а результаты сильно варьируются от лаборатории к лаборатории. Это частично объясняется тем, что протоколы с добавлением только отдельных молекул не могут воссоздать то микроокружение, которое необходимо для созревания ооцита в нативном фолликуле [17]. В результате процессы в ядре и цитоплазме клетки, которые в норме идут в точной синхронизации, начинают рассогласовываться.
Конечно, микроокружение важно. И неслучайно в организме созревание ооцита сопровождается формированием плотного слоя гранулезных клеток, которые соединяются с ним посредством щелевых контактов. Эти «мостики» предоставляют ооциту необходимое разнообразие аминокислот, энергетических субстратов, сигнальных молекул, синтезируют эстрадиол и паракринные факторы (активин, ингибин, KIT-лиганд), которые поддерживают рост и созревание клетки (рис. 5) [19].
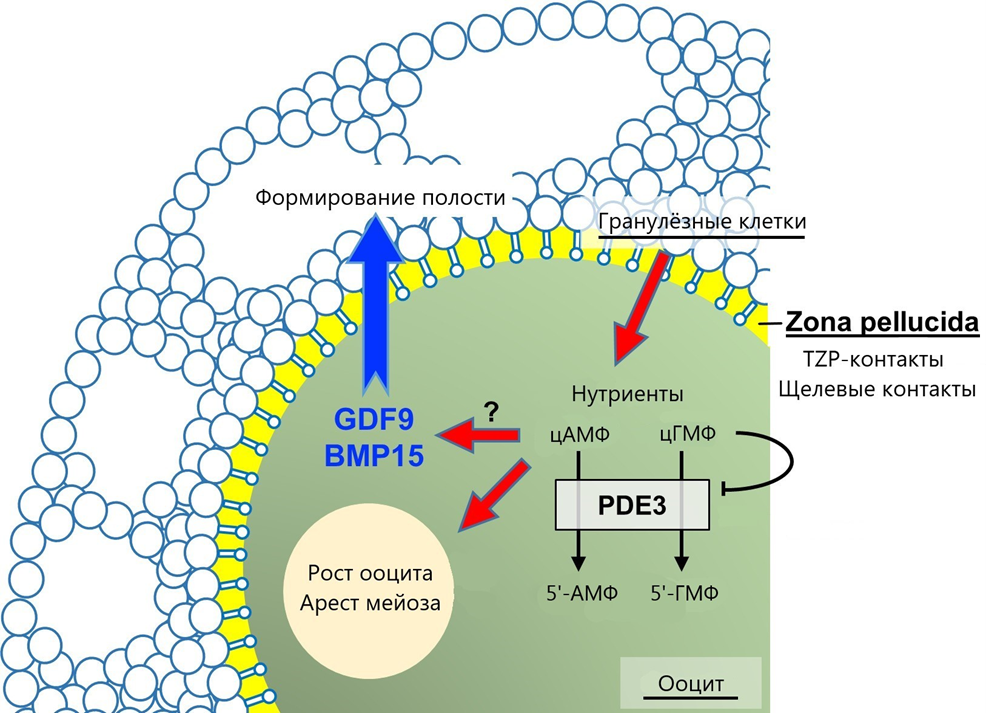
Рисунок 5. Схематическая коммуникация между ооцитами и гранулезными клетками. Питательные вещества, а также вторичные мессенджеры цАМФ и цГМФ (циклический аденозинмонофосфат и циклический гуанозинмонофосфат) транспортируются из гранулезных клеток в ооцит через TZP- и щелевые контакты. Этот поток сигналов поддерживает рост и стабилизирует блокировку мейоза ооцита через подавление активности PDE3 (фосфодиэстераза). Ооцит на такое воздействие активно регулирует поведение гранулезных клеток посредством синтеза белков GDF9 и BMP15. Эти факторы связываются с рецепторными комплексами гранулезных клеток, повышая метаболическую активность последних, а также стимулируя их пролиферацию и формирование антральной полости.
На первый взгляд очевидно, что достаточно просто совместно культивировать и ооциты, и гранулезные клетки пациентки, тогда проблема микроокружения будет решена. Но так она не решается. Во-первых, связано это с тем, что состав таких клеточных популяций непоследователен, а значит, протокол IVM невозможно будет стандартизировать, и результаты так и останутся низковоспроизводимыми. Во-вторых, выделение и очистка клеток сопряжены со значительными техническими сложностями, и зачастую просто невозможно получить достаточное количество поддерживающих клеток, не подвергая пациентку дополнительным рискам для здоровья. Наконец, сама причина бесплодия у некоторых женщин может быть связана с нефункциональностью фолликулярных клеток, что делает их использование в совместном культивировании с ооцитами неэффективным [21].
И именно здесь на помощь приходит наш главный герой — компания Gameto! Вместо использования клеточного материала пациентки, Gameto использует стандартизированные поддерживающие клетки яичников (ПКЯ), которые могут стабильно сосуществовать с незрелыми ооцитами в системе in vitro. Если коротко, исследователи берут линию индуцированных плюрипотентных стволовых клеток (ИПСК) и внедряют в них транскрипционные факторы, специфичные для гранулезных клеток. Такие инженерные структуры превращаются в эти самые ПКЯ и умеют производить эстрадиол, поддерживать развитие ооцитов и формировать мини-фолликулы.
Копнем поглубже
Манипуляции с транскрипционными факторами — дело небезызвестное. К слову, именно так и были получены индуцированные плюрипотентные стволовые клетки, за что в 2012 году японец Синъя Яманака и Джон Гёрдон из Англии получили Нобелевскую премию. Ученые обнаружили, что для перепрограммирования дифференцированной клетки достаточно активировать всего четыре гена ─ Myc, Oct3/4, Sox2 и Klf4. В зрелых соматических клетках эти гены выключены, но их искусственная активация откатывает клетку до исходного, недифференцированного состояния [22]. Затем такой клетке можно задать новую, нужную для исследователей судьбу ─ скажем, заставить ее стать нейроном, фибробластом или клеткой эндотелия [23]. Поэтому логично, что классическая сегодня технология перепрограммирования привела Gameto к вопросу: можно ли получить гранулезные клетки из ИПСК, чтобы улучшить созревание ооцитов in vitro? Ответ оказался утвердительным. Ученые собрали панель из 35 генов транскрипционных факторов, которые достоверно связаны с развитием гранулезных клеток, и протестировали их в ИПСК. Гены внедряли в индуцируемые плазмидные векторы, доставляли в клетки методом электропорации и запускали экспрессию такой конструкции в стимулирующей среде. В итоге из всего букета факторов до финиша дошла минимальная комбинация из двух генов — NR5A1 + RUNX1/2, ─ достаточная для получения гранулезоподобных клеток: уже через пять дней культивации появлялись клетки с характерной морфологией и маркером CD82 на их поверхности. Дополнительные факторы FOXL2 и GATA4 не были критически необходимы, но повышали стабильность инженерных клеток и поддерживали их фенотип. Очень важно, что в культурах не обнаруживали неперепрограммированные стволовые клетки, что указывает на высокий уровень безопасности создаваемых ПКЯ [24].
Получив свои гранулезоподобные клетки, исследователи сделали следующий закономерный шаг ─ проверили, смогут ли поддерживающие клетки обеспечить ооциту необходимые сигналы для роста и созревания в совместной культуре. Потому что именно гранулезные клетки формируют физиологичную микросреду, в которой ооцит проходит путь от примордиального состояния до зрелого — MII. Они стабилизируют транскрипционную программу ооцитов и регулируют темпы созревания. Теоретически такое совместное культивирование должно повышать вероятность получения зрелой, способной к оплодотворению яйцеклетки без агрессивной гормональной стимуляции и с меньшим риском для пациентки. На практике дела пошли еще лучше: ооциты очень и очень хорошо созревали и демонстрировали полноценную способность к оплодотворению, правильному дроблению и формированию бластоцист с эуплоидным набором хромосом и нормальным эпигенетическим профилем [21].
Дальнейший фронт работы компании был направлен на оптимизацию протоколов: ученые заменили все компоненты на максимально качественные и безопасные, включая среду для роста клеток и саму линию стволовых клеток. Они решили использовать линию VCT-37-F35 — клинически пригодную линию ИПСК, полученную из фибробластов кожи здорового донора, которую они перепрограммировали под свои задачи. После оптимизации стали доступны воспроизводимые клинические партии ПКЯ (коммерческое название — Fertilo), которые всесторонне протестировали ─ от оценки экспрессии генов до анализа созревания ооцитов у мышей. Был проведен и тест безопасности. Так как продукт, по сути, создавался из стволовых клеток, очень важно было убедиться, что в клетках эмбриона или в организме пациентки их не останется. Результат ─ не наблюдаются [25]!
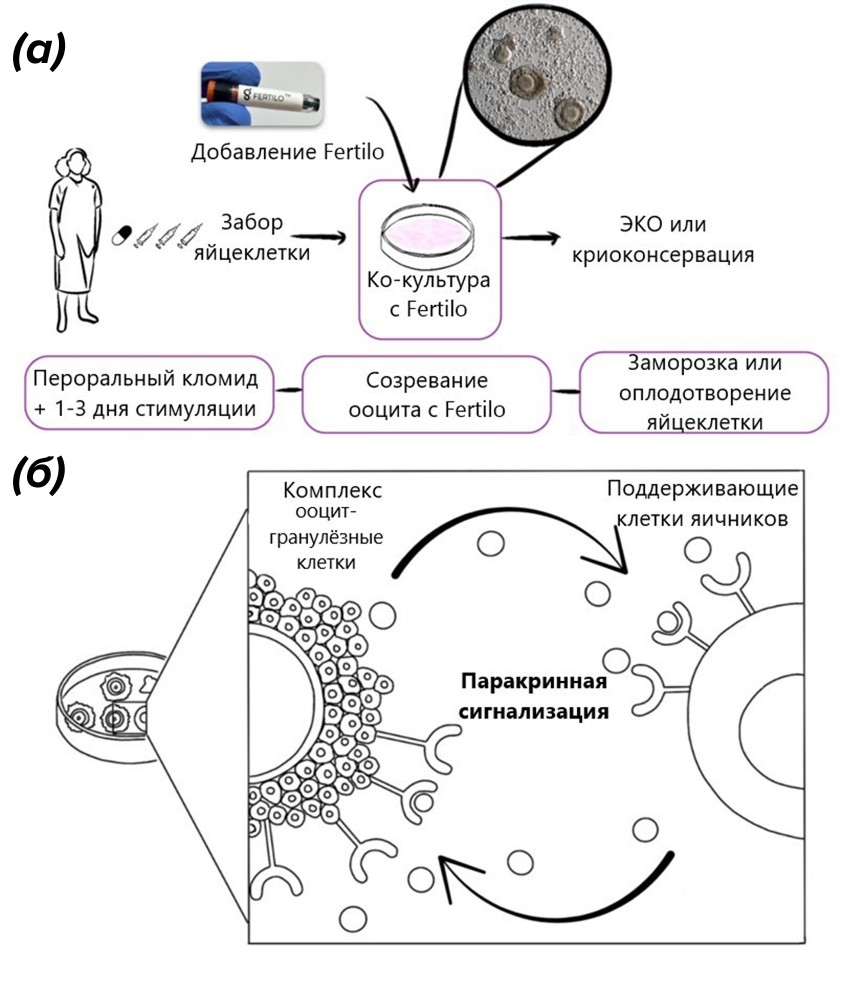
Рисунок 6. (а) — протокол, который предлагает компания Gameto. Смущение может вызвать слово «Кломид» — это цитрат кломифена, который нам встретился в тексте. Он блокирует эстрогеновые рецепторы в гипоталамусе, повышая секрецию ГнРГ и, как следствие, стимулируя выработку ФСГ и ЛГ для «пробуждения» и роста фолликулов. Затем следует сокращенная стимуляция гонадотропинами, забор незрелых фолликулов и их «доращивание» в культуральной среде с поддерживающими клетками яичников; (б) — коммуникация ооцитов и ПКЯ происходит путем паракринной сигнализации, а не с помощью щелевых контактов, какие есть между ооцитом и гранулезными клетками.
В лабораторных условиях все получилось отлично, самое время переходить к клиническим испытаниям. Протокол, как мы уже выяснили, делает акцент на создании максимально естественной среды для созревания яйцеклетки вне организма. Тем не менее, минимальная гормональная стимуляция все же присутствует. Чаще всего пациентке назначают цитрат кломифена в течение пяти дней. Он стимулирует естественную выработку ФСГ гипофизом. При необходимости, если размер фолликулов оказывается недостаточным, протокол дополняют низкодозными инъекциями рекомбинантного ФСГ (обычно не более трех дней). Когда диаметр ведущего фолликула достигает 10–12 мм, возможно введение триггера овуляции — рекомбинантного ХГЧ. Однако его применение в протоколе Fertilo является опциональным: триггер используют не для полноценной индукции овуляции, а для облегчения извлечения фолликулов за счет разрыхления комплекса «ооцит—гранулезные клетки». Через 34–36 часов после триггера выполняют пункцию фолликулов, а при его отсутствии — через 42–46 часов.
Полученные ооциты на этом этапе, как правило, еще незрелые. Поэтому их дальнейшее дозревание происходит уже в лаборатории — в специализированной среде in vitro, где яйцеклетки совместно культивируют с ПКЯ. Примерно через 30 часов оценивают, достигла ли яйцеклетка зрелой стадии. Перед оплодотворением ее полностью очищают от ПКЯ и собственных гранулезных клеток сначала ферментативно — с помощью гиалуронидазы, — а затем механически. Дальнейшие шаги не отличаются от классического ЭКО: яйцеклетки оплодотворяют путем инъекции сперматозоидов в ее цитоплазму (ИКСИ), эмбрионы выращивают до стадии бластоцисты, оценивают их качество и проводят генетическое тестирование. Параллельно эндометрий матки подготавливают к имплантации, чтобы обеспечить оптимальные условия для переноса эмбриона и наступления беременности (рис. 6).
Как я уже писала, сейчас препарат проходит III фазу клинических испытаний, которую планируют закончить к 2028 году. Однако благодаря технологии Fertilo уже появились на свет 6 здоровых детей, и более 20 женщин находятся на разных сроках беременности. Первый ребенок, та самая девочка из Перу, родилась на 38,5 неделе беременности с массой тела 3255 г и ростом 49,5 см. Данные показатели находятся в пределах абсолютной нормы для новорожденных. Она получила оценку 9/9 баллов по шкале Апгар ─ стандартизированной системе, которая используется для быстрой оценки состояния новорожденного сразу после родов и спустя 5 минут. Шкала оценивает сердечный ритм, дыхание, мышечный тонус, рефлексы и цвет кожи. Максимальная оценка равняется 10 баллам, и значения 7–10 считаются нормальными и в большинстве случаев выставляются полностью здоровым младенцам [25]. Поэтому полученные показатели подтверждают, что дети, рождающиеся с использованием Fertilo, здоровы, а родители ощущают бесконечное счастье при первой улыбке своих малышей. А мне, в свою очередь, приятно узнавать, что научные разработки находят применение в повседневной жизни; они дарят людям возможности, которые казались навсегда закрытыми. Пусть это продолжается и впредь.
Резюмирую и заключаю
Очень долгое время исследования женского репродуктивного здоровья развивались медленно, отчасти из-за хронической нехватки финансирования. Однако в последние годы ситуация начала меняться. Конечно, Gameto приложила здесь немало усилий. За 4 года существования компания привлекла около 127 миллионов долларов венчурного финансирования. Их флагманский проект — препарат Fertilo — одобрен в Перу, Мексике, Австралии, Японии, Индии, Сингапуре и ряде стран Латинской Америки. На мой взгляд, Gameto — это наглядный пример того, как фундаментальные научные разработки открывают двери в мир бизнеса и индустрии, а классические ученые и врачи успешно берут на себя роль предпринимателей. Технологическая платформа компании формировалась и развивалась в тесном сотрудничестве с академическими группами, в частности, с лабораторией Джорджа Чёрча и с Институтом биологической инженерии Висса при Гарвардском университете, что позволило эффективно переводить научные открытия в терапевтические разработки. При этом Gameto продолжает оставаться частью научного сообщества, регулярно представляя результаты своих исследований на ведущих отраслевых конференциях, включая ежегодное собрание Американского общества репродуктивной медицины (ASRM) и Международного общества исследований стволовых клеток (ISSCR).
С точки зрения клинического внедрения, технология выглядит очень перспективно. Она легко может интегрироваться в лаборатории вспомогательных репродуктивных технологий, не требует приобретения нового оборудования и опирается на единый стандартизированный источник ИПСК, а не на собственные клетки пациентки. Такой весомый аргумент говорит в пользу масштабируемости, воспроизводимости и экономичности процедуры по сравнению с индивидуальными ко-культурами клеток или традиционными протоколами стимуляции яичников. Более того, технология эффективно подстраивается под разные протоколы стимуляции и поэтому может использоваться как в строгих IVM протоколах, так и в мягких сокращенных циклах ЭКО. Интересно и то, что незрелому комплексу «ооцит—гранулезные клетки» не требуется прямой контакт с инженерными ПКЯ: ооциту достаточно паракринных сигналов, которые эти клетки выделяют в среду. Поэтому систему легко адаптировать под разные форматы и условия ─ от культуральных планшетов до автоматизированных систем. Единственное, исследователям не до конца понятен точный механизм взаимодействия ооцитов с поддерживающими клетками. Чтобы его изучить, нужны более длительные наблюдения и выборка побольше [21]. Тем не менее, предварительные результаты указывают на перспективность технологии с точки зрения ее стабильности и безопасности. И это уже большой шаг вперед в области женского здоровья.
Еще два стремительных шага компании направлены на создание так называемого «овароида», или органоида яичника, а также разработку импланта для контроля менопаузы ─ все это тоже с применением их инженерных клеток. Органоиды — это трехмерные структуры, которые имитируют клеточный состав и функциональные свойства реального органа. Они моделируют взаимодействия разных типов клеток, позволяя исследовать патогенез заболеваний, тестировать лекарственные препараты и изучать естественные процессы в органе в лабораторных условиях. Так вот, в сотрудничестве с Гарвардом и университетом Дьюка компания разработала органоид яичника под названием Deovo, состоящий полностью из человеческих клеток, что, в общем-то, удалось впервые (ранее создавали химерные, где половые клетки были человеческие, а поддерживающие — мышиные). По мнению ученых, такая модель поможет лучше понять механизмы заболеваний яичников и оценивать эффективность препаратов в максимально приближенных к реальному органу условиях, без необходимости экспериментов на животных [24].
Ameno — имплант для смягчения симптомов менопаузы − находится на доклинической стадии. В 2024 году компания выиграла грант от программы ARPA-H Sprint for Women’s Health на 10 миллионов долларов для продолжения исследования и внедрения разработки в клинику. В основе Ameno также лежат ПКЯ, имплантирование которых планируется с помощью нескольких способов: например, с помощью подкожного импланта, состоящего из микрокапсул с ПКЯ, которые заключены в биосовместимый каркас, или интравагинального гормонального кольца. Ameno будет имитировать естественную ось гипофиз-яичник, выступая в роли регулятора, который сможет бережно поддерживать необходимый уровень гормонов в ответ на сигналы организма.
Определенно, успех компании, которой всего четыре года, впечатляет. Во всем мире только два продукта на основе ИПСК дошли до III фазы клинических испытаний: кандидат для лечения остеоартрита (CYP-004, Cynata Therapeutics) и наш главный герой — Fertilo. И все же путь ИПСК от лабораторной разработки до масштабной клинической практики пока не преодолен. Почему так? На этот вопрос вам поможет ответить статья «Такие разные стволовые клетки» [26]. А я свой рассказ завершаю.
Литература
- Путь к тысячам аптек начинается с одной молекулы;
- «За экстракорпоральное оплодотворение» — это не тост, а Нобелевская премия!;
- Deepika Krishna, Snehal Dhoble, Gautham Praneesh, Suvarna Rathore, Amit Upadhaya, Kamini Rao. (2016). Gonadotropin-releasing hormone agonist trigger is a better alternative than human chorionic gonadotropin in PCOS undergoing IVF cycles for an OHSS Free Clinic: A Randomized control trial. J Hum Reprod Sci. 9, 164;
- P. Humaidan, S.M. Nelson, P. Devroey, C.C. Coddington, L.B. Schwartz, et. al.. (2016). Ovarian hyperstimulation syndrome: review and new classification criteria for reporting in clinical trials. Hum. Reprod.. 31, 1997-2004;
- Alexander M. Kotlyar, David B. Seifer. (2023). Women with PCOS who undergo IVF: a comprehensive review of therapeutic strategies for successful outcomes. Reprod Biol Endocrinol. 21;
- Hizkiyahu Ranit, Herzberg Shmuel, Athavale Ahlad, Greenbaum Shirley, Harari Meny, et. al.. (2024). Is there a preferred time interval between gonadotropin-releasing hormone (GnRH) agonist trigger and oocyte retrieval in GnRH antagonist cycles? A retrospective cohort of planned fertility preservation cycles. J Assist Reprod Genet. 41, 1531-1538;
- Noemie Sachs-Guedj, Roger Hart, Antonio Requena, Vanessa Vergara, Nikolaos P. Polyzos. (2023). Real-world practices of hormone monitoring during ovarian stimulation in assisted reproductive technology: a global online survey. Front. Endocrinol.. 14;
- Об адаптации, регуляции и прочих приключениях мозга во время материнства;
- Elizabeth Lumley, Alicia O'Cathain, Sarah Drabble, Clare Pye, Kate Brian, Mostafa Metwally. (2023). Managing ovarian hyperstimulation syndrome: A qualitative interview study with women and healthcare professionals. Journal of Clinical Nursing. 32, 6599-6610;
- Mausumi Das, Weon-Young Son. (2023). In vitro maturation (IVM) of human immature oocytes: is it still relevant?. Reprod Biol Endocrinol. 21;
- Maria Marchante, Ferran Barrachina, Sabrina Piechota, Marta Fernandez-González, Alexa Giovannini, et. al.. (2024). Donor side effects experienced under minimal controlled ovarian stimulation with in vitro maturation vs. conventional controlled ovarian stimulation for in vitro fertilization treatment. F&S Science. 5, 242-251;
- Michel De Vos, Michaël Grynberg, Tuong M. Ho, Ye Yuan, David F. Albertini, Robert B. Gilchrist. (2021). Perspectives on the development and future of oocyte IVM in clinical practice. J Assist Reprod Genet. 38, 1265-1280;
- Gregory Pincus, Barbara Saunders. (1939). The comparative behavior of mammalian eggs in vivo and in vitro. VI. The maturation of human ovarian ova. Anat. Rec.. 75, 537-545;
- J. G. Thompson, R. B. Gilchrist. (2013). Pioneering contributions by Robert Edwards to oocyte in vitro maturation (IVM). Molecular Human Reproduction. 19, 794-798;
- R. G. EDWARDS. (1965). Maturation in vitro of Mouse, Sheep, Cow, Pig, Rhesus Monkey and Human Ovarian Oocytes. Nature. 208, 349-351;
- Kwang Yul Cha, Jung Jin Koo, Jung Jae Ko, Dong Hee Choi, Sei Yul Han, Tae Ki Yoon. (1991). Pregnancy after in vitro fertilization of human follicular oocytes collected from nonstimulated cycles, their culture in vitro and their transfer in a donor oocyte program. Fertility and Sterility. 55, 109-113;
- Robert B Gilchrist, Tuong M Ho, Michel De Vos, Flor Sanchez, Sergio Romero, et. al.. (2024). A fresh start for IVM: capacitating the oocyte for development using pre-IVM. Human Reproduction Update. 30, 3-25;
- Sofia Makieva, Juan J Fraire-Zamora, Omar Farhan Ammar, George Liperis, Flor Sanchez, et. al.. (2024). Road to in vitro maturation (IVM), from basic science to an informed clinical practice. Human Reproduction. 39, 2638-2643;
- Md Hasanur Alam, Takashi Miyano. (2020). Interaction between growing oocytes and granulosa cells in vitro. Reprod Medicine & Biology. 19, 13-23;
- Fiona H Thomas, Barbara C Vanderhyden. (2006). Oocyte-granulosa cell interactions during mouse follicular development: regulation of kit ligand expression and its role in oocyte growth. Reprod Biol Endocrinol. 4;
- Sabrina Piechota, Maria Marchante, Alexa Giovannini, Bruna Paulsen, Kathryn S Potts, et. al.. (2023). Human-induced pluripotent stem cell-derived ovarian support cell co-culture improves oocyte maturation in vitro after abbreviated gonadotropin stimulation. Human Reproduction. 38, 2456-2469;
- Нобелевская премия по физиологии и медицине (2012): индуцированные стволовые клетки;
- Как сделать нейрон из фибробласта?;
- Merrick D Pierson Smela, Christian C Kramme, Patrick RJ Fortuna, Jessica L Adams, Rui Su, et. al.. (2023). Directed differentiation of human iPSCs to functional ovarian granulosa-like cells via transcription factor overexpression. eLife. 12;
- Bruna Paulsen, Ferran Barrachina, Sabrina Piechota, Alexander D. Noblett, Mark Johnson, et. al. Translation of a human induced pluripotent stem cell-derived ovarian support cell product to a Phase 3 enabling clinical grade product for in vitro fertilization treatment — openRxiv;
- Такие разные стволовые клетки.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚