Как бактерии ведут список своих врагов: что CRISPR рассказал о тайной жизни C. botulinum
19 марта 2026
Как бактерии ведут список своих врагов: что CRISPR рассказал о тайной жизни C. botulinum
- 217
- 0
- 2
Художественная визуализация концепции CRISPR-кассет как хранилища информации о взаимодействиях бактерий с бактериофагами.
Рисунок в полном размере.
-
Авторы
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Как человек запоминает важные встречи, лица и детали, так и бактерии хранят «память» о своих самых опасных врагах. Такой памятью служит система CRISPR-Cas, фиксирующая следы прошлых атак бактериофагов. Анализируя эти генетические «воспоминания», можно восстановить историю взаимодействий бактерии с фагами и понять, какие из них представляли для нее наибольшую угрозу. В этой статье мы расскажем о том, как по структуре CRISPR-Cas систем бактерии Clostridium botulinum можно реконструировать ее фаговое прошлое и почему это знание важно для развития более точных и безопасных подходов к фаготерапии в эпоху снижающейся эффективности антибиотиков.
Конкурс «Био/Мол/Текст»-2025/2026
Эта работа опубликована в номинации «Своя работа» конкурса «Био/Мол/Текст»-2025/2026.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
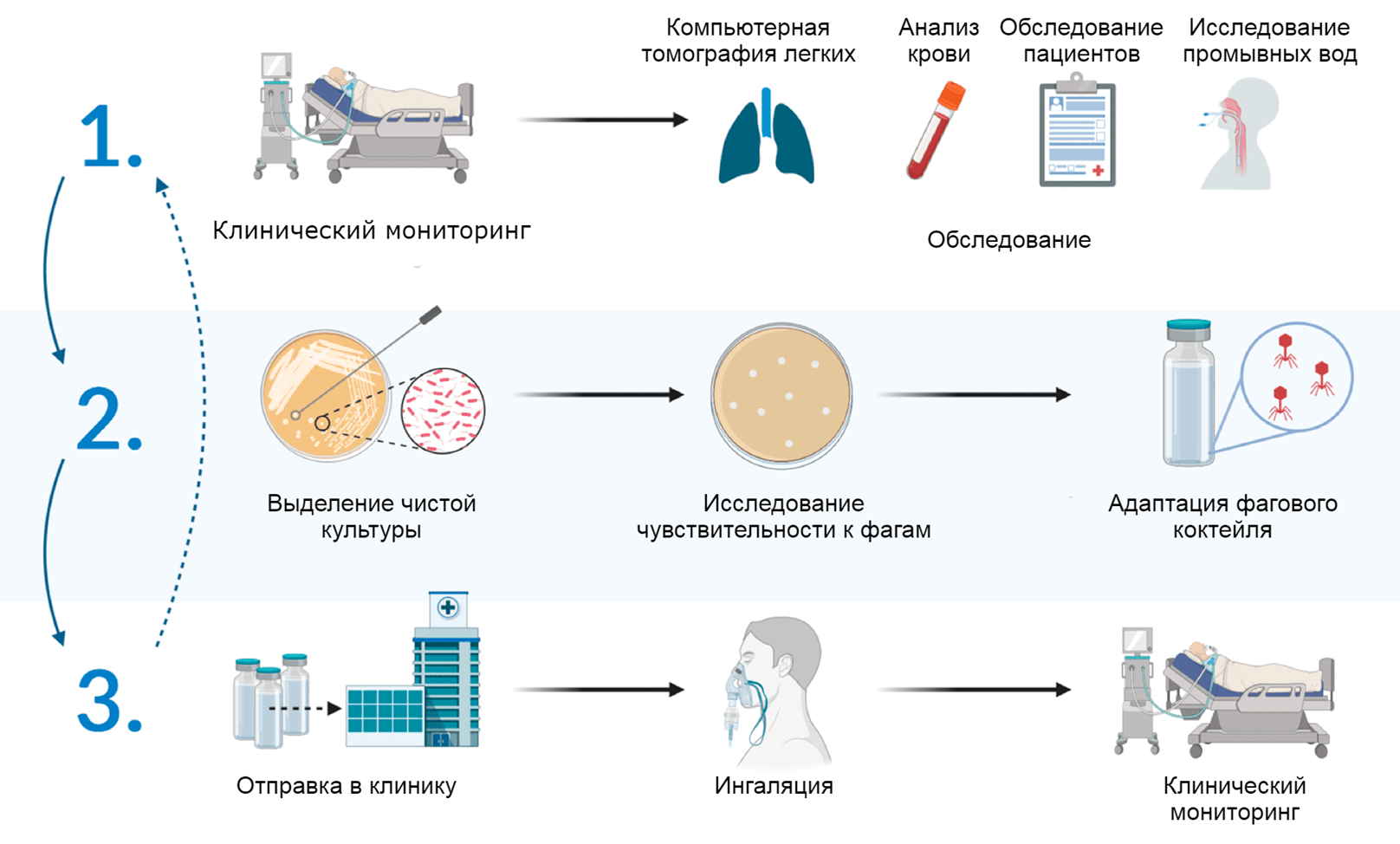
Представьте себе бактерию, способную за считанные часы лишить человека возможности дышать. Ботулизм, вызываемый бактериями Clostridium botulinum, — это тяжелая нейроинфекция, при которой поражение нервной системы развивается стремительно и может приводить к параличу дыхательной мускулатуры. Даже при своевременной медицинской помощи течение заболевания остается крайне опасным, а исход во многом зависит от скорости диагностики и начала лечения (рис. 1) [1], [2].
Ботулинический нейротоксин (BoNT) является одним из самых мощных известных биологических веществ, смертельная доза которого составляет всего 0,3 нг/кг для человека. В сравнении для близкого по механизму действия тетанотоксина, продуцируемого Clostridium tetani, летальная доза составляет около 1 нг/кг, тогда как батрахотоксин — небелковый нейротоксин, вырабатываемый некоторыми видами лягушек-древолазов рода Phyllobates, — требует порядка 2000 нг/кг для летального исхода [3], [4].
Рисунок 1. Обзор путей инфицирования C. botulinum и клиническая прогрессия ботулизма.
адаптировано из [1]
C. botulinum относится к бактериям, которые развиваются в бескислородной среде. У человека эта бактерия обычно обнаруживается в кишечнике и на слизистых оболочках. В природе же она встречается чаще всего в воде, почве, на растениях, которые поедают сельскохозяйственные животные, затем выделяют эти бактерии вместе с фекалиями обратно в почву, способствуя их дальнейшему распространению. В основном нейротоксин (BoNT) в организм человека попадает вместе с пищей в желудочно-кишечный тракт и через кровь разносится по всему организму, проникая в нервные и мышечные узлы.
Принципиальным является вопрос о существовании в природной среде у C. botulinum биологических антагонистов и о том, какими способами этот микроорганизм им противостоит. На сегодняшний день известно, что многие представители прокариот в своей эволюционной истории приобрели особые структуры в своих геномах — CRISPR-Сas системы, являющихся самыми древними системами адаптивной иммунной защиты от бактериофагов, плазмид и других мобильных генетических элементов [5]. Поэтому анализ CRISPR-Cas систем в геномах C. botulinum может рассматриваться как источник информации не только о ее устойчивости в различных экосистемах, но и о потенциальных направлениях разработки альтернативных антибактериальных стратегий.
В условиях нарастающей множественной лекарственной устойчивости бактерий антибиотикотерапия все чаще оказывается неэффективной, что делает актуальным поиск альтернативных подходов борьбы с данным патогеном [6]. Фаготерапия имеет длительную историю применения, однако ее эффективность в отношении C. botulinum существенно ограничена недостатком данных о специфичности фагов к отдельным штаммам бактерии. Исходя из этого, необходимы новые подходы к поиску и созданию эффективных стратегий борьбы с данным патогеном.
В нашем исследовании мы задали ключевой вопрос: какие вирусы ранее инфицировали C. botulinum и оставили следы в ее геноме [7]? Были проанализированы полные геномы 52 патогенных штаммов C. botulinum из разных регионов мира, представленных в международных базах генетических данных NCBI, и с помощью геномных и биоинформатических методов восстановлена их CRISPR-память о прошлых фаговых инфекциях. Такой подход позволяет реконструировать эволюционную историю взаимодействий C. botulinum с бактериофагами и рассматривать CRISPR-кассеты как источник информации о перенесенных вирусных инфекциях. Полученные данные свидетельствуют о том, что фаги могут рассматриваться не только как факторы давления на бактериальные популяции, но и как потенциальные инструменты для разработки таргетных антибактериальных стратегий.
Бактериальный «антивирус»
CRISPR-Cas — это система безопасности бактерий, одна из древнейших форм адаптивной иммунной защиты живых систем, возникшая почти 4 миллиарда лет назад. Ее часто сравнивают с «встроенным антивирусом» клетки, поскольку она позволяет распознавать и нейтрализовывать чужеродный генетический материал. У человека эту функцию выполняет иммунная система, способная запоминать ранее встреченные патогены. У бактерий отсутствует иммунитет в привычном нам понимании, однако CRISPR-Cas обеспечивает им функционально схожий механизм защиты.
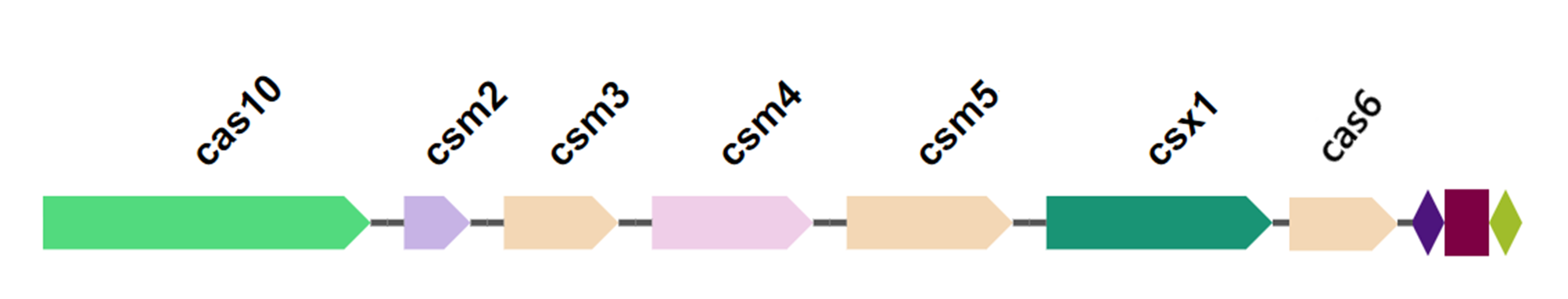
CRISPR-Cas система (clustered regularly interspaced short palindromic repeats) и ассоциированные с ней белки Cas (от англ. CRISPR-associated proteins) стали одним из ключевых открытий современной молекулярной биологии [8], [9]. CRISPR-кассеты — это участки ДНК (локусы) в геномах прокариот, состоящие из коротких идентичных повторов длиной 30–40 пар нуклеотидов, разделенных уникальными спейсерными последовательностями сходной длины [10]. Вблизи этих локусов располагаются гены, кодирующие CRISPR-ассоциированные белки Cas (рис. 2). CRISPR-Cas системы обнаружены примерно у 50% всех известных бактерий и у более чем 90% архей, что подчеркивает их фундаментальное значение для жизнедеятельности прокариот. В 2020 году за работы по практическому использованию CRISPR-Cas для редактирования генома Нобелевская премия по химии была присуждена Эммануэль Шарпантье и Дженнифер Даудне [11], [12].
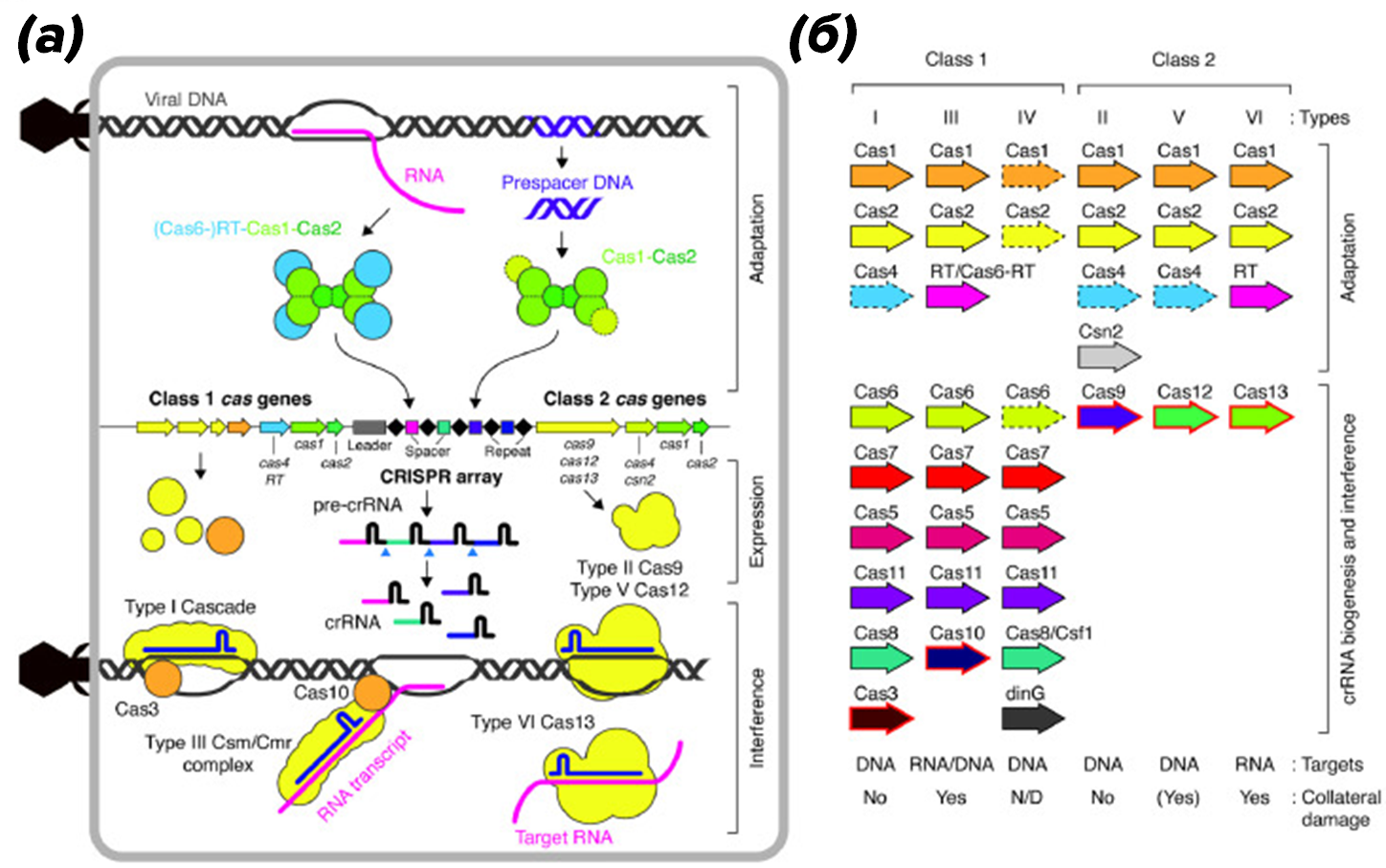
Рисунок 2. Схема механизма и классификации систем CRISPR-Cas. (а) — cхема адаптивного иммунитета CRISPR-Cas. При адаптации чужеродная ДНК (серые спиральные линии) или РНК (розовые линии) могут быть захвачены и интегрированы в CRISPR-массив с помощью комплексов Cas1-Cas2. (б) — классификация и структура генов систем CRISPR-Cas. Классификация в первую очередь основана на эффекторных генах.
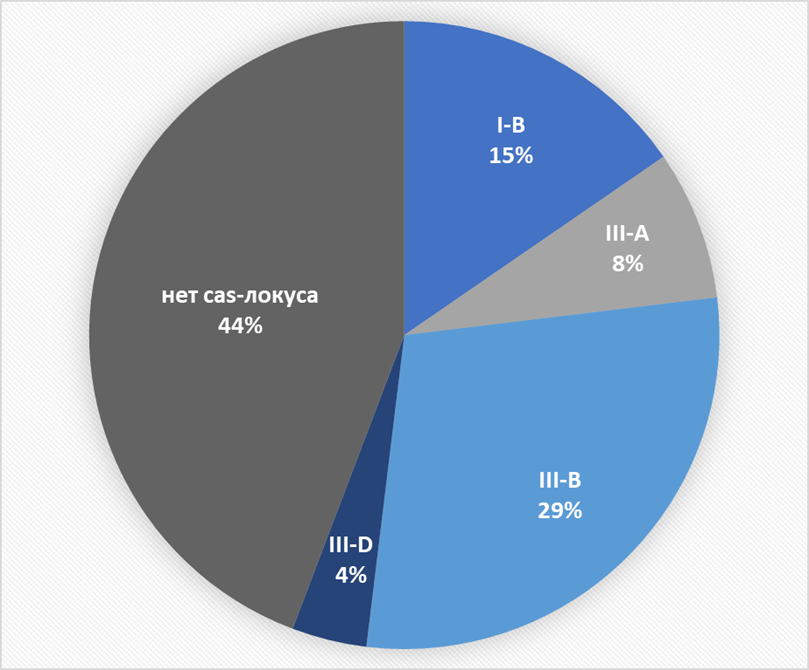
Эндогенные CRISPR-Cas системы широко представлены и у C. botulinum. По данным геномных исследований, они обнаруживаются у большинства анализируемых штаммов и преимущественно относятся к подтипам Type I-B и Type III (III-A, III-B, III-D), тогда как более редкие варианты (Type II-C и Type V-U) выявлены лишь в отдельных штаммах некоторых филогенетических групп [13–16].
Анализ спейсеров показал, что CRISPR-кассеты C. botulinum преимущественно нацелены на плазмиды и профаги, а не на гены ботулинического токсина, что указывает на их потенциальную роль в регуляции горизонтального переноса генетических элементов и стабилизации генома, а не в прямой инактивации факторов вирулентности [14], [17]. При этом штаммы с неполными или ослабленными CRISPR-Cas системами характеризуются большим числом экстрахромосомных элементов, тогда как наличие функциональных систем коррелирует с более стабильной геномной архитектурой [15].
Вместе с тем, большинство существующих выводов основано на биоинформатических предсказаниях и не сопровождается функциональной валидацией, а данные о прямом участии эндогенных CRISPR-Cas систем C. botulinum в защите от бактериофагов остаются ограниченными, особенно для штаммов групп II и III [14], [18]. В этой связи системный анализ CRISPR-кассет и их спейсерного состава представляет собой перспективный подход к реконструкции фаговых взаимодействий C. botulinum и поиску потенциальных штаммоспецифичных бактериофагов.
Для чего нужна фаготерапия
Бактериофаги — вирусы, специфически инфицирующие бактерии, — рассматриваются как перспективная альтернатива традиционным антибиотикам в условиях роста глобальной угрозы множественной лекарственной устойчивости патогенных микроорганизмов [19]. Фаги широко распространены в природе и характеризуются высокой специфичностью к бактериальным хозяевам при отсутствии токсичности для эукариотических клеток, что делает их потенциально безопасными для применения у человека [20], [21].
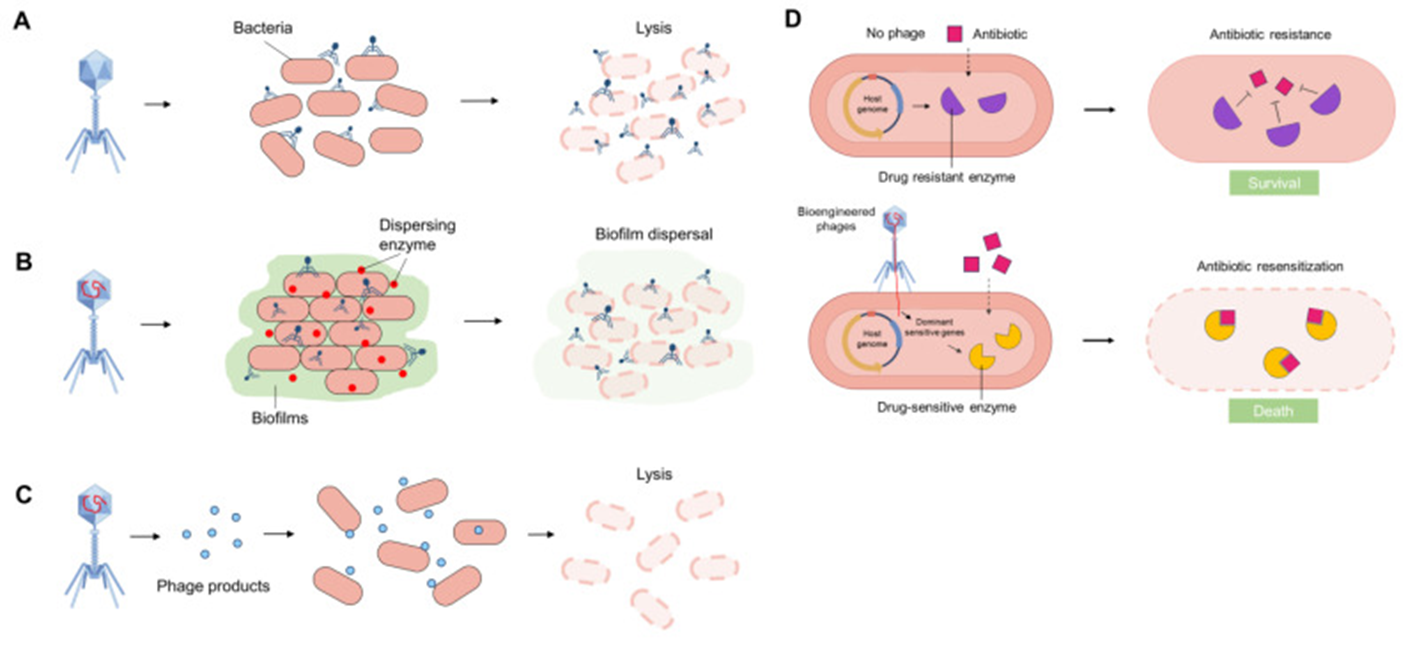
Фаготерапия имеет длительную историю применения и в последние годы вновь привлекает внимание исследователей и клиницистов. Ее эффективность продемонстрирована в ряде доклинических и клинических исследований, в том числе при лечении инфекций кожи, дыхательных путей и мочевыводящей системы [22], [23] (рис. 3А). В странах Восточной Европы, включая Россию и Грузию, фаготерапия продолжает использоваться на практике, демонстрируя благоприятный профиль безопасности [19]. Одним из ключевых преимуществ фаготерапии является возможность подбора фагов, специфичных для отдельных штаммов бактерий (рис. 3Б).
Однако универсальность данного подхода ограничена биологическими особенностями конкретных патогенов. В случае C. botulinum применение фаготерапии сопряжено с рядом принципиальных трудностей.При ботулизме ключевым фактором патогенеза является ботулинический нейротоксин, поэтому антибактериальные стратегии могут быть эффективны преимущественно на ранних этапах заболевания — в период прорастания спор и вегетативного роста бактерий, когда снижение бактериальной нагрузки потенциально может дополнять лечение антитоксином [18].
На сегодняшний день прямые доказательства эффективности фаготерапии против C. botulinum ограничены. Клинические испытания отсутствуют, однако описаны фаговые эндолизины с узкой специфичностью. Так, эндолизин CBO1751 продемонстрировал in vitro активность против вегетативных клеток C. botulinum группы I, снижая их жизнеспособность на 2–4 логарифмических порядка в течение 60 минут [24]. При этом его активность не распространяется на штаммы групп II и III, что существенно ограничивает практическое применение (рис. 4).
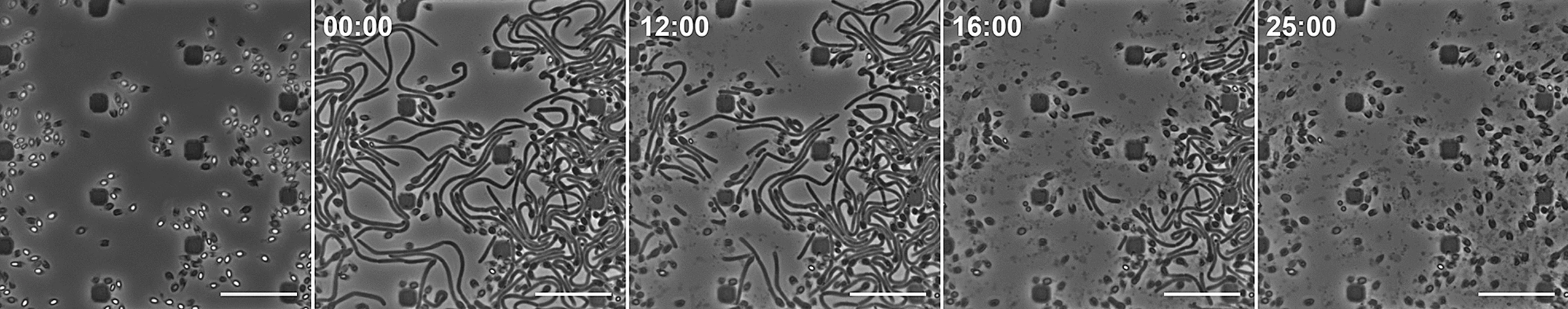
Рисунок 4. Лизис вегетативных клеток C. botulinum ATCC3502 под действием фагового эндолизина CBO1751. Слева показаны споры C. botulinum в микрофлюидной камере до обработки. Справа — последовательные кадры таймлапс-микроскопии, демонстрирующие разрушение клеток после добавления CBO1751 (20 мкМ). Масштабная линейка — 2 мкм. Квадратные элементы на изображении соответствуют структурным опорам микрофлюидной камеры.
Дополнительные ограничения связаны с особенностями фаговой биологии C. botulinum. Гены ботулинического токсина типов C и D ассоциированы с лизогенными фагами, и фаг-инфекция может влиять на регуляцию токсинпродукции, особенно у штаммов группы III с нестабильной лизогенией [25], [26]. Это создает потенциальные риски при использовании природных фагов и требует строгой оценки безопасности.
В связи с этим современные исследования фокусируются на более контролируемых фаговых инструментах, включая синтетические эндолизины и комбинированные терапевтические подходы, а также на поиске штаммоспецифичных решений [21]. Для C. botulinum ключевым становится вопрос точного подбора фаговых агентов, что невозможно без понимания истории фаговых взаимодействий бактерии и механизмов ее защиты.
Поиск фаговых следов в геномах C. botulinum
Чтобы реконструировать историю взаимодействий C. botulinum с бактериофагами, недостаточно иметь доступ к геномным данным — важно корректно интерпретировать их структуру и содержание. Основной задачей на этом этапе было не только выявление элементов CRISPR-Cas систем, но и подтверждение достоверности каждого обнаруженного сигнала, отражающего прошлые вирусные взаимодействия.
Мы отобрали для исследования 52 генома патогенных штаммов C. botulinum, представленных в международных базах генетических данных NCBI. Все они собраны в виде цельных кольцевых хромосом. Это принципиально важно: CRISPR-кассеты часто располагаются на границах сборочных фрагментов, и, если геном неполный, часть CRISPR может исчезнуть или «разрываться». Полная хромосома — это гарантия, что память бактерии сохранилась в своем естественном виде.
Первым этапом исследования был поиск cas-генов, кодирующих белки, обеспечивающие функционирование CRISPR-Cas систем. Наличие таких генов в геноме служит надежным маркером присутствия CRISPR-Cas иммунитета у прокариот [8], [9]. Для их идентификации использовалась программа MacSyFinder, предназначенная для поиска генетических систем на основе их структурной и функциональной организации, а не только формального сходства последовательностей [27], [28].
В отличие от методов, основанных на прямом поиске по названию гена или локальном выравнивании последовательностей, MacSyFinder использует профили скрытых марковских моделей (Hidden Markov Models, HMM), описывающие консервативные аминокислотные мотивы белков Cas. Такой подход позволяет учитывать эволюционную вариабельность белковых последовательностей и выявлять гены даже при низком уровне прямого сходства [28].
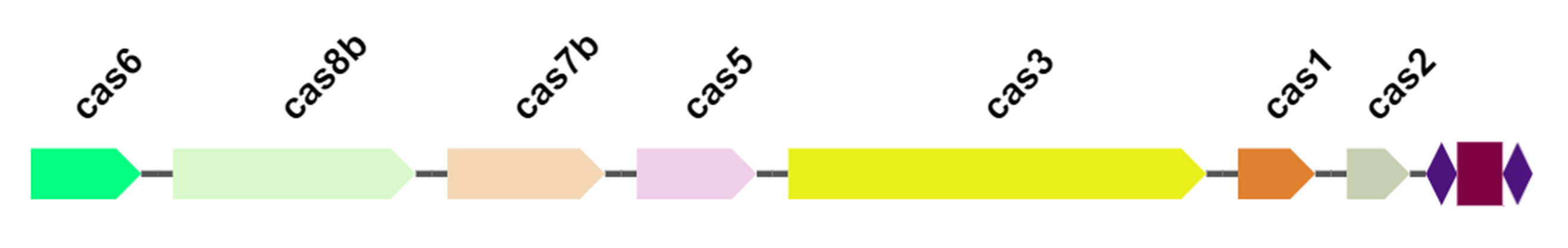
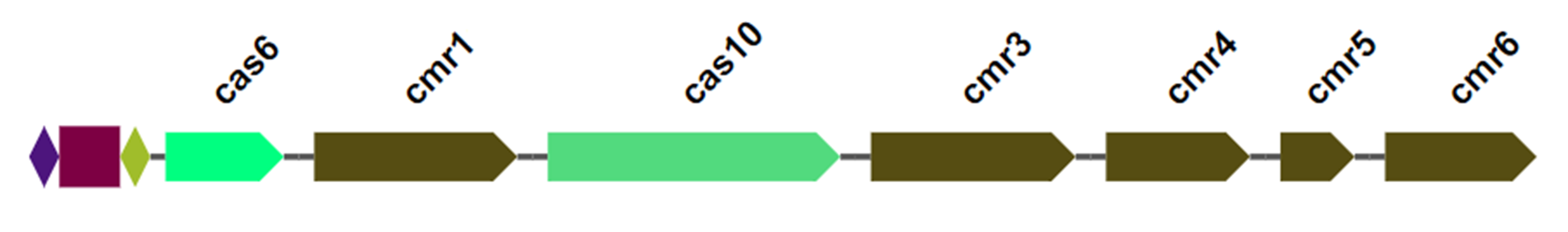
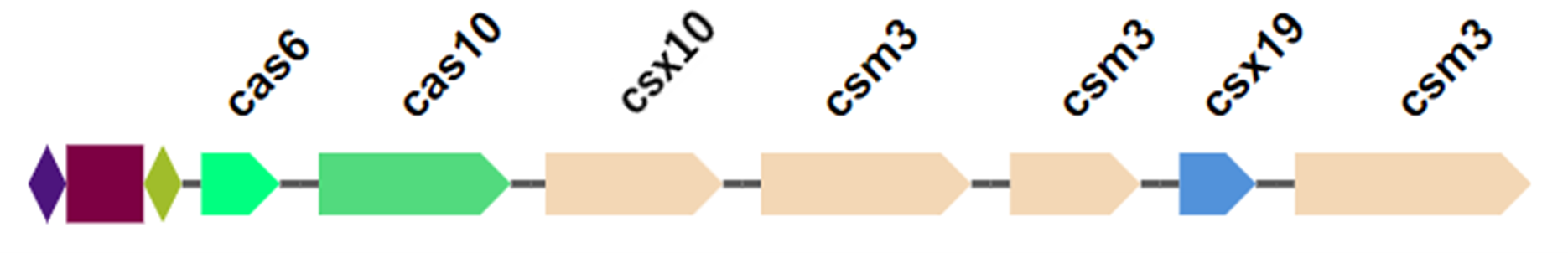
Поиск cas-генов осуществлялся с использованием HMM-профилей из специализированных доменных баз данных PFAM и TIGRFAM, содержащих курируемые описания функциональных семейств и консервативных белковых доменов [27], [28]. Это позволило корректно идентифицировать cas-гены, которые в ряде геномов оказались фрагментированными или некорректно аннотированными вследствие особенностей автоматической аннотации [28]. В результате анализа 125 геномов C. botulinum cas-гены были обнаружены в 48 геномах, что указывало на присутствие CRISPR-Cas систем или их компонентов (рис. 5Б). Все выявленные cas-кластеры относились к классу I и были представлены преимущественно системами типа III (20 из 27 полных систем), а также типом I (рис. 5В—Д, рис. 6).
После идентификации cas-генов следующим шагом стало определение соответствующих им CRISPR-кассет — массивов повторов и спейсеров, составляющих «память» бактериального иммунитета.Здесь мы сознательно выбрали стратегию «трех независимых источников истины».
CRISPRFinder сначала находит в геномной последовательности участки с максимальными повторениями и затем проверяет, укладываются ли они в типичную CRISPR-архитектуру (повтор—спейсер—повтор) — поэтому он хорошо распознает «классические», четко организованные кассеты [27].
PILER-CR идет другим путем: он ищет повторы, группируя и выравнивая похожие повторяющиеся фрагменты по всему геному, поэтому часто находит массивы, где повторы уже немного разошлись из-за мутаций [29].
CRT использует автоматический проход по геному и выделяет кандидаты CRISPR, опираясь на регулярность чередования повторов и спейсеров и внутренние критерии качества массива — это снижает риск ложноположительных находок [30].
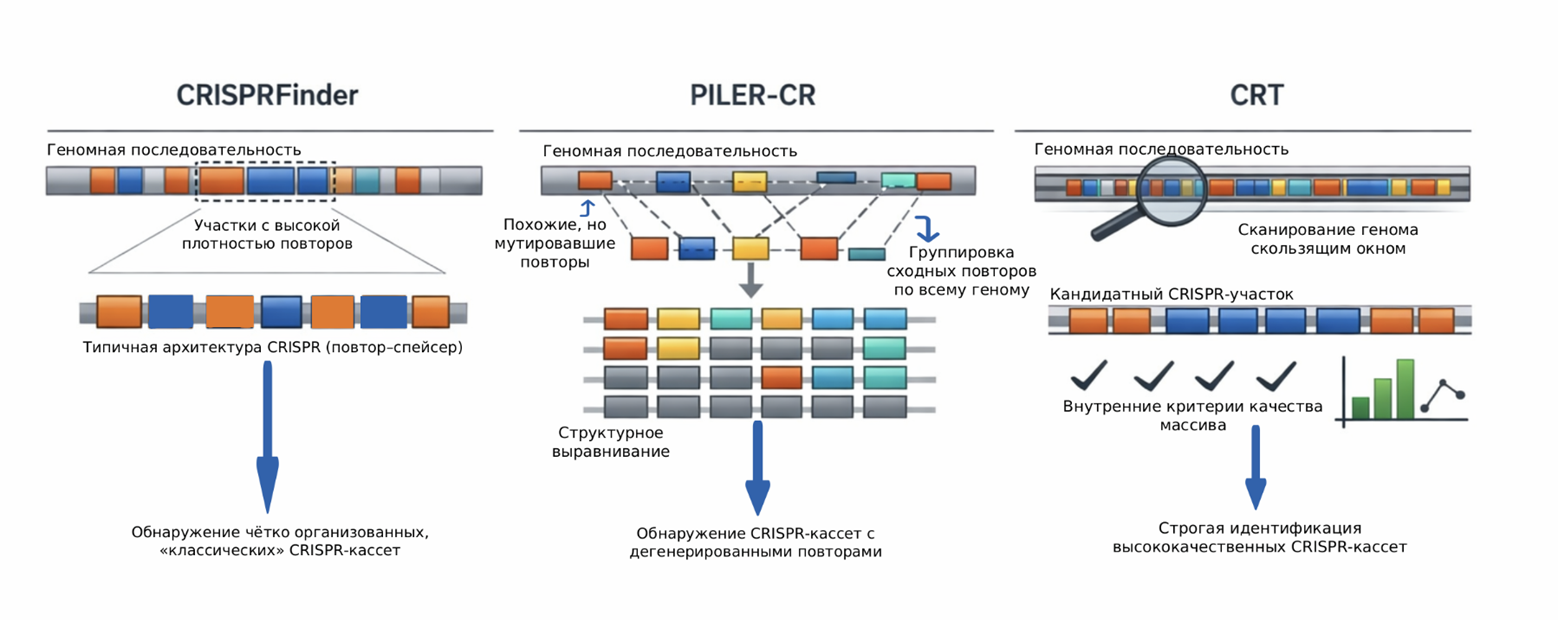
Рисунок 6. Различные стратегии поиска CRISPR-кассет: CRISPRFinder ориентирован на классическую архитектуру массива, PILER-CR — на выравнивание сходных повторов, CRT — на регулярность и качество структуры массива.
Использование нескольких алгоритмов позволило получить согласованные результаты и повысить надежность идентификации CRISPR-кассет: массивы, обнаруженные всеми тремя методами, рассматривались как достоверные (рис. 7).
Когда все спейсеры были собраны, возник ключевой вопрос: какие именно вирусы оставили эти следы в геномах C. botulinum?
После формирования полного набора спейсеров ключевым вопросом стало определение их происхождения — выявление бактериофагов, с которыми C. botulinum взаимодействовала в прошлом. Для этого использовался инструмент CRISPRTarget, сопоставляющий последовательности спейсеров с известными вирусными геномами. Анализ проводится в два этапа: каждый спейсер фрагментируется, после чего его части сравниваются с последовательностями из базы данных RefSeq—Viral [31]. Такой подход позволяет выявлять как полные, так и частичные совпадения между спейсерами и вирусными геномами.
В основе работы CRISPRTarget лежит алгоритм BLASTn, который оценивает не только факт совпадения, но и его длину, ориентацию и статистическую значимость [32], что особенно важно при анализе коротких спейсерных последовательностей длиной 30–40 нуклеотидов.
В результате анализа для части спейсеров были выявлены достоверные соответствия с геномами бактериофагов, инфицирующих Clostridium и родственные им бактерии. В то же время, значительная доля спейсеров не имела совпадений в существующих базах данных, что может указывать на взаимодействие с фагами, утраченными в ходе эволюции или еще не представленными в секвенированных коллекциях.
Для исключения ложноположительных результатов все автоматические совпадения были дополнительно проверены вручную на основе BLASTn-выравниваний, полученных в CRISPRTarget. Для каждого соответствия оценивались положение протоспейсера в вирусном геноме, длина и степень идентичности выравнивания, а также его уникальность по отношению к другим вирусным последовательностям. Короткие, неспецифичные и повторяющиеся совпадения были исключены из дальнейшего анализа.
В совокупности, примененный подход позволил сформировать надежный набор соответствий между спейсерами CRISPR-кассет C. botulinum и геномами бактериофагов, что дало возможность реконструировать спектр фаговых взаимодействий, характерных для анализируемых штаммов.
Что рассказала нам иммунная память бактерии
Когда мы собрали и сопоставили данные, стало ясно: иммунная память C. botulinum устроена куда сложнее, чем можно было ожидать. В общей сложности мы нашли 1277 уникальных спейсера — это своего рода молекулярные «отметки», которые бактерия оставляет после встречи с вирусами. Но оказалось, что распределены они крайне неравномерно: у одних штаммов — всего один-два спейсера, у других — десятки, у некоторых — более 70. По сути получается, что одни штаммы пережили лишь несколько столкновений, а другие — были атакованы вирусами столько раз, что накопили настоящие архивы.
Интересно и другое: в некоторых геномах в хромосоме одновременно присутствовали две разные CRISPR-Cas системы. Это как если бы в клетке работали сразу два уровня иммунной обороны. И еще один важный результат — в большинстве CRISPR-кассет повторяется один и тот же мотив: TAAATACATCTCATGTTAATGTTCAAC (рис. 7).
Рисунок 7. Консенсусная лого-последовательность, полученная в результате выравнивания CRISPR-повторов суперкласса А семейства 7.
<[7]
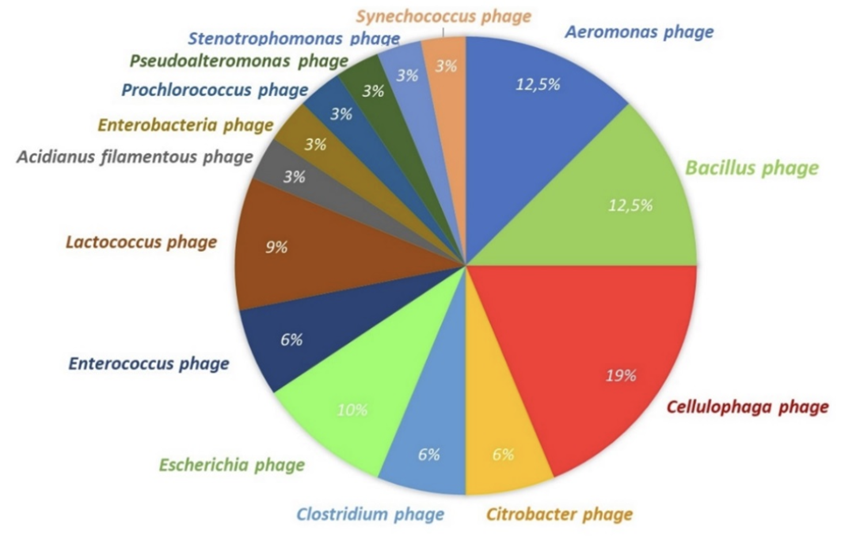
Рисунок 8. Идентифицированные через протоспейсеры фаги, хозяевами которых являются данные виды бактерий.
<[7]
Мы сравнили его со справочником повторов в базе CRISPRmap — и выяснили, что он относится к суперклассу A, семейству 7, мотиву 6. Проще говоря: это высококонсервативный тип повторов, характерный для различных бактерий и архей.
Самый интригующий этап — это сопоставление спейсеров с известными бактериофагами. Когда мы отправили найденные последовательности в программную систему CRISPRTarget, стало понятно, что иммунная память C. botulinum охватывает очень широкий круг вирусов (рис. 8). Всего было идентифицировано 33 протоспейсера, соответствующих разным фагам. Наиболее частые совпадения относятся к фагам бактерий рода Cellulophaga — около 19% совпадений. Эти бактерии обитают в морских отложениях и водорослях, что согласуется с тем фактом, что штаммы C. botulinum нередко обнаруживаются именно в почве и донных отложениях.
Далее по частоте следуют фаги родов Aeromonas и Bacillus (~12,5%). Обе группы связаны с водной средой и почвенными биотопами, а бактерии Aeromonas могут быть и патогенами человека. Следующая группа — фаги, ассоциированные с: Clostridium, Enterococcus, Escherichia, Lactococcus. Часть этих бактерий является представителями нормальной кишечной микрофлоры человека, что указывает на вероятность взаимодействия C. botulinum с кишечной средой.
Менее многочисленные группы представлены фагами: Citrobacter, Prochlorococcus, Pseudoalteromonas, Stenotrophomonas, Synechococcus. И здесь также прослеживается связь с почвенными, морскими и кишечными экологическими нишами. Эти связи согласуются с разнообразием природных ниш, которые C. botulinum может занимать.
Рисунок 9. Места приобретения иммунитета к фагам штаммов C. botulinum.
Если рассматривать полученные результаты в совокупности, становится ясно, что C. botulinum не является бактерией, жестко привязанной к одной экологической нише. Разнообразие CRISPR-кассет и спейсеров, а также их частичные соответствия как известным, так и неописанным бактериофагам, указывает на то, что разные штаммы бактерии на протяжении эволюции взаимодействовали с вирусами, характерными для различных сред — водных, почвенных, кишечных и, вероятно, морских экосистем.
Такая «мозаичная» CRISPR-память отражает сложную экологическую историю C. botulinum и объясняет, почему универсального фага против этого патогена, вероятно, не существует. В то же время, именно эта особенность делает CRISPR-анализ ценным инструментом для разработки фаготерапии: информация о составе спейсеров позволяет перейти от случайного подбора фагов к их целенаправленному отбору с учетом экологического и эволюционного контекста конкретных штаммов (рис. 9).
CRISPR как источник информации о фаговых взаимодействиях
Анализ CRISPR-кассет показал, что в геномах C. botulinum содержится не случайный набор фрагментов, а структурированная информация о прошлых взаимодействиях с бактериофагами. Совокупность спейсеров отражает длительное эволюционное давление со стороны вирусов и позволяет рассматривать патоген как активный элемент сложных экологических систем, включающих почвенные, водные и кишечные ниши.
CRISPR-память C. botulinum может быть использована как источник данных о спектре фагов, с которыми бактерия сталкивалась в прошлом, об условиях ее существования и потенциальных путях циркуляции в природе. Такой подход позволяет перейти от описательного изучения патогена к анализу его эволюционных взаимодействий с вирусами на геномном уровне и формирует основу для более рационального выбора антибактериальных стратегий.
Заключение
В ходе работы с использованием биоинформатических методов были идентифицированы полные CRISPR-Cas системы и CRISPR-кассеты в геномах Clostridium botulinum, охарактеризован их спейсерный состав и выявлены протоспейсеры, соответствующие бактериофагам. Обнаруженные совпадения указывают на то, что фаги, уже распознанные CRISPR-системами бактерии, не могут рассматриваться в качестве эффективных терапевтических агентов против данного возбудителя.
Полученные результаты показывают, что разработка фаговых препаратов против C. botulinum должна опираться на анализ низкого или отсутствующего взаимодействия между фагами и CRISPR-кассетами бактерии. Такой подход позволяет отказаться от эмпирического отбора фагов методом проб и ошибок и перейти к более обоснованному выбору кандидатов на основе геномных данных.
Использование информации, зафиксированной в CRISPR-Cas системах, создает предпосылки для разработки штаммоспецифичных фаговых коктейлей, мониторинга циркуляции C. botulinum в природных экосистемах и оценки рисков возникновения новых вспышек ботулизма. Для патогена, способного вызывать тяжелые и быстро прогрессирующие формы заболевания, такие подходы имеют принципиальное значение для повышения эффективности и безопасности потенциальных терапевтических стратегий.
Литература
- Alexander M. Rawson, Andrew W. Dempster, Christopher M. Humphreys, Nigel P. Minton. (2023). Pathogenicity and virulence of Clostridium botulinum. Virulence. 14;
- Andrew T. Carter, Michael W. Peck. (2015). Genomes, neurotoxins and biology of Clostridium botulinum Group I and Group II. Research in Microbiology. 166, 303-317;
- Одна маленькая лягушка и 10 000 мышей, 20 человек или два слона;
- Столбнячная палочка: токсична и смертельно опасна;
- CRISPR-системы: иммунизация прокариот;
- Антибиотики и антибиотикорезистентность: от древности до наших дней;
- G. A. Teterina, V. P. Salovarova, Yu. P. Dzhioev, N. A. Arefieva, A. Yu. Borisenko, et. al.. (2025). Identification and diversity analysis of CRISPR-Cas systems in the pathogenic strains of Clostridium botulinum to create eco-friendly phage preparations. Izvestiâ vuzov. Prikladnaâ himiâ i biotehnologiâ. 15, 224-233;
- Mohan Babu, Natalia Beloglazova, Robert Flick, Chris Graham, Tatiana Skarina, et. al.. (2011). A dual function of the CRISPR–Cas system in bacterial antivirus immunity and DNA repair. Molecular Microbiology. 79, 484-502;
- Rodolphe Barrangou, Luciano A. Marraffini. (2014). CRISPR-Cas Systems: Prokaryotes Upgrade to Adaptive Immunity. Molecular Cell. 54, 234-244;
- Gyeong-Seok Oh, Seongjin An, Sungchul Kim. (2024). Harnessing CRISPR-Cas adaptation for RNA recording and beyond. BMB Rep. 57, 40-49;
- А. А. Шмакова, О. П. Шмакова, А. А. Карпухина, Е. С. Васецкий. . (2022). CRISPR/CAS: ИСТОРИЯ И ПЕРСПЕКТИВЫ. Онтогенез, 53;
- РНК, ножницы, геномы: объявлены лауреаты Нобелевской премии по химии 2020;
- Manica Negahdaripour, Navid Nezafat, Nasim Hajighahramani, Seyyed Soheil Rahmatabadi, Younes Ghasemi. (2017). Investigating CRISPR-Cas systems in Clostridium botulinum via bioinformatics tools. Infection, Genetics and Evolution. 54, 355-373;
- Travis G. Wentz, Benjamin J. M. Tremblay, Marite Bradshaw, Andrew C. Doxey, Shashi K. Sharma, et. al.. (2022). Endogenous CRISPR-Cas Systems in Group I Clostridium botulinum and Clostridium sporogenes Do Not Directly Target the Botulinum Neurotoxin Gene Cluster. Front. Microbiol.. 12;
- Cédric Woudstra, Caroline Le Maréchal, Rozenn Souillard, Marie-Hélène Bayon-Auboyer, Isabelle Mermoud, et. al.. (2016). New Insights into the Genetic Diversity of Clostridium botulinum Group III through Extensive Genome Exploration. Front. Microbiol.. 7;
- Thibault Le Gratiet, Caroline Le Marechal, Marie Devaere, Marianne Chemaly, Cédric Woudstra. (2021). Exploration of the Diversity of Clustered Regularly Interspaced Short Palindromic Repeats-Cas Systems in Clostridium novyi sensu lato. Front. Microbiol.. 12;
- Kathleen N. McAllister, Joseph A. Sorg. (2019). CRISPR Genome Editing Systems in the Genus Clostridium : a Timely Advancement. J Bacteriol. 201;
- Patrick L. Wagner, Matthew K. Waldor. (2002). Bacteriophage Control of Bacterial Virulence. Infect Immun. 70, 3985-3993;
- Rajesh V. Wagh, Ruchir Priyadarshi, Ajahar Khan, Zohreh Riahi, Jeyakumar Saranya Packialakshmi, et. al.. (2025). The Role of Active Packaging in the Defense Against Foodborne Pathogens with Particular Attention to Bacteriophages. Microorganisms. 13, 401;
- A. V. Letarov. (2020). History of Early Bacteriophage Research and Emergence of Key Concepts in Virology. Biochemistry Moscow. 85, 1093-1112;
- Nicole Mihelson, Dorian B. McGavern. (2021). Viral Control of Glioblastoma. Viruses. 13, 1264;
- Бактериофаги в медицине;
- Бактериофаги для отделения интенсивной терапии: российские исследователи проверили новый подход;
- Zhen Zhang, Meeri Lahti, François P. Douillard, Hannu Korkeala, Miia Lindström. (2020). Phage lysin that specifically eliminates Clostridium botulinum Group I cells. Sci Rep. 10;
- K Oguma, H Iida, M Shiozaki, K Inoue. (1976). Antigenicity of converting phages obtained from Clostridium botulinum types C and D. Infect Immun. 13, 855-860;
- Yoshihiko Sakaguchi, Tetsuya Hayashi, Ken Kurokawa, Keisuke Nakayama, Kenshiro Oshima, et. al.. (2005). The genome sequence ofClostridium botulinumtype C neurotoxin-converting phage and the molecular mechanisms of unstable lysogeny. Proc. Natl. Acad. Sci. U.S.A.. 102, 17472-17477;
- I. Grissa, G. Vergnaud, C. Pourcel. (2007). CRISPRFinder: a web tool to identify clustered regularly interspaced short palindromic repeats. Nucleic Acids Research. 35, W52-W57;
- Paul C. Lott, Ian Korf. (2014). StochHMM: a flexible hidden Markov model tool and C++ library. Bioinformatics. 30, 1625-1626;
- Robert C Edgar. (2007). PILER-CR: Fast and accurate identification of CRISPR repeats. BMC Bioinformatics. 8;
- Charles Bland, Teresa L Ramsey, Fareedah Sabree, Micheal Lowe, Kyndall Brown, et. al.. (2007). CRISPR Recognition Tool (CRT): a tool for automatic detection of clustered regularly interspaced palindromic repeats. BMC Bioinformatics. 8;
- Ambarish Biswas, Joshua N. Gagnon, Stan J.J. Brouns, Peter C. Fineran, Chris M. Brown. (2013). CRISPRTarget. RNA Biology. 10, 817-827;
- Ying Chen, Weicai Ye, Yongdong Zhang, Yuesheng Xu. (2015). High speed BLASTN: an accelerated MegaBLAST search tool. Nucleic Acids Research. 43, 7762-7768.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚