
SciNat за ноябрь 2025 #5: кошки из Египта, жаростойкий птичий грипп и контроль аппетита
30 ноября 2025
SciNat за ноябрь 2025 #5: кошки из Египта, жаростойкий птичий грипп и контроль аппетита
- 89
- 0
- 0
Кошки из Эллинистического Египта. Домашние кошки в настоящее время распространены по всему миру, однако анализ ДНК древних останков в Европе и Анатолии позволяет предположить, что их распространение человеком началось лишь около 2000 лет назад, в эпоху Римской империи, вероятно, из Северной Африки. — The cat diaspora out of Africa.
-
Автор
-
Редактор
Из нового выпуска дайджеста SciNat вы узнаете, чем опасны для нас птичьи вирусы и какие белки влияют на теломеры. Мы расскажем, как влияют на мозг препараты для контроля пищевого поведения и когда люди начали разводить разные породы собак. А также о новой системе работы с данными на основе искусственного интеллекта, которая предлагает новые способы по созданию лекарств.
Эпидемиология
Вирусы гриппа А птичьего происхождения устойчивы к высоким температурам у млекопитающих

При заражении млекопитающих вирусами гриппа у них часто повышается температура тела в качестве иммунного ответа. Возникающая в результате лихорадка может защитить от тяжелой формы заболевания, но эта защита преодолевается вирусами птичьего гриппа, которые эволюционировали для размножения при более высокой температуре тела птиц.
Вирусы гриппа А, которые циркулируют среди птиц, отлично чувствуют себя в их кишечнике при температуре 40–42 oC. Но, когда они попадают к людям, адаптированные к нам вирусы гриппа размножаются при более низкой температуре — около 33 oC в верхних дыхательных путях. Повышение температуры тела — это древний способ борьбы с инфекциями у теплокровных животных, включая нас. Но работает ли оно напрямую против вирусов или же мобилизует иммунную систему? Ученые решили проверить, может ли повышение температуры остановить грипп.
Специально для эксперимента, исследователи создали похожие вирусы на основе человеческого штамма PR8, который вызывает болезнь у мышей, но не опасен для людей. Они заменили часть белка PB1 в одном вирусе на «птичью» версию, сделав его устойчивым к высоким температурам (40 oC). Теперь у них были два вируса: один, как человеческий, плохо размножающийся при жаре, и другой — похожий на птичий — устойчивый к ней. В лаборатории птичьи вирусы пандемий 1918, 1957 и 1968 годов тоже имели такой белок, что делало их более опасными.
В экспериментах на мышах без лихорадки оба вируса вызывали тяжелую болезнь. Но когда ученые искусственно повысили температуру тела мышей (имитируя лихорадку на 2 oC), результат изменился: человеческий вирус стал слабым, вызывая лишь легкие симптомы, а птичьи мутанты продолжали буйствовать, усиливая тяжесть заболевания.
Это доказывает, что лихорадка — мощное оружие против гриппа. Повышение температуры на пару градусов превращает смертельную болезнь в легкую простуду для вирусов, адаптированных к людям. Но птичьи вирусы, устойчивые к жаре, обходят эту защиту, что объясняет, почему они вызывают пандемии. — Avian-origin influenza A viruses tolerate elevated pyrexic temperatures in mammals, «Биомолекула»: «Грипп».
Молекулярная биология
Быстрая компенсаторная эволюция в составе мультибелкового комплекса сохраняет целостность теломер
Теломеры играют роль защитных «колпачков» на концах хромосом, предотвращая их «слипание» и ошибочное распознавание клеткой как повреждения ДНК. У плодовой мушки Drosophila melanogaster эту защиту обеспечивают белки HOAP и HipHop, являющиеся частью крупного белкового комплекса. Однако эти белки со временем мутируют, особенно под влиянием «эгоистичных» генетических элементов, таких как мобильные ретротранспозоны, которые пытаются захватить теломеры для своего размножения. Это создает внутригеномный конфликт: эволюция меняет эти белки, но может нарушить работу комплекса.
Главная цель исследования Лина и коллег — разобраться, разрушают ли такие мутации взаимодействие между белками и грозят ли они потерей ключевых функций, а также как природа это преодолевает. Они провели эволюционно-ориентированные эксперименты, чтобы смоделировать конфликт в действии.
Ключевое открытие — HOAP эволюционировал адаптивно, чтобы ограничивать эгоистичные теломерные ретротранспозоны, что привело к положительному отбору на шесть аминокислот в HipHop. Эти изменения, вероятно, возникли под давлением мобильных элементов, стремящихся «взломать» комплекс. Когда ученые заменили HipHop у D. melanogaster на версию из близкородственного вида Drosophila yakuba, HOAP не смог нормально прикрепиться к теломерам, вызвав их летальное слияние и снижение материнской фертильности — эмбрионы развивались плохо, поскольку комплекс не работал своевременно.
Решение проблемы заключается в межмолекулярной компенсаторной эволюции: фертильность и защита теломер восстановились, если скорректировать те шесть аминокислот в HipHop (сделав их совместимыми с HOAP того же вида) или ввести HOAP из исходного вида. Это демонстрирует, как взаимные адаптации белков сохраняют жизненно важные функции под натиском эгоистичных элементов.
В целом, такие внутригеномные конфликты — обычное следствие эволюции, но они рискуют нарушить критически важные комплексы, предотвращающие рак и старение (не только у мух, но и у людей). Эксперименты из работы в Nature (от Коринн Симонти и коллег) показывают, как эволюция не просто меняет белки, а тщательно балансирует их взаимодействия, чтобы избежать катастрофы, помогая понять, как геном справляется с самоуничтожением собственных частей. — Rapid compensatory evolution within a multiprotein complex preserves telomere integrity, «Биомолекула»: «Мода на ретро. Где встречается обратная транскрипция, и как она эволюционировала».
Медицина
Как препараты от ожирения подавляют «пищевой шум» в мозге
Исследователи идентифицировали нейронный биомаркер компульсивной тяги к еде и показали, что он подавляется препаратом для похудения Mounjaro. Препарат для лечения ожирения тирзепатид, известный как Mounjaro или Zepbound, способен снижать активность мозга, связанную с навязчивыми мыслями о еде — так называемым пищевым шумом. Ученые под руководством Кейси Хэлперна впервые использовали имплантированные электроды для прямого измерения влияния подобных препаратов на мозг людей с тяжелым ожирением. Особенно значимо исследование одной участницы, которая начала принимать высокую дозу тирзепатида: это позволило увидеть, как препарат подавляет паттерны компульсивного поведения.
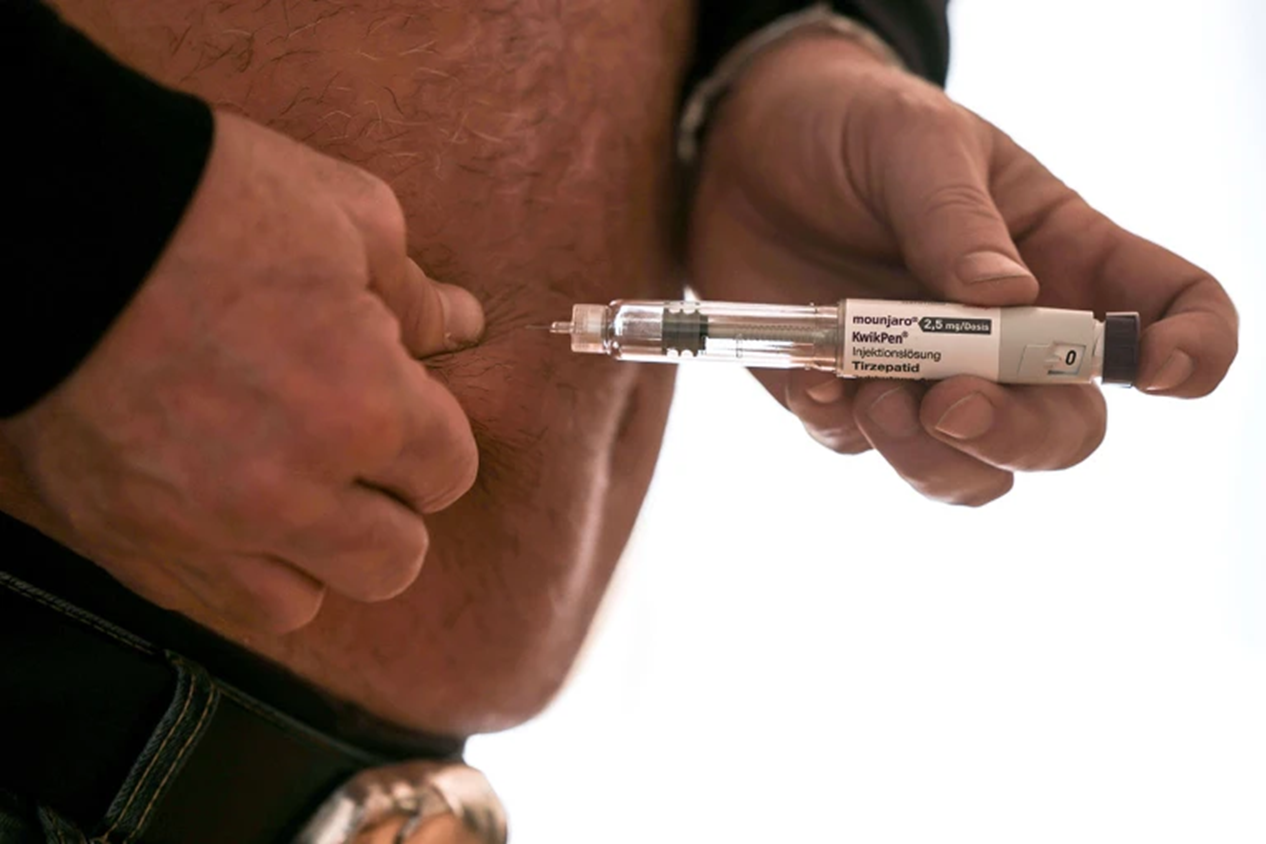
Такие препараты, как «Оземпик» и Mounjaro, воздействуют на рецепторы GLP-1 в мозге, регулируя аппетит.
Электрод был размещен в прилежащем ядре мозга — области, отвечающей за вознаграждение и тесно связанной с рецепторами GLP-1, которые имитируют эти препараты. У первых участников эпизоды сильного пищевого шума сопровождались всплесками низкочастотной активности мозга, что стало маркером чрезмерной тяги. После начала приема тирзепатида такие паттерны существенно снижались, помогая понять, как препарат сдерживает голод.
Это открытие, опубликованное в журнале Nature Medicine, дополняет усилия по глубокому стимулированию мозга для борьбы с ожирением, особенно у тех, кому не помогают другие методы. Оно проливает свет на нейронные механизмы, стоящие за успехом тирзепатида в контроле веса. — How obesity drugs quiet ‘food noise’ in the brain, «Биомолекула»: «Оземпик: больше, чем средство для похудения», «Аппетит как мишень: почему все попытки обуздать ожирение и диабет проваливались, пока не появились агонисты рецепторов инкретинов».
Палеонтология
Как древние люди разводили и продавали первых домашних собак
Анализ окаменелостей, черепов и геномов собак и волков показывает, что процесс одомашнивания начался тысячи лет назад, задолго до викторианской эпохи, когда заводчики активно формировали современные породы. Ученые изучили более 600 трехмерных моделей черепов собак и волков, живших за последние 50 000 лет, и выявили характерные отличия в строении собачьего черепа: укороченная и расширенная морда по сравнению с волчьей. Эта отличительная форма впервые появилась у останков возрастом около 11 000 лет, найденных на северо-западе России, где геномы образцов оказались ближе к домашним собакам.

Современные хаски имеют родственные связи с ранними арктическими собаками.
После этого периода у собак, связанных с поздними охотниками-собирателями и ранними земледельцами, произошел быстрый рост разнообразия форм и размеров черепа, который охватил более половины вариаций, известных у современных пород. Причины такого раннего разнообразия могут включать целенаправленную селекцию для различных потребностей людей: охоты, охраны территорий или даже коммуникации. Экстремальные формы, такие как плоские морды мопсов или бульдогов, не встречаются в древних находках и, вероятно, развились гораздо позже.
Второе исследование сосредоточилось на геномах 17 древних собак из Восточной Азии и Центральной Евразии за последние 10 000 лет. Сравнение с ранее опубликованными данными указывает на то, что древние популяции высоко ценили уникальные черты своих собак и могли торговать ими по всему миру, способствуя распространению одомашненных животных. Эти открытия, опубликованные в журнале Science, проливают свет на культурную роль собак в человеческом обществе, но остается открытым вопрос точного времени, места и причин изначального одомашнивания волков. — How ancient humans bred and traded the first domestic dogs, «Биомолекула»: «Чертог разума».
Фармакология
Система активного обучения с использованием транскриптомного анализа выявляет модуляторы фенотипов заболеваний
Фенотипический поиск лекарств — это подход, когда ученые ищут препараты, влияющие на поведение клеток в целом, а не только на одну конкретную мишень. Он особенно полезен для сложных болезней с множеством причин, которые часто игнорируют традиционные методы. Но чтобы превратить данные о генах (геномные сигнатуры) в реальные химические соединения, нужны гибкие инструменты. Исследователи разработали такую систему, чтобы упростить этот процесс.
Одноклеточные карты генной активности (транскриптомные атласы) подробно показывают, как клетки меняются при болезнях. Аналогично, химические вещества оставляют «следы» в генах, когда на них воздействуют. Ученые предположили: если сравнить эти следы с желаемыми изменениями в клетках, можно быстро отобрать перспективные молекулы для тестирования. Это сэкономит время и ресурсы, позволяя использовать точные, но медленные анализы.
Для этого ученые создали rugReflector — модель глубокого обучения, обученную на огромной базе Connectivity Map (CMap), где собраны эффекты почти 10 тысяч веществ на 52 типах клеток. Модель ранжирует молекулы по тому, насколько они могут вызвать нужные генетические изменения, заданные пользователем на основе атласов. Плюс, добавили активное обучение: система итеративно уточняет цели, комбинируя генные данные с наблюдениями за клетками, — это создает «замкнутый цикл», где лаборатория и алгоритм работают рука об руку.
Команда собрала набор данных из 1,2 миллиона клеток, подвергнутых 88 химическим воздействиям в 10 линиях нормальных и раковых клеток (используя одноклеточное секвенирование РНК). Добавив публичные данные из CMap и SciPlex, они доказали: DrugReflector точно предсказывает эффекты даже на новых примерах, обходя конкурентов.
В моделях крови модель помогла найти вещества, вызывающие дифференцировку (специализацию) мегакариоцитов и эритроцитов — с точностью в 10 раз выше случайного выбора. В онкологии она восстановила известные лекарства и пути для двух типов рака. Для углубления в мегакариоциты создали еще один набор данных: стволовые клетки крови с отслеживанием генов и фенотипа (внешних признаков) под действием веществ. Сопоставив данные, ученые улучшили сигнатуру — точность выросла вдвое. Это выявило ключевые генетические изменения и оптимальные состояния клеток для терапии. Дополнительные эксперименты с CRISPR подтвердили: есть два типа индукторов мегакариоцитов, и даже частичное блокирование синтеза холестерина может направить клетки в нужное русло.
Модели на основе генной активности мастерски связывают биологию болезней с химией лекарств, помогая находить вещества для сложных клеточных процессов. Предложенная система активного обучения объединяет машинное обучение, генный скрининг и анализ фенотипа — это ускоряет поиск препаратов, учитывая всю сложность заболеваний. В итоге она выявляет ключевые «узлы» для терапии и находит молекулы с многогранными механизмами действия, открывая путь к новым лекарствам. — Active learning framework leveraging transcriptomics identifies modulators of disease phenotypes, «Биомолекула»: «Поиск лекарственных мишеней».
Видеоверсия дайжеста SciNat за ноябрь 2025.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚




