
Союз листа и металла: искусственный фотосинтез
18 марта 2016
Союз листа и металла: искусственный фотосинтез
- 3827
- 1
- 6
Реально ли объединить биоинженерную мысль и миллиарды лет эволюции?
-
Автор
-
Редакторы
Бесконтрольное потребление ископаемых ресурсов привело мир на порог эколого-энергетического кризиса. В подобной обстановке необходим принципиально иной источник энергии, который, с одной стороны, вписывался бы в наш нефтяной мир, а с другой — был бы возобновим, экологически чист и экономически выгоден. Возможное решение — искусственный фотосинтез (ИФ), благодаря которому на свет уже появились рукотворные установки для синтеза органики из электричества, света, а также удивительные полупроводниковые бронебактерии-фотосинтетики.
Глобальный энергетический кризис, или Зачем нужен искусственный фотосинтез
Сегодня и без того большое население планеты увеличивается на 1% ежегодно [1]. Растущие с каждым годом энергетические потребности человечество удовлетворяет прежде всего за счет ископаемых ресурсов. Но уже ни для кого не секрет, что запасы нефти и угля ограничены и в большинстве случаев невозобновимы [2]. Когда их объемы перестанут соответствовать глобальным темпам развития (или даже израсходуются), мир столкнется с энергетическим кризисом небывалых масштабов.
Уже сейчас можно наблюдать ожесточенную борьбу, развязавшуюся на мировой арене за крупные источники ископаемого топлива. В перспективе горючего будет всё меньше, а конфликты интересов будут происходить всё чаще.
Последние два века человечество было ослеплено доступностью ископаемых энергоносителей и разработало множество основанных на них технологий, без которых жизнь сегодня просто немыслима. Сначала были уголь и паровозы, затем люди научились получать электричество, сжигая тот же уголь, производить газовые плиты, частный и общественный транспорт — всё это требует расхода запасенных миллионы лет назад органических веществ. Используя энергию этих веществ, человечество совершило скачок во многих областях общественной жизни: численность мирового населения превысила 7 млрд [3], в пустынях возникли цветущие города и государства, производственные мощности и уровень потребления увеличиваются год от года. Без сомнения, современный мир немыслим без угля, нефтепродуктов и газа.
Здесь проявляется дилемма современной энергетики: с одной стороны, абсолютно очевидна необходимость перехода на возобновляемые источники энергии, с другой — мир не приспособлен для потребления такой энергии. Однако в последнее десятилетие всё активнее ведутся разработки источника энергии, который мог бы решить эту дилемму. Речь идет об искусственном фотосинтезе (ИФ) — способе превращать энергию солнца в удобную форму органического горючего.
Нельзя забывать, что сжигание топлива приводит к массивным выбросам СО2 в атмосферу, негативно влияющим на состояние всей биосферы. В крупных городах это влияние особенно заметно: тысячи дымящих машин и предприятий образуют смог, и каждый горожанин, выбравшись за город, прежде всего восхищается свежим воздухом. Создание источника энергии, который подобно растениям поглощал бы СО2 и вырабатывал О2, могло бы остановить идущую на всех парáх деградацию окружающей среды.
Таким образом, ИФ — потенциальное решение как мирового энергетического, так и экологического кризисов. Но как же работает ИФ и чем он отличается от природного?
Несовершенство зелени
При естественном фотосинтезе энергия света поглощается специальными фоточувствительными молекулами — растительными (или бактериальными) пигментами, которые при этом дестабилизируются и могут легко отдать один из своих электронов [4]. Оторвавшийся от пигмента электрон наделен большой энергией, и он использует её, чтобы с поглощением протона восстанавливать вещества только на одной стороне мембраны, что приводит к перепаду концентраций Н+ на разных сторонах мембраны (рис. 1, 2).
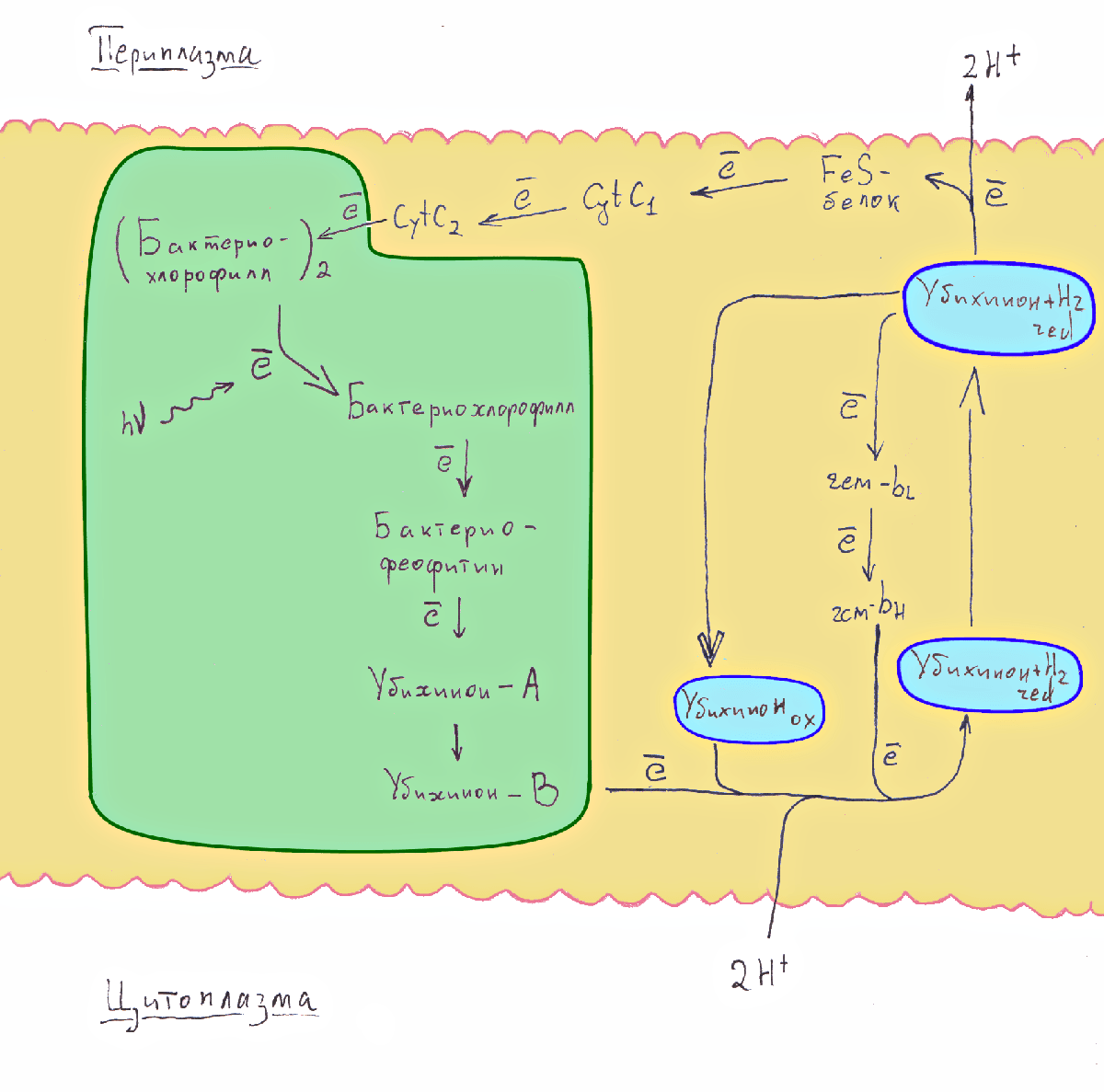
Рисунок 1. Циклический фотосинтез у пурпурных бактерий. Энергия фотона выбивает электрон из бактериохлорофилла в составе фотосистемы. Электрон через цепь переносчиков поступает на внутреннюю сторону мембраны, где помогает убихинону присоединить два протона из цитоплазмы. Убихинон, диффундировавший на внешнюю сторону мембраны, высвобождает протоны в периплазму и отдает ранее полученный электрон другой цепочке переносчиков, возвращающих его на исходное место. В результате на один фотон приходится два перенесенных через мембрану протона. Образующийся в ходе работы фотосистемы протонный градиент — универсальная форма запасания энергии [4].
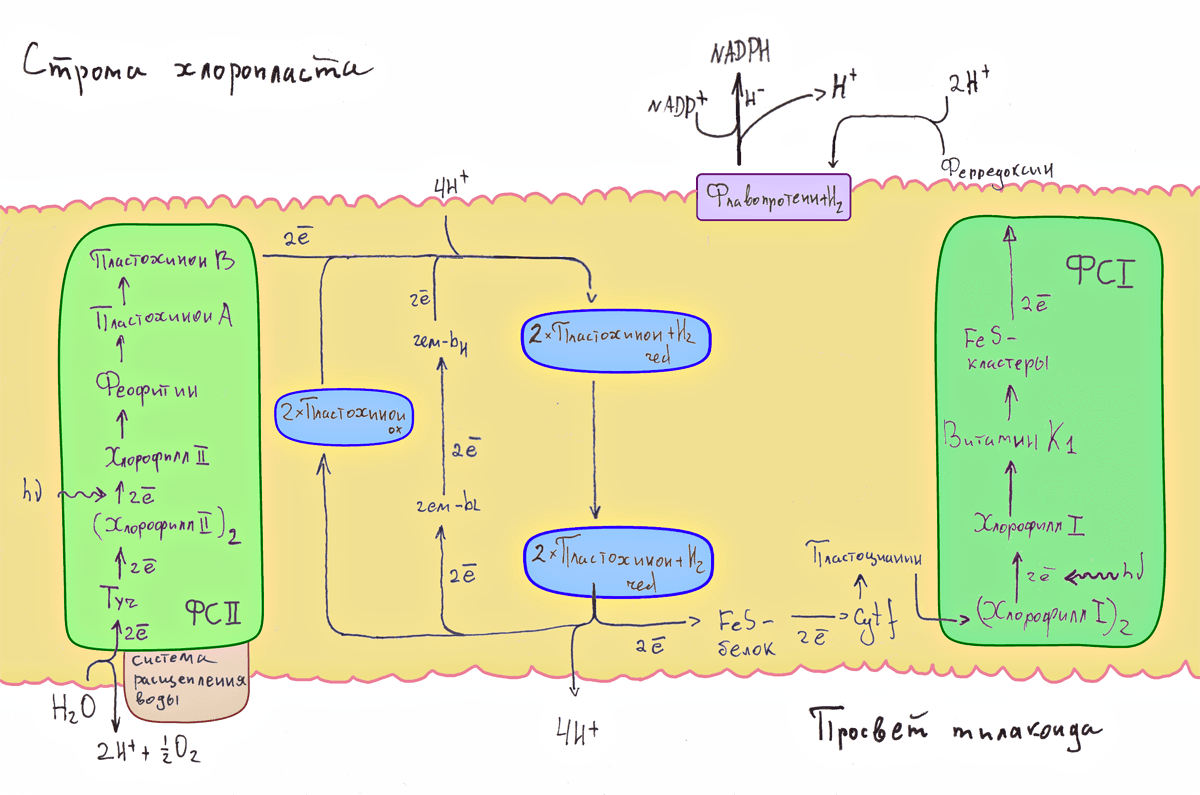
Рисунок 2. Нециклический фотосинтез у растений. Электрон покидает возбужденный светом хлорофилл фотосистемы II (ФС-II), а получившуюся «дырку» заполняют электроны, высвободившиеся при расщеплении воды. Конечный приёмник электронов — не пигмент фотосистемы, как у пурпурных бактерий, а НАДФ+. Еще одно отличие — у растений две фотосистемы (ФС-I и ФС-II) образуют сопряженный механизм, и для одного такта его работы требуется поглощение двух фотонов [4]. На рисунке не показан b6f-комплекс.
Полученный градиент H+ предоставляет энергию для синтеза АТФ с помощью фермента АТФ-синтазы, подобно тому, как падающая вода становится источником энергии для водяной мельницы (рис. 3). АТФ — универсальный переносчик химической энергии в клетке и участвует в абсолютном большинстве энергозатратных реакций, в том числе — в реакциях цикла Кальвина, обеспечивающих превращение СО2 в восстановленную органику [5]. В этом цикле бóльшая часть энергии расходуется на борьбу с побочными реакциями. Есть и другие пути ассимиляции углерода — например, путь Вуда-Льюнгдала, о котором будет написано дальше.
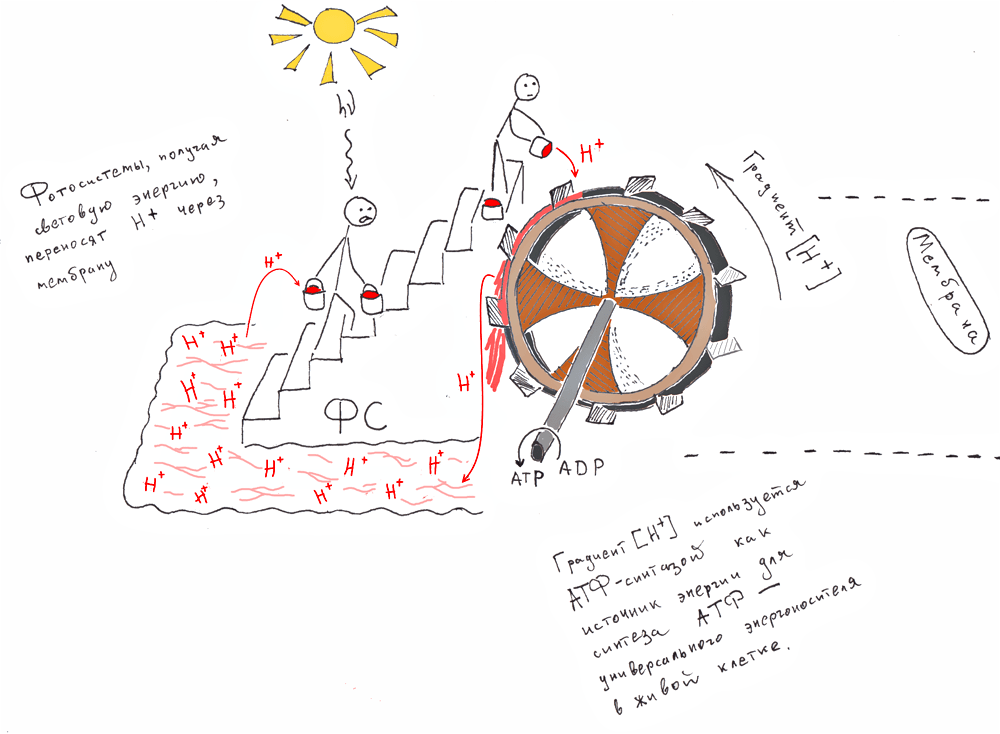
Рисунок 3. Запасание энергии света. При фотосинтезе белки-фотосистемы переносят протоны через мембрану за счет энергии фотонов. Фермент АТФ-синтаза сбрасывает образующийся градиент концентраций Н+ и производит универсальный переносчик энергии в клетке — АТФ. Аналогия с вращающейся водяной мельницей, на самом деле, очень близка к реальности.
Хотя фотосинтез в конечном счете обеспечивает всю биосферу энергией, КПД этого процесса оставляет желать лучшего (табл. 1). Рекордсмен фотосинтеза — выращиваемое для производства биотоплива сорго, у которого эффективность перевода солнечной энергии в химическую составляет 6,6%. Для сравнения: у картофеля, пшеницы и риса — около 4% [6].
| Причина потери энергии | Потеря энергии | Остаток |
|---|---|---|
| Поглощение фотонов только видимой части спектра | 47% | 53% |
| Лишь часть светового потока проходит через фотосинтезирующие части листа | 70% | 37% |
| Хотя в видимом свете есть высоко- и низкоэнергетические фотоны, все они поглощаются фотосистемами как низкоэнергетические (своеобразный принцип каравана) | 24% | 28% |
| Потери при синтезе глюкозы | 68% | 9% |
| Очистка листа от побочных продуктов фотосинтеза (см. фотодыхание) | 32% | 6% |
В то же время типичный КПД для современных солнечных батарей — 15-20%, а опытные образцы достигли значения 46% [7], [8]. Такая разница в КПД рукотворных фотоячеек и живых растений объясняется прежде всего отсутствием стадий синтеза. Но есть и более тонкое отличие: растительные фотосистемы извлекают энергию только из фотонов видимого света с длинами волн 400–700 нм, причем выход от высокоэнергетических фотонов ровно такой же, как и от низкоэнергетических. Полупроводники, применяемые в солнечных батареях, улавливают фотоны более широкого спектра. А для максимального выхода в одну батарею объединяются материалы, созданные специально для разных частей спектра солнечного света.
Конечная цель инженеров ИФ — создать установку (или искусственный организм), который бы осуществлял фотосинтез лучше растений. Сегодня биоинженерная мысль достигла уровня, на котором можно попытаться это сделать. И от года к году попытки ученых становятся всё ближе и ближе к заветной цели, заставляя нас дивиться невероятным открытиям.
Такой разный ИФ
Самая простая схема ИФ — полностью абиотический синтез органики на катализаторе. В 2014 году был открыт рутениевый катализатор, который при освещении синтезирует метан из H2 и СО2 [9]. При оптимальных условиях, подразумевающих нагрев до 150 °С и интенсивное освещение, один грамм этого катализатора создает один миллимоль метана в час, что, конечно же, очень мало. Сами ученые, исследующие катализатор, признают, что такая скорость реакции при довольно высокой стоимости катализатора слишком низка для его практического применения.
Реальный фотосинтез — многостадийный процесс, на каждой стадии которого происходит потеря энергии [10]. Отчасти это даже хорошо, потому что открывает большой простор для оптимизации. В случае же абиогенного фотосинтеза всё, что можно сделать — это придумать принципиально новый катализатор.
Совершенно иной подход к ИФ — создание биореакторов, работающих на солнечной энергии. В таких биореакторах, как ни странно, используют нефотосинтезирующие микроорганизмы, которые всё же могут фиксировать СО2, используя иные источники энергии.
Ознакомимся с несколькими типами конструкций аппаратов для ИФ на конкретных примерах.
В 2014 году были опубликованы результаты испытаний установки, которая переводит ток в биомассу с рекордным КПД 13% [11]. Чтобы получить ИФ-реактор, достаточно подключить солнечную батарею. Эта установка по сути является электрохимической ячейкой (рис. 4а), где два электрода помещены в питательную среду с бактериями Ralstonia eutropha (они же — Cupriavidus necator). При подведении внешнего тока катализатор на аноде проводит расщепление воды на кислород и протоны, а катализатор на катоде — восстановление протонов до газообразного водорода. R. еutropha получает энергию для ассимиляции СО2 в цикле Кальвина за счет окисления Н2 ферментом гидрогеназой.
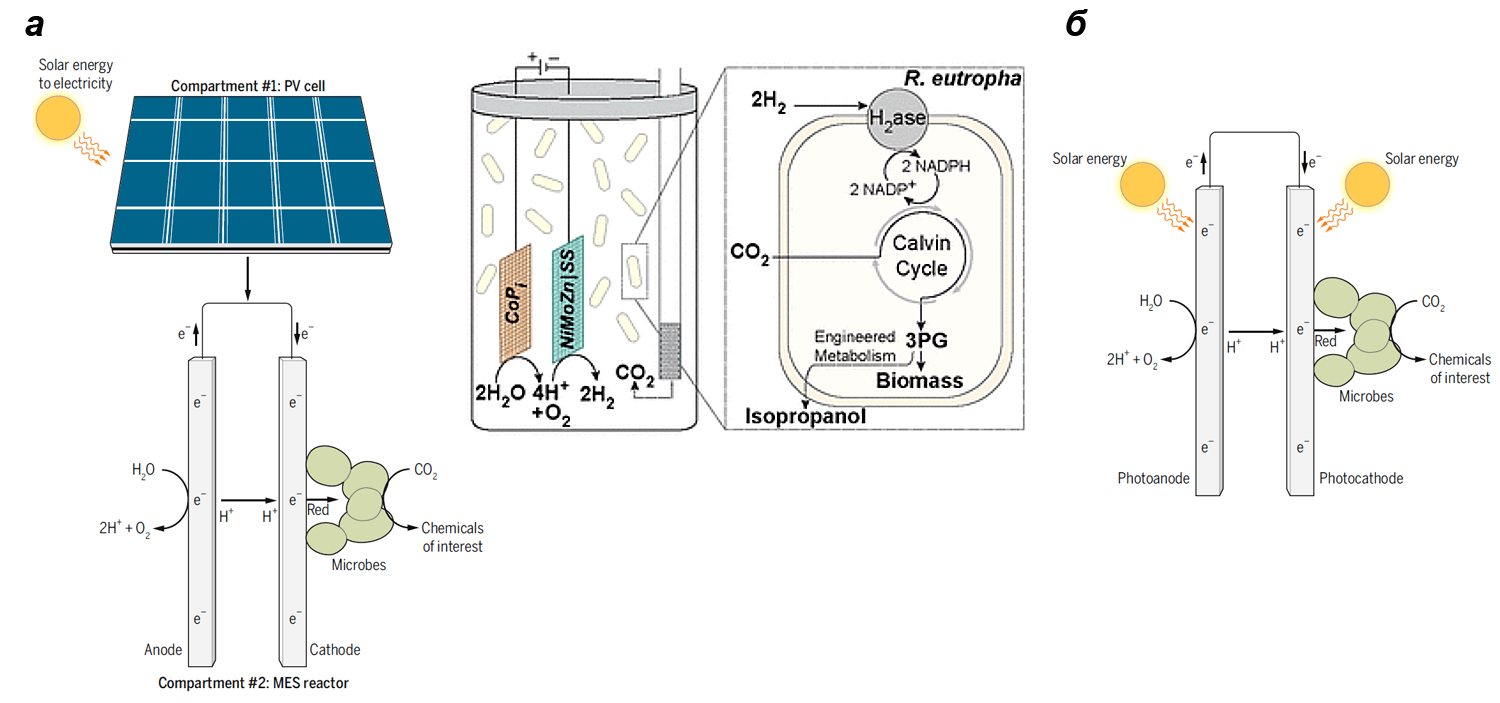
Рисунок 4. Биореакторы для ИФ на базе электрохимических ячеек. Ток может генерироваться за счет фотолиза воды на аноде при помощи солнечной батареи (а) или без неё (б). В обоих случаях забранные у воды электроны обеспечивают микробам-автотрофам восстановительные эквиваленты, необходимые для фиксации СО2.
Согласно расчетам разработчиков, совмещение их установки с типичной солнечной батареей (18% КПД) приведет к суммарной эффективности фотосинтеза 2,5%, если переводить всю энергию света в рост биомассы, и 0,7% — если использовать генетически модифицированных бактерий, синтезирующих бутанол. Такой результат сравним с эффективностью фотосинтеза в реальных растениях, хотя и не достигает уровня культурных растений. Способность R. еutropha синтезировать органику при наличии Н2 очень интересна не только в контексте ИФ, но и как возможное приложение водородной энергетики [12].
В 2015 году ученые из Калифорнии создали не менее интересную установку, где стадии светопоглощения и синтеза связаны более тесно [13]. Фотоанод сконструированного реактора при освещении расщепляет воду на кислород, протоны и электроны, которые направляются по проводнику к катоду (рис. 4б). Чтобы повысить скорость фотолиза воды, идущего на границе раздела фаз, фотоанод сделан из кремниевых нанопроводков, многократно увеличивающих его поверхность.
Катод этой установки состоит из «леса» TiO2-наностержней (рис. 5а), среди которых растут бактерии Sporomusa ovata. Электроны от фотоанода поступают именно к этим бактериям, которые используют их как восстановительные эквиваленты для превращения растворенного в среде СО2 в ацетат.
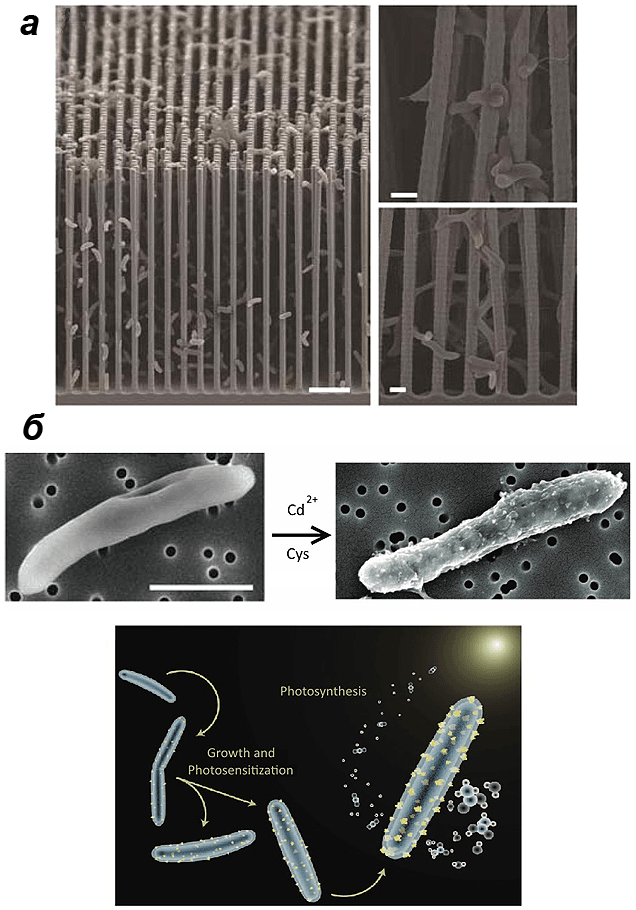
Рисунок 5. Искусственный фотосинтез немыслим без наноматериалов. а — В ИФ-реакторе из статьи [13] СО2 фиксируют бактерии, растущие в «нанолесу» из кремниевых стрежней, покрытых TiO2 (слой 30 нм); этот нанолес создает необходимые бактериям анаэробные условия и повышает поверхностную плотность контактов бактерий с проводником. б — При принципиально ином подходе не бактерий помещают на полупроводник, а полупроводник — на бактерий; благодаря панцирю из CdS, умирающие на свету бактерии становятся фотосинтетиками.
Нанолес из TiO2 выполняет сразу несколько функций: обеспечивает высокую плотность бактерий на контакте, защищает облигатно анаэробных S. ovata от растворенного в среде кислорода и тоже может преобразовывать свет в электричество, помогая бактериям фиксировать СО2.
S. ovata — бактерии с очень гибким метаболизмом, который легко подстраивается под рост в так называемом электротрофном режиме. Они фиксируют СО2 по пути Вуда-Льюнгдала, в котором на рост биомассы идет только 10% ацетата, а оставшиеся 90% выбрасываются в окружающую среду.
Но сам по себе ацетат особой ценности не представляет. Для его перевода в более сложные и дорогие вещества в реактор вносят генетически модифицированных Escherichia coli, синтезирующих из ацетата бутанол, изопреноиды или полигидроксибутират. Последнее вещество E. coli производит с наибольшим выходом.
Что же до КПД всей установки, то он весьма низок. Только 0,4% солнечной энергии получается перевести в ацетат, а превращение ацетата в полигидроксибутират идет с КПД 50%. Суммарно только 0,2% световой энергии удается запасти в виде органики, которую можно дальше использовать как топливо или сырьё для химпроизводства. Разработчики считают основным своим достижением то, что созданная ими установка может использоваться для совершенно разных химических синтезов без принципиальных изменений в конструкции. В этом видна аналогия с природным фотосинтезом, где из полученного при ассимиляции СО2 3-фосфоглицерата в конечном счете синтезируются всевозможные органические вещества [14].
В обеих описанных технологиях разработчики пытались совместить совершенство полупроводников как поглотителей световой энергии с каталитической мощью биологических систем. И обе полученные установки представляли собой «обратные» топливные элементы, где ток используется для синтеза веществ.
При принципиально ином подходе отдельные клетки объединяются с полупроводниками в единое целое. Так, в самом начале 2016 года была опубликована работа, в которой бактерию-ацетоген Moorella thermoacetica выращивали в среде с высоким содержанием цистеина и кадмия [15], [16]. В результате обычно погибающая на свету М. thermoacetica покрывалась панцирем из CdS (полупроводника) и тем самым не только получала защиту от солнца, но и становилась фотосинтетиком: электроны от CdS поступали в путь Вуда-Льюнгдала (рис. 5б).
Опыты над такой «бронированной» бактерией показали, что СО2 фиксируется не только на свету, но и в темноте (при соблюдении суточного цикла). Причина этого — накопление метаболитов фотосинтеза на свету в таком количестве, что клетки не успевают их перерабатывать. Основное преимущество таких бактерий в сравнении с вышеописанными ячейками — самоорганизация. Для ячеек необходимо заранее изготавливать наноматериалы и катализаторы, а сами эти детали со временем только изнашиваются. В случае М. thermoacetica фотосинтетические единицы делятся, сами производят и ремонтируют всё необходимое, если в среде достаточно кадмия и цистеина. Этих бактерий пока не исследовали как источник топлива, но по значениям квантового выхода фотосинтеза они не уступают растениям.
Ждать осталось недолго...
Технологии ИФ находятся пока на стадии прототипов, но их разработчики видят большой простор для оптимизации. Оптимизировать можно полупроводники-светоуловители, микроорганизмы, пространственную организацию бактерий, прочие катализаторы. Но прежде всего необходимо решить проблему стабильности. КПД изготовленных установок заметно падает уже спустя несколько дней работы. Полностью готовый прибор для ИФ, подобно любой живой системе, должен регенерировать и самовоспроизводиться. В этой связи особенно интересны М. thermoacetica, к которым эти свойства относятся в полной мере.
И хотя существующие образцы далеки от совершенства, работы в области ИФ ценны прежде всего тем, что показывают принципиальную возможность встроить солнечную энергетику в мир, захваченный двигателем внутреннего сгорания. Ветряки и солнечные батареи, безусловно, обладают высоким КПД и уже практически полностью обеспечивают энергопотребление в Уругвае и Дании, а ГЭС — важные узлы в энергосети многих стран [17], [18]. Но замена горючего электричеством в большинстве случаев требует кардинальной перестройки энергосетей и не всегда возможна.
Дальнейшее развитие ИФ требует массивных инвестиций. Можно представить, что фирмы — производители солнечных батарей, которым футурологи прочат мировое господство в области энергетики уже к 2030 [19], будут заинтересованы в развитии этой пока молодой и неопытной науки на стыке биоэнергетики, материаловедения и наноинженерии. Кто знает, может ИФ и не станет повседневностью будущего, а может, работа над ним даст толчок водородной энергетике или биофотовольтаике [20], [21]. Ждать осталось недолго, поживем — увидим.
Литература
- Population Pyramids of the World from 1950 to 2100. (2013). PopulationPyramid.net;
- Корзинов Н. (2007). Нефть — живая и мертвая: Откуда взялось черное золото. «Популярная механика»;
- 7 000 000 000;
- Скулачев В.П., Богачев А.В., Каспаринский Ф.О. Мембранная биоэнергетика: Учебное пособие. М.: Изд-во МГУ, 2010. — 368 с.;
- Кто на самом деле крутит углеродное колесо;
- Slattery R.A. and Ort D.R. (2015). Photosynthetic energy conversion efficiency: setting a baseline for gauging future improvements in important food and biofuel crops. Plant Physiol. 168, 383–392;
- Dimroth F., Grave M., Beutel P., Fiedeler U., Karcher C., Tibbits T.N.D. et al. (2014). Wafer bonded four-junction GaInP/GaAs//GaInAsP/GaInAs concentrator solar cells with 44.7% efficiency. Prog. Photovoltaics. 22, 277–282;
- New world record for solar cell efficiency at 46%. (2014). RenewEconomy;
- O’Brien P.G., Sandhel A., Wood T.E., Jelle A.A., Hoch L.B., Perovic D.D. et al. (2014). Photomethanation of gaseous CO2 over ru/silicon nanowire catalysts with visible and near-infrared photons. Adv. Sci. 1;
- Hall D.O. and Rao K.K. Photosynthesis (6th Edition). Cambridge: Cambridge University Press, 1999. — 214 p.;
- Torella J.P., Gagliardi C.J., Chen J.S., Bediako D.K., Colón B., Way J.C. et al. (2014). Efficient solar-to-fuels production from a hybrid microbial—water-splitting catalyst system. PNAS. 112, 2337–2342;
- Бактерии для водородной энергетики;
- Liu C., Gallagher J.J., Sakimoto K.K., Nichols E.M., Chang C.J., Chang M.C., Yang P. (2015). Nanowire-bacteria hybrids for unassisted solar carbon dioxide fixation to value-added chemicals. Nano Lett. 15, 3634–3639;
- Волонтер фотосинтеза;
- Sakimoto K.K., Wong A.B., Yang P. (2016). Self-photosensitization of nonphotosynthetic bacteria for solar-to-chemical production. Science. 351, 74–77;
- Элементы: «Нефотосинтезирующую бактерию можно обучить фотосинтезу, поместив ее в подходящую среду»;
- Neslen A. (2015). Wind power generates 140% of Denmark’s electricity demand. The Guardian;
- Watts J. (2015). Uruguay makes dramatic shift to nearly 95% electricity from clean energy. The Guardian;
- Raj A. (2014). Kurzweil: solar energy will be unlimited and free in 20 years. Business Insider;
- Zhang T. (2015). More efficient together: Hybrid bioinorganic photosynthesis yields a wide range of chemicals. Science. 350, 738–739;
- Биофотовольтаика. По-настоящему зелёная энергия;
- Намсараев З. (2014). Биотопливо — один из кандидатов на роль технологии будущего. «Постнаука».
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚




