
Академия и бизнес воскрешения
25 февраля 2026
Академия и бизнес воскрешения
- 123
- 0
- 0
Взаимодействие науки и бизнеса приводит к удивительным результатам, одним из которых может стать воскрешение шерстистого мамонта.
Рисунок в полном размере.
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Мировой рынок биотехнологий на 2025 год оценивается в 1,77 миллиардов долларов. Ожидается, что к 2035 году рынок превысит 6,34 миллиардов долларов, расширяясь в среднем на 13,6% ежегодно. При этом в данный момент академическая среда США оправляется от урезания администрацией финансирования STEM-исследований (англ. Science, Technology, Engineering and Mathematics — естественные науки, технология, инженерия и математика. Результатом сокращений стал переход некоторых ученых из научных институтов в частные компании. Возможно, что сочетание этих факторов даст масштабный толчок развитию биотехнологического бизнеса как в США, так во всем мире.
Заметными событиями 2025 года стали громкие новости о воскрешении лютоволка и мамонта биотехнологической компанией Colossal Biosciences. В этой статье рассмотрена тесная связь академических достижений и работы биотехнологических компаний на примере задачи воскрешения вымерших видов.
Конкурс «Био/Мол/Текст»-2025/2026
Эта работа опубликована в номинации «Академия & Бизнес»» конкурса «Био/Мол/Текст»-2025/2026.

Генеральный партнер конкурса и партнер номинации — международная инновационная биотехнологическая компания BIOCAD.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Генетика вымирания
Концепция вымирания видов описана с помощью модели Extinction vortex — вихря вымирания (рис. 1). Разрушение среды обитания приводит к низкому качеству оставшейся среды обитания, изоляции между оставшимися популяциями и снижению численности популяции. Это приводит к постепенному увеличению инбридинга (близкородственного скрещивания), потере генетического разнообразия (многообразия внутри вида) и снижению приспособленности (характеристики, позволяющей организму выживать), что приводит к дальнейшему сокращению численности популяции вплоть до вымирания. Сокращение численности популяции также повышает восприимчивость к воздействию случайных факторов и катастроф [1].
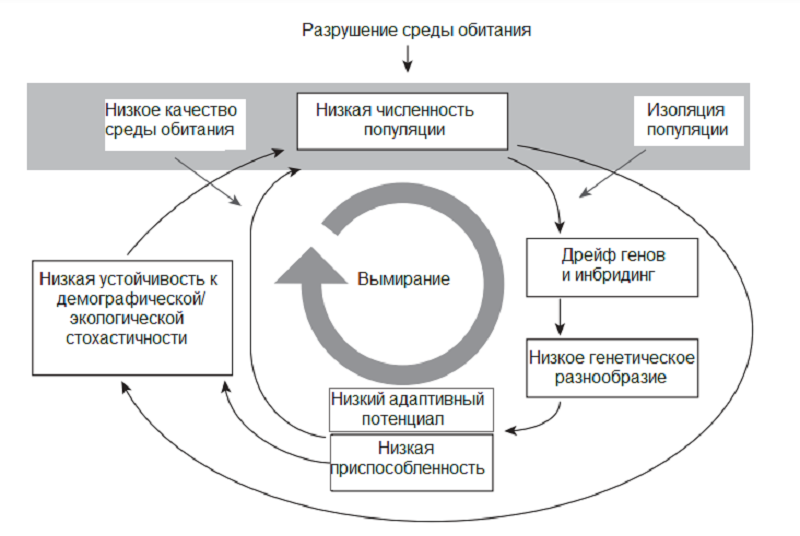
Рисунок 1. Extinction vortex — концепция, описывающая спиральную негативную динамику, ведущую к вымиранию вида.
Иллюстрацией эффекта extinction vortex является вымирание стеллеровой коровы, почвой для которого стала фрагментация ареала и низкое генетическое разнообразие в результате инбредной депрессии (снижения жизнеспособности из-за близкородственного скрещивания). Человеческая деятельность довела дело до печального финала [2].
Маркетинг вымирания
Усилия по сохранению вымирающих видов с помощью биотехнологий ведутся уже давно. Запускаются программы поддержания численности видов (например, фонд Rhino Species направлен на сохранение различных видов носорогов), замораживаются образцы клеток (самый крупный банк замороженных образцов — The Wildlife Biodiversity Bank), используются методы клонирования и анализа ДНК (рис. 2) [3].
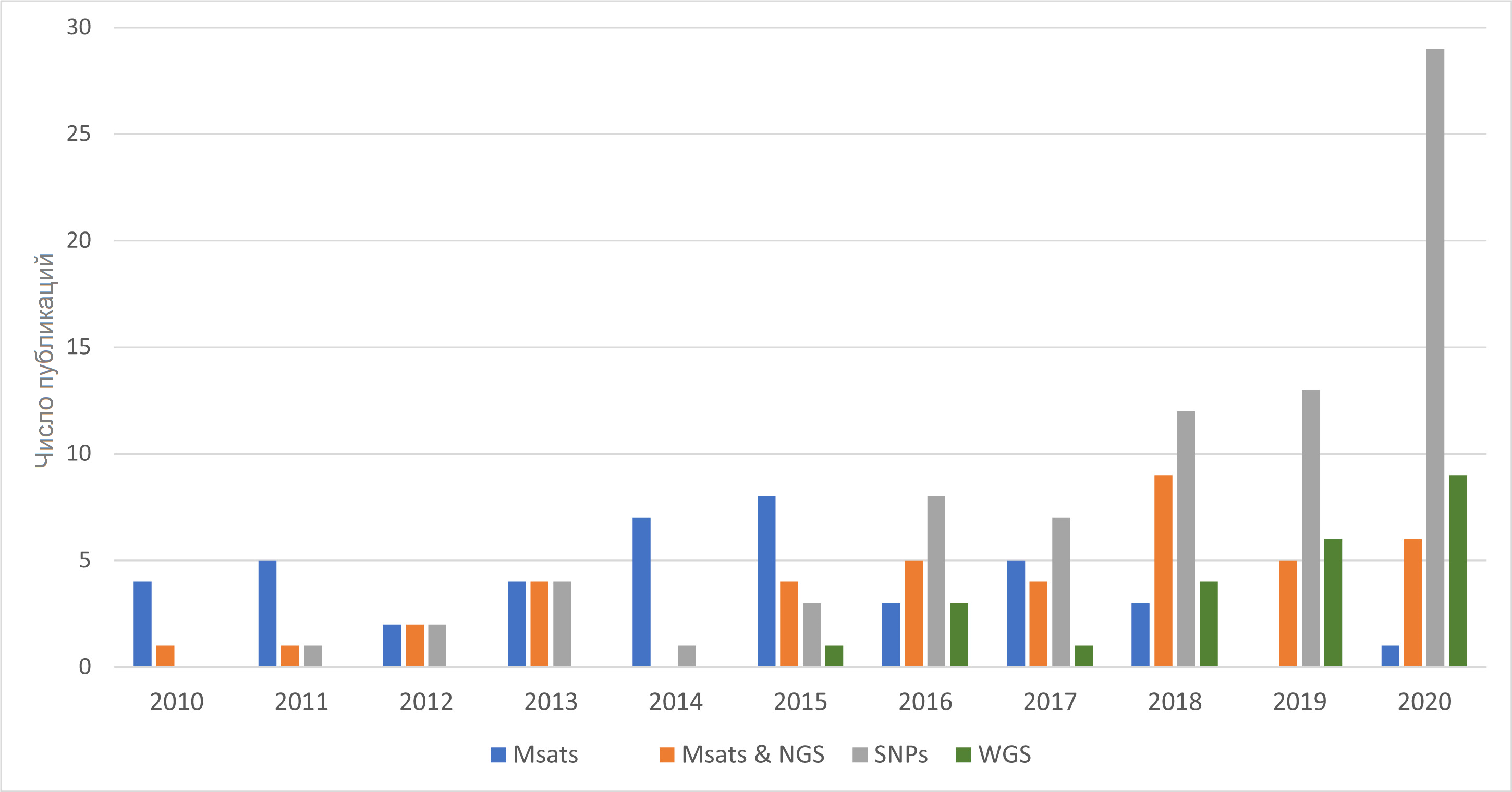
Рисунок 2. Количество публикаций, в которых используется ядерная ДНК для сохранения видов, находящихся под угрозой исчезновения. В исследованиях используются как микросателлитные маркеры Msats (короткие повторяющиеся последовательности ДНК), так и данные секвенирования следующего поколения NGS (next-generation sequencing). С помощью NGS находят однонуклеотидные полиморфизмы SNPs (single-nucleotide polymorphisms), представляющие собой различия в нуклеотидах ДНК между особями и являющиеся наиболее популярным средством в современных исследованиях структуры популяций. Результаты полногеномного секвенирования WGS (whole-genome sequencing), также получаемые технологией NGS, могут быть использованы самостоятельно или в сочетании с микросателлитными маркерами.
Подробнее о микросателлитах читайте на «Биомолекуле»: «Повтор, еще повтор!» [4].
Однако сохранение биологического разнообразия — цель важная, но плохо продаваемая. Последствия смерти последнего самца северного белого носорога, умершего в 2018 году [5], совсем не очевидны . Получить финансирование на проект, направленный на спасение человечества от рака, гораздо проще из-за очевидности пользы. В то же время, проект по спасению вымирающих носорогов неизбежно столкнется с вопросами целесообразности.
Подробнее о спасении северного белого носорога читайте на «Биомолекуле»: «Репродуктивная биология: не время умирать» [6].
После 2025 года обсуждение вымирающих видов трудно представить без упоминания Colossal Biosciences. Зайдем на сайт, подробно рассказывающий о направлениях деятельности компании.
Рисунок 3. Главная страница сайта компании Colossal Biosciences.
На главной странице сайта компании рассказывается о намерении воскрешать вымершие виды, включая шерстистых мамонтов (рис. 3). Цель поражает воображение и привлекает инвестиции от людей далеких сфер деятельности, таких как, например, режиссера «Властелина колец» Питера Джексона. Компания ведет работу и в направление сохранения видов еще только на грани вымирания.
Однако привлечение инвестиций в компанию, которая не генерирует непосредственную прибыль, является амбициозной задачей. В результате новости о рождении ужасного волка становятся действительно громкими [7]. Но стоит ли за громкими именами и новостями реальная технология? И возможно ли достижение такое непростой цели как воскрешение мамонтов усилиями только научных институтов или только частных компаний?
Технология воскрешения
На примере девяти шагов по воскрешению шерстистого мамонта рассмотрим задачи, стоящие перед компанией. Для оценки масштаба подробнее остановимся на этапах, связанных с работой биоинформатиков (подробнее об этом разделе «сухой» биологии читайте на «Биомолекуле»: «Автостопом по биоинформатике» [8]):
Шаг 1. Извлечение ДНК индийского слона из образца ткани живого животного
А зачем компании нужна ДНК индийского слона? Оказывается, по данным филогении именно индийский слон наиболее генетически близок к шерстистому мамонту (рис. 4) [9]. ДНК индийского слона — необходимый ресурс, влияющий на успех последующих шагов.
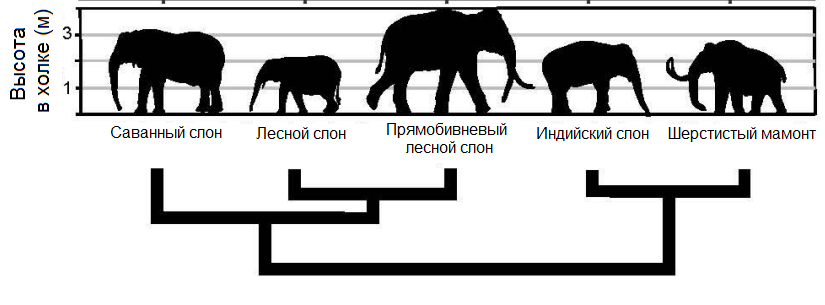
Рисунок 4. Филогенетическое дерево шерстистого мамонта и слонов, полученное методом присоединения ближайших соседей (Neighbor-Joining) на основе различий в геномах Хоботных. Заметно, что мамонт ближе всего именно к индийскому (азиатскому) слону.
Образец кожи, например, был взят у взрослого самца индийского слона в возрасте 50 лет из зоопарка Сан-Диего, Калифорния. Фибробласты (клетки кожи, отвечающие за образование коллагена) были выделены из данного образца и культивированы в Frozen Zoo (крупнейшем банке живых клеток, хранящихся при температуре около –200 oC). Выбор фибробластов обусловлен их доступностью, простотой культивирования, возможностью перепрограммирования в лаборатории в плюрипотентные стволовые клетки (такие клетки можно превратить в любую клетку организма), а также их способностью выделять факторы роста клеток в окружающую среду. ДНК из фибробластов слона была секвенирована для дальнейшей сборки генома.
Шаг 2. Секвенирование ДНК индийского слона и сборка генома
Секвенирование (установление порядка расположения строительных кирпичиков молекулы ДНК — нуклеотидов) полного генома с каждым годом становится все доступнее и является выполнимой задачей (подробнее читайте: «12 методов в картинках: секвенирование нуклеиновых кислот» [10], «Нанопоровое секвенирование: на пороге третьей геномной революции» [11]).
А вот сборка генома млекопитающего — задача уже не столь простая и очевидная. Геном индийского слона большой, состоит из 27 неполовых хромосом и двух половых (X, Y).
Для таких трудоемких задач разработан стандартизированный план действий в рамках проекта VGP (The Vertebrate Genomes Project, Проект Геномов Позвоночных), ставящего целью получить высококачественные последовательности всех хромосом генома для 70 тысяч живущих позвоночных [12]. Согласно данным GenomeArk (ресурса для хранения и скачивания сырых данных секвенирования и сборок геномов в рамках VGP и смежных проектов ), на данный момент полностью собраны геномы 409 видов, идет работа над сборкой геномов 47 видов и получены сырые данные еще для 51 вида позвоночных.
Огромное количество данных, используемых учеными (например, сборки геномов Позвоночных от проекта VGP), хранятся с помощью сервиса от частной компании Amazon (облачная система хранения Amazon S3).
Для сборки генома индийского слона потребовались 3 технологии секвенирования: PacBio Hifi reads, Bionano optical maps и Arima HiC reads (рис. 5). Зачем так много?
- Длинные последовательности ДНК, полученные технологией PacBio Hifi, составляют основу сборки генома. Однако с их помощью получается собрать только контиги (фрагменты ДНК, секвенированные без пропусков). Качественная же сборка генома должна содержать контиги в правильном порядке с минимальным количеством пробелов между ними.
В 2020 году компания PacBio представила технологию высокоточного секвенирования (HiFi), позволяющую получать риды длиной 10–25 кб (то есть 10–25 тысяч нуклеотидов) с минимальной точностью 99% (Q20). - Результаты технологии Bionano optical maps (оптическое геномное картирование) позволяют объединить последовательности, полученные в предыдущем шаге, а также точно упорядочить и ориентировать их относительно друг друга.
Одна из самых популярных технологий оптического картирования разработана в компании Bionano Genomics [13]. - Для получения еще более качественной сборки генома слона потребуется технология HiC, позволяющая получить информацию о взаимодействии разных участков ДНК друг с другом.
Технология HiC, предоставляется, например, компанией Arima [14], [15].
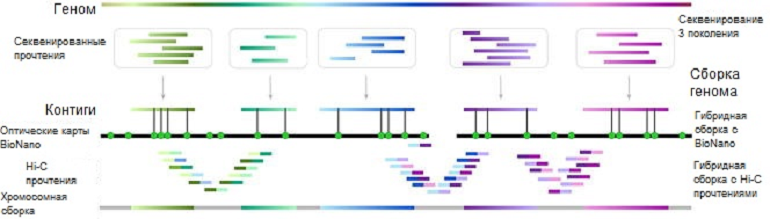
Рисунок 5. Схема сборки генома с использованием разных технологий.
Несмотря на продуманный алгоритм сборки генома позвоночных животных, требуется еще и ручная проверка получившейся сборки, проводимая учеными. Обязательным является и аннотация полученного генома — то есть определение границ генов и других элементов в геноме и установление их функций.
Шаг 3. Сбор жизнеспособных образцов тканей шерстистого мамонта, выделение и секвенирование ДНК
Необходимо собрать много образцов тканей шерстистого мамонта, хорошо сохранившихся из-за вечной мерзлоты и пригодных для дальнейших исследований. Часто такими образцами служат зубы или кости животных.
Однако древняя геномная и митохондриальная ДНК, которую удается извлечь из образцов, распадается на маленькие фрагменты (до 100 нуклеотидов). На краях фрагментов часто происходит мутация цитозинового нуклеотида в урациловый (превращение происходит из-за потери молекулой цитозина аминогруппы, рис. 6). Для последующего секвенирования фрагменты ДНК необходимо размножить с помощью ДНК-полимеразы, которая урациловый нуклеотид будет копировать как тиминовый, а вовсе не цитозиновый. ДНК современных людей (например, палеонтологов) и микроорганизмов часто контаминирует (загрязняет) полученные образцы [16]. Все эти факторы создают трудности в секвенировании древней ДНК и ее последующей сборки в единый геном.
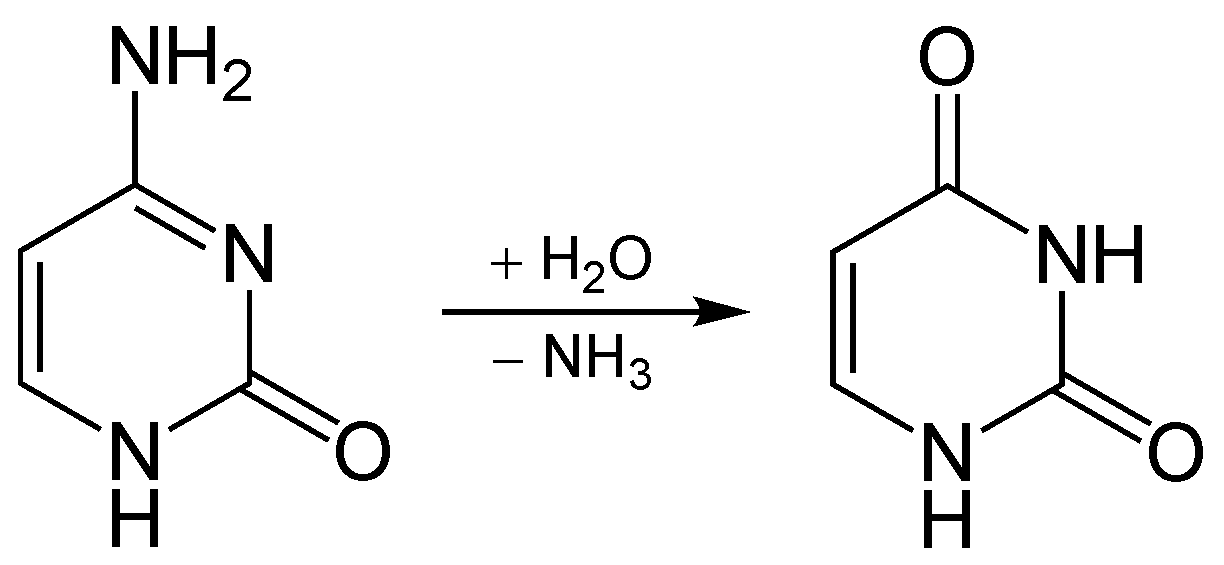
Рисунок 6. Деаминирование цитозина и превращение в урацил.
Несмотря на все трудности, благодаря усилиям палеогенетиков удается получить достаточно хорошие образцы, которые передаются биологам для секвенирования. Затем данные берут биоинформатики, улучшая их качество и делая сборки с помощью различных компьютерных программ.
И, конечно, данный шаг требует как опытных ученых, так и секвенаторы, оборудование и реагенты, закупаемые у частных компаний.
Шаг 4. Сравнение ДНК мамонта и индийского слона
Теперь необходимо сравнить ДНК мамонта и индийского слона и найти отличия, которые позволили мамонту отлично приспособиться к уникальной экосистеме — тундростепям.
В исследовании 2023 года, например, сравнили 23 генома шерстистых мамонтов и 7 геномов индийских слонов. Все геномы слонов и 10 геномов мамонтов обладают покрытием больше x10 (значит, каждый нуклеотид при секвенировании был прочитан в среднем больше 10 раз), что является показателем высокого качества данных [17]. Исследователи нашли много различий в генах, способствующих росту шерсти (AHNAK2, KRT8, FLG), связанных с обменом жира (ACADM, APOB) и термочувствительностью (SCN10A, гены семейства TRP), а также гены, отвечающие за иммунитет. Вероятно, эти гены в геноме индийского слона станут мишенью для геномного редактирования CRISPR.
По словам сооснователя и генерального директора Colossal Бенна Ламма, на данный момент компанией проанализировано 54 генома мамонтов. Использовались как ранее опубликованные данные из открытых источников, так и образцы, полученные компанией. CEO компании отмечает, что такой массив данных получен благодаря тесному сотрудничеству компании с различными учеными и университетами (например, Университетом Стокгольма). Полное интервью Бенна Ламма можно прочитать здесь.
Шаг 5. Создание модифицированных генов и внедрение их в геном слона
Следующим шагом станет редактирование генома индийского слона, чтобы максимально приблизить его к геному мамонта. Теперь, когда основные отличия в геномах установлены, на помощь придет технология CRISPR.
Нобелевская премия 2020 года по химии присуждена Эмманюэль Шарпантье и Дженнифер Дудне за разработку метода геномного редактирования CRISPR-Cas9. Без этого научного открытия осуществить планы компании Colossal Biosciences было бы намного труднее. Подробнее о CRISPR читайте на «Биомолекуле» [18].
Редактирование генов с помощью CRISPR на сегодняшний день является сложной, но выполнимой научной задачей. Технология позволяет вырезать из ДНК определенный участок и вставить на его место другой, полученный в лаборатории.
Проверить, насколько модификация генов приводит к появлению желаемого признака, можно с использованием лабораторных мышей, которые размножаются гораздо быстрее слонов. Например, известны аналоги генов мышей и мамонтов, связанных с холодостойкостью (ген TGFA, например, отвечает за структуру шерсти, а FABP2 — за обмен жиров). Редактирование этих генов у мышей по образу генов мамонта позволит увидеть результат подобного редактирования и сделать выводы о его эффективности.
На данный момент Colossal Biosciences заявляют, что планируют редактировать сразу 65 генов. Наличие качественной сборки референсного генома индийского слона (см. шаг 2) и достоверные сведения о различиях геномов мамонтов и слона (см. шаг 4) облегчают процесс создания библиотек и редактирования генома. А проверить успешность редактирования генома можно за счет секвенирования гибридного генома и его сравнения с геномами мамонта и слона.
Шаг 6. Модификация яйцеклетки индийского слона
На данном шаге действительно потребуется яйцеклетка слона, но не вся. Ядро будет удалено, а на его место подсадят ядро с гибридным геномом слона и мамонта. Под действием электрического стимула яйцеклетка делится и превращается в эмбрион.
Данная технология клонирования успешно использовалась, например, в создании клона лошади Пржевальского по имени Курт (рис. 7). Донором яйцеклетки и суррогатной матерью успешно выступила домашняя лошадь. Спустя 3 года после рождения Курта родился еще один жеребенок Пржевальского, Олли.
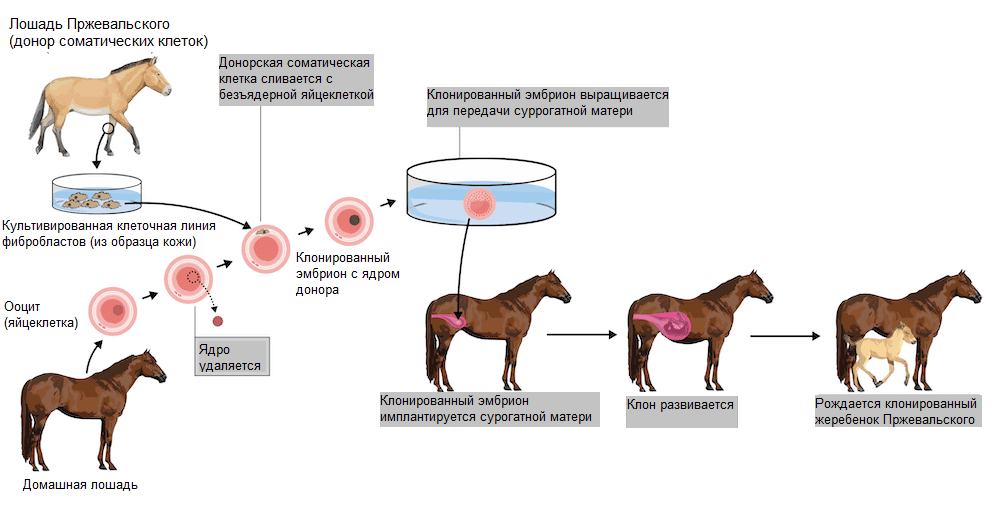
Рисунок 7. Технология клонирования лошади Пржевальского.
Шаг 7. Имплантация эмбриона суррогатной африканской слонихе
Модифицированная яйцеклетка превращается в эмбрион, который имплантируют суррогатной матери. Найти подходящее животное для данной цели довольно сложно, однако сама технология имплантации уже не так невероятна. Например, имплантация эмбриона северного белого носорога была осуществлена в организм южного белого носорога.
Шаг 8. Вынашивание
Развитие в утробе у африканских слонов обычно занимает 18–22 месяца. Не исключен вариант использования искусственной матки, находящейся в разработке [19]. На данный момент не существует технологии, в которой возможно развитие млекопитающего от эмбриона до новорожденного.
Животноводческие компании могут быть заинтересованы в инвестициях в данную технологию, когда процесс воскрешения мамонта дойдет до этого шага.
Шаг 9. Та-дам! Рождение шерстистого мамонта
Новорожденный будет гибридом с генетическими признаками шерстистого мамонта и индийского слона (рис 8).

Рисунок 8. Life imitates art.
Спустя 9 невероятно сложных шагов мы добрались до рождения мамонтенка! На примере данного процесса видно, насколько наука и биотехнологический бизнес сейчас тесно переплетены. Ученые компании Colossal Biosciences пользуются как достижениями и связями академической среды (например, инструментом CRISPR или сотрудничеством с Университетом Швеции), так и технологиями, предоставляемыми частными компаниями (PacBio, Bionano Genomics, Arima, Amazon и др.). Интенсивное использование бизнесом средств маркетинга для привлечения инвестиций может вызывать недоумение, как в случае с лютоволком. Однако финансовые возможности позволяют ученым так активно работать над воскрешением вымерших видов, развивать передовые технологии, в будущем применимые во множестве областей, и привлекать внимание к проблемам вымирающих видов.
Литература
- Ab P. Grootjans, Rudy Van Diggelen, Hans Joosten, Alfons J. P. Smolders. (2012). Restoration of Mires. Restoration Ecology. 203-213;
- Исторический геном стеллеровой коровы проливает свет на причины ее вымирания;
- Carolyn J. Hogg, Kym Ottewell, Peter Latch, Maurizio Rossetto, James Biggs, et. al.. (2022). Threatened Species Initiative: Empowering conservation action using genomic resources. Proc. Natl. Acad. Sci. U.S.A.. 119;
- Повтор, еще повтор!;
- N+1: «Клетки кожи северного белого носорога превратили в предшественники яйцеклеток»;
- Репродуктивная биология: не время умирать;
- PCR News: «Рождение „лютоволка“: фэнтези, НФ или технология»;
- Автостопом по биоинформатике;
- Marc Tollis, Elliott Ferris, Michael S Campbell, Valerie K Harris, Shawn M Rupp, et. al.. (2021). Elephant Genomes Reveal Accelerated Evolution in Mechanisms Underlying Disease Defenses. Molecular Biology and Evolution. 38, 3606-3620;
- 12 методов в картинках: секвенирование нуклеиновых кислот;
- Нанопоровое секвенирование: на пороге третьей геномной революции;
- Arang Rhie, Shane A. McCarthy, Olivier Fedrigo, Joana Damas, Giulio Formenti, et. al.. (2021). Towards complete and error-free genome assemblies of all vertebrate species. Nature. 592, 737-746;
- PCR News: «Оптическое картирование структурных вариаций геномов людей из разных регионов мира выявило различия»;
- Неуловимая архитектура хроматина мухи;
- Alice Maria Giani, Guido Roberto Gallo, Luca Gianfranceschi, Giulio Formenti. (2020). Long walk to genomics: History and current approaches to genome sequencing and assembly. Computational and Structural Biotechnology Journal. 18, 9-19;
- Древняя ДНК: привет из прошлого;
- David Díez-del-Molino, Marianne Dehasque, J. Camilo Chacón-Duque, Patrícia Pečnerová, Alexei Tikhonov, et. al.. (2023). Genomics of adaptive evolution in the woolly mammoth. Current Biology. 33, 1753-1764.e4;
- Просто о сложном: CRISPR/Cas;
- SciNat за сентябрь 2023 #3: психоделики на страже ментального здоровья, искусственная матка и умные птицы.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚





