Максим Никитин: «Если я сделаю лекарство и выведу его в клинику, значит, все было не зря»
14 декабря 2024
Максим Никитин: «Если я сделаю лекарство и выведу его в клинику, значит, все было не зря»
- 1736
- 0
- 1
Максим Никитин в лаборатории.
Центр научных коммуникаций МФТИ, Вера Павлова
-
Автор
-
Редакторы
Максим Никитин заведует лабораторией нанобиотехнологий в МФТИ, руководит направлением «Нанобиомедицина» в университете Сириус, член президиума Совета при президенте РФ по науке и образованию. Звучит внушительно, но это — качественные метрики. Что касается количественных, то индекс Хирша у Максима Никитина — 38. Лет ему столько же. А чем занимается Максим Никитин и почему занимается тем, чем занимается, об этом он сейчас сам расскажет.
Биология в Московском физтехе
XXI век называют «веком живых систем», изучение которых возможно только на стыке наук — математики, физики, химии и биологии. «Биомолекула» представляет серию материалов о том, как занимаются биологией в Московском физико-техническом институте (МФТИ).
— Слушайте, я открыл Google и посмотрел, за что вас коллеги любят. Что я вижу: PNAS, самосборка наночастиц с участием белков [1]. Дальше — Nature nanotechnology, Biocomputing based on particle disassembly [2]. Потом Nature biomedical engineering, работа про разгон эритроцитов для продления времени жизни наночастиц в организме [3]. А венчает все это четвертая работа, в Nature Chemistry — про «коммутацию цепей как фундаментального механизма хранения информации в ДНК» [4], [5]. Я так понимаю, что поначалу у вас все шло про доставку лекарств и смежные вещи. С наночастицами, как термином, я как будто бы знаком: его особенная популярность приходится на нулевые–десятые, и, насколько я понимаю, хайп этого всего уже поутих.
— Ну нет. Вы про мРНК-вакцины слышали [6]? Это наночастицы. Потому что вообще технология доставки генетического материала с помощью липидных частиц, ну то, что дошло до рынка, это наночастицы. Так что хайп — не хайп, все это продолжается.
Ну а мы вообще связаны со всем, что нано-, и всем, что био- . У нас есть любимые органические наночастицы, есть любимые неорганические частицы, мы с ними работаем. Нам интересно научиться доставлять их, например, точно в опухоль после системного введения — опухоль тут просто потому, что мы в основном работаем на модели рака. Для нас главное — попасть туда, куда надо, и не затронуть здоровые ткани. В отличие от тех, кто напрягается над тем, грубо говоря, как убить или вылечить патогенную клетку — какими-нибудь белками-токсинами или антителами. Для нас в первую очередь наука заключается в том, чтобы попасть точно в цель.
На «Биомолекуле» был большой и хороший обзор на эту тему: «Невидимая граница: где сталкиваются “нано” и “био”» [7]. — Ред.
— А! Просто когда я слышу про наночастицы, я думаю про всяческие металлические сущности . Вот эти все идеи, что мы закинем металлический нанопорошок в организм человека, его частицы доберутся до каких-нибудь опухолей, мы их активируем, и они начнут там протыкать своими острыми гранями клеточные мембраны.
— Тут нет такого, что строго неорганические частицы лучше, чем органические. Скорее наоборот, чем ближе к природе, тем лучше. Просто мы используем стратегию не какой-нибудь модификации клеточного иммунитета, а у нас задача с нуля создать — так называемый bottom-up approach, когда мы что-то химически синтезируем, и оно работает с каким-то суперпримитивным не то чтобы интеллектом, но с какой-то логикой. Логикой, близкой к той, в которой работают клетки.
Скорее всего, Ивану на ум приходят квантовые точки, которые действительно содержат атомы разных металлов, правда, «острых граней» у них вроде бы нет: «Квантовые точки — наноразмерные сенсоры для медицины и биологии» [8]. Кстати, за их изучение год назад вручена Нобелевская премия: «Наночастицы для окраски биомолекул и QLED-дисплеев — за что вручили Нобелевскую премию по химии (2023)» [9]. — Ред.
— Это прям синтетическая биология, получается? Мы хотим сделать инструмент, который будет исполнять функции, которые мы в него заложим. И поскольку мы рациональным дизайном занимаемся, отсюда, собственно, у вас и появляется биокомпьютинг.
— Да-да. Упомянутая вами статья 2014 года в Nature nanotechnology как получилась: мне казалось, что все современные системы доставки очень примитивные. Там была большая область до этого так называемых smart polymers — умных полимеров. Они могли, например, при нагревании расшириться, или светом как-то модифицироваться могли, и выпускали низкомолекулярную нагрузку. Но эти стимулы, которыми вызывали ответ — pH, свет, температура, окислительно-восстановительный (редокс) потенциал и так далее — очень неспецифические.
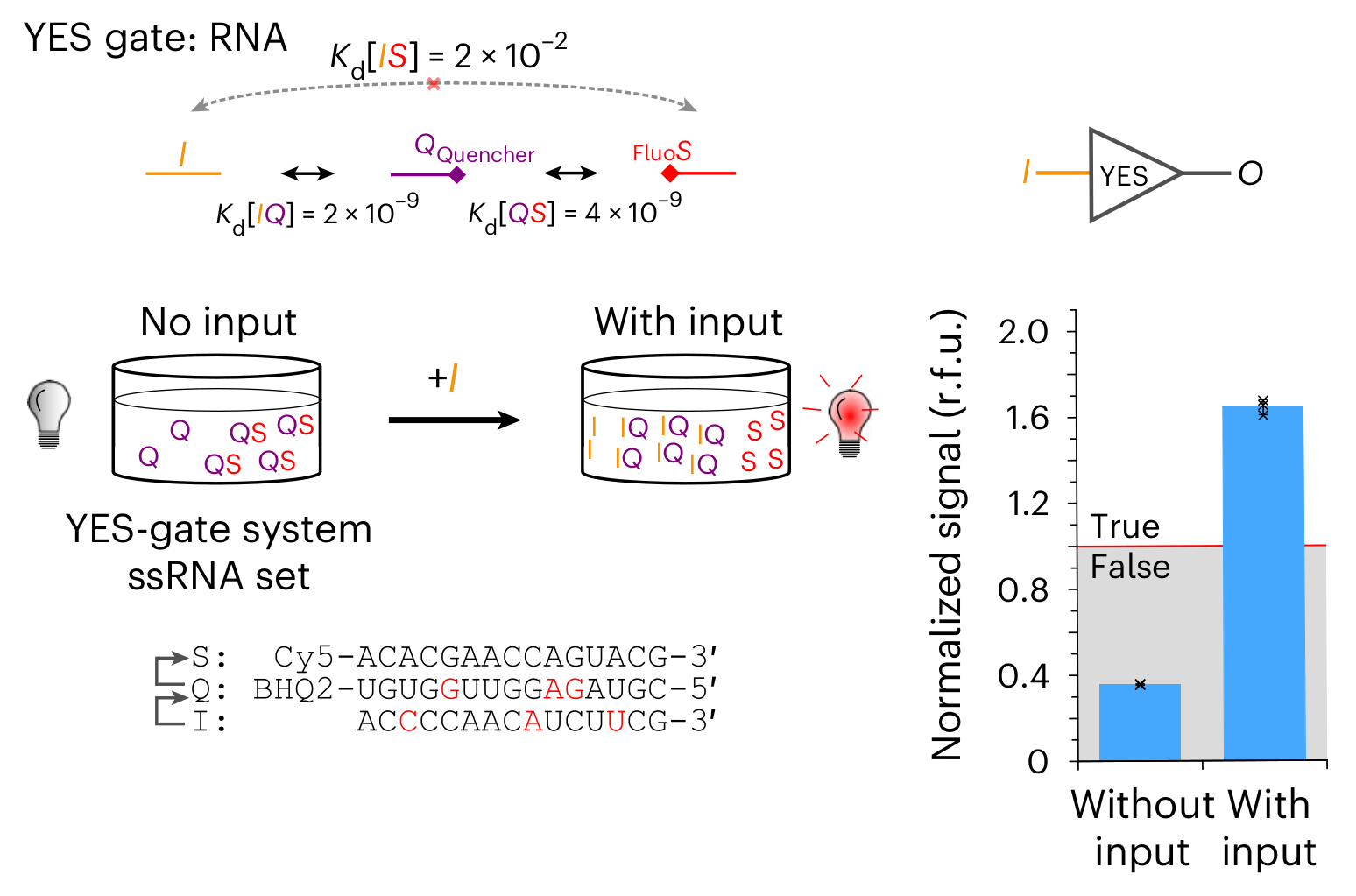
Я этим был внутренне неудовлетворен, мне хотелось, чтобы мы научились делать что-нибудь сложное. Чтобы мы могли доставлять, используя более сложный анализ микроокружения, согласно булевой алгебре, ну это пока. Понятно, что цифровая система редко в биологических системах природой используется. Но тем не менее, чтобы анализировать сразу несколько систем, поскольку они сложные, многофакторные, очень удобно использовать булеву алгебру: есть маркер — это 1, нет маркера — 0. Соответственно, мне в такой постановке хотелось создать частицу, которая могла бы строго отслеживать много параметров, а не только один — не просто наличие одного маркера на клеточной стенке, а сразу многих параметров, в том числе растворимых, и после как-то атаковать мишень (рис. 1). Это, собственно, и удалось сделать в той работе.
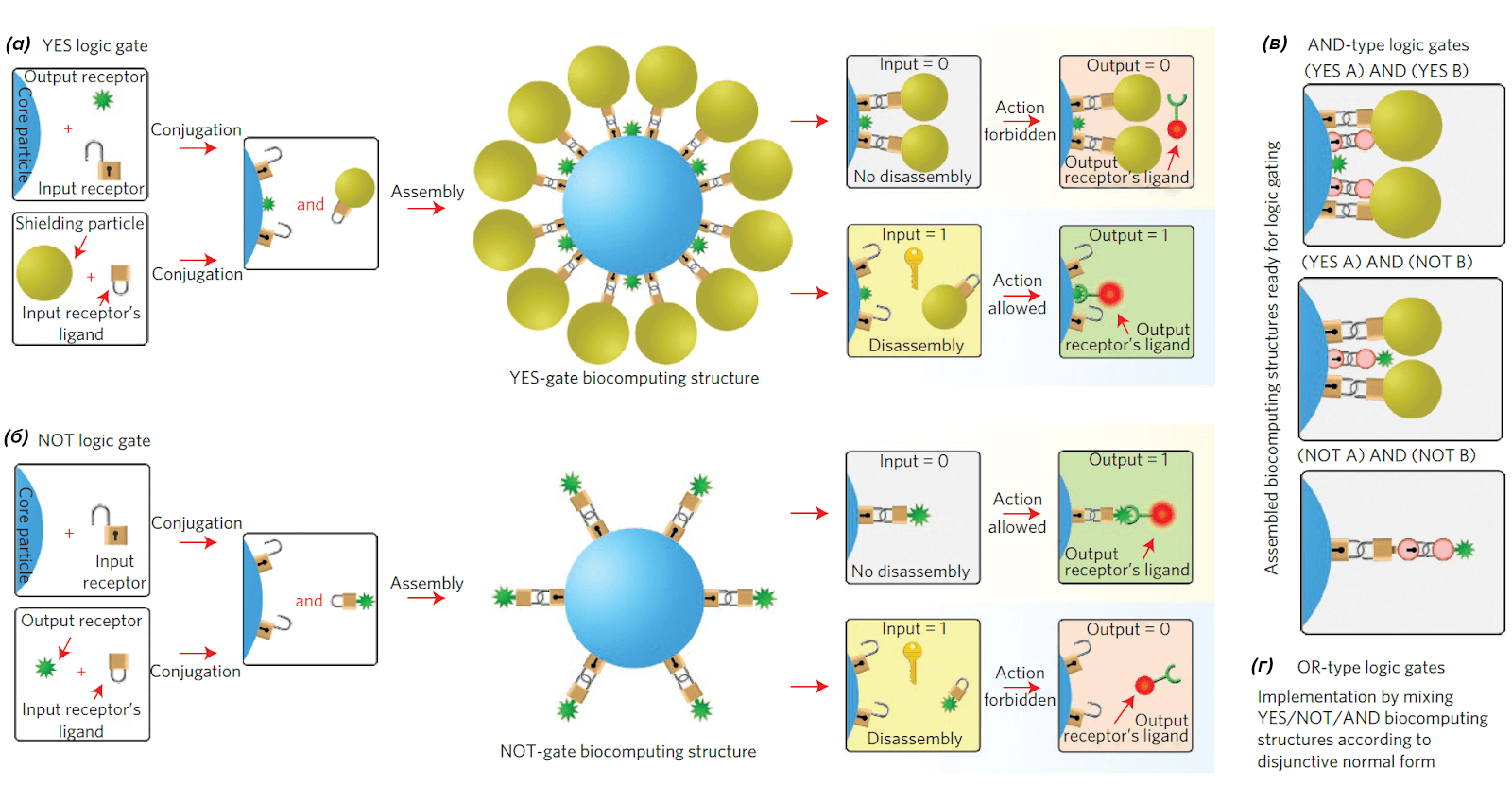
Рисунок 1. Наночастицы в роли элементарных единиц молекулярного компьютера. Показано концептуальное устройство частиц, реализующих основные логические вентили — ДА (а), НЕ (б), И (в) и ИЛИ (г).
— А это, получается, концептуально та же идея, которую мы в контрасте используем. Вводим контраст, опухоль набирает соответствующие частицы, и мы благодаря этому смотрим, как она выглядит. И отсюда берется следующий шаг: а давайте, мол, еще что-нибудь с опухолью делать будем, не просто смотреть. А вы, соответственно, отказываетесь от такого подхода и говорите: давайте сделаем инструмент, который сам разберется.
— Не совсем. Проблема тут — ну вот даже с контрастом. На данный момент нет идеального контраста. Есть технологии, которые позволяют контрастирование картинки за счет того, что либо мы вкололи в сосуд, питающий опухоль, либо вкололи какой-то контраст для очень конкретной, специфической опухоли. А для огромного числа других видов опухолей не получается это сделать, это плохо работает. Для этих вещей — и не только для этих — нам не столь важно диагностировать, сколько важно, диагностировав, туда же и доставить. Допустим, есть вот астробластома — такой ежик растет в головном мозге. И оттого, что мы ее там нашли… Как лечить-то? Ее нельзя удалить хирургически, а значит надо что-то как-то туда доставить. А как доставить ? Для этого нам хорошо бы иметь частицу, которая сама и диагностирует, и тут же, если надо, что-то убьет.
Для доставки в мозг особо актуален гематоэнцефалический барьер, который просто так доставить ничего в мозг не позволяет: «Сквозь тернии к нервам: особенности доставки лекарств в нервную систему» [10]. — Ред.
— Хорошо. Давайте тогда от этого перекинем мостик в биокомпьютинг. Для меня этот термин связан с идеей всех этих универсальных вычислителей. Давайте, мол, сделаем машину Тьюринга, но на базе нуклеиновых кислот. Вот там Адлеман, 1994 год — у него там, условно говоря, семь пробирок считали граф какой-то за семь дней. А потом, насколько понимаю, это все загнулось, просто потому что, если вам нужны вычислители, хорошо бы чтобы они все-таки быстро это делали. И это проще сделать на железе. Тем более что тогда как раз случился хайп вокруг квантовых вычислителей. А сейчас у нас нейронки, все эти GPU и так далее. А когда мы говорим о биокомпьютинге в вашем случае — вы же не универсальный вычислитель строите, я правильно понимаю?
— У меня нет сейчас задачи посчитать что-то эффективнее и лучше, чем электрический компьютер. Вообще в мире биомолекулярных систем, которые могут реализовать полную булеву алгебру, мало. Считанные единицы. Две из них — мои! (Смеется.)
А сама область, она не то чтобы заглохла. На самом деле она активно продолжает развиваться. Вот, опять же, та же самая статья 2014 года: я там, думаю, процитировал буквально все статьи, которые чего-то добились, каких-то крутых результатов. Их там было штук 40, это буквально все, что было. А в 2018 году мы сделали обзор в Chemical Reviews о разных системах биокомпьютинга, где у нас там, по-моему, уже 400 ссылок. И мы позиционировали этот обзор как последний, который может обозреть вообще всю область. И мы при этом не рассматривали системы, в которых считают внутри клетки. Смотрели только внеклеточный компьютинг. А на самом деле есть еще огромная область, где клетки заставляют считать. Но это все-таки другая область. Потому что, ну клетка сама по себе — суперкомпьютер. И от того, что мы нашли какие-то пути, которые выдают какое-то вычисление, это примерно как, не знаю, доисторический человек находит айфон случайно, и, открыв приложение калькулятора, говорит: о! я создал калькулятор! Но его создал кто-то другой, а он его нашел. В то время как, если вы заставили безжизненную пробирку считать, это действительно создали компьютер.
Вот мы обозревали системы внеклеточные, и даже какие-то работы, наверное, не вошли, но 400+ работ — это вот такой порядок. А сейчас уже нельзя одной работой всю область обозреть. Так что рост тут экспоненциальный в действительности. Но вообще такие системы, они очень тяжелые — сложно придумать новую систему. Это я к вашему тезису про то, что хайп был, но закончился. Нет. Он только зреет еще.
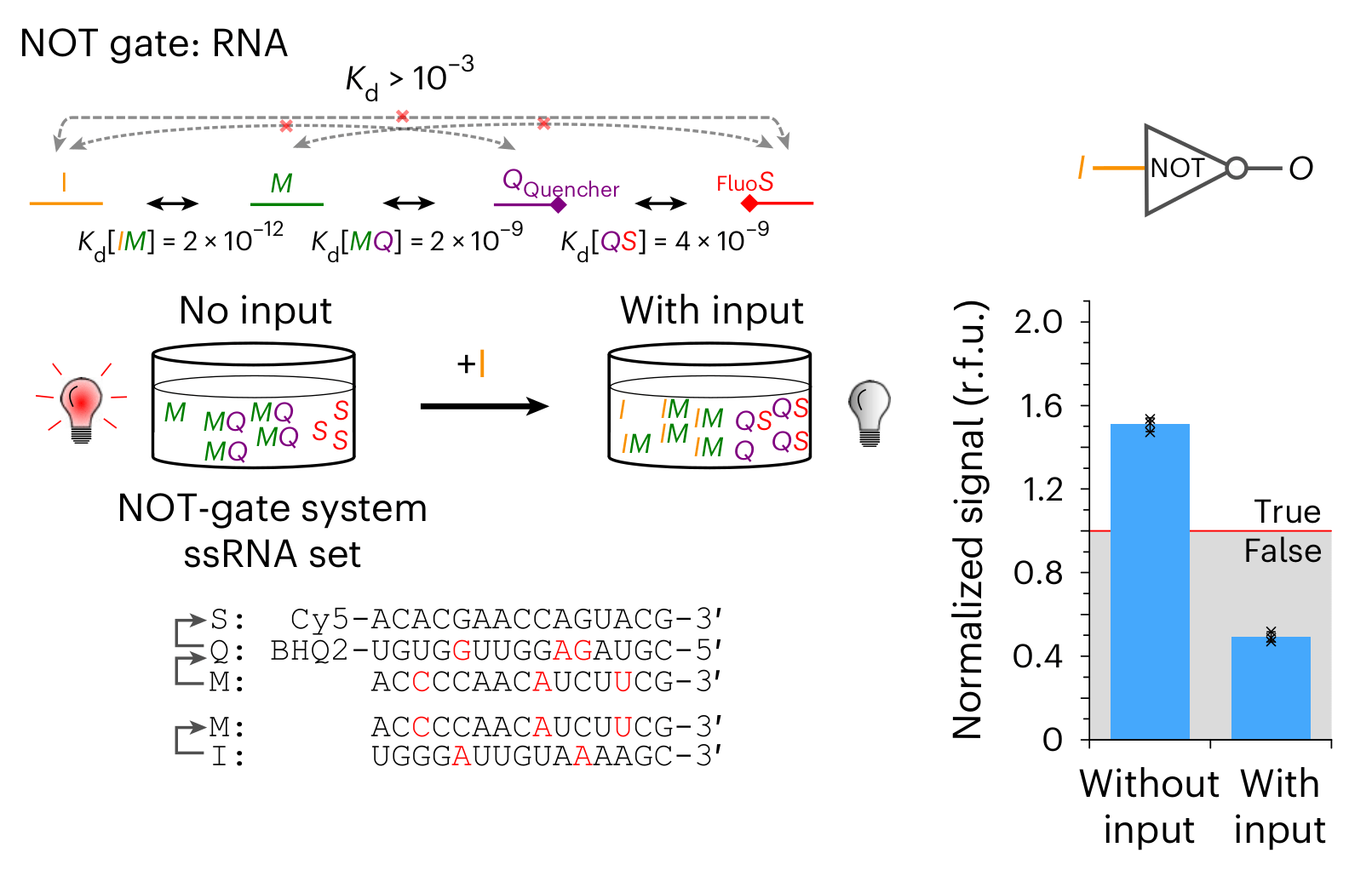
А то, что меня воодушевляет в нашей истории с коммутацией, это первый обнаруженный биомолекулярный неживой (неклеточный) механизм, который поистине природный. Все, что было сделано до того, — очень искусственные системы. Создавались очень необычные структуры из ДНК, каких-то ферментативных систем, но они неестественные, не встречаются в природе. Тот же Адлеман, который начинал всю эту историю, он там шифровал в последовательности ДНК, грубо говоря, остров и мост между островом. Ну таких систем нет в организме, и вообще в природе. А в коммутации я использовал базовое состояние молекул в любом растворе (рис. 2). Я не требовал от молекул ничего волшебного. Никакой определенной структуры, никакой определенной конструкции, чтобы они были как-то ограничены в объеме или еще что-то. Я показал, что такие системы могут существовать и функционировать в любом биомолекулярном бульоне.
Эта идея Максима Никитина была пересказана в одной из статей «Биомолекулы»: «Молекулярная коммутация — новый механизм регуляции генов и не только» [5], написанной школьником (!) и получившей первое место в номинации «Школьная» 2023 года (см. также рис. 2–4). — Ред.
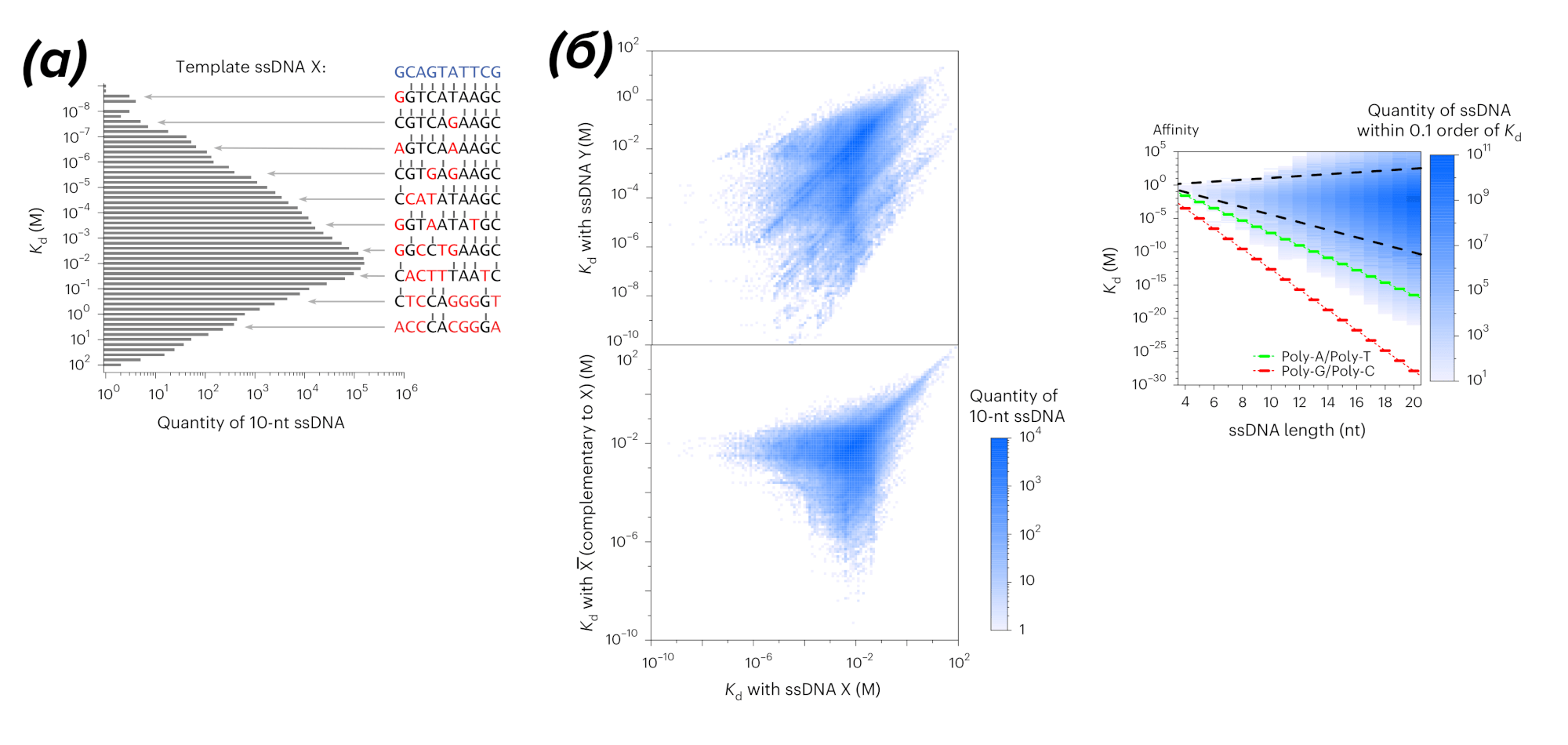
Рисунок 2. Одномерный (а) и двумерный (б) континуум аффинности — количество цепочек ДНК, имеющих определенное сродство (аффинность) к одной и более определенными цепями ДНК. Хотя «плотность» графика может особо не впечатлять, стоит заметить, что рассматриваются олигонуклеотиды длиной всего в 10 нуклеотидов. У более длинных молекул континуум аффинностей будет намного более обширным. На графике показано количество цепочек ДНК, имеющих определенное сродство к цепочке X, которая выбрана случайно. На графиках (б) оттенками синего обозначено количество возможных цепей ДНК с разным сродством к цепочке X и цепочке Y или X, где X — это случайная цепочка ДНК длиной 10 нуклеотидов, X — цепь, комплементарная X, а Y — другая случайная цепь ДНК той же длины. Снизу показан разброс аффинности для оцДНК (одноцепочечной ДНК) различной длины, оттенками синего показаны количества оцДНК с определенной аффинности к случайной оцДНК определенной длины. Зеленая линия — аффинность комплекса из 2 цепей — одна содержит только аденин, вторая — только тимин. Красная линия показывает то же, но для гуанина и цитозина.
статья в Nature Chemistry [4]; подпись составлена Дмитрием Козловым в публикации «Молекулярная коммутация — новый механизм регуляции генов и не только» [5]
— Правильно ли я понимаю, что, строго говоря, это все интересно уже не постольку, поскольку к доставке лекарств имеет отношение, а это такая фундаментальная вещь — вам интересно заниматься созданием таких систем, которые могли бы потенциально стать универсальным вычислителем. Или тут есть какая-то прямая связь?
— Смотрите, первая технология (вычислительная система на наночастицах) действительно касается только доставки лекарств. Там мы не мыслили категориями, что тут какой-то компьютер будет или еще что-то. Тут очень строго обозначенная область применения. А история с коммутацией сильно шире. Когда я изначально об этом думал, оно двигалось не совсем по такой траектории, что-де ты хочешь придумывать лекарства, и тебе приходят в голову идеи только про лекарства. Оно как-то снизошло откуда-то сверху, и тут уж что придумалось, то и придумалось. Я ее вижу так: это действительный механизм хранения информации, альтернативный всей системе двойной спирали Уотсона — Крика, центральной догме молекулярной биологии. Там у нас что: ДНК кодирует РНК, которая кодирует белок. И дальше уже народ думает внутри этого пространства. Вот какие-то белки или РНК регулируют экспрессию, еще что-то и так далее.
А тут история шире. Коммутация — это некий механизм хранения информации, но пока мы еще не очень понимаем, чего именно, какой именно информации. Это не обязательно даже только про управление экспрессией генов. Может быть, там какая-то другая история. Она может быть опосредована ДНК, а может какими-то другими молекулами. Вот что я постулирую. Все, что я говорю в той статье, распространяется не только на ДНК. В основе этого механизма заложен закон действующих масс, а он относится к любым молекулам — и малым молекулам, и белкам и так далее.
Те примеры вычислительных систем, которые я показывал в статье, были ограничены ДНК и РНК только потому, что на данный момент легко предсказывать аффинности для нуклеиновых кислот. А для малых молекул и для белков это сейчас нерешаемая задача. Ну лет через 10 это будет уже очень легко решаемой задачей, и тогда-то ту же самую коммутацию очень просто будет показать на других молекулах.
Соответственно, это такой фундаментальный принцип хранения информации. Есть шанс, что его можно использовать для доставки лекарств. Ну и мы понимаем, как это сейчас сделать. Также существует шанс, что он может иметь отношение к природе нейродегенеративных заболеваний. Когда нейрон пытаются заполнить информацией и нужно ее обработать, он может это делать через механизм коммутации. Точно так же — ну вот я начал с ДНК, ее проще делать — берет свое начало история про регулирование экспрессии белков. Соответственно, это та подчасть, которая влияет на центральную догму.
То есть то, как раньше искали регуляторные последовательности, сейчас это может сильно измениться. Я в своей статье показал, пока на модели разрушенной клетки, что ДНК, максимально некомплементарная гену, может, тем не менее, регулировать его работу, его экспрессию. Что противоречит вообще и полностью целиком всему тому, что было написано о том, как надо искать регуляторные последовательности. Но это только малая часть той истории, которую я показал.
И с этой точки зрения, естественно, мне этим суперинтересно заниматься, не только с точки зрения доставки лекарств, а потому что такое происходит очень редко. Я кайфую от того, что реально мы 70 лет не замечали этого. Причем, как я на лекциях сейчас рассказываю, все, что я показал в данной статье, мог бы показать любой второкурсник, которому читали курс химии. Сейчас я школьникам читаю лекции и у всех спрашиваю, знают ли они закон действующих масс? Все, кто его знают, а это иногда седьмой-девятый класс с химическим или биологическим уклоном, могли бы увидеть эту историю и точно так же рассказать. Но мы просто 70 лет не думали об этом.
— Ага-ага. Что я понял: вот у нас есть центральная догма, и это парадигма в каноническом смысле. Что такое парадигма и почему они вообще хороши? Отвечает Томас Кун: парадигма дает нам фрейм, внутри которого мы можем просто решать задачи [11]. Внутри этого фрейма мы понимаем, как вопрос можно поставить и как нельзя. Можем формулировать задачи. И мы понимаем, чего ожидать, когда мы будем их решать. А у вас тут, кажется, есть сильное заявление, что, мол, парадигму надо двигать! Пора ли? Пока что вы нашли, что называется, нарушение, которое с ней не бьется. Верно?
— Не совсем. Была некая аксиоматика в рамках этой парадигмы. Что она нам задавала: если одна цепь ДНК хочет передать информацию другой цепи ДНК, то две цепи должны быть в высокой степени комплементарны. Да, сейчас активно исследуются SNP (англ. single nucleotide polymorphism), однонуклеотидные полиморфизмы. Откуда они в этой парадигме берутся? Есть ультрафиолет, космические лучи, что-такое воздействовало на ген, превратилась одна буква в другую, и вот на месте идеальной пары возникла какая-то нестыковка.
— Пренебрежимая причем зачастую, не так ли?
— Да-да. Зачастую она ни на что особенно не влияет. Вырожденность кода, вот это все . При этом откуда появилась эта аксиоматика? Я ее попытался проследить, и начинаю с этого все свои презентации теперь. Когда Уотсон и Крик опубликовали свою статью о двойной спирали, они там сделали важное заявление, более или менее бездоказательное [12]. А именно то, что, если последовательность букв на одной цепи известна, то последовательность другой цепи уже предопределена. И вот отсюда как раз исходит постулат, что если одна цепь хочет пообщаться с другой, они должны быть комплементарны. Аксиома была ими произнесена. И почему она была принята за аксиому, на мой взгляд? Потому что эта фраза как раз была очень важна в их статье. Без нее они не могли сделать следующий вывод: что это дает возможность показать предполагаемый механизм копирования информации в клетках.
Это отсылка к термину Ниренберга и Бернфилда. Вырожденность генетического кода выражается в том, что одну и ту же аминокислоту кодируют сразу несколько кодонов. Например, фенилаланин кодируется и как UUU, и как UCU; лейцин кодируется аж шестью вариантами: UUA, UUG, CUU, CUC, CUA, CUG; и так далее. Соответственно, замена одного нуклеотида в кодоне зачастую никак не влияет на работу генов.

Рисунок 3. Максим Никитин во время использования микропипетки.
Центр научных коммуникаций МФТИ
— Вы репликацию ДНК имеете в виду?
— Да, репликацию. Как раз в этой статье в Nature они сказали: раз одно предопределяет второе, то механизм нам понятен. Они еще скорее всего ничего не знали про детали репликации. Но, я думаю, им очень хотелось это произнести. Потому что именно поэтому получалось, что их открытие двойной спирали — не работа в области структурной биологии, а сверхосновополагающая работа, закладывающая весь фундамент молекулярной биологии. Они открывали не двойную спираль ДНК, а то, как копируется вся биологическая информация. Еще не были известны ферменты, которые это обусловливают, но уже сразу стало понятно, что копируется именно так. Это было высказывание без определения каких-либо границ его применимости. Я, конечно, тут несколько зарываюсь, это безусловно было великое открытие, и я не хочу за них додумывать, но я для себя пытаюсь объяснить их логику, понять, откуда аксиома возникла.
И настолько всех, скорее всего, это все впечатлило, что у биологов очень глубоко засело: если есть какая-то ДНК, то полезная ей цепь должна быть комплементарной. Все, что сделано на данный момент до моей статьи, как мне кажется — точнее, все, что я видел, — оно как раз в этой парадигме и существовало. Ну давайте еще сильнее сузим мое утверждение: я могу с уверенностью сказать, безо всяких оговорок, что все искусственные системы процессинга информации, все эти ДНК-вычислители, они все базировались на том, что если одна цепь передает информацию другой, то она ей полностью комплементарна. В случае со strand displacement она частично комплементарна, но доменами — тут полностью комплементарна, а тут полностью некомплементарна.
А я как раз задался вопросом: что будет, если мы запретим ДНК встречаться с идеальной парой? Почему я здесь говорю именно о запрете: потому начиная где-то с 15–20 букв, если у вас есть одна цепочка ДНК, которая полностью комплементарна другой цепочке ДНК, то сила их взаимодействия настолько велика, что они всегда будут в связи. Они никогда не разъединятся сами по себе. Двойная спираль очень хорошо стабилизируется. Сходу сейчас не помню точные цифры, но если у вас цепочка из 50+ букв, то время жизни этого комплекса (в идеальных условиях) составляет величину уже сопоставимую с временем существования планеты. Они никогда не развалятся. Соответственно, если в растворе рядом есть полностью комплементарные цепочки, то они всегда свяжутся.
А я как раз начал думать: давайте выкинем идеальную комплементарную цепь и посмотрим, а что будет в таком бульоне, когда у нас там много олигонуклеотидов, одноцепочечных ДНК. И понял, что там тоже вполне можно хранить информацию — совсем не так, как по Уотсону и Крику в первичной последовательности. При этом я показал, что мы много информации можем там сохранить. А раз информацию хранить можно, в чем тут получается фишка — каждая пробирка, в которой есть одноцепочечная ДНК или РНК, она хранит какую-то информацию, она там есть. Вопрос в том, что именно там хранится, что-то бесполезное или что-то полезное? Вот этого мы пока не знаем. Но то, что информация там сохранена, это безусловно.
Я рад одному тому, что меня осенила такая идея, которую нельзя ограничивать каким-то одним применением — что то ли это компьютер, то ли это какая-то фундаментальная история, то ли еще что-то. Оно — все сразу. Нам интересно и какие-то прикладные вещи из нее как можно быстрее извлечь. В частности, для того чтобы генотерапевтические препараты были более безопасными. И какие-то следующие шаги.
Во мне вообще сидит мысль такого рода. С раком, например, борются уже очень длительное время. И, конечно же, есть шанс, что мы на правильном пути — биология в целом развивается экспоненциально, очень активно, — и есть шанс, что рак мы не победили просто потому, что слишком мало времени прошло. Но в целом мы уже так много пытаемся найти… И биоинформатика, и скрининги по всем генам, и еще что-то: вот как отличить опухолевую ткань от неопухолевой [13]? И как бы не сложилась пока цельная, четкая картинка. И у меня есть ощущение, что это может быть из-за того, что мы не там ищем. Просто наборы генов, просто экспрессия генов или вообще на уровне нуклеотидов — не факт, что они подскажут ответ. И я вполне допускаю, что в этом феномене коммутации какие-то ответы как раз и зашифрованы. И ответы, которые там зашифрованы, в стандартной парадигме принципиально нельзя обнаружить.
Я показываю на своих лекциях буквально следующее: вы можете сколько угодно рассказывать, какие у вас гены, как вы просчитали регуляторику и так далее, но если вы не знаете, какие олигонуклеотиды есть в этой клетке, то, если я прав, вы не сможете автоматически сказать, будут ли побочные эффекты у вашего препарата. Вы просто не можете этого предсказать. А информации о том, какие малые ДНК и РНК содержатся в каждой клетке, у нас сейчас нет в принципе. А следовательно, если мы туда не посмотрим, то — опять же, если я прав — вы точно каких-то эффектов не найдете.
Соответственно, теперь, когда мы знаем о том, что есть такой механизм и могут быть эффекты, связанные с коммутацией, можно их искать. Вся красота этой истории, наверное, скрывается в том числе в этом: обнаружить реализацию коммутации в живых клетках очень сложно, но если ты даже знаешь о том, что коммутация существует, то ее спонтанно обнаружить в клетке практически невозможно.
— Получается, что до того, как вы обратили внимание на то, что, возможно, есть еще и такой механизм, как коммутация, мы ряд наблюдаемых эффектов списывали просто на случайность?
— Да. Мы видим какую-то побочку, она достоверная, но мы не знаем, почему она произошла. Я не говорю, однако, что мы все побочные эффекты мгновенно поймем. Есть шанс, что мы объясним только какую-то часть, но — тем не менее.
— Хорошо. Расскажите, пожалуйста, анекдот, в какой момент из космоса эта мысль упала в вашу голову?
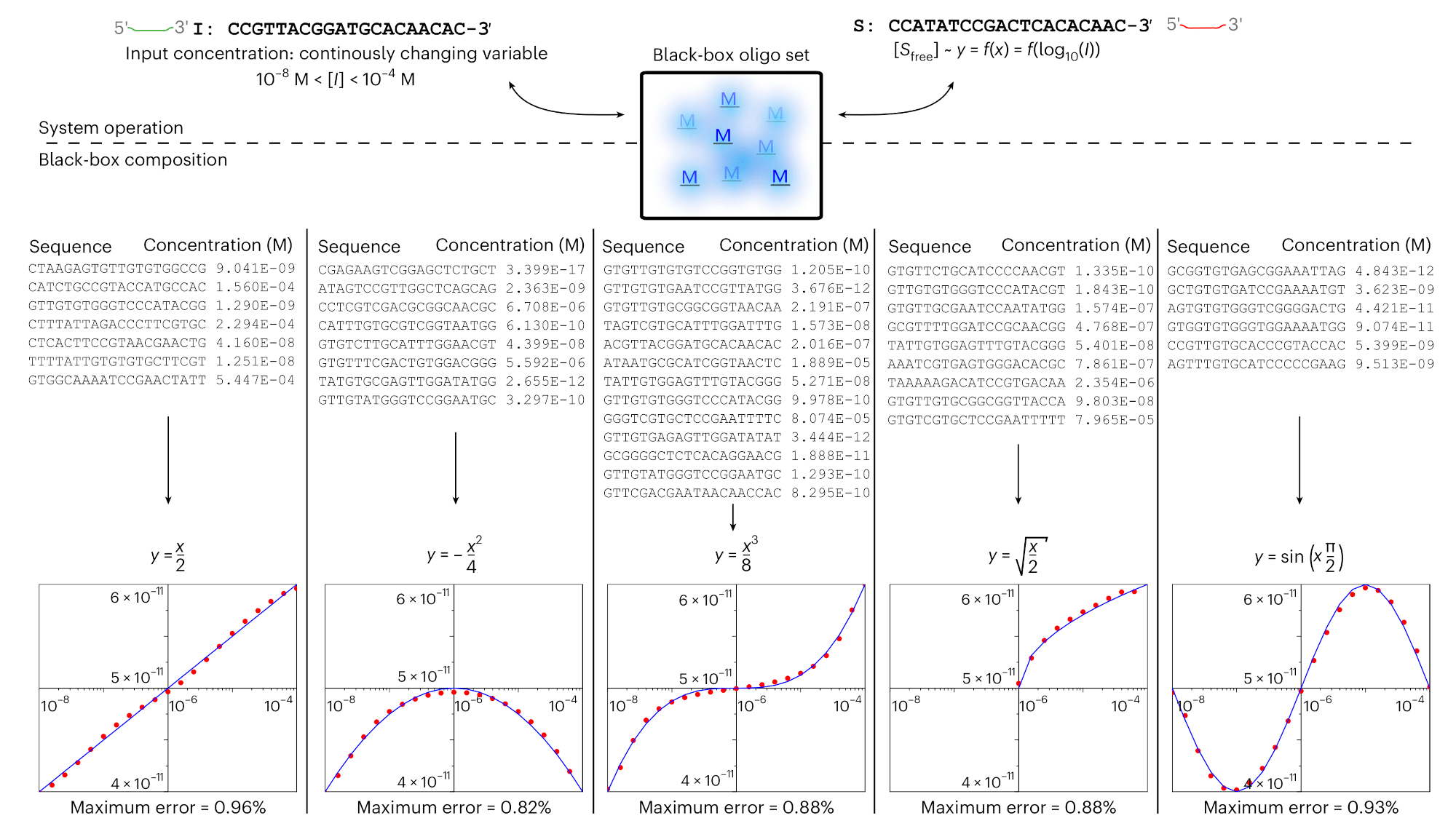
— Я изначально придумал такой концепт: что можно, подбирая разные олигонуклеотиды с разными аффинностями, решить задачку: Y = sin(X). И это была первая задача, которую я пытался сделать, но это у меня никак не получалось. Я ее забрасывал, пытался как-то иначе решать... Это был мучительный процесс. При всем при этом я никак не мог придумать, как ее упростить.
И для меня это сейчас удивительно, потому что я параллельно сделал историю с булевой алгеброй на наночастицах. Я ту работу уже опубликовал, а как сделать коммутацию в булевой алгебре, мне не приходило в голову долго. Я думал, думал, думал, и в какой-то момент оно — бац! — и пришло, и после того процесс пошел как по маслу. Я придумал формат, как должны взаимодействовать олигонуклеотиды, чтобы заработала булева алгебра. Это в итоге оказалось просто. Точнее, когда я сейчас смотрю на это, я не понимаю, почему так долго не мог этого придумать. Но в тот момент оно реально было сложно. Я не видел этого решения никак — и это при том, что у меня был опыт в биомолекулярном компьютинге. Не знаю, почему так. Сейчас я сложил три олигонуклеотида — ну тоже, опять же, когда читаю лекции студентам, я показываю, и даже уже нарисованы картинки: вот у вас три олига, как сделать YES гейт? И народ не может придумать. Так что, видимо, это действительно не так уж и легко. (Смеется.)
Ну а когда оно придумалось, дальше пошло легко, и я даже решил ту, изначальную задачку, про Y = sin(X). Ну у меня после длительной работы по булевой алгебре, у меня уже и все скрипты были написаны, и так далее. Так что это было легко. Ну не легко, от начальной идеи про Y = sin(X) до публикации статьи про коммутацию цепей прошло девять лет, но у меня все получилось (рис. 3–5).
— И с тех пор мир не будет прежним — как минимум, для вас?
— Для меня он уже не был прежним где-то сильно посередине этой работы. В чем крутость нашего мозга, как мне кажется, и вообще, почему круто быть ученым? Когда ты придумываешь решение, у тебя настолько быстро мозг работает… У меня вот дважды такие математические истории были, где я математику продумывал, именно правильность того, как должна математика сработать. И здесь как: ты что-то придумал, но сразу же начинаешь сомневаться, а все ли функции ты сделал, весь компьютер будет работать или нет? Ты в голове это начинаешь прокручивать, и там как раз я поражался тому, насколько быстро мой мозг работает. Ты и слова не успеваешь произносить. Потому что обычно, когда ты думаешь, ты все-таки это вербализуешь, типа: а что, если я сделаю то-то и то-то?.. А здесь же оно внутри мозга то ли картинками летит, то ли еще как-то происходит, но ты придумываешь всю историю, не продумывая толком ни одного слова, и это такой красивый процесс, просто супер! Короче говоря, всем желаю такое пережить.
— Получается, для решения таких задач надо быть одновременно математиком и биологом. Что для вас первично? Вы решаете задачи как математик и думаете как математик, или думаете скорее как биолог?
— Я точно думаю с логикой математика в первую очередь. Я не очень понимаю, правда, что именно вы подразумеваете под логикой биолога — надо договориться о терминологии. Биология ведь часто описательная наука, в которой очень сложные эксперименты. Типа, ты там долго мучаешься, а потом делаешь какой-то вывод. Часто этот вывод ты не можешь подкрепить математической логикой. Ты набрел на что-то и сделал следующую гипотезу, которая, возможно, поможет вылечить рак. Но любой крутой биолог понимает, что ему придется вводить дополнительные аксиомы, а то это ни на чем не основано.
Так что если я могу какие-то соображения провести со строгой математикой, конечно, я в первую очередь это сделаю. Но если я по каким-то причинам этого сделать не могу, мне тоже приходится аксиоматику допускать, тогда уже я мыслю как биолог. Это не вина биологической науки. Это просто сложность биологического объекта, что мы не можем математически его описывать.
— А дело тут, наверное, в том, что в математике есть мощный формальный аппарат уже. Поэтому ты можешь двумя формулами обойтись, и коллеги поймут.
— Да.
— Есть такой пример. Был такой логик Сол Крипке. Он написал книжку «Именование и необходимость». Он в самом начале говорит: ребята, вообще говоря, все то, что я дальше скажу, это будет разбор на уровне метафизики. И это так, потому что мне надо вам, философам, это все объяснить, так что тут будет целая книжка. Так-то на уровне модальной логики оно все быстрее было бы, я бы две формулы написал на доске и ушел, и все — вся проблема решена. И тут то же самое. Вы в математическом фреймворке быстрее решаете задачу, но есть проблема с ее трансляцией дальше.
— Не совсем. Мне часто говорят: а давай мы сделаем какие-нибудь симуляции на компьютере, еще что-то. Я соглашаюсь: давайте сделаем, с удовольствием — но, как правило, никакого отношения к реальности это, к сожалению, иметь не будет. Надо делать эксперименты. Просто потому, что система настолько сложна. То есть настолько много факторов есть, которые мы не учтем в формулах, что как бы это довольно мало, очень ограниченно будет. Граница применимости будет суперузкой. Поэтому надо делать эксперимент, но, конечно, и продолжать развивать предсказательную область.
Но, опять же, мне кажется, что мы просто не очень правильно мыслим, вообще воспринимаем биологию. Я такую аналогию часто использую: если вспомнить про наше восприятие земной и небесной сферы, были же очень крутые математики, которые в геоцентрической системе очень здорово описывали положение дел на небосклоне. Но как только мы поставили Солнце в центр, все эти сложные циклоиды превратились в простые эллипсы, и все. Сложная система колоссально упростилась.
У меня ощущение такое, что мы биологическую систему сейчас описываем суперсложно, и не можем пока по-другому. У нас не получается, нет какой-то красоты этой системы. У нас получается некая загадочная сущность, и как-то оно слишком все сложно работает. А мне кажется, что есть некий формат, в котором мы сможем сказать: вот четыре уравнения Максвелла, и все будет работать. Мне кажется, что коммутация — это точно недостающий ключ, возможно один из нескольких, которые потребуются.
Мне, как только я пришел в биологическую область, очень не нравилось понятие молекулярных путей, molecular pathways, что-де одна молекула взаимодействует с той и так далее. Мне это прямо сильно не нравилось с какой точки зрения: я вижу, что это создано просто оттого, что нам всегда не хватает чувствительности приборов. Нам неизвестна никакая пороговая константа аффинности, которая скажет: вот это значимо, а вот это незначимо. Я не понимал, как эта грань вообще может возникнуть. То есть это не природная грань. Это грань, которая, скорее всего, была вынужденно выбрана экспериментаторами. Но как? Сначала был такой-то pathway в 1970-х годах, а теперь-то оказалось, что он на самом деле масштабнее и многограннее. А из-за чего? Да просто приборы стали более чувствительными, и мы увидели, что там на самом деле больше взаимодействий.
С этой точки зрения то, к чему я призываю в случае с моей коммутацией, — у меня тут нет понятий сильного и слабого взаимодействий, я просто говорю, что все едино, я рассматриваю все. И я вижу, что в этом есть много сущностного. Соответственно, когда я думаю о том, как происходила эволюция от первичных молекул — даже не то что первичного бульона, а именно молекул, — я понимаю, что олигонуклеотиды могли возникнуть. Но потом-то — ну двойная спираль сходу? Вероятность того, что два зеркальных олигонуклеотида возникнут сразу и заплетутся, она же очень низкая.
Скорее всего, возникло много разных олигонуклеотидов, они сложились в какую-то сложную систему и там как-то начали хранить информацию. Но уже дальше оттуда началось — может быть, там была какая-то проторибосома [14], какая-то низкоаффинная система, которая начала что-то ферментативно делать. Ведь одноцепочечные олигонуклеотиды — очень хорошие ферменты. Был сначала какой-то ферментативный конструкт, и потом это все до такой степени доэволюционировало, что начало достраивать двойную спираль, и она уже начала хранить информацию долгосрочно.
— Я думаю, я понял фишку. Сейчас я попробую сформулировать, а вы скажете, правильно это или нет. Вот у нас есть центральная догма молекулярной биологии, ее придумал Крик на семинаре Гамова. С ней все классно. Сейчас вы говорите: ребята, все хорошо, но есть уровень ниже, который нам еще предстоит хорошо расписать. И есть подозрения — а в вашем случае, думаю, уже и убежденность, — что вместе с этим мы получим правила, которые позволят редуцировать, собственно говоря, центральную догму к более базовому уровню. Так же, как мы сейчас можем классическую механику, на самом деле, переложить на квантмех. Это будет сложнее выглядеть, но мы понимаем сейчас, что классическая механика это частный случай квантовой механики. Там есть еще много задач, которые нужно решить, но в целом мы нашли более фундаментальное поле для описания того, как мир устроен.
— Мне страшновато вслух так формулировать — весьма нескромно.
— Поэтому я так сформулировал. Нужно же начинать?
— В целом — да. Именно поэтому я на семинарах когда рассказываю, оговариваю следующее, самое важное — что я не могу поверить в «изначальную рибосому». Как будто стукнуло молнией и появилась рибосома. Был предыдущий уровень. И точно так же я не могу представить себе, что этот уровень исчез, когда появилась рибосома. То есть как я вижу эту систему вообще, глобально, в клетке и так далее? Я в статье этого очень аккуратно коснулся, потому что откровенно стремно было. В Nature, как мы знаем, запрещают философствовать. Можно, конечно, этим заниматься, но в других журналах. Я даже подумывал написать в Philosophical Magazine, чтобы было красиво: много крутой физики начала XX века в Philosophical Magazine публиковалось.
Соответственно, я думал именно в формате того, что надо пытаться проанализировать, и мы сейчас пытаемся провести такую работу. Мы должны понять, как у нас копилась информация вначале, до рибосом. Моя гипотеза заключается в следующем: когда рибосома появилась, уже было то, что я назвал «информационным гомеостазом». Грубо говоря, если есть рибосома и есть, например, рицин, который отщепляет всего одну букву от рибосомы, и она инактивируется полностью. В таких условиях сложно представить себе, что такая штуковина могла появиться и эффективно работать. Плюнь — и она сдохнет! Соответственно, скорее всего, была некая система вокруг нее из малых молекул, которые делали так, чтобы эта система была устойчива. И над ней потихоньку возникла надстройка, которую описывает центральная догма. Но я не могу представить себе, чтобы эта надстройка резко лишила себя всей этой поддержки со стороны других молекул. Это все равно как если бы появились многоклеточные, и всех одноклеточных не стало.
Точно так же я имею глубокую убежденность, что не могла высокоаффинная химия взять и избавиться от всего того полезного, что было накоплено к тому моменту в низкоаффинной химии.
— Окей, все это я понял. Давайте вернемся к чуть более прозаическим штукам: вновь обращаясь к списку работ, который мне показывает Google Scholar, я вижу, что, вообще говоря, вы работаете в тесной группе соавторов. Нередко — с отцом. А как это устроено? Вы прям на кухне разгонять начинаете?
— Действительно, у меня отец — заведующий лабораторией в Институте общей физики РАН. И я там как-то был в этой лаборатории, прямо с малых лет. Не знаю, то ли он меня приводил на экскурсию, то ли родителям просто не с кем было меня оставить дома, и тогда они меня брали на работу.
Потом в какой-то момент, когда я был в восьмом классе, случилась забавная вещь — я стал осваивать 3D-графику. И в какой-то момент я выпрашивал у отца компьютер посильнее, потому что имеющаяся машина не могла уже тянуть моих запросов. Он ответил: ладно, только ты тогда мне сделай презентацию. Тогда еще большая часть презентаций на конференциях, даже на международных, шла на «прозрачках». Ну то есть потихоньку там уже пробирался PowerPoint, конечно. А я отцу нарисовал 3D-анимацию… правда, ничего не понимал, что я рисую. Он говорит: рисуй то-то. Я ему это все нарисовал, и он рассказал потом, что это был фурор: он вышел на конференции и стал показывать не просто текстовые слайды, а видео! И это было «вау». Все потом обсуждали, как это он сделал? Таким было мое боевое крещение. Ну и мне уже тогда стало интересно, а что же такое я рисую.
Потом в выпускных классах, 10-м или 11-м, я учился во «Второй школе», а Институт общей физики был рядом, через дорогу — нас независимо от отца повели на экскурсию.
— К отцу?
— Нет, отцовской лаборатории в программе не было, мы как раз ходили по другим. Меня очень впечатлила лаборатория газовых лазеров. Там они поставили эксперимент, который, как я понимаю, они показывали Хрущеву, когда начинали «Звездные войны» финансировать. В общем, супермощный лазер супергромко бабахнул, там что-то вроде 200 килоампер, 200 киловольт, в общем, какие-то невообразимые цифры, меня это очень впечатлило. Я тогда возьми и спроси: можно мы будем к вам ходить работать? В то время это было как-то не принято. Сейчас-то вся проектная деятельность, «Сириус» и так далее — школьники в науке делают больше, чем многие студенты. А тогда не было такой традиции, чтобы школьников пускали в лаборатории. В общем, заведующий лабораторией страшно удивился, но они нам как-то это организовали. Мы к ним приходили, делали очень примитивную работу, но для меня это был какой-то совершенно наикрутейший мир. В общем, я тогда и решил, что не пойду программировать профессионально после школы, а стану заниматься наукой.
И уже где-то с третьего курса я начал — сначала с отцом поработал, потом сделал с ним один проект, вышла у меня статья после третьего курса. Я ему помогал, где-то в чем-то он просил меня помочь, где-то мне просто было интересно посмотреть, как там и что. А на четвертом курсе я пошел в Институт биоорганической химии и там начал работать уже по биологии. И карьера моя дальше в этой области завязалась. А отец делал крутые биосенсоры — магнитные и оптические. Я был его «руками биолога», если можно так выразиться. Помимо своего научного проекта, который я делал в ИБХ, я еще забрал отцовские приборы и на них делал какую-то интересную науку с биологической точки зрения. Поэтому у меня много работ в соавторстве с ним. То есть там задействованы отцовские приборы, а я сначала с наночастицами, потом с животными, потом еще с чем-то их применял.

Рисунок 7. Герой интервью и система для наблюдения за ростом клеток cellVivo.
Центр научных коммуникаций МФТИ
— Это, конечно, мощное преимущество, когда можно с отцом посидеть и все то, что у вас в голове не укладывается, обсудить. Это так работает? Или вы, скорее, более прикладную пользу друг другу приносите?
— В начале моей карьеры это было, мы много общались с ним. В этом плане он мне много чем помог, многому научил и наставил. Но на самом деле, мне кажется, где-то в районе пятого курса — об этом мне мама си-и-ильно позже рассказала, — отец пришел к ней и сказал: «Я поговорил с Максимом, конечно, не ученый он. Ничего особо придумать интересного не может, вряд ли что-то получится и что-то сработает. Скорее всего, он все-таки программист». В общем, был и такой момент в моей научной карьере. (Смеется.)
— А помимо отца? Есть же все равно люди, на которых смотришь и равняешься.
— Скажем так: мы очень много общались по науке с моим научным руководителем Сергеем Михайловичем Деевым. У нас действительно были разговоры до двух-трех часов ночи. Я кайфовал. Это было очень интересно. Мы и обсуждали какие-то новые идеи, не только эксперименты. Он учил меня взрослой, научной жизни, и за это я ему чрезвычайно благодарен. Но у меня как-то складывалось иначе, чем у них… С тем же отцом, когда я общаюсь — он ведь тоже Физтех оканчивал, как и мама, — он говорил, что весь курс у него мечтал о Нобелевской премии, что это было главное. А у меня такого устремления никогда не было.
Я для себя сформулировал так: если я за свою жизнь сделаю лекарство и выведу его в клинику, значит, все было не зря. И в этом плане наша работа в Nature Biomedical Engineering — я считаю, что это точно крутая терапия, точно крутой метод и его точно надо выводить в клинику. Если не мы, то кто-нибудь другой его точно доведет. Нам не на все времени и рук хватает, конечно.
— Довольно часто, когда ты говоришь с учеными, чьи работы имеют прикладное значение, они говорят: все это очень хорошо, я очень рад, но мне-то, конечно, тут просто повезло с этим, я к этому не стремился. Так-то мне «просто интересно». Я получаю огромное удовольствие от того, что я что-то понимаю, а там уж как оно применяется, ну я очень рад.
— Я не такой, да. И с таким подходом тоже довольно часто сталкивался. Я удивляюсь каждый раз. Скажем так: я понимаю, что образно во времена какого-нибудь Бенджамина Франклина единовременно на планете было всего десять активных физиков, и они занимались наукой в свободное от чего-либо время. Но сейчас уже мир не такой. Сейчас ученых очень много. Научный мир очень конкурентен. И фундаментальную науку ученые должны делать в свободное от прикладной науки время.
Мы, конечно, можем изучать фундаментально рак, разные процессы в этом. Это круто, но у тебя же все есть, чтобы делать лекарства! В таком раскладе, на мой взгляд, ограничивать себя, что ты прямо весь такой фундаментальный исследователь, уже непозволительная роскошь. При этом, опять же, если меня спросят, допустим, а как я предложил бы это зарегулировать, я буду существенно менее жесток в своих высказываниях. Это нежная и деликатная область, в которой не должно быть перегибов. Но — да, у меня именно такая цель: надо делать лекарства, разрабатывать принципиально новые методы лечения.
Я начал карьеру, именно исходя из этой логики — что мне надо делать что-нибудь полезное, чтобы мне кто-то сказал «спасибо» реально именно за то, что мы что-то сделали. Не за шесть страниц текста, над которыми я семь лет корпел, а чтобы что-то пощупать можно было. В самом начале карьеры, конечно, я хотел опубликоваться в журналах семейства Nature. Но у меня была такая логика, и чем я активно горжусь: что все наши публикации в семействе Nature полностью российские. Мы сделали все от начала до конца. Это не те такого рода статьи, где российский вклад очень ограничен, и там присутствуют еще триста соавторов из других стран, и вся интеллектуальная собственность тоже у них. Нет, во всех трех моих работах в Nature Nanotechnology, Nature Biomedical Engineering, Nature Chemistry вся интеллектуальная собственность наша. Все придумано и реализовано у нас. Этим я горжусь. Вначале я хотел сделать это, чтобы привлечь к своему мнению какое-то внимание. Мне тогда было важно показать, что нужно, наконец, сделать для российской науки быструю доставку реагентов. Для меня это был социально значимый проект.
В итоге-то меня увидели, услышали и так далее. И я преуспел — мы научились в рамках грантов РФФИ полностью официально закупать реагенты за рубежом и привозить их из Англии, США за неделю (!) от идеи, что нам надо что-то закупить до доставки к нам в лабораторию. К сожалению, РФФИ закрыли. Такова была логика в первом случае.
После первой публикации в Nature вторая логика была такова: надо сделать вторую, иначе все будут говорить, что первая была случайностью. Закрепить. Когда уже закрепил, в третьей, было уже просто интересно. Там я понимал, что интересность истории настолько высока, что мне не интересна конкретно Nature. Для меня это был способ просто…
— Читателя получить. Когда там вышло, просто больше народу прочитает.
— Да, я рассчитывал на то, что когда я доделаю работу с тем уровнем проработанности, который я закладывал… Я мог бы опубликовать ее вообще на середине. Там было достаточно материала. Я сделал сильно больше, чем требовалось для публикации. Я мог разделить еще на несколько статей, но не захотел этого. Мне была нужна одна цельная история. И сто процентов людей в этой области, с кем я общался, мне говорили: «Слушай, это должно было быть в главной Nature, что за фигня?»
— Да, и у меня уже появился такой вопрос за время нашей беседы.
— Потому что то, что я показал, — до меня было много статей в Science, Nature и так далее, где люди сделали более узкие вещи. Там были сильно более простые вещи, более искусственные системы, про которые было понятно, что они дальше не пойдут. Но вышло вот так. Я отослал, естественно, во флагман Nature, где мне сказали: мы без проблем опубликуем, но ты докажи in vivo, что это реализуется. Я строго понимаю, что как только мы докажем это in vivo…
— Это будет флагман.
— Да там и Нобелевская премия будет некой формальностью. Это будет реальным переосмыслением всей биологии. Совсем всей.
— А вы докажете?
— Конечно, докажем! (Пауза. Смеется.) Другое дело — есть шанс, что нас кто-то обгонит.
— Мы начали вообще с вопроса, кто для вас образец для подражания, герой.
— С этой точки зрения я не выделяю какие-то конкретные истории. Безусловно, есть люди, которыми я восхищаюсь, как из великих, типа Эйнштейна, но тут я скорее восхищаюсь Королёвым.
— Потому что он дела делал?
— Это был величайший ученый. Да, наверное, для теории относительности нужен великий мозг. Но тут нужна какая-то великая организаторская составляющая. Короче говоря, у Королева был невероятно сложный проект.

Рисунок 8. Максим Никитин за работой.
Центр научных коммуникаций МФТИ
— И Курчатов тогда должен быть в этом списке, я так подозреваю?
— М-м-м. Скажем так: сегодня Курчатова в России очень активно почитают. А Королёв, на мой очень субъективный взгляд, получает меньше внимания, чем Курчатов. Не знаю, мне так кажется. Но самое главное, я почти уверен, что никто из нынешних американцев не знает, кто такой Королёв. Гагарина народ знает, а про Королёва я далеко не так уверен; мне кажется, что его не знают 99,9% населения Америки. Как вы думаете?
— Ну как же. Сериал идет на Apple TV в жанре альтернативной истории, в котором все крутится вокруг того, что Королев не умер, и американцы проиграли лунную гонку. Им приходится Марс штурмовать и т. д. Все на этом строится. For all Mankind называется.
— Вопрос, как много людей смотрело этот сериал. Знаете, когда я придумал свою первую идею про биокомпьютинг, я активно размышлял. У меня было два варианта. Первый вариант был — написать нескольким заведующим лабораториями за рубежом, приехать и сделать это у них за два месяца. Это был бы простой вариант. И можно было быстро опубликоваться, может быть, даже и во флагманском Nature. Или пытаться сделать это в России, где вероятность успеха была сильно ниже. И я выбрал второй путь в том числе из-за Королёва.
— Ad astra, это, конечно, хорошо, но ценность состоит в per aspera?
— Не, дело не в per aspera. Мне хотелось бы, чтобы это была российская история. Я уж не знаю, были ли шансы у Королёва уехать, не думаю, но мы здесь не в ту сторону сворачиваем. У меня они были. А вышло — так. Из современников, безусловно, есть ученые, которых я сильно уважаю, но я бы не сказал, что у меня есть некий пример, чтобы я прямо хотел так же, копировал стиль или что-нибудь подобное. У меня таких кумиров нет.
Есть ровно один человек, у которого я в своей жизни взял автограф — это Михаил Михайлович Жванецкий. Это смешная история. Я был в «Гнезде глухаря», там есть маленький зал, где большие артисты делают камерные концерты. Я туда пришел, и как раз дело было пока я работал над статьей в Nature Nanotechnology. Там проходит концерт, все в восторге и все такое. И выстраивается очередь, чтобы получить автограф. Думаю, такое дело, а чего бы мне и не присоединиться? Там еще друзья мои были, которые сказали, что они точно за этим идут. Говорю, ну давайте я с вами постою. Стоим, стоим, и тут я понимаю, что изо всей бумаги у меня только мой лабораторный журнал. И что вообще не понимаю, как в принципе просят автограф, что говорить-то надо? Я мямлю что-то такое: «Михаил Михайлович, я Максим Никитин, молодой ученый…» — не знаю, что делать, и подсовываю ему свой журнал. Он пишет: «Ученому Максиму от неученого Жванецкого». Так что у меня журнал подписан таким великим человеком — очень бережно его храню!
Опубликовано при поддержке гранта Минобрнауки России в рамках федерального проекта «Популяризация науки и технологий» № 075-15-2024-571.
Литература
- Maxim P. Nikitin, Tatiana A. Zdobnova, Sergey V. Lukash, Oleg A. Stremovskiy, Sergey M. Deyev. (2010). Protein-assisted self-assembly of multifunctional nanoparticles. Proc. Natl. Acad. Sci. U.S.A. 107, 5827-5832;
- Maxim P. Nikitin, Victoria O. Shipunova, Sergey M. Deyev, Petr I. Nikitin. (2014). Biocomputing based on particle disassembly. Nature Nanotech. 9, 716-722;
- Maxim P. Nikitin, Ivan V. Zelepukin, Victoria O. Shipunova, Ilya L. Sokolov, Sergey M. Deyev, Petr I. Nikitin. (2020). Enhancement of the blood-circulation time and performance of nanomedicines via the forced clearance of erythrocytes. Nat Biomed Eng. 4, 717-731;
- Maxim P. Nikitin. (2023). Non-complementary strand commutation as a fundamental alternative for information processing by DNA and gene regulation. Nat. Chem. 15, 70-82;
- Молекулярная коммутация — новый механизм регуляции генов и не только;
- мРНК-вакцина на страже коллективного иммунитета: за что вручили Нобелевскую премию в 2023 году;
- Невидимая граница: где сталкиваются «нано» и «био»;
- Квантовые точки — наноразмерные сенсоры для медицины и биологии;
- Наночастицы для окраски биомолекул и QLED-дисплеев — за что вручили Нобелевскую премию по химии (2023);
- Сквозь тернии к нервам: особенности доставки лекарств в нервную систему;
- Kuhn T.S. The structure of scientific revolutions. Chicago: University of Chicago Press, 1962. — 264 p.;
- J. D. Watson, F. H. C. Crick. (1953). Molecular Structure of Nucleic Acids: A Structure for Deoxyribose Nucleic Acid. Nature. 171, 737-738;
- Антон Буздин: «Юлий Цезарь определял центр мира как то место, куда воткнуты орлы его легиона. Я стараюсь следовать его примеру»;
- РНК у истоков жизни?.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚