
SciNat за февраль 2026 #4: новый тип модуляторов GPCR и «биологические часы» для болезни Альцгеймера
22 февраля 2026
SciNat за февраль 2026 #4: новый тип модуляторов GPCR и «биологические часы» для болезни Альцгеймера
- 150
- 0
- 1
На обложке свежего выпуска Science — новый вид спинозавра Spinosaurus mirabilis, обнаруженный в пустыне Сахара. Его анатомия, а также локализация раскопок проливают свет на особенности экологии этих вымерших животных. — Scimitar-crested Spinosaurus species from the Sahara caps stepwise spinosaurid radiation.
-
Автор
-
Редактор
В новом дайджесте «Биомолекулы» мы расскажем о дизайне искусственных белков для перепрограммирования клеточных рецепторов GPCR, об «умных» имплантах, растущих вместе с сердцем ребенка, анализах крови, способных предсказать точное время начала болезни Альцгеймера, а также об открытии нового вида спинозавра.
Нейробиология
Новые «биологические часы» предупредят о наступлении болезни Альцгеймера
Развитие болезни Альцгеймера связано с накоплением в тканях мозга двух типов патологических белков: бета-амилоида и тау-белка, имеющих аномальную пространственную структуру (рис. 1). Бета-амилоид скапливается в бляшки снаружи клеток, а тау-белок образует нейрофибрилярные клубки внутри нейронов, разрушая их структуру. Ученые установили, что появление фосфорилированной формы тау-белка в крови у пациента помогает предсказать развитие болезни за несколько лет до ее начала. Дело в том, что первые отдаленные симптомы болезни Альцгеймера можно обнаружить с помощью позитронно-эмиссионной томографии, когда начинают появляться первые бета-амилоидные бляшки (10–20 лет до развития первых симптомов). При этом, с появлением первых симптомов болезни количество бляшек стабилизируется. Количество нейрофибрилярных клубков на основе тау-белка, напротив, начинает увеличиваться гораздо позже, по мере развития симптомов заболевания.
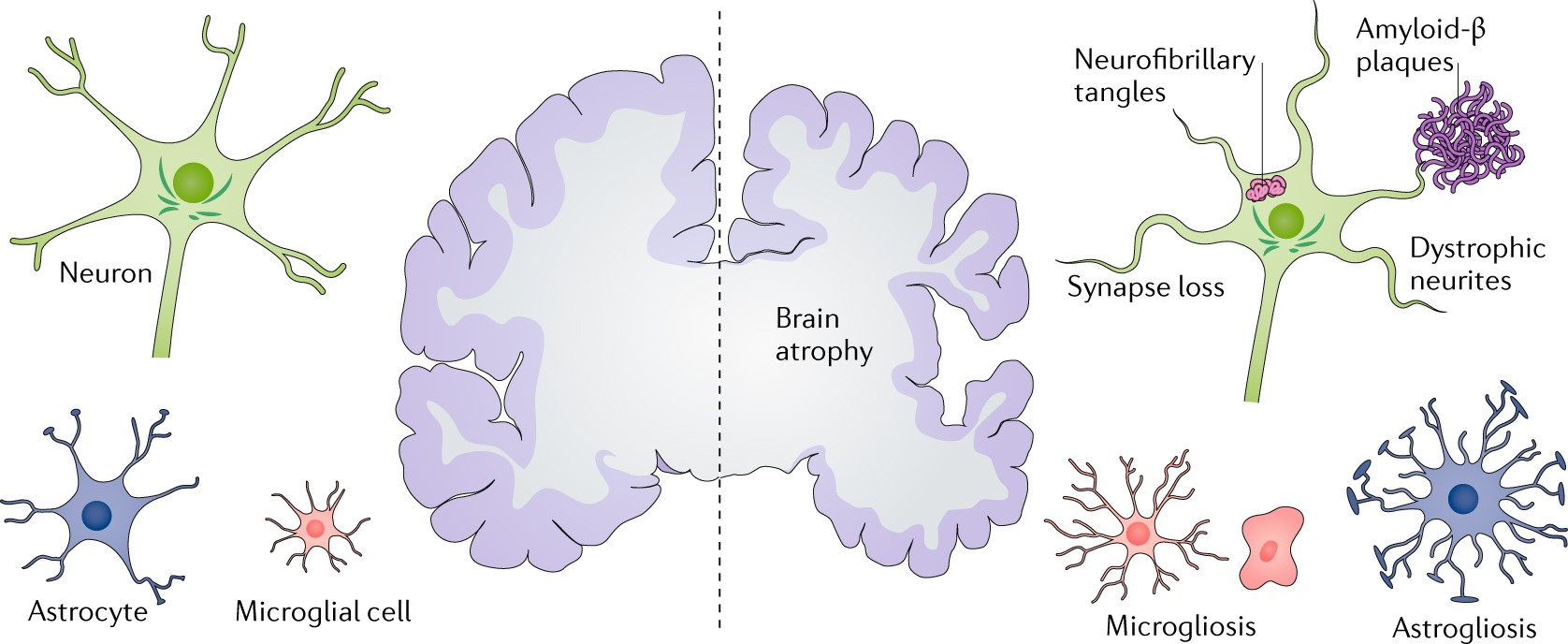
Рисунок 1. Схема строения головного мозга и морфологии клеток нервной ткани в норме (слева) и на фоне развития болезни Альцгеймера (справа).
Лечение пациентов на более ранней доклинической стадии болезни Альцгеймера, до развития значительной нейродегенерации, может быть более эффективным. Новое исследование демонстрирует, что анализ крови на уровень фосфорилированного тау-белка (p-tau217) позволяет с высокой точностью предсказать появление симптомов болезни Альцгеймера и начать терапию уже на самых ранних стадиях. Метод коррелирует накопление специфического белка с возрастом пациента, обещая доступную диагностику для оценки рисков у людей старше 50 лет. Поскольку патология Альцгеймера у разных людей прогрессирует по единому сценарию, уровни специфических белков позволяют создать модель «биологических часов» заболевания. Эти «часы» точнее хронологического возраста: они определяют момент старта болезни и позволяют с высокой точностью предсказать время появления первых клинических симптомов. — Predicting onset of symptomatic Alzheimerʼs disease with plasma p-tau217 clocks, «Биомолекула»: «На руинах памяти: настоящее и будущее болезни Альцгеймера».
Кальциевые каналы необходимы для развития нейровоспаления
Наш головной мозг изолирован от остального организма с помощью гематоэнцефалического барьера. Обычные клетки иммунной системы не могут его преодолеть, и поэтому защитой нейронов от «непрошенных гостей» занимаются специальные клетки микроглии — резидентые иммунные клетки головного мозга. Клетки микроглии активируются при травме и в случае инфекции, способствуя развитию воспалительного процесса. Группа исследователей из США и Канады установили, что для активации микроглиальных клеток необходим белок Orai1.
Orai1 (Calcium release-activated calcium channel protein 1) — кальциевый канал, вовлеченный в огромное количество физиологических процессов, от активации Т-лимфоцитов до мышечного сокращения. «Выключение» гена Orai1 в этом типе клеток нарушило способность микроглии переходить в реактивное состояние и подавило развитие воспаления. Введение липополисахарида (ЛПС) мышам с дефицитом Orai1 привело к подавлению экспрессии провоспалительных факторов IL-1β и IL6 в гиппокампе. При этом, активность противовоспалительных факторов, BDNF и ARG1, наоборот, повысилась. Следствием этих биохимических изменений стало снижение дезадаптивного поведения у мышей с нокаутом Orai1: поведение избегания и поиск вознаграждения у таких мышей были более выражены, чем у контрольной группы на фоне введения ЛПС. Таким образом, Orai1 может быть важной мишенью для борьбы с нарушениями поведения на фоне воспаления. — Microglial reactivity and neuroinflammation-driven changes in motivational behaviors are regulated by Orai1 calcium channels, «Биомолекула»: «Загадочный кальциевый язык».
Онкология
Полиморфизм в гене BDNF связан с периферической нейропатией при онкологии
При лечении онкологических заболеваний врачи часто сталкиваются с нейропатией, вызванной химиотерапевтическим лечением. Группа исследователей изучила данные, собранные от пациентов с колоректальным раком, и обнаружила, что восприимчивость пациента к развитию нейропатии связана с полиморфизомом в гене BDNF. Белок BDNF — нейротрофический фактор, который поддерживает рост нервных клеток. Оказалось, что аллель BDNF Val66 повышает восприимчивость к нейропатии при лечении оксалиплатином, тогда как аллель Met66, наоборот, обеспечивает защитное действие. Вариант BDNF Val66 широко распространен в Азии (49%), и от 1 до 20% среди других этнических группах. Ученые установили, что защитный механизм связан с активацией сигнального пути, опосредованного p75NTR (один из рецепторов BDNF), который нарушается у аллели Val66.
На основании полученных данных ученые разработали две терапевтические стратегии. В первом случае они использовали модулятор p75NTR, а во втором — собственную разработку, соединение СN016 с выраженным противовоспалительным эффектом. Испробовав обе стратегии на гуманизированных мышах c полиморфизмом BDNF на фоне введения оксалиплатина, исследователи показали значительный нейропротекторный эффект. — BDNF Val66Met protects oxaliplatin-induced peripheral neuropathy in patients with colorectal cancer, «Биомолекула»: «BDNF: почему спорт — это жизнь?».
Структурная биология
Экзоскелет для рецептора: мы стоим на пороге новой эры в фармакологии?
В 2024 году произошло поистине эпохальное событие: Нобелевская премия по химии была вручена за проектирование «дизайнерских», не существующих в природе молекул белков c помощью новой программы Rosetta, а также за разработку алгоритма AlphaFold2 для предсказания трехмерной структуры уже существующих белков. «Биомолекула» подробно писала об этих открытиях и стоящих за ними ученых. На этой неделе мы увидели первые результаты применения этих технологий. Группа китайских исследователей разработала подход, с помощью которого можно с нуля строить регуляторы рецепторов, сопряженных с G-белками (GPCR), используя технологии искусственного интеллекта и модели машинного обучения.
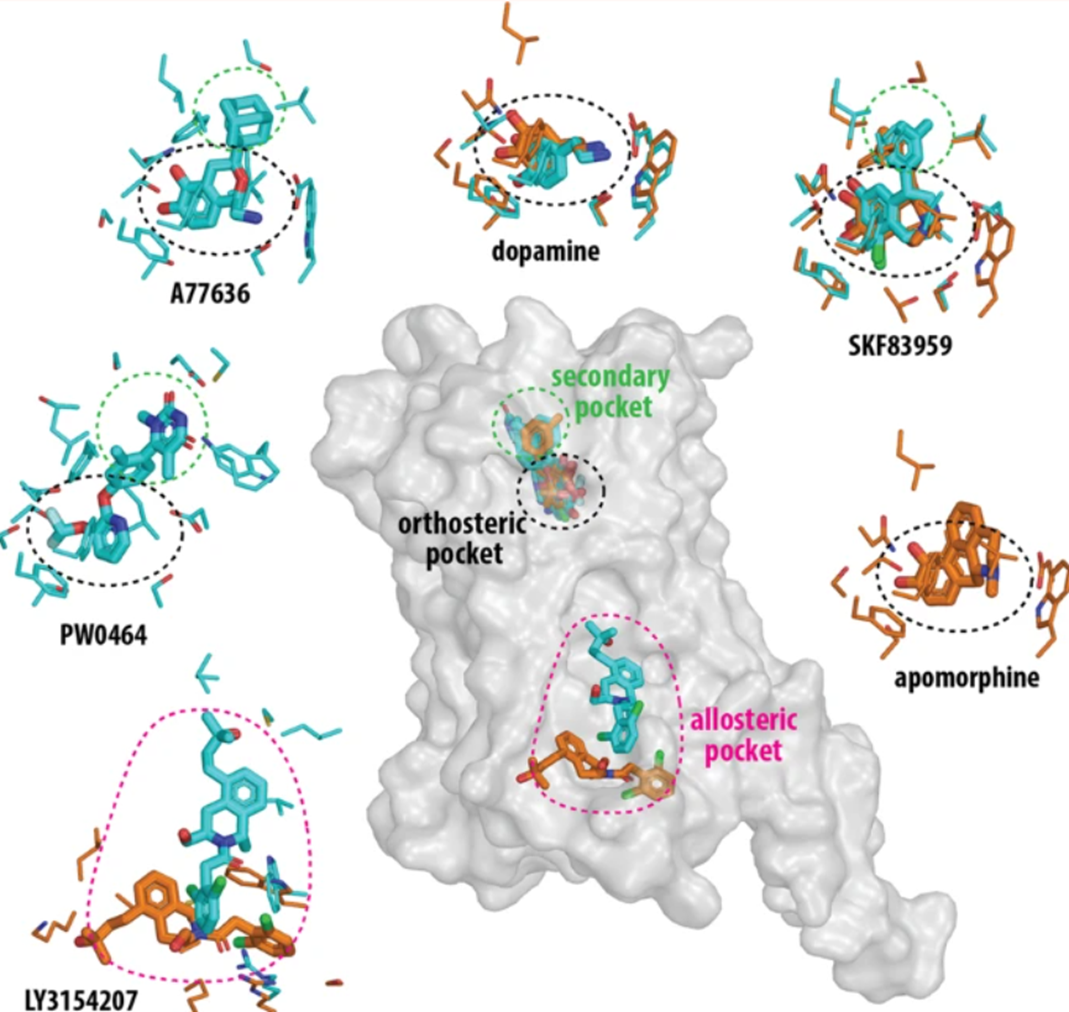
Рисунок 2. Структура D1-дофаминового рецептора. На схеме указаны ортостерический и аллостерический участки связывания регуляторов.
Рецепторы GPCR не нуждаются в особом представлении, ведь это самые популярные мишени современной фармакологии (вспомнить хотя бы рецептор GLP-1, на который действует знаменитый семаглутид). Препараты, регулирующие работу GPCR — это либо ортостерические регуляторы (связываются с той же частью белка, что и природные лиганды), либо аллостерические (действуют на какую-либо другую часть молекулы GPCR, рис. 2). Однако разработка таких препаратов — это в большей степени «подбор отмычки вместо ключа», то есть поиск той особенной молекулы, которая сможет подействовать на рецептор лучшим образом, чем другие.
Но это было вчера. Cheng и соавторы отошли от старой парадигмы и сконструировали абсолютно новые белки, никогда ранее не существовавшие в природе, которые специфично связываются с GPCR и могут влиять на его активность. GPCR exoframe modulator (GEM) связываются с трансмембранным доменом белка, стабилизируя ту или иную его конформацию (укладку), действуя как своего рода экзоскелет. Такой способ активации (или стабилизации) рецептора может быть особенно актуальным, если рецептор уже имеет нарушенную конформацию из-за мутации и поэтому работает неправильно или не работает вообще. В таком случае GEM может действовать как «корсет», поддерживающий правильную форму белка, что позволяет ему сохранять активность.
Белки GEM работают как аллостерические модуляторы: могут быть положительными (усиливать активность рецептора — PAM), отрицательными (подавляют работу рецептора) или выполняют роль bias-агониста, смещая активность рецептора в отношении одного из внутриклеточных сигнальных путей. Исследователи испытали новую технологию на дофаминовых рецепторах D1. Cконструированные ими белки GEM — agoPAM — полностью восстановили активность мутантных рецепторов.
Эта работа дает надежду на то, что эра случайных находок в фармакологии может подойти к концу и что теперь мы не будем искать новые препараты вслепую, а сможем «спроектировать» специальную вспомогательную молекулу для каждого «сломанного» рецептора, как инженер проектирует новую деталь для самолета. — De novo design of GPCR exoframe modulators, «Биомолекула»: «Несуществующие в природе белки́ — за что вручили Нобелевскую премию по химии (2024)», «Рецепторы в активной форме», «Проблема фолдинга белка», «Аллостерические регуляторы GPCR: ключи от всех замков».
Трансплантология
Новый стент будет расти вместе с маленьким пациентом при врожденном пороке клапанов сердца
Лечение врожденных дефектов клапанов сердца у детей — это всегда борьба со временем. Основная проблема в том, что искусственный клапан не растет вместе с организмом. В настоящее время в детской кардиохирургии для решения этой проблемы используют разные подходы: от операций по замене клапана до использования баллонного катетера, который вводится через бедренную артерию и расширяет стент с клапаном до нужного размера. В последнем случае это все равно операция, хоть и менее инвазивная, плюс существует риск повреждения сердца. Авторы данного исследования разработали «умный» саморасширяющийся стент из нитинола, который избавляет от необходимости повторных операций. Благодаря свойствам материала, клапан плавно увеличивается в диаметре, подстраиваясь под рост тканей, что подтвердили успешные тесты на поросятах, где устройство выросло с 8 до 13 мм за шесть недель (рис. 3). Свиное сердце по многим параметрам похоже на сердце человека, что позволяет тестировать на нем медицинские устройства в реальном размере. Кроме того, сердце поросенка отличается феноменальной скоростью роста, что помогло исследователям устроить настоящий «тест-драйв» нового стента, ведь за 6 недель это сердце вырастает так же, как у ребенка за несколько лет. Подобные адаптивные технологии обеспечат долгосрочное решение для врожденных пороков сердца. — Engineering surgery-free prosthetic heart valve growth.
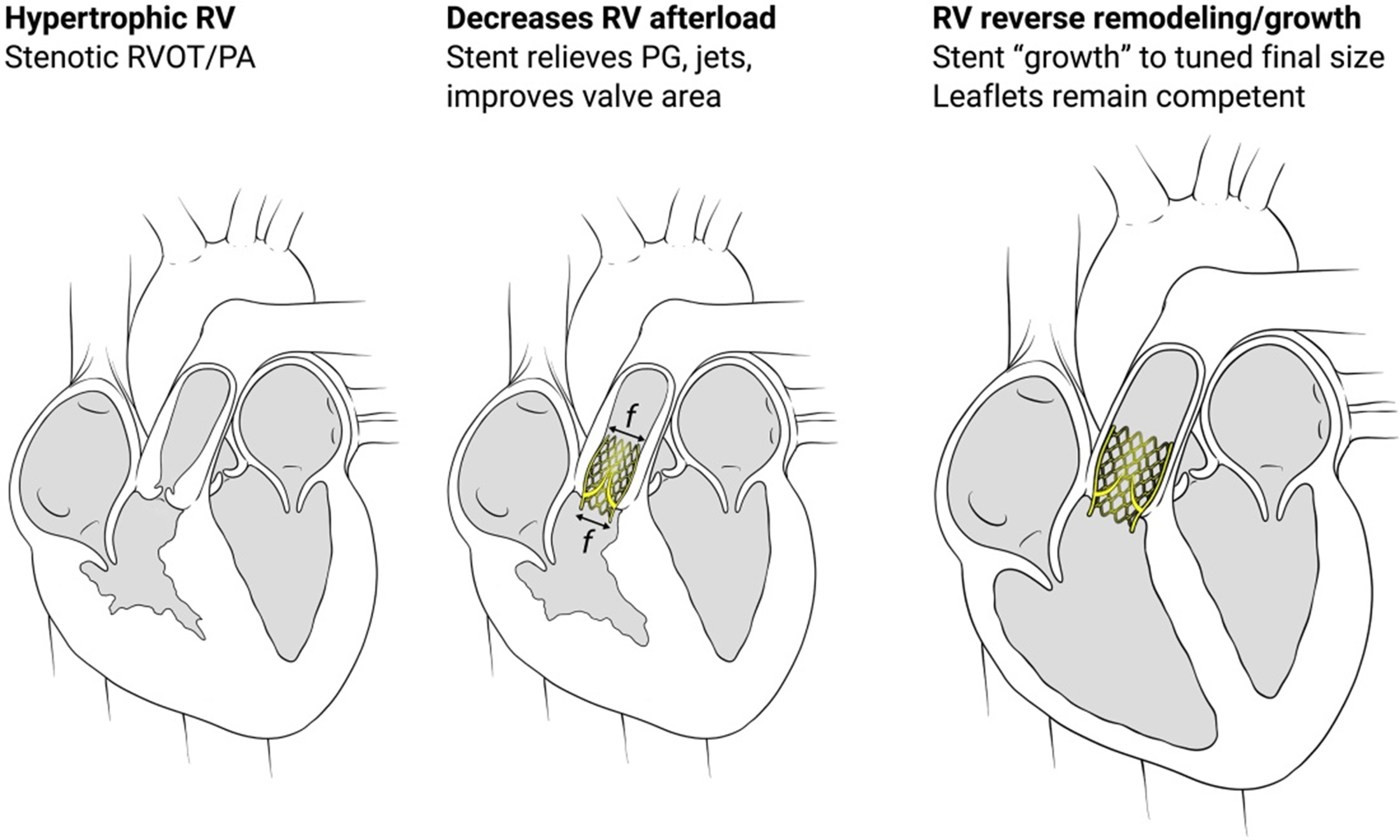
Рисунок 3. Спонтанно растущий клапанный стент. Слева: стеноз правого желудочка у младенца. RVOT — выходной тракт правого желудочка. PA — легочная артерия. В центре: имплантированный стент немедленно снижает нагрузку за счет увеличения площади отверстия. Затем энергия пружины постепенно высвобождается для дальнейшего расширения трансплантата за счет радиальной силы (f) до его окончательного размера (справа), после чего он работает как стандартный стентированный клапан с приемлемым диаметром. Стент разработан таким образом, чтобы створки оставались функциональными на протяжении всего диапазона расширения, а также чтобы позволить желудочку нормально расти в течение этого периода. PG — градиент давления.
Палеонтология
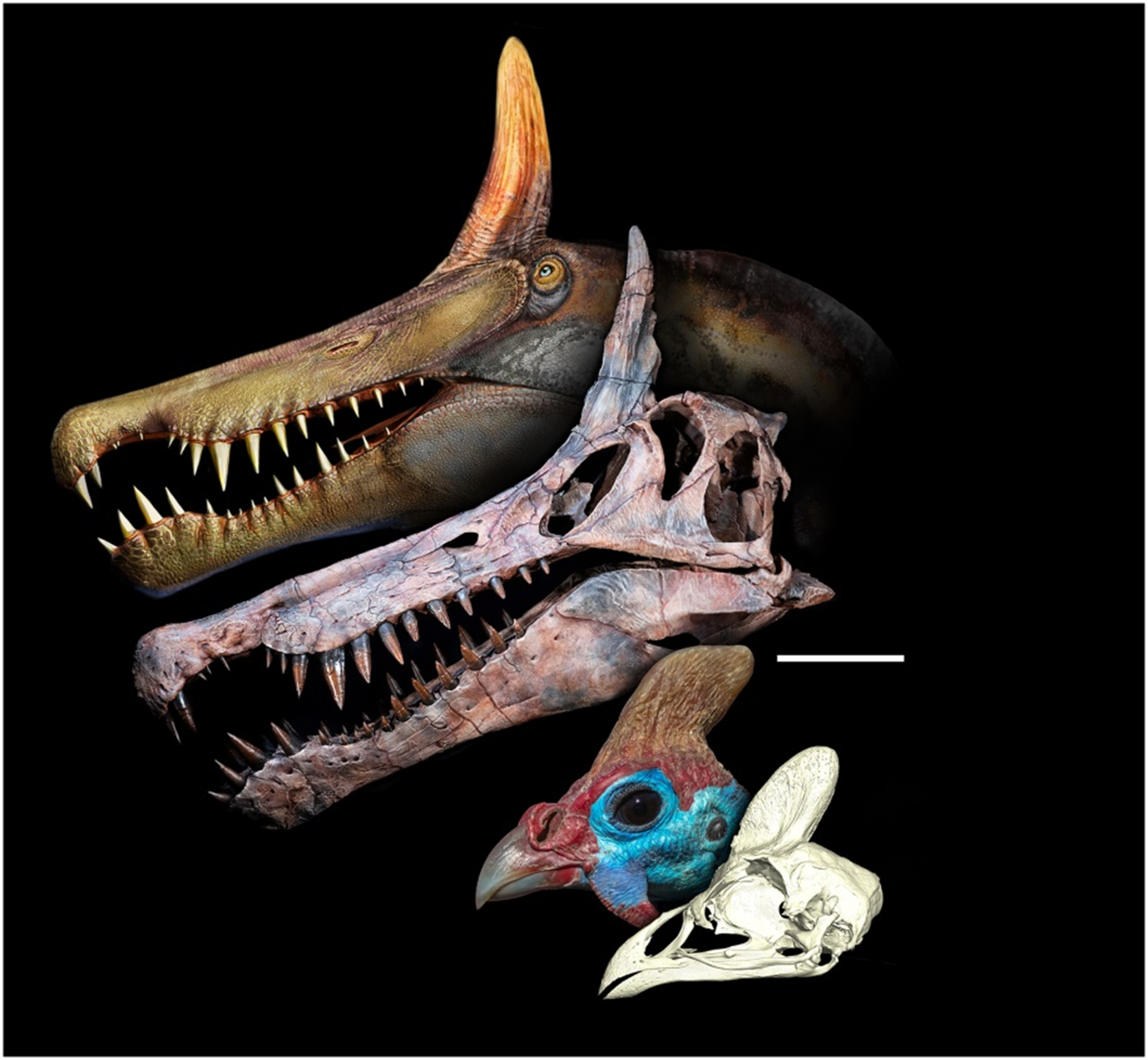
Рисунок 4. Костяные гребни вымерших динозавров и живущих ныне птиц. У найденного S. mirabilis самый высокий гребень на голове среди всех тероподных (двуногих) динозавров. На картинке — сравнение с гребнем ныне живущей цесарки шлемоносной (Numida meleagris). Ученые предполагают, что такой гребень использовался для демонстрации: готовности к спариванию, устрашению конкурентов или просто помогал особям этого вида узнавать друг друга в густых зарослях болотных растений.
Находка в Сахаре раскрыла тайну жизни спинозавра
Популярный образ спинозавра как «подводного монстра» из кино окончательно уступает место реальности: новое открытие в Сахаре доказывает, что этот гигант был скорее «супер-цаплей», чем крокодилом. Новые данные из центральной Сахары, основанные на открытии нового вида Spinosaurus mirabilis с характерным высоким черепным гребнем, подтверждают гипотезу о том, что спинозавры были высокоспециализированными прибрежными хищниками мелководья, а не полностью водными животными (рис. 4). Анализ пропорций тела относит этих динозавров ближе к болотным птицам, таким как цапли, что указывает на их адаптацию к засадному образу жизни на берегах и в мелких водоемах. Около 95 млн лет назад резкое повышение уровня моря положило конец распространению этих рептилий. — Scimitar-crested Spinosaurus species from the Sahara caps stepwise spinosaurid radiation.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚




