Теломерные фаги: «серые кардиналы», сумевшие удивить ученых
28 января 2026
Теломерные фаги: «серые кардиналы», сумевшие удивить ученых
- 252
- 0
- 3
Случайность помогла ученым обнаружить два белка — токсин и антитоксин, — закодированные в геноме необычных бактериофагов. Возможно, это открытие поможет в борьбе с антибиотикорезистентными бактериями.
Рисунок в полном размере.
-
Автор
-
Редакторы
Авторы «Биомолекулы» рассказывали о фагах много. Этим вирусам даже посвящен целый спецпроект на сайте. Но фаги не перестают удивлять и преподносить сюрпризы. В сегодняшнем обзоре одного научного исследования мы расскажем о необычной разновидности бактериофагов, на которые долго не обращали внимания; о том, как они наделяют бактерии некоторыми преимуществами; и как могут быть потенциально полезны в борьбе с опасными инфекциями.
Бактериофаги — вирусы, поражающие бактерии , — бывают вирулентными, умеренными, а еще... теломерными. О существовании последних известно уже не первое десятилетие, и их всегда считали некой диковинкой, не заслуживающей особого внимания. Но не так давно они смогли удивить ученых. Этот тип вирусов оказался весьма распространенным, и он умеет производить мощное «химическое оружие» против болезнетворных микроорганизмов.
Читайте спецпроект «Биомолекулы» о бактериофагах, например, статьи: «Огромный и загадочный мир бактериофагов» [1], «Бактериофаги в медицине» [2] и «Заклятые друзья и закадычные враги: как бактериофаги и бактерии сосуществуют миллионы лет» [3].
Всё началось с того, что ученые из Университета Монаша в Австралии решили изучить геном условно-патогенных бактерий рода Klebsiella. А дальше, как нередко бывает в науке, вмешалась счастливая случайность. Геномный анализ показал, что в 10% исследованных геномов бактерий присутствуют гены теломерного фага под названием NAR688. Это стало для ученых неожиданностью: раньше считалось, что данная разновидность бактериофагов встречается очень редко.
Но раз они на самом деле так распространены, значит, в них есть что-то интересное? Ученые продолжили исследовать фаг NAR688 и, действительно, обнаружили весьма занимательные (и потенциально полезные для медицины) находки [4].
Новый класс бактериоцинов: телоцины
Проведя протеомный анализ, исследователи обнаружили в зараженных клебсиеллах девять белков, кодируемых генами вируса NAR688. Шесть из них участвуют в регуляции и поддержании генома фага, распределении его ДНК между дочерними клетками во время деления. Один из обнаруженных белков входит в состав хвостовой трубки вириона.
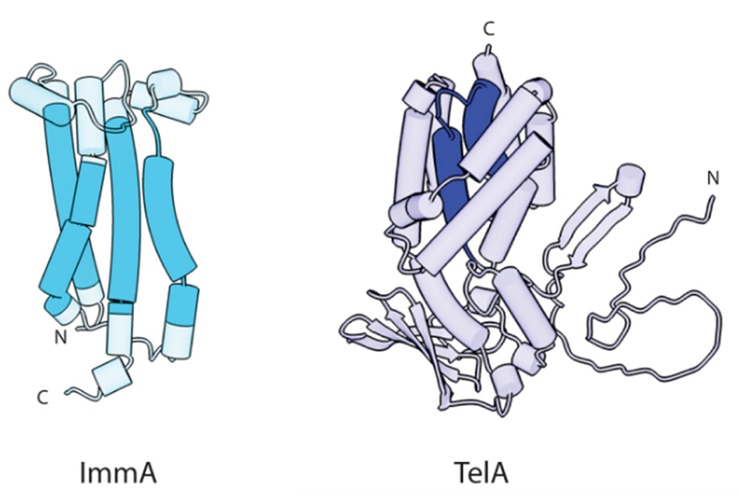
Два других белка оказались намного интереснее. Анализ их структуры и аминокислотной последовательности выявил неожиданные функции:
- Один из белков, получивший название TelA, оказался токсином, а именно порообразующим бактериоцином, уничтожающим чувствительные к нему бактериальные клетки.
- Второй белок окрестили ImmA. Он, наоборот, обладает защитной функцией, инактивируя токсин [4].
Австралийские исследователи решили, что нужно немного усовершенствовать терминологию, и предложили называть бактериоцины, кодируемые теломерными фагами, телоцинами.
Взаимовыгодный союз фага и бактерии
Эксперименты показали, что телоцин TelA, действительно, подавляет рост чувствительных к нему клебсиелл и дает преимущество микроорганизмам, зараженным фагом NAR688. Таким образом, отношения между бактерией и вирусом можно охарактеризовать как мутуалистические. Бактериофаг помогает клебсиеллам процветать и подавлять сородичей, а бактерии обеспечивают размножение фага.
Дальнейший анализ показал, что в клебсиеллах обитают еще как минимум четыре теломерных фага, в генах которых закодирована структура телоцинов. Эти фаги были названы TelB, TelC, TelD и TelE. А соответствующие пары «токсин:защитный белок» обозначили как TelB:ImmB, TelC:ImmC, TelD:ImmD и TelE:ImmE.
Самым эффективным оказался TelB: он уничтожил 51 из 53 протестированных штаммов незараженных бактерий. Второе и третье место заняли TelA и TelE, уничтожившие, соответственно, 31 и 30 штаммов. TelC оказался эффективен против 10 штаммов, а TelD — только против трех.
Был обнаружен у клебсиелл и теломерный фаг, у которого нет гена телоцина. Его назвали NAR033, а все подобные «нетоксичные» вирусы авторы исследования предложили обозначать как Tel0. Геномы всех перечисленных бактериофагов схематически представлены на рис. 2 [4].
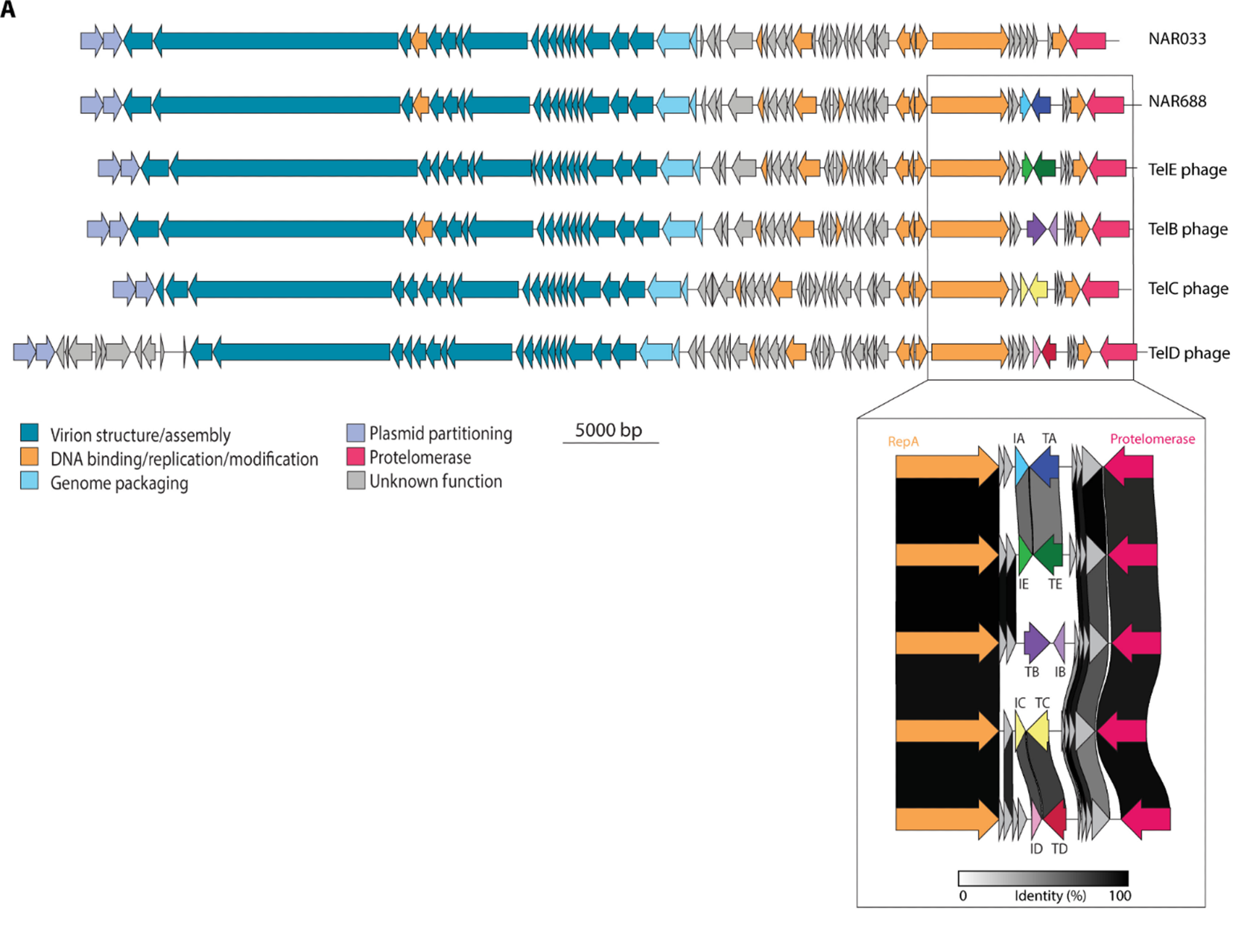
Рисунок 2. Геномы шести теломерных фагов Klebsiella. В пяти присутствуют гены телоцинов (NAR688, TelB, TelC, TelD, TelE), в одном — отсутствует (NAR033).
Мало того, поиск по базе данных белков NCBI помог выявить неописанные ранее белки теломерных фагов в 13 родах микроорганизмов. Это говорит о том, что данная разновидность бактериофагов сильно недооценена. Они намного более распространены, чем было принято считать, и могут выполнять важные биологические функции, а также, возможно, иметь практическое значение для борьбы с опасными болезнетворными бактериями [4].
Чем это открытие полезно для медицины?
Борьба с бактериальными инфекциями в современном мире становится всё более сложным делом, потому что появляется всё больше бактерий, устойчивых к антибиотикам, а разработка новых антибактериальных препаратов находится в глубокой стагнации — мы писали об этом в особом спецпроекте: «Антибиотики и антибиотикорезистентность: от древности до наших дней» [11].
Многие ученые, работающие над этой проблемой, и врачи-инфекционисты хорошо знают, насколько страшно звучит аббревиатура ESKAPE. Она составлена из первых букв названий бактерий, которые обладают множественной лекарственной устойчивостью и представляют серьезнейшую угрозу для здоровья людей: Enterococcus faecium (фекальный энтерококк), Staphylococcus aureus (золотистый стафилококк), Klebsiella pneumoniae (клебсиелла пневмонии, палочка Фридлендера), Acinetobacter baumannii (ацинетобактер), Pseudomonas aeruginosa (синегнойная палочка) и Enterobacter spp. (энтеробактеры) [12].
Из-за бактерий, устойчивых к антибиотикам, ежегодно погибают почти 5 миллионов человек [13]. Ученые постоянно ищут новые способы борьбы с этими патогенами. В качестве альтернативы антибиотикам рассматриваются бактериофаги, антимикробные пептиды, бактериоцины и другие варианты.
Австралийские авторы научной работы считают, что телоцины могут быть полезны в борьбе с патогенами. В частности, с помощью них можно контролировать популяции Klebsiella spp. в больничных условиях [4]. Найдут ли загадочные теломерные фаги и кодируемые ими токсины в итоге применение в клинической практике — покажет время. Пока еще эти вирусы скрывают много тайн, и связаны они не только с медициной, но и с вопросами эволюции, экологии микроорганизмов. Вероятно, это создаст поводы для новых интересных исследований и открытий в будущем.
Литература
- Огромный и загадочный мир бактериофагов;
- Бактериофаги в медицине;
- Заклятые друзья и закадычные враги: как бактериофаги и бактерии сосуществуют миллионы лет;
- Sally M. H. Byers, Andrea Rocker, To N. T. Nguyen, Natalia C. Rosas, George Taiaroa, et. al.. (2025). Telomere bacteriophages are widespread and equip their bacterial hosts with potent interbacterial weapons. Sci. Adv.. 11;
- Бактериоцины — ноухау биомедицины;
- Войны клонов. Фаговые камикадзе в борьбе за субстрат;
- Пожиратели бактерий: убийцы в роли спасителей;
- Антибиотики прямо под нашим носом;
- Paul D. Cotter, Colin Hill, R. Paul Ross. (2005). Bacteriocins: developing innate immunity for food. Nat Rev Microbiol. 3, 777-788;
- Fatima R. Ulhuq, Giuseppina Mariano. (2022). Bacterial pore-forming toxins. Microbiology. 168;
- Антибиотики и антибиотикорезистентность: от древности до наших дней;
- William R. Miller, Cesar A. Arias. (2024). ESKAPE pathogens: antimicrobial resistance, epidemiology, clinical impact and therapeutics. Nat Rev Microbiol. 22, 598-616;
- Mohammed Seid, Berari Bayou, Addis Aklilu, Dagimawie Tadesse, Aseer Manilal, et. al.. (2025). Antimicrobial resistance patterns of WHO priority pathogens at general hospital in Southern Ethiopia during the COVID-19 pandemic, with particular reference to ESKAPE-group isolates of surgical site infections. BMC Microbiol. 25.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚