Восстановлению подлежит: как вернуть зрение?
09 марта 2026
Восстановлению подлежит: как вернуть зрение?
- 489
- 0
- 1
Рисунок в полном размере.
иллюстрация Софии Ващенко
-
Автор
-
Редакторы
-
Иллюстратор
Статья на конкурс «Био/Мол/Текст»: В статье описаны последние исследования в области восстановления зрения, результатом которых стала разработка лекарственного препарата на основе моноклональных антител к белку, предотвращающему регенерацию глиальных клеткок сетчатки — клеток Мюллера. Слепоту можно победить?
Конкурс «Био/Мол/Текст»-2025/2026
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2025/2026.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

Партнер номинации — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Ключевые проблемы потери зрения
Зрение является самым важным из чувств человека. С его помощью на протяжении всей жизни мы получаем основное количество информации об окружающем мире [1], а также формируем большую часть воспоминаний.
По данным ВОЗ, нарушения зрения выявлены не менее чем у 2,2 миллиарда человек во всем мире. Они возникают в любом возрасте, однако большинство страдающих дегенеративными изменениями сетчатки — люди старше 50 лет. Поскольку средняя продолжительность жизни населения продолжает расти [2], заболеваемость также будет увеличиваться, поэтому нарушения зрения — серьезная и актуальная проблема, которая требует новых методов решения.
Основной фактор, ограничивающий восстановление зрения у млекопитающих — отсутствие способности клеток сетчатки к регенерации. Они, как и другие нейроны большинства тканей центральной нервной системы, не могут обновляться, в отличие, например, от клеток кожи.
В последние годы активно исследуются возможности восстановления функций сетчатки (о новых методах терапии можно прочитать на «Биомолекуле» [3], [4]). Было установлено, что регенерация сетчатки в первую очередь зависит от клеток Мюллера (КМ), которые при определенных условиях могут переходить в нервные клетки-предшественники.
Клетки Мюллера — предшественники нейронов?
КМ являются основными глиальными клетками сетчатки (составляют около 90% клеток ретинальной глии) и обеспечивают ее жизнедеятельность за счет доставки питательных веществ и кислорода к нервным клеткам и удаления из них ненужных продуктов обмена [5]. Каждая КМ является центром функциональной нейрональной колонки, из которых состоит сетчатка (рис. 1). Такое положение позволяет КМ обеспечивать анатомическую и функциональную связь между нейронами, кровеносными сосудами, полостью стекловидного тела и субретинальным пространством.
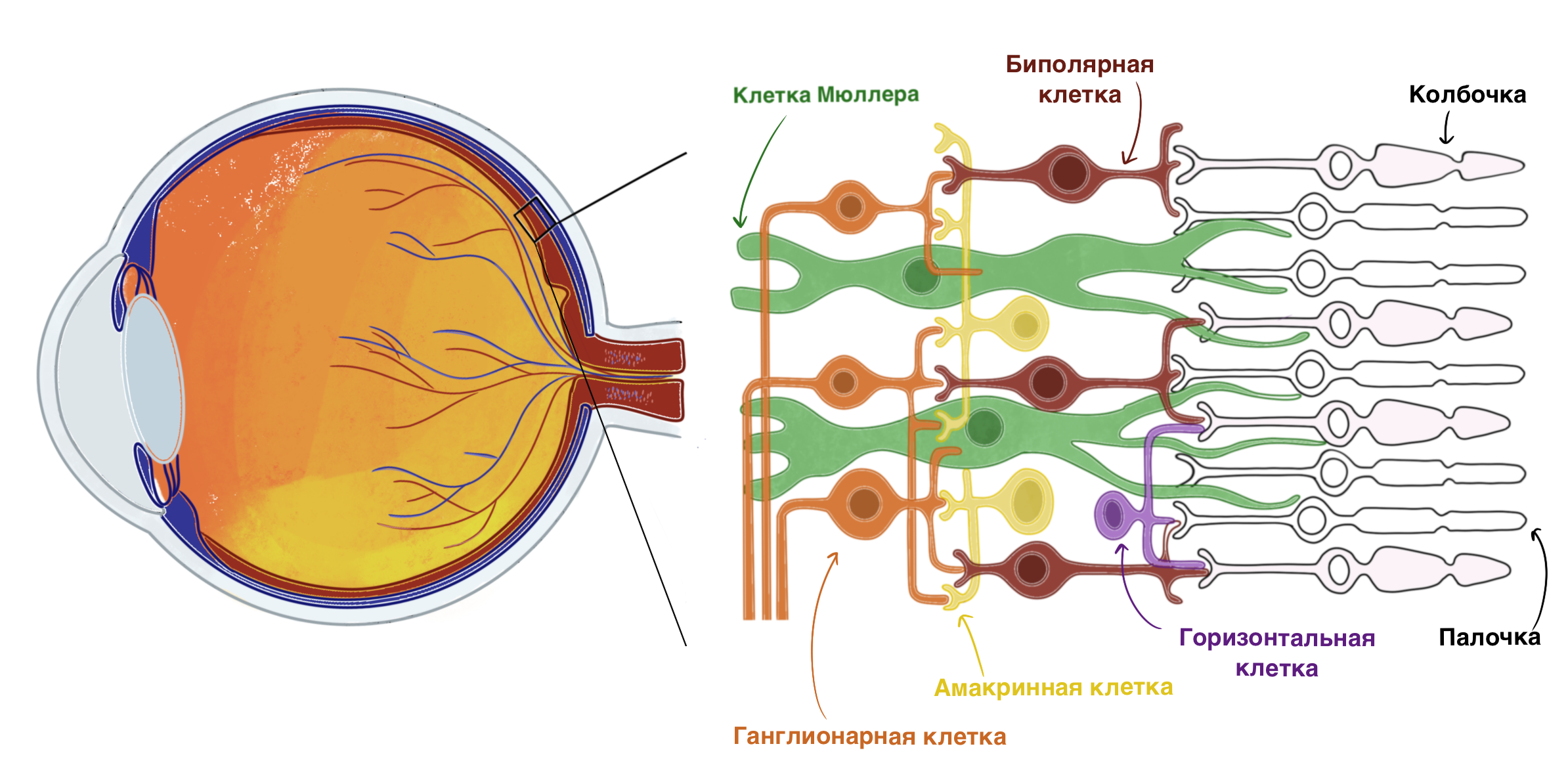
Рисунок 1. Строение сетчатки. Каждая КМ проходит через все слои сетчатки и своими отростками окружает кровеносные сосуды и нейроны, в том числе одну колбочку и до десяти палочек.
иллюстрация Софии Ващенко
В последнее время изучается способность клеток к дедифференцировке, пролиферации и дифференцировке в другие типы клеток (за открытие такой возможности в 2012 году дали Нобелевскую премию [6]). КМ — не исключение.
Как упоминалось ранее, у млекопитающих клетки сетчатки не способны к регенерации и реагируют на повреждение глиозом (нейроны заменяются глиальными клетками). Но есть позвоночные животные, КМ которых участвуют в регенерации нейронов. Так, повреждение сетчатки рыб и земноводных приводит к перепрограммированию генома КМ — они приобретают свойства стволовых. Образуются полипотентные клетки-предшественники, которые в последующем могут дифференцироваться во все основные типы клеток сетчатки [5].
КМ человека не функционируют в качестве клеток-предшественников в сетчатке in vivo, однако могут ими стать при определенных условиях, например, под воздействием факторов роста, различных цитокинов и при активации некоторых сигнальных путей [7–8]. Природа этих регуляторных факторов по большей части остается неизвестной, поэтому КМ являются интересной и перспективной для изучения точкой приложения терапии многих заболеваний сетчатки. Об исследованиях в данной области и пойдет речь далее.
Открытие новой мишени: отчего люди не видят так, как рыбы?
Описываемые результаты были получены учеными из Корейского института передовых технологий (KAIST), а также компании Celliaz Inc., и опубликованы в конце марта 2025 года [10].
Исследования проводили на рыбках данио-рерио (о них можно прочитать в материале «Биомолекулы» [11]) и мышах нескольких линий. Для моделирования ретинопатии использовали N-метил-N-нитрозомочевину (MNU).
В ходе экспериментов было обнаружено, что у мышей с повреждениями сетчатки, вызванными MNU, в КМ значительно усиливалось накопление белка Prox1, в отличие от здоровых мышей. У данио-рерио такого эффекта не наблюдалось (рис. 2).
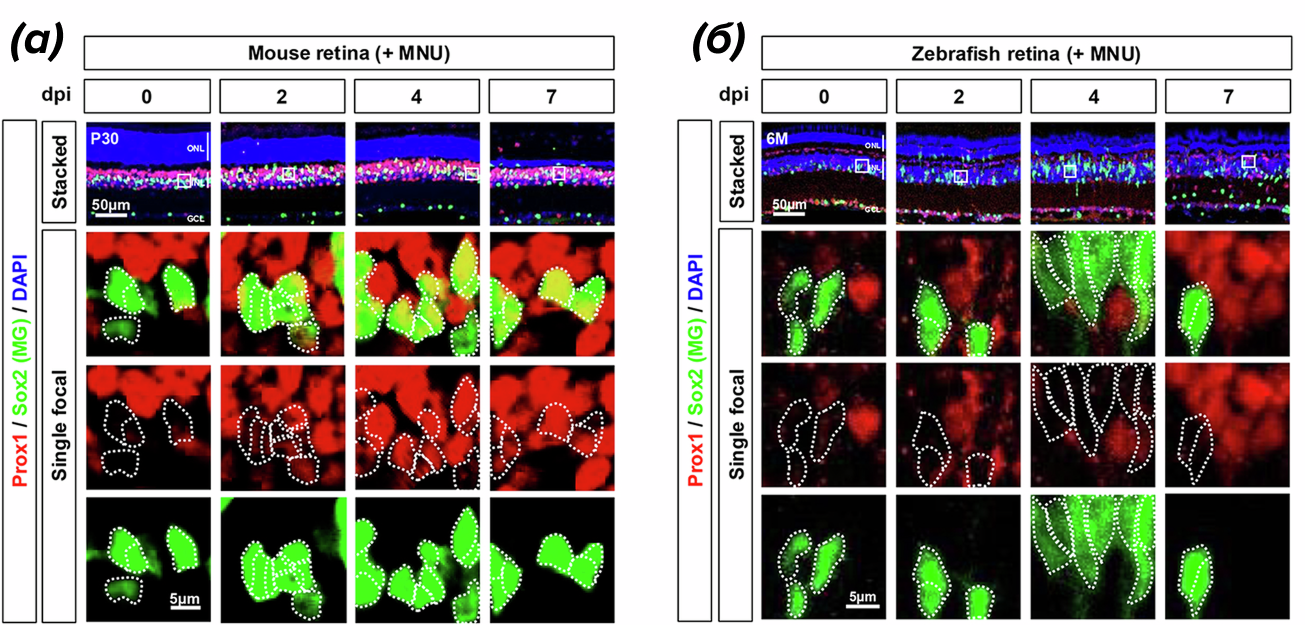
Рисунок 2. Распределение белка Prox1 в сетчатке мышей (а) и рыбок данио-рерио (б) по дням (0, 2, 4, 7) после повреждения сетчатки, вызванным MNU. Срезы сетчатки были окрашены кроличьими антителами к Prox1 (красный цвет) и козьими антителами для визуализации КМ (зеленый цвет). КМ также очерчены пунктирными линиями.
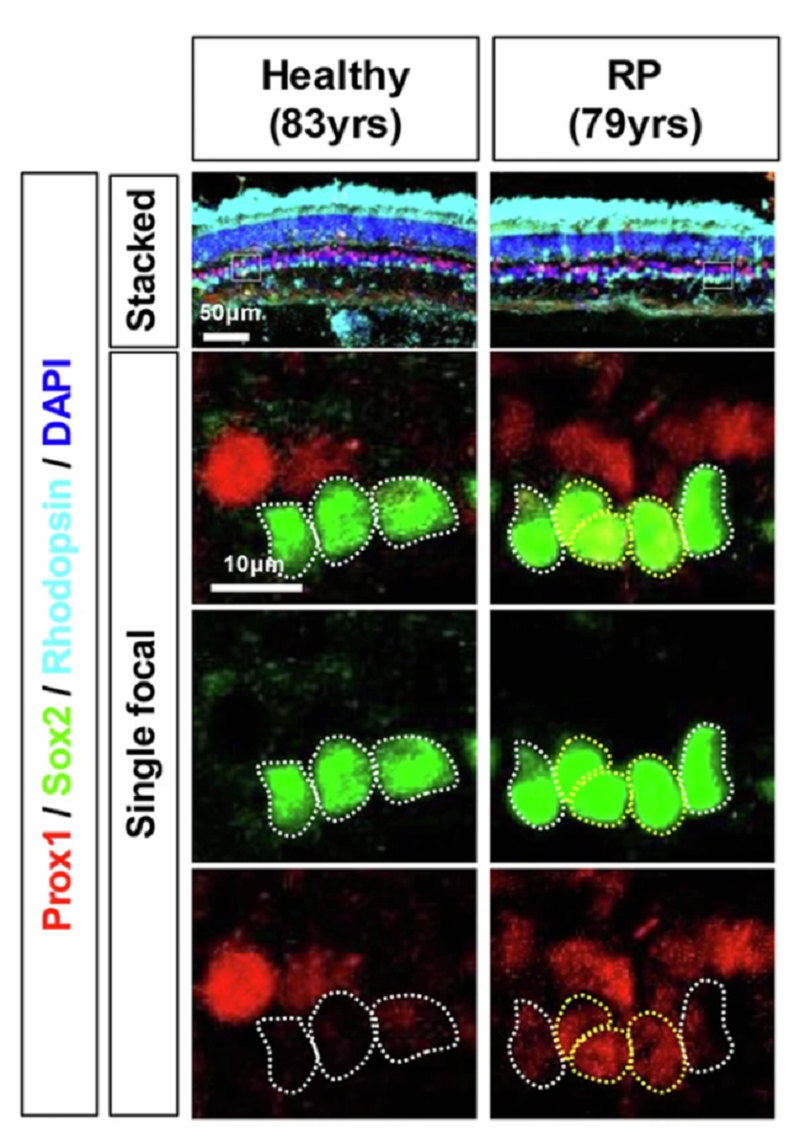
Рисунок 3. Распределение белка Prox1 в сетчатке человека без заболеваний сетчатки (Healthy) в возрасте 83 лет и человека с пигментным ретинитом (RP) в возрасте 79 лет. Срезы сетчатки были окрашены кроличьими антителами к Prox1 (красный цвет) и козьими антителами для визуализации КМ (зеленый цвет). КМ также очерчены пунктирными линиями.
Аналогичные результаты были получены при исследовании сетчатки мышей, ретинопатию у которых вызывали тремя различными способами: интенсивным световым воздействием, интравитреальным введением N-метил-D-аспартата (NMDA), а также действием дифтерийного токсина А. Это свидетельствует о том, что накопление Prox1 в КМ является общей реакцией на повреждение сетчатки у мышей, независимо от типа дегенерации ее клеток.
В ходе дальнейших исследований было выяснено, что Prox1 не экспрессируется эндогенно в КМ, а приобретается от соседних нейронов сетчатки (включая ганглиозные, биполярные и амакриновые клетки) посредством межклеточного переноса белка.
Также Prox1 был обнаружен в КМ человека с пигментным ретинитом, в отличие от КМ здорового донора (рис. 3).
Глаза человека были получены в сотрудничестве с банком донорских глаз Lionizers Gift of Sight Eye Bank и извлечены в течение 12 часов после смерти.
Таким образом, при ретинопатии Prox1 выявляется в КМ у мышей и человека, но отсутствует у рыб. Это дает основания предположить связь накопления Prox1 с невозможностью регенерации сетчатки. Введя рекомбинантные белки Prox1 внутриглазно, исследователи подавили пролиферацию пигментных клеток сетчатки у данио-рерио. Эти результаты свидетельствуют о том, что экзогенный Prox1 действительно является препятствием для регенерации сетчатки, опосредованной КМ, и указывают на то, что терапия против Prox1 является перспективной стратегией для восстановления способности сетчатки млекопитающих к регенерации.
Разработка стратегии терапии: нарушение межклеточного переноса белка
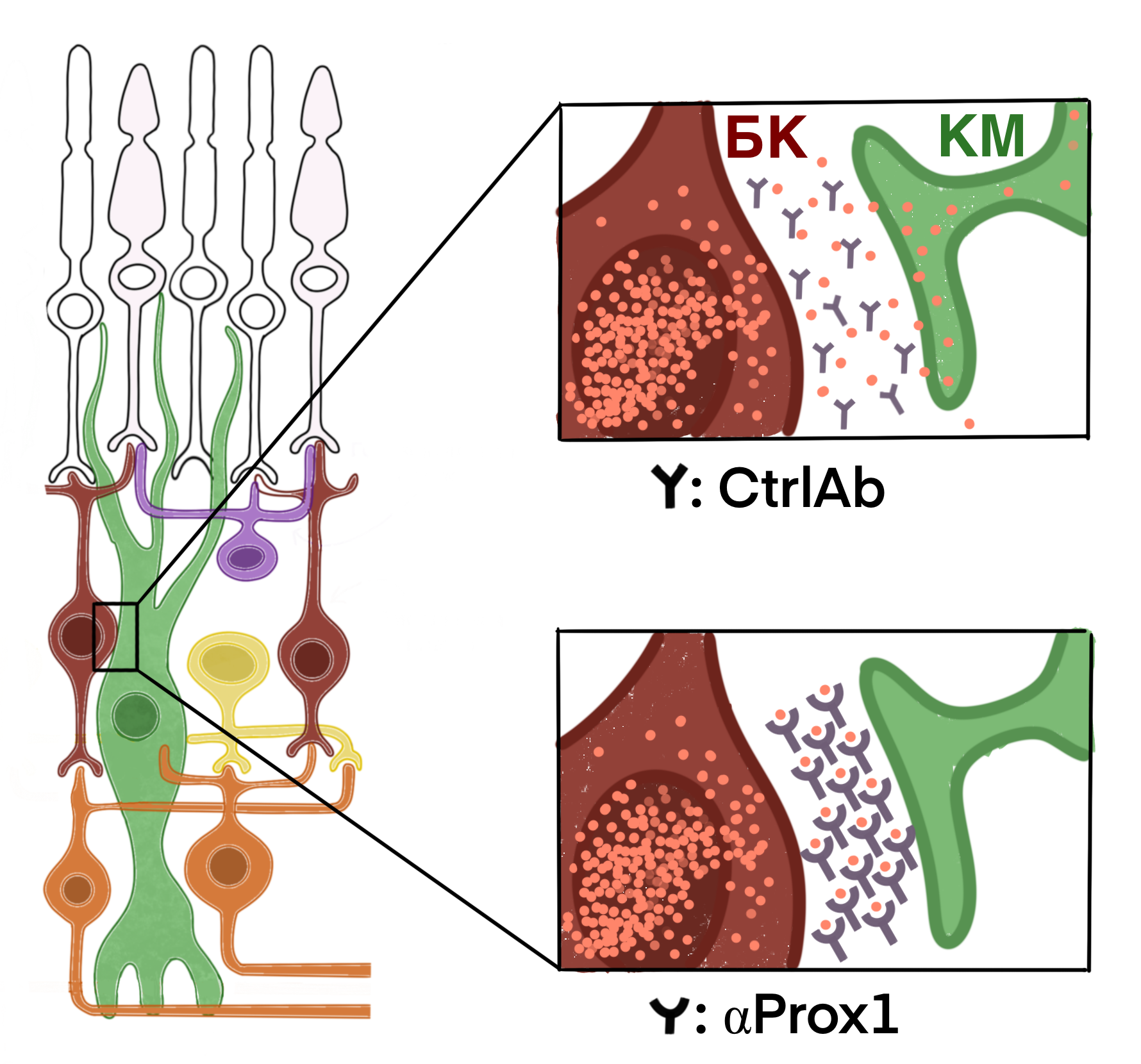
На основании этого открытия группа ученых разработала метод восстановления регенеративной способности КМ путем аденоассоциированной вирусной доставки антитела против Prox1 с целью связывания этого белка во время межклеточного переноса, чтобы препятствовать его накоплению в КМ (про использование аденоассоциированных вирусов и моноклональных антител в терапии различных заболеваний можно прочитать на «Биомолекуле»: [12], [13]).
Исследователи отобрали антитело, специфичное к белку Prox1. Клон гена иммуноглобулина был получен в виде scFv (от англ. single-chain fragment variable — вариабельный одноцепочечный фрагмент), объединен с метками для обнаружения и введен в геном аденоассоциированного вируса (AAV). В результате получена конструкция AAV2-αProx1.
Для экспериментальных сравнений тем же методом получили контрольную конструкцию AAV2-Ctrl Ab, в основе которой использован scFv, не обладающий сродством к Prox1.
Очищенные с помощью ультрацентрифугирования AAV2-αProx1 и AAV2-Ctrl Ab в стерилизованном фосфатно-солевом буфере вводили мышам интравитреально. Через 21 день вызывали повреждение сетчатки мышей внутрибрюшинным введением MNU. Также для визуализации пролиферирующих (активно делящихся) клеток использовали 5-этинил-2’-дезоксиуридин (EdU) (рис. 4).
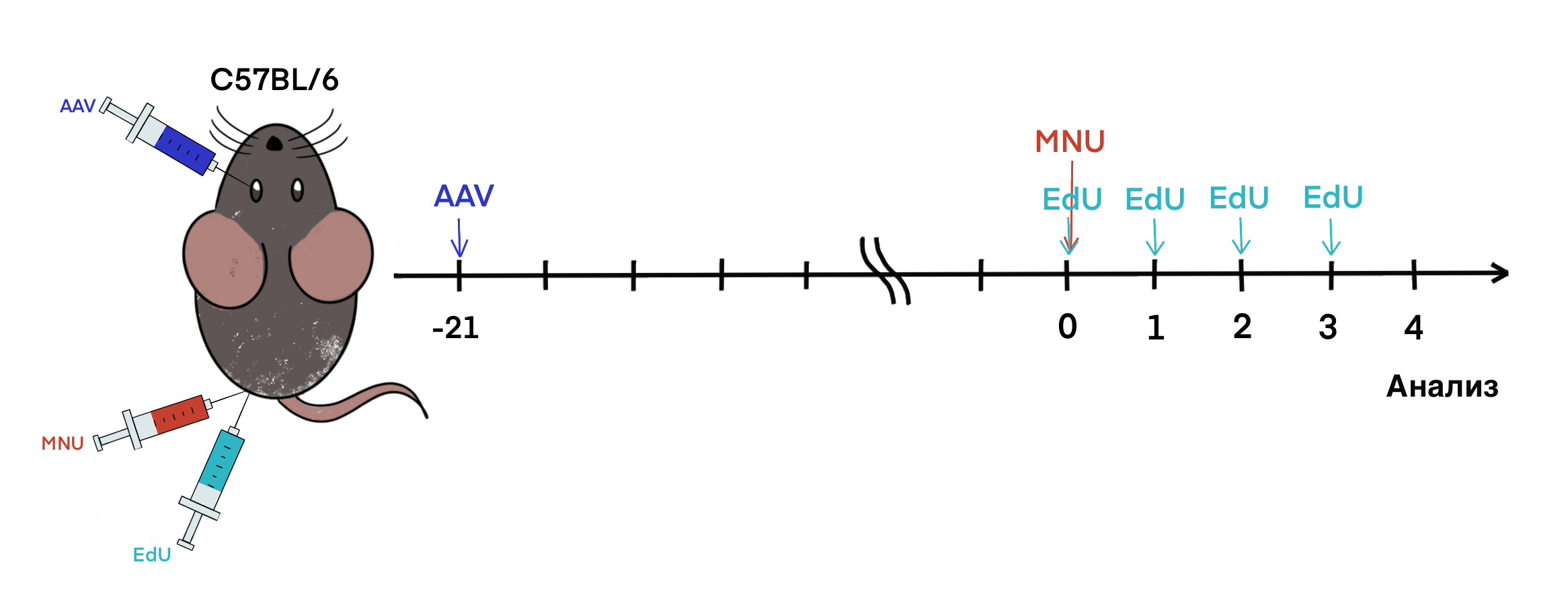
Рисунок 4. Схема введения конструкций на основе AAV, а также MNU и EdU по дням.
иллюстрация Софии Ващенко, адаптировано из [10]
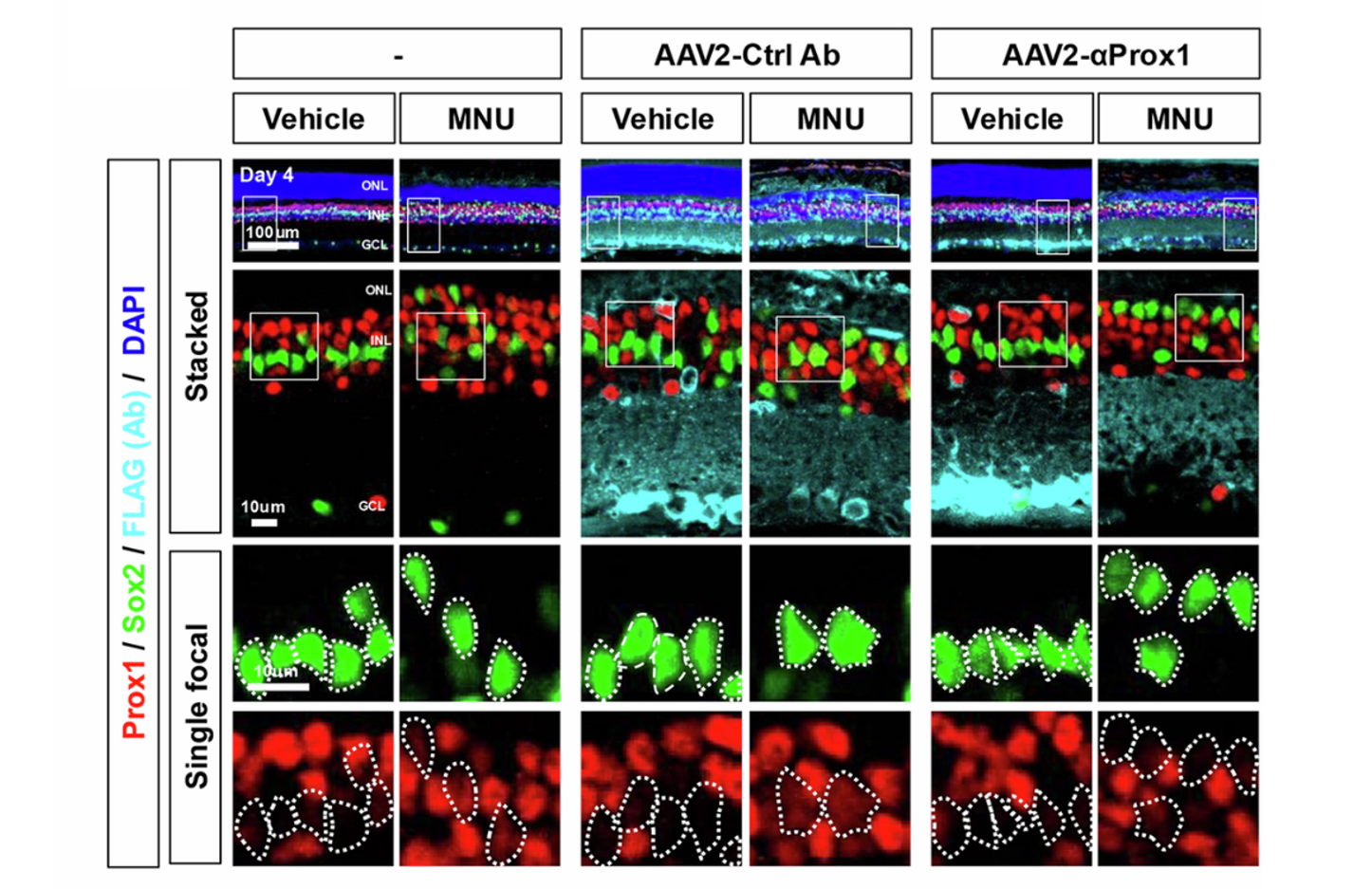
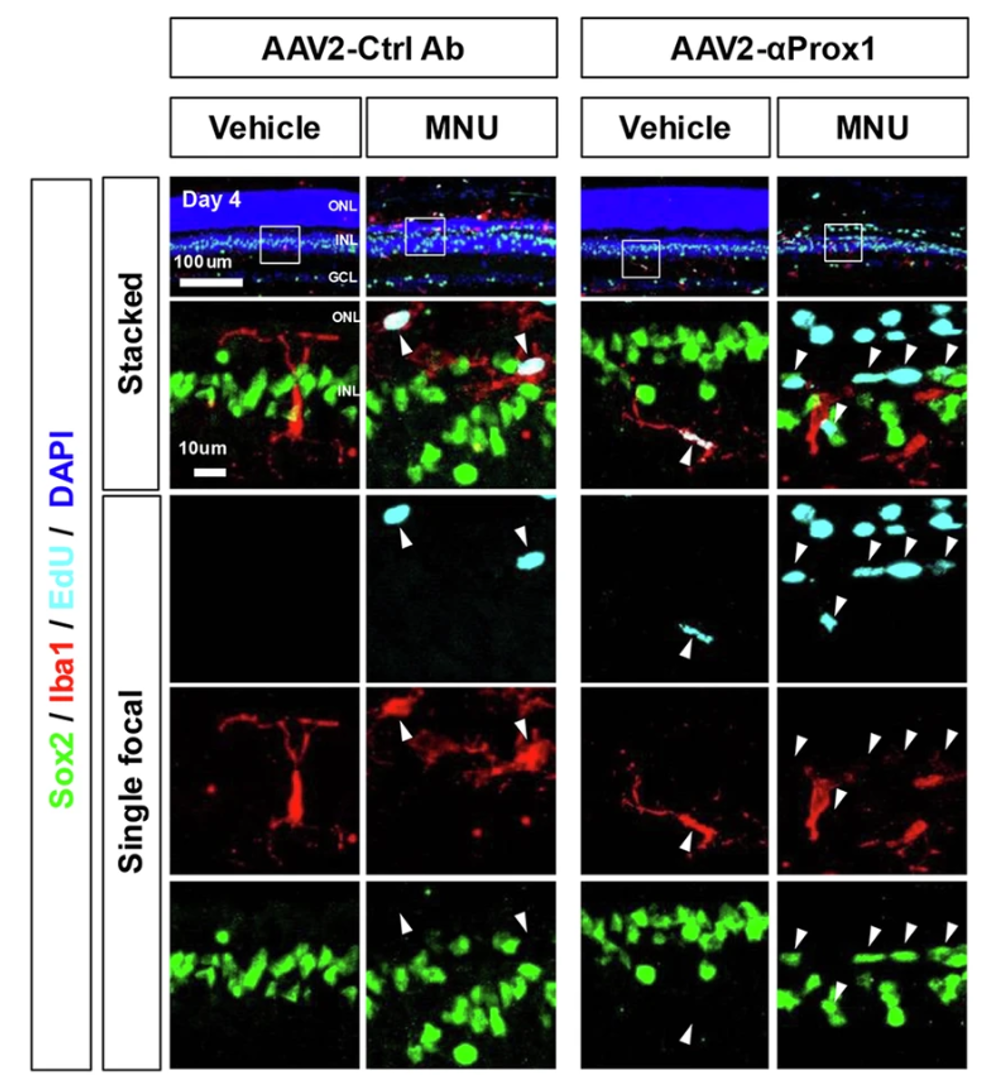
У мышей, которым ввели AAV2-αProx1, накопление Prox1 в КМ подавлялось без изменения уровня Prox1 в нейронах сетчатки. При введении контрольного антитела AAV2-Ctrl Ab такого эффекта не наблюдалось (рис. 5А, Б). Кроме того, количество пролиферирующих КМ в поврежденной сетчатке мышей, которым ввели AAV2-αProx1, значительно увеличилось (рис. 5В).
Полученные результаты свидетельствуют о том, что КМ приобретают пролиферативный потенциал при снижении уровня Prox1, перенесенного из нейронов сетчатки.
Несмотря на это, у травмированных мышей, получавших AAV2-αProx1, количество клеток, помеченных EdU, было существенно ниже, чем у рыбок данио — в среднем 3 клетки на область у мышей по сравнению с 28 клетками на область у рыбок. Поэтому одного лишь блокирования Prox1 может быть недостаточно для полного восстановления регенеративной способности сетчатки млекопитающих до уровня сетчатки рыб, так что данный вопрос требует дальнейших исследований.
Для другого эксперимента отобрали мышей, которые имеют мутации в гене пигментного ретинита и начинают терять зрение с двухмесячного возраста. Им вводили AAV2-αProx1 либо AAV2-Ctrl Ab в возрасте двух месяцев и исследовали сетчатку в возрасте шести месяцев (рис. 6).
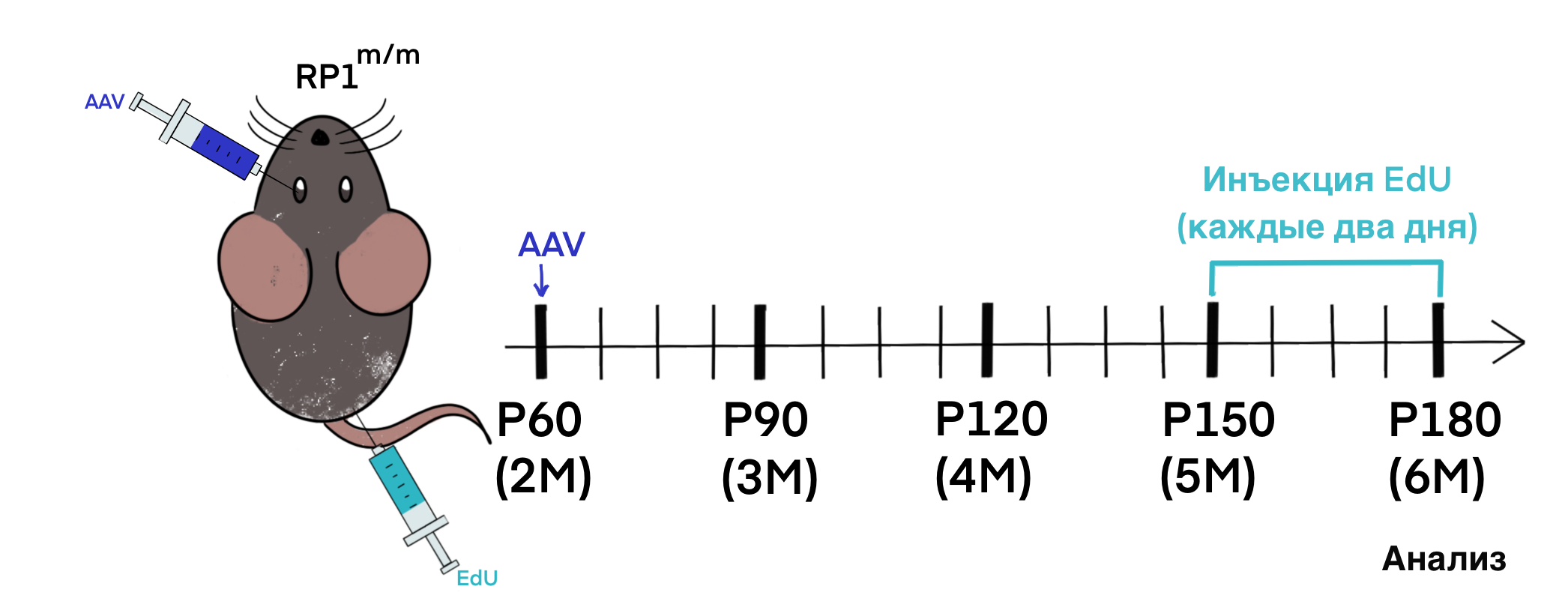
Рисунок 6. Схема введения конструкций на основе AAV, а также EdU по дням. Под шкалой обозначен возраст мышей (Р — дни, М — месяцы).
иллюстрация Софии Ващенко, адаптировано из [10]
У группы, получавшей антитела к Prox1, острота зрения восстановилась, в отличие от мышей, получавших контрольные антитела. Однако улучшение зрения не сохранялось в течение более чем 6 месяцев после лечения. Ограниченная продолжительность эффекта, вероятно, обусловлена особенностями AAV2-αProx1, что приводит к потере экспрессии αProx1. Поэтому для повышения долгосрочной эффективности такого лечения необходимо изменить дизайн конструкции.
Помимо иммуногистохимического исследования срезов сетчатки, эффективность использования антител оценивали с помощью регистрации электроретинограммы (ЭРГ) и определения остроты зрения мышей с помощью системы OptoMotry (Cerebral Mechanics). Для этого мышей адаптировали к окружающему освещению в течение 30 минут, а затем помещали на платформу, расположенную на высоте 60 см от пола, в окружении экранов, на которых отображались черно-белые вертикальные полосы (рис. 7). Если мышь переставала двигаться и начинала следить за движением полос, поворачивая голову, это считалось успешным визуальным обнаружением. Пороги обнаружения определяли с помощью программного обеспечения OptoMotry [14], [15].

Рисунок 7. Система OptoMotry (Cerebral Mechanics). Top mirror — верхнее зеркало; Bottom mirror — нижнее зеркало; Platform (Mouse Holder Platform) — платформа, на которой располагается мышь; Camera — камера, фиксирующая положение мыши; Screen — экран; Detection Computer — компьютер с программным обеспечением, детектирующим положение мыши.
Результаты обоих методов исследования подтвердили эффективность AAV2-αProx1. Таким образом, аденоассоциированная вирусная доставка антител против Prox1, которые блокируют межклеточный перенос белка Prox1 из нейронов сетчатки и тем самым препятствует его накоплению в КМ, может стать эффективной терапевтической стратегией при дегенеративных заболеваниях сетчатки, поскольку способствует ее регенерации и восстановлению зрения.
Перспективы инновационного метода терапии
Будущие исследования компании Celliaz Inc. будут направлены на изучение дополнительных факторов, которые потенциально могут повысить эффективность данного терапевтического подхода, увеличить долгосрочность действия антител, а также обеспечить устойчивую пролиферации КМ, так как в рамках исследования уровня пролиферации КМ сетчатки рыбок данио-рерио одним лишь блокированием переноса Prox1 достигнуть не удалось.
В случае успешного завершения доклинических испытаний препарата, который на данном этапе получил название CLZ001, компания планирует начать клинические исследования к 2028 году.
И, хотя на данный момент препарат испытан только на животных, в обозримом будущем он может применяться при различных дегенеративных заболеваниях сетчатки, для которых отсутствуют эффективные методы лечения, и приблизить человечество к победе над слепотой. Будущее — это не то, куда мы идем, а то, что мы создаем.
Литература
- Michael Hoffmann. (2016). Vision: Elementary and Complex Visual Processing. Cognitive, Conative and Behavioral Neurology. 51-82;
- Stein Emil Vollset, Hazim S Ababneh, Yohannes Habtegiorgis Abate, Cristiana Abbafati, Rouzbeh Abbasgholizadeh, et. al.. (2024). Burden of disease scenarios for 204 countries and territories, 2022–2050: a forecasting analysis for the Global Burden of Disease Study 2021. The Lancet. 403, 2204-2256;
- Вижу цель: новые технологии для незрячих;
- Свет в конце туннеля: генная терапия болезней зрения;
- М. В. Тихонович, С. А. Гаврилова, И. Э. Иошин. (2020). Клетки Мюллера: Genii loci. Физиол. человека. 46, 129-136;
- Нобелевская премия по физиологии и медицине (2012): индуцированные стволовые клетки;
- Nikolas L. Jorstad, Matthew S. Wilken, William N. Grimes, Stefanie G. Wohl, Leah S. VandenBosch, et. al.. (2017). Stimulation of functional neuronal regeneration from Müller glia in adult mice. Nature. 548, 103-107;
- Kai Yao, Suo Qiu, Yanbin V. Wang, Silvia J. H. Park, Ethan J. Mohns, et. al.. (2018). Restoration of vision after de novo genesis of rod photoreceptors in mammalian retinas. Nature. 560, 484-488;
- Shweta Singhal, Bhairavi Bhatia, Hari Jayaram, Silke Becker, Megan F. Jones, et. al.. (2012). Human Müller Glia with Stem Cell Characteristics Differentiate into Retinal Ganglion Cell (RGC) Precursors In Vitro and Partially Restore RGC Function In Vivo Following Transplantation. Stem Cells Translational Medicine. 1, 188-199;
- Eun Jung Lee, Museong Kim, Sooyeon Park, Ji Hyeon Shim, Hyun-Ju Cho, et. al.. (2025). Restoration of retinal regenerative potential of Müller glia by disrupting intercellular Prox1 transfer. Nat Commun. 16;
- Модельные организмы: данио рерио;
- Время первых: как аденоассоциированные вирусы стали лучшими в доставке генов in vivo;
- Терапевтические моноклональные антитела;
- Friedrich Kretschmer, Szilard Sajgo, Viola Kretschmer, Tudor C. Badea. (2015). A system to measure the Optokinetic and Optomotor response in mice. Journal of Neuroscience Methods. 256, 91-105;
- Cong Shi, Xuedong Yuan, Karen Chang, Kin-Sang Cho, Xinmin Simon Xie, et. al.. (2018). Optimization of Optomotor Response-based Visual Function Assessment in Mice. Sci Rep. 8.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚