
Роль слабых взаимодействий в биополимерах
20 марта 2015
Роль слабых взаимодействий в биополимерах
- 12493
- 0
- 10
Слабый пол, слабые связи... А слабые ли? Природа имеет на сей счет собственное мнение.
Рисунок в полном размере.
фотография с сайта photochronograph.ru
-
Автор
-
Редакторы
Давайте поговорим о роли слабых взаимодействий в биологических макромолекулах. Хотя они и слабые, их влияние на живые организмы отнюдь не ничтожно. Скромный набор видов слабых связей в биополимерах обусловливает всё многообразие биологических процессов, на первый взгляд никак не связанных между собой: передачу наследственной информации, ферментативный катализ, обеспечение целостности организма, работу природных молекулярных машин. А определение «слабые» не должно вводить в заблуждение — роль этих взаимодействий колоссальна.
Эта работа публикуется в рамках конкурса научно-популярных статей, проведенного на конференции «Биология — наука 21 века» в 2015 году.
Почему статья названа именно так? Потому что до сравнительно недавнего времени слабым взаимодействиям в химии (в биохимии, в частности, тоже) уделялось явно недостаточное внимание. Исследователи рассуждали приблизительно так: «Ковалентная связь прочная, поэтому свойства любого вещества определяются в первую очередь характером ковалентных взаимодействий между атомами. А слабые взаимодействия — водородные, ионные, электростатические связи — на то и слабые, что их роль в формировании свойств вещества второстепенная». Только с развитием таких неклассических направлений в химии, как супрамолекулярная [1] и координационная химия, к слабым взаимодействиям появился должный интерес. Более того, выяснилось, что в функционировании живой клетки слабые взаимодействия между атомами и молекулами зачастую играют главную роль.
Дело в том, что наряду с видимым недостатком, вытекающим из самогό определения «слабый» (водородная связь, к примеру, в 15–20 раз менее прочна, чем «сильная» ковалентная), у интересующих нас взаимодействий есть и преимущество — они значительно легче возникают и рвутся. Для образования или разрыва ковалентных связей требуется химическая реакция с затратой энергии, длящаяся внушительный промежуток времени, нуждающаяся в катализе, и так далее. А для формирования слабых взаимодействий достаточно изменения конформации молекулы . И если упомянутую живую клетку рассматривать как сложную молекулярную машину, то именно слабые взаимодействия оказываются в ней рычагом самого тонкого управления, чутко и, главное, быстро реагирующим на любые изменения внешней среды.
Невнимание к таким взаимодействиям дорого обходится биологам, фармацевтам и даже больным — часто именно в области конформационной динамики биомолекул кроется разгадка селективности лекарств и коварных эволюционных планов по развитию резистентности: «Изучение эволюции белков уточнило механизм действия противоопухолевого лекарства иматиниб» [2]. — Ред.
Связанные одной цепью
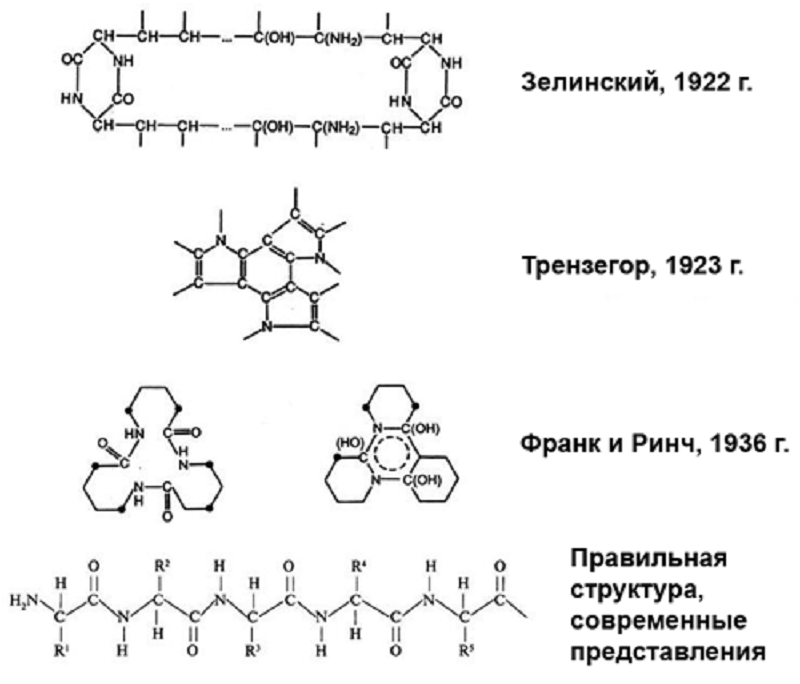
Рисунок 1. Предположения о структуре белка в двадцатые-тридцатые годы ХХ века.
Однако еще несколько десятилетий назад об этой роли слабых взаимодействий в живых системах никто не догадывался. К примеру, на исходе XIX века Эмиль Фишер доказал, что белок является линейным полиамидом, состоящим из остатков α-аминокислот. В наши дни это представление стало аксиомой. Теперь уже мало кто помнит о том, что в первой четверти ХХ века самые маститые ученые усомнились в правоте Фишера и высказали ряд своих предположений о структуре белка — достаточно оригинальных, хотя в настоящее время представляющих чисто исторический интерес (рис. 1). Ход их рассуждений был приблизительно таков. Если белок, по Фишеру, является линейным полимером, то он должен представлять собой нитевидную молекулу, сворачивающуюся в беспорядочный клубок. Каким образом такая молекула выполняет биологические функции? Следует добавить, что в то время уже возникли представления о глобулярных белках. Компактная глобулярная форма белковой молекулы на первый взгляд расходилась с представлениями немецкого химика.
В свете представлений 20–30-х годов прошлого века белковая глобула представляет собой сшитый полимер, состоящий из устойчивых шестичленных циклов, соединенных, разумеется, прочными ковалентными связями. По представлениям русского химика (и создателя угольного противогаза) Н.Д. Зелинского, например, белок состоит из дикетопиперазиновых циклов, представляющих собой внутренние амиды аминокислот. Ряд других химиков представлял белковую глобулу как конденсированную полиароматическую систему, включающую в себя азотистые гетероциклы, а наличие аминокислот в белковых гидролизатах, по их мнению, артефакт, возникающий в результате раскрытия гетероциклов при гидролизе.
Только начиная с сороковых годов ХХ века усилиями таких выдающихся ученых, как Лайнус Полинг, Розалинд Франклин, Джеймс Уотсон, Фрэнсис Крик и Морис Уилкинс, была показана возможность формирования устойчивых структур биополимеров за счет слабых взаимодействий. Дж. Уотсону, Ф. Крику и М. Уилкинсу в 1962 году была присуждена Нобелевская премия по физиологии и медицине за «открытия в области молекулярной структуры нуклеиновых кислот и их значимости для передачи генетической информации». Р. Франклин, к сожалению, до заслуженной премии не дожила (зато Л. Поллинг становился нобелиатом дважды). В те годы стало ясно, что будь белковая глобула сшитым полициклом, она бы, конечно, отличалась высокой устойчивостью, но биологические функции выполнять не смогла, поскольку не была бы способна реагировать на внешние воздействия. Это была бы «мертвая» молекула.
В этом месте следует обратить внимание на любопытный факт. Несмотря на то, что теория Зелинского не подтвердилась, она послужила толчком для формирования химии дикетопиперазинов — направления, приведшего к созданию ряда лекарственных препаратов. Вторичные метаболиты дикетопиперазиновой природы, в том числе и с лекарственной активностью, обнаружены и в живой природе, пусть не в составе белков. Так изначально неверная гипотеза принесла полезный практический результат — явление, встречающееся в науке нередко.
Bond. Hydrogen Bond
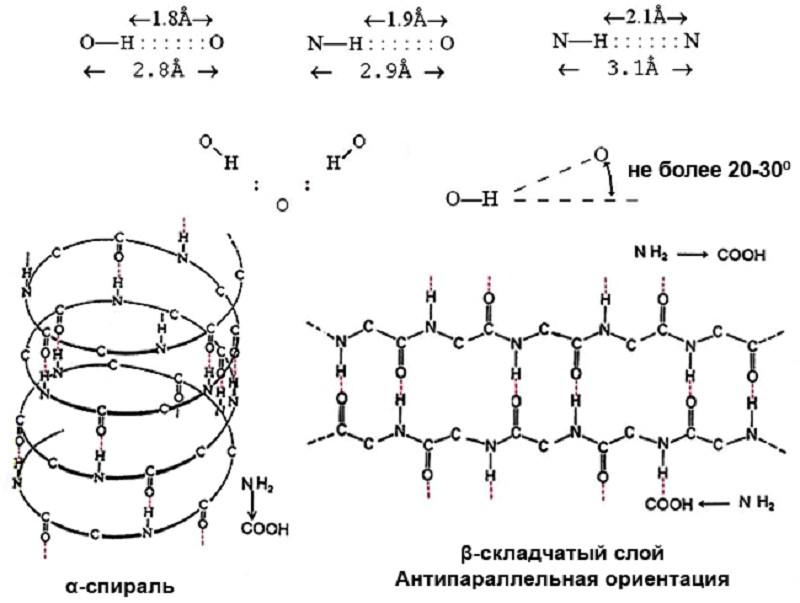
Рисунок 2. Водородные связи в белках.
Одним из самых распространенных видов слабых взаимодействий являются водородные связи, возникающие при наличии в молекулах полярных групп — гидроксилов, аминогрупп, карбонилов и т.д. В макромолекулах биополимеров, как правило, полярные группы широко представлены (за исключением разве что натурального каучука). Особенностью водородной связи является то, что ее прочность зависит не только от расстояния между группами, но и от их пространственного расположения (рис. 2). Самая прочная связь образуется, когда все три задействованных в ее образовании атома располагаются на одной прямой длиной около 3 Å. Отклонение на 20–30° считается критическим: дальнейшее увеличение угла ведет к катастрофическому снижению прочности вплоть до полного исчезновения связи. А это энергетически невыгодно. Поэтому водородные связи служат стабилизаторами структур биополимеров, придают им жесткость. Например, открытая Л. Полингом α-спираль — один из типов вторичной структуры белка — стабилизируется водородными связями, образующимися между атомами водорода при азоте и карбонильными группами пептидных связей на соседних витках спирали [3], [4]. В 1954 году «за изучение природы химической связи и его применение к объяснению строения сложных молекул» Полинг получил свою первую Нобелевскую премию — по химии. Второй (тоже «единоличной») — премии мира — он удостоился в 1962 г., но совсем за другую деятельность.
Слава двойной спирали
Изображенная на рисунке 3 изящная двойная спираль ДНК узнаваема сразу. Сейчас, пожалуй, ни одна голливудская постановка не обходится без изображения этой молекулы, которому малограмотные в естественных науках продюсеры фильмов придают поистине мистический смысл. На самом деле нативная ДНК состоит из двух зеркально отражающих друг друга (комплементарных) макромолекул, соединенных водородными связями наподобие застёжки «молния». Нуклеотиды, из которых состоят макромолекулы, содержат четыре азотистых основания, два из которых являются производными пурина (аденин и гуанин), а два других — производными пиримидина (тимин и цитозин). Отличительной особенностью этих веществ является способность избирательно формировать водородные связи друг с другом. Аденин легко образует двойную водородную связь с тимином или урацилом, однако комплекс с цитозином оказывается значительно менее прочным. Гуанин, напротив, склонен создавать тройную связь с цитозином. Другими словами, основания «узнают» друг друга. Причем сродство это столь велико, что комплексы аденин–тимин (А–Т) и гуанин–цитозин (Г–Ц) кристаллизуются как самостоятельные вещества.
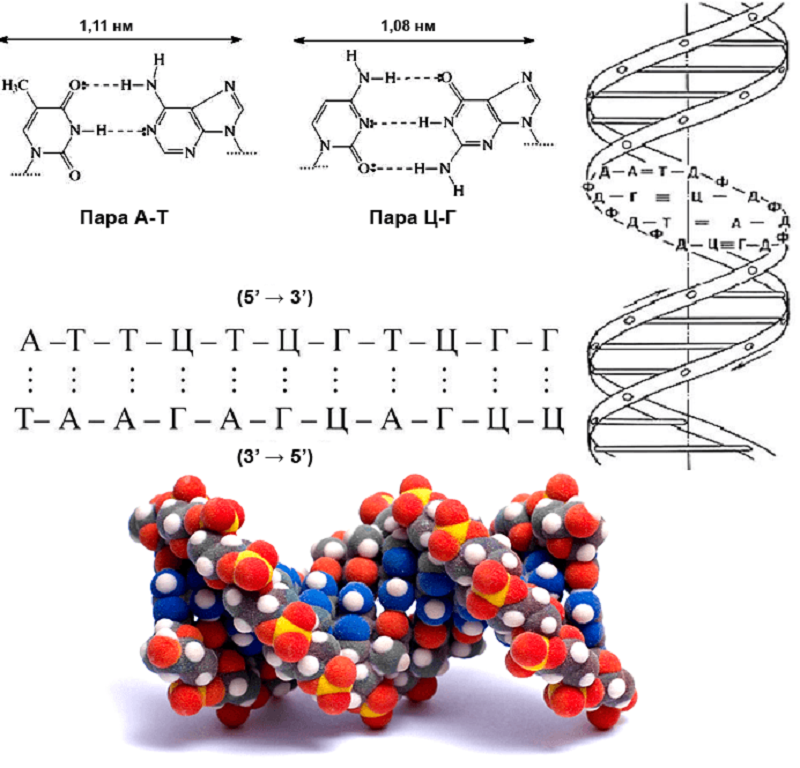
Рисунок 3. Вверху: Стабилизирующие структуру ДНК водородные связи между азотистыми основаниями. Внизу: модель одного витка ДНК в B-форме, созданная на основе данных рентгеноструктурного анализа. Цвет атомов: кислород — красный, углерод — серый, водород — белый, азот — синий, фосфор — желтый.
рисунок с сайта www.visual-science.com
Разумеется, так же они ведут себя и в составе полинуклеотидов. Водородные связи между А–Т и Г–Ц-парами сшивают между собой две нити ДНК, формируя знаменитую двойную спираль. Это же сродство оснований позволяет строить комплементарную полинуклеотидную цепочку на матрице существующей. Нуклеиновые кислоты — единственные известные науке молекулы, способные размножаться (реплицироваться). Это свойство позволило им стать носителями наследственной информации [5].
Очевидно, что тройная водородная связь в паре Г–Ц прочнее, чем двойная в А–Т. Судя по всему, это, как и физико-химическое сродство между первичными аминокислотами и определенными нуклеотидами, сыграло немалую роль в становлении генетического кода [6]. ДНК, богатые Г–Ц-парами, подвергаются тепловой денатурации (говоря профессиональным языком молекулярных биологов — «плавятся», хотя к процессу плавления в строгом смысле слова денатурация ДНК не относится) при более высокой температуре. Например, ДНК термофильных бактерий денатурирует при температуре, приближающейся к 100 °С, а искусственная ДНК, состоящая из одних А–Т-пар — всего при 65 °С. «Плавление» ДНК косвенно проявляется через гиперхромный эффект — усиление поглощения ультрафиолетового света с длиной волны 280 нм азотистыми основаниями, которые в нативной молекуле ДНК упакованы внутрь спирали и поглощают слабо.
Выходит, что фундамент жизни — наследственность — сводится к формированию водородных связей. А ведь наследственность — только один из множества примеров. Вся молекулярная биология держится на межмолекулярном распознавании, а оно, в свою очередь, — на слабых взаимодействиях. Это все генетические ферменты, рибосома, тРНК, РНК-интерференция и т.д. Это иммунитет. Это многочисленные варианты взаимодействия рецептор—лиганд. В конечном итоге — сама жизнь!
Разумеется, создав совершенный механизм передачи наследственной информации, природа позаботилась и о способе его поломки. Миметики пиримидиновых оснований 5-галогенурацилы (5-фторурацил, 5-бромурацил и др.) относятся к классу супермутагенов — в их присутствии частота генных мутаций возрастает на несколько порядков. Вероятно, данное свойство 5-галогенурацилов связано с существованием их в двух таутомерных формах: в нормальной кетоформе они образуют двойную водородную связь с аденином, «выдавая» себя за тимин, а в редкой енольной форме становятся аналогами цитозина и образуют тройную связь с гуанином (рис. 4). Такое «двуличие» 5-галогенурацилов ведет к нарушению строгости репликации и возможному закреплению мутации, если им удается встроиться в нуклеотид [7].

Рисунок 4. Механизм мутагенного воздействия 5-галогенурацилов (на примере 5-бромурацила).
Сила имени Ван-дер-Ваальса
Водородные связи, конечно же, не единственный вид слабых взаимодействий. Ван-дер-Ваальсовы взаимодействия играют в живой природе не меньшую роль.
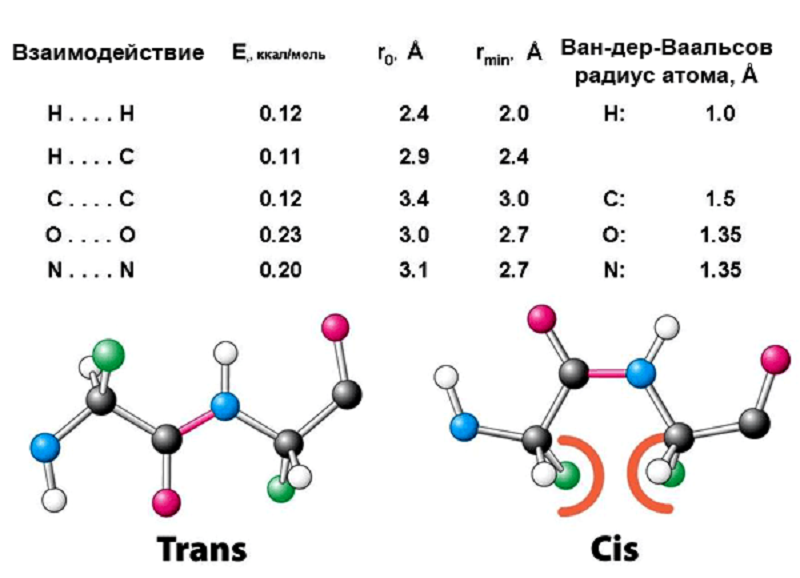
Рисунок 5. Характерные параметры потенциалов Ван-дер-Ваальсовых взаимодействий.
Например, пептидная связь в белке (связь между α-карбоксильной группой одной аминокислоты и α-аминогруппой другой аминокислоты, определяющая формирование первичной структуры белка) из-за амидного сопряжения принимает sp2-гибридизацию и становится очень сходной с классической двойной связью в алкенах (рис. 5). Как и все sp2-структуры, пептидная связь плоская, и свободное вращение боковых радикалов вокруг нее невозможно. Это предопределяет наличие цис–транс изомерии [8]. Как и в случае алкенов, транс-изомеры полипептидов значительно более устойчивы. Дело в том, что в цис-положении боковые радикалы сближаются на критическое расстояние 2,8 Å, в котором наблюдается Ван-дер-Ваальсово отталкивание их электронных оболочек (рис. 5), разумеется, энергетически невыгодное для молекулы.
Однако среди 20 стандартных протеиногенных аминокислот есть одна выделяющаяся из общего ряда — пролин. Строго говоря, пролин даже не является аминокислотой, поскольку у него нет свободной аминогруппы — это иминокислота, аммонийный азот которой входит в пирролидиновое кольцо. Так вот, благодаря такому массивному заместителю цис-пептидная связь, образуемая азотом пролина, оказывается более устойчивой, чем в случае других аминокислот. Примерно 10% остатков пролина в белке имеют цис-конформацию. В местах их расположения наблюдаются изломы полипептидной цепи, служащие границами доменов. Таким образом эта иминокислота вносит дополнительные «краски» в спектр возможных конформаций белковых молекул, выполняющих бесчисленное множество жизненно важных функций [9].
Головоломка-«змейка», или Сказ о торсионных углах
Молекулы биополимеров зачастую имеют очень высокую молекулярную массу — до сотен тысяч и даже миллионов дальтон. Столь массивные молекулы содержат бесчисленное множество атомных групп и теоретически способны принимать астрономическое количество конформаций. На практике же любой биополимер в стандартных условиях стремится принять нативную конформацию, в которой он существует в живом организме. Сходу данный парадокс нелегко объяснить. В самом деле, что мешает гибкой молекуле при непрерывном тепловом движении менять свою геометрию бесконечно?
Ответ кроется в том, что изменение конформации молекулы полипептида всегда начинается с изменения углов между атомными группами основной цепи полипептида (на жаргоне называемой «бэкбоном»), так называемых торсионных углов, обозначаемых греческими буквами Φ (для связей углерод–азот) и Ψ (для связей углерод–углерод). Оказалось, что далеко не все теоретически предсказанные значения торсионных углов способны реализоваться в действительности.
Известные индийские ученые Рамачандран и Сасисекхаран исследовали конформации белковых цепей, и плодом их усилий стала карта конформаций, носящая их имя (рис. 6). Белое поле на карте — запрещенные значения углов, обведенное оранжевым и заштрихованное — разрешенные, но невыгодные, а обведенное красным и плотно заштрихованное — нативная конформация белка. Видно, что почти вся карта окрашена в белый цвет. Таким образом, нативная конформация белка в условиях живого организма — наиболее энергетически выгодная, и белок самопроизвольно принимает именно ее. Если бы биополимеры обладали большей конформационной свободой, четко отлаженная работа живой молекулярной машины стала бы невозможной [10].
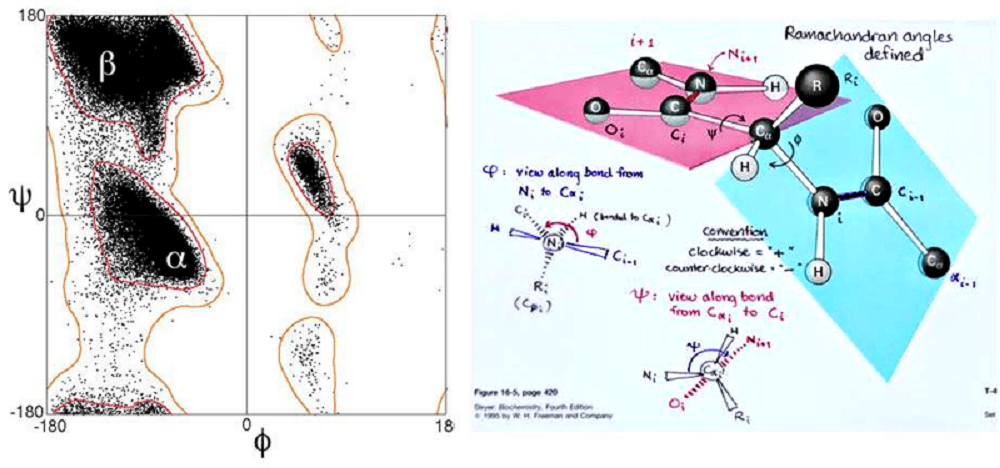
Рисунок 6. Зависимость пространственной структуры полипептидов от торсионных углов. Слева: карта Рамачандрана-Сасисекхарана для запрещенных (белое поле) и разрешенных (заштрихованные поля) конформаций крупных аминокислотных остатков при вращении по торсионным углам Φ и Ψ в белковой цепи. (Именно эти углы определяют всё конформационное разнообразие линейных полипептидных цепочек.) По осям абсцисс и ординат откладываются значения углов Φ и Ψ от –180° до +180°. В обведенной красным области разрешены все конформации боковой группы по углу χ1 для α-спиралей и β-складок; в обведенной оранжевым области часть углов χ1 запрещена. (Углы χ определяют разрешенные положения для боковых заместителей аминокислотных остатков в белке, не влияя на пространственный тип укладки в целом.) Справа: Обозначения торсионных углов Φ и Ψ в полипептидной молекуле. Именно они позволяют белковым цепям принимать, как головоломке-«змейке», огромное разнообразие наблюдаемых типов укладки белковых молекул.
Современная компьютерная биофизика стремится построить реалистичную модель биополимеров, чтобы только на основании последовательности молекулы (ее первичной структуры) можно было бы предсказать пространственное строение, поскольку в природе мы наблюдаем, что именно так и происходит: процесс самопроизвольного сворачивания белка в «нативную» конформацию называют фолдингом (от англ. to fold — сворачивать, складывать). Однако понимание физики этого процесса еще далеко от идеального, и современные вычислительные алгоритмы, хотя и дают обнадеживающие результаты, пока далеки от окончательной победы в состязании [11], [12].
Боязнь воды, и причем тут структура биомолекул
Гидрофобные взаимодействия не являются самостоятельным видом слабых связей: они являются следствием неспособности ряда молекул образовывать водородные связи и склонности неполярных (гидрофобных) фрагментов слипаться вместе, выталкивая из своей массы полярные (гидрофильные) [13].
Большинство биополимеров в природе находится в водном окружении. А вода, в свою очередь, является сильно ассоциированной жидкостью, «сшитой» трехмерной сетью водородных связей (рис. 7). Этим объясняется аномально высокая температура кипения воды: даже жидкая вода имеет подобие кристаллической решетки. С такой структурой Н2О связана и избирательная растворимость в ней различных веществ. Соединения, способные образовывать водородные связи в силу наличия полярных групп (сахароза, этиловый спирт, аммиак), легко встраиваются в «кристаллическую решетку» воды и прекрасно растворимы. Вещества, лишенные полярных групп (бензол, четыреххлористый углерод, элементная сера), не способны «пробить» сеть водородных связей и смешаться с водой. Соответственно, первую группу веществ именуют «гидрофильными» (водолюбивыми), а вторую — «гидрофобными» (водоотталкивающими).
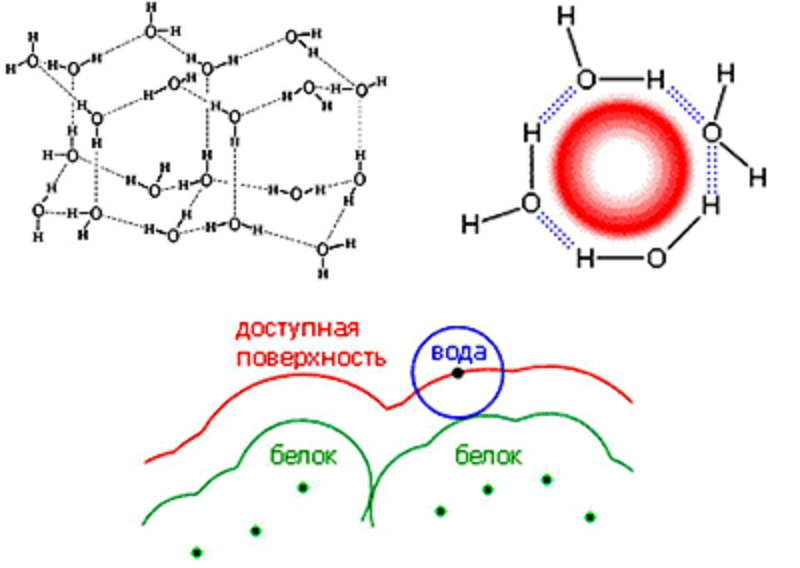
Рисунок 7. Гидрофобные связи в белке. Вверху слева: нормальный лед. Пунктир — Н-связи. В ажурной структуре льда видны небольшие полости, окруженные молекулами Н2О. Вверху справа: схема нерегулярной упаковки связанных водородными связями молекул Н2О вокруг неполярной молекулы. Внизу: доступная для воды поверхность внедренной в воду молекулы белка [14]. Зеленые точки показывают центры граничащих с водой атомов; зеленая линия — их Ван-дер-Ваальсовы оболочки. Молекула воды представлена синим шариком (радиус 1,4 Å). Доступная для воды поверхность (красная линия) создается центром этого шарика, когда он обкатывает погруженную в воду молекулу, касаясь Ван-дер-Ваальсовых поверхностей ее внешних атомов.
Контакт воды с гидрофобной поверхностью энергетически крайне невыгоден. Вода стремится сохранить водородные связи, но на границе раздела фаз правильная трехмерная сеть образоваться не может (рис. 7). В результате здесь меняется структура воды: она становится более упорядоченной, молекулы утрачивают подвижность, т.е. фактически вода замерзает при температуре выше 0 °С! Естественно, вода стремится свести невыгодное взаимодействие к минимуму. Этим объясняется, например, то, почему мелкие капельки масла на поверхности воды стремятся слиться в одну большую каплю: фактически это сама водная среда сталкивает их вместе, стремясь уменьшить площадь поверхности контакта.
Белки и нуклеиновые кислоты содержат как гидрофильные, так и гидрофобные фрагменты. Поэтому молекула белка, оказавшись в водной среде, сворачивается в глобулу таким образом, что гидрофильные остатки аминокислот (глутамин, глутаминовая кислота, аспарагин, аспарагиновая кислота, серин) оказываются на ее поверхности и контактируют с водой, а гидрофобные (фенилаланин, триптофан, валин, лейцин, изолейцин) — внутри глобулы и контактируют друг с другом, т.е. образуют между собой гидрофобные контакты . То есть процесс сворачивания белка в третичную структуру подобен процессу слияния капель масла, а характер третичной структуры каждого белка определяется взаимным расположением аминокислотных остатков. Отсюда правило — все последующие (вторичная, третичная и даже четвертичная) структуры белка определяются его первичной структурой.
Это до конца верно только для небольших и растворимых в воде белков, а белки, встроенные в биомембрану, или большие белковые комплексы могут быть устроены сложнее. Мембранные белки, например, организованы почти с точностью до наоборот, потому что контактируют не с полярным растворителем, а с гидрофобной средой липидного бислоя: «Физическая водобоязнь» [13]. — Ред.
Как уже было сказано, двойная спираль ДНК образуется за счет водородных связей между основаниями. Однако в пределах каждой цепочки соседние азотистые основания уложены в «стопку» гидрофобными контактами (в данном случае называемыми «стэкинг-взаимодействиями»). Гидрофильный сахарофосфатный остов молекулы ДНК, в свою очередь, взаимодействует с водой.
Иными словами, нативная структура большинства биополимеров (за исключением, например, белков, погруженных в липидные мембраны клеток) формируется водным окружением — естественной средой внутри любого живого организма. С этим связана мгновенная денатурация биополимеров при контакте с органическими растворителями.
Благодаря гидрофильной поверхности нативные молекулы биополимеров покрыты объемной гидратной оболочкой («гидратной шубой»). О том, насколько велика и прочно связана эта шуба из молекул воды, свидетельствует тот факт, что все полученные белковые кристаллы примерно на 60% состоят из связанной воды. При этом трудно отказаться от мысли, что гидратная шуба является такой же неотъемлемой частью молекулы белка, как и сама полипептидная цепь, хотя такая идея противоречит устоявшимся представлениям об индивидуальности химических веществ. И всё же очевидно, что гидратная оболочка способна определять свойства биополимера и его функции, а популярные в наши дни представления о структурировании воды наполняются новым (научным) смыслом.
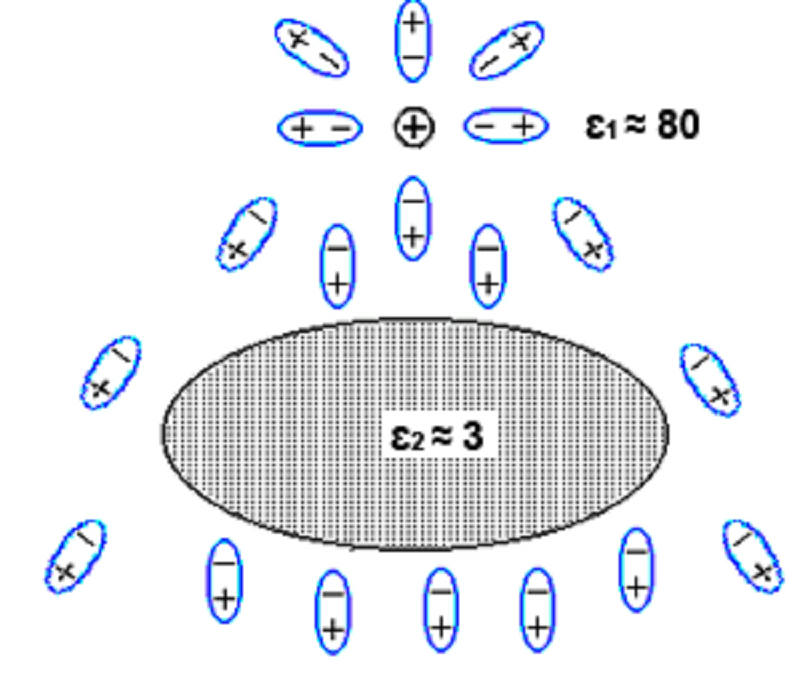
Рисунок 8. Электростатическое взаимодействие между белком и водным окружением. Ориентация молекул воды (изображены в виде диполей) вокруг белка и заряда (изображен положительным просто для определенности).
Заряд бодрости
Конечно, поверхности молекул биополимеров свойственна не только гидрофильность. Их поверхность, как правило, несет еще и электрический заряд. Белки содержат заряженные карбоксильные и аминогруппы, нуклеиновые кислоты — фосфатные группы, полисахариды — карбоксильные, сульфатные и боратные. Поэтому еще одним видом слабых взаимодействий, присущих биополимерам, являются ионные связи — как внутренние, между радикалами самой молекулы, так и внешние — с ионами металлов или с соседними макромолекулами (рис. 8).
Грамотная координация
Разумеется, нельзя не упомянуть еще один важный вид слабых взаимодействий — координационную связь. На рисунке 9 показан искусственный комплекс трехвалентного кобальта с синтетическим лигандом — этилендиаминтетрауксусной кислотой (ЭДТК, EDTA). Природные комплексы биополимеров, разумеется, имеют более сложную структуру, но в целом очень сходны с представленным. Комплексы с поливалентными металлами характерны для белков и полисахаридов. Металлопротеины представляют собой обширнейший класс биополимеров. К ним относятся белки-переносчики кислорода, многие ферменты, мембранные белки — звенья электронтранспортных цепей. Металлопротеины обладают ярко выраженной каталитической активностью. И хотя непосредственным катализатором является ион переходного металла, полипептидные цепи служат мощнейшим усилителем катализа, а кроме того, они способны направлять активность металла, подавлять его побочные каталитические свойства, тем самым на порядки повышая эффективность катализа. Таким способом достигается совершенство метаболических процессов и возможность необычайно тонкой их регуляции.
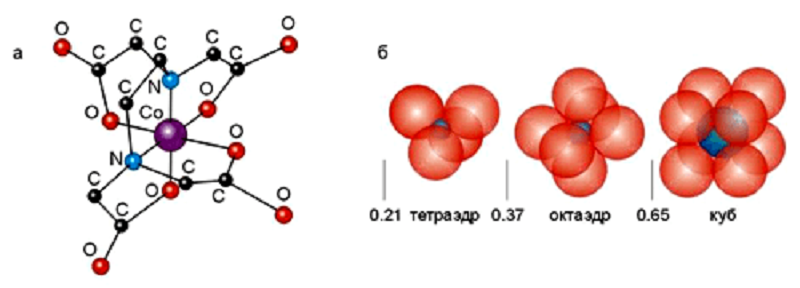
Рисунок 9. Координационные связи. а — Структура октаэдрического комплекса, образованного атомом Со3+ с ЭДTК. б — Характерная координация центрального иона при различном соотношении его радиуса с радиусами окружающих его доноров электронов.
Вторичные структуры
Для белков характерны два вида вторичных структур. Об α-спирали выше говорилось не раз. Здесь можно добавить только, что возможны α-спирали двух видов — правозакрученные (обозначаются буквой R) и левозакрученные (обозначаются буквой L). В природе известны только правозакрученные спирали — они значительно более стабильны (рис. 10). Разумеется, образование α-спирали возможно только из одного оптического изомера аминокислот.
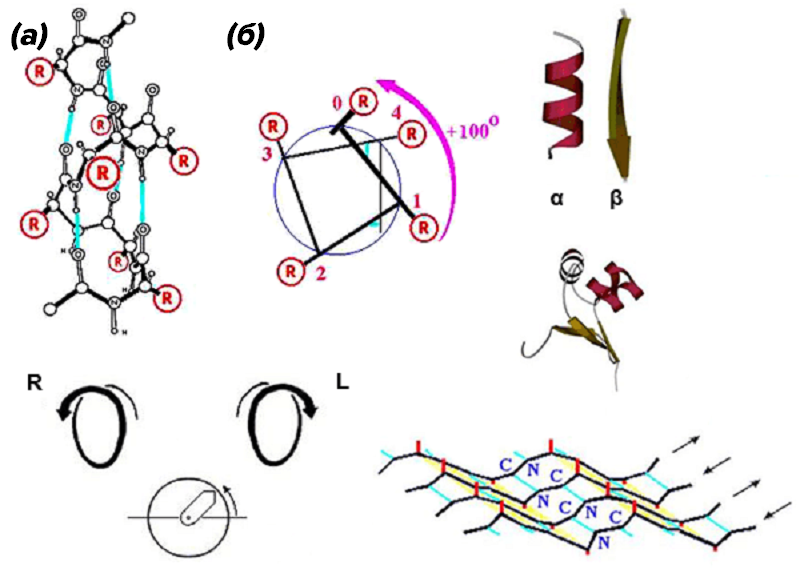
Рисунок 10. Вторичные структуры белка. Вверху слева: правая α-спираль. а — Атомарная структура. R — боковые группы. Голубые линии — водородные связи. б — Схематическое изображение одного витка той же α-спирали (вид с торца). Стрелка показывает поворот спирали (в расчете на один остаток) по мере ее приближения к нам (номера остатков при этом убывают). Вверху справа: вторичная структура полипептидной цепи (α-спираль и тяж β-листа) и третичная структура — полипептидная цепь, уложенная в глобулу. Внизу слева: правые (R) и левые (L) спирали. Под ними показан отсчет положительного угла в тригонометрии, при этом «близкая к нам» стрелка вращается против хода часов (соответствует R-спирали). Внизу справа: лист β-структуры имеет складчатую поверхность. Боковые группы (маленькие отростки) расположены на складках и обращены в ту же сторону, что и складка, т.е. направленные вниз и вверх боковые группы чередуются вдоль β-тяжа.
Другая распространенная структура белка — складчатый β-лист. Если в α-спирали водородные связи образуются между витками, то в β-листе — между соседними тяжами, формирующими крупную складчатую двумерную структуру («лист»). Такая структура характерна для ряда фибриллярных белков, например, фиброина натурального шелка. Несмотря на то, что отдельно взятая водородная связь не отличается прочностью, благодаря огромному количеству и правильному чередованию таких связей достигается очень крепкое сшивание цепей. Это в свою очередь делает шелковую нить феноменально прочной на разрыв — более прочной, чем стальная проволока такого же диаметра.
Весь спектр конформаций
О роли слабых взаимодействий в биополимерах свидетельствуют спектроскопические методы исследования. На рисунке 11 представлены фрагменты спектров ИК (инфракрасных) и КД (кругового дихроизма) синтетического полипептида полилизина, находящегося в трех конформациях — α-спирали, β-листа и неупорядоченного клубка. Поразительно, но спектры совершенно не совпадают, как будто бы сняты с трех различных веществ. То есть в данном случае слабые взаимодействия определяют свойства молекулы не в меньшей степени, чем ковалентные связи.
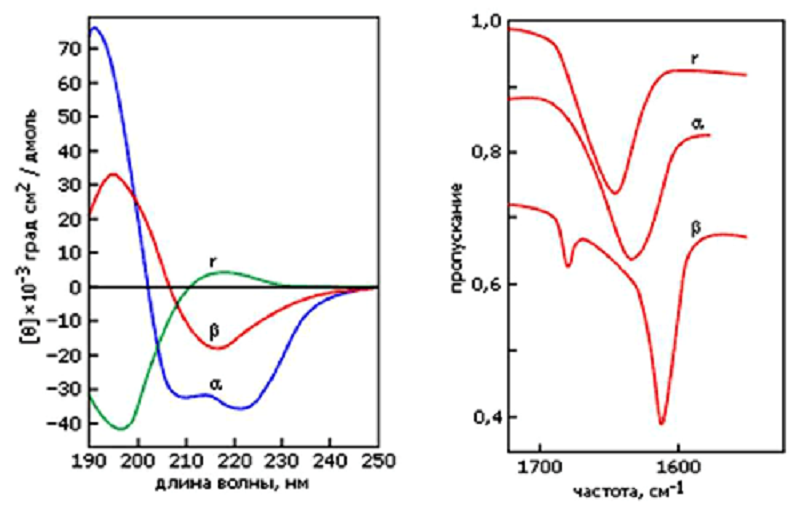
Рисунок 11. Сравнение спектров поглощения трех конформаций полилизина. Слева: характерные формы спектров КД (в «дальнем» УФ) для полилизина в конформации α-спирали, β-структуры и неупорядоченного клубка (r). Справа: характерные формы ИК-спектров пропускания, измеренных в тяжелой воде (D2O) для полилизина в тех же конформациях. Измерения в данном случае проводились в области «амид I», отражающей колебания С=О связи.
Двадцать в степени N
Число конформаций белковых цепей многократно возрастает из-за обилия аминокислот, входящих в их состав. Протеиногенных аминокислот двадцать, и отличает их многообразие боковых радикалов. У глицина, например, боковой радикал сводится к единственному атому водорода, тогда как у триптофана он представляет собой массивный и сложный по структуре остаток скатола. Радикалы бывают гидрофобные и гидрофильные, кислые и основные, ароматические, гетероциклические и содержащие серу.
Разумеется, свойства боковых радикалов аминокислотных остатков отражаются на конформационных свойствах полипептидной цепи. Они, в частности, влияют на величины торсионных углов и вносят поправки в карты Рамачандрана. Еще от них зависит заряд белковой молекулы, ее изоэлектрическая точка — один из важнейших показателей свойств белка (рис. 12). Например, остаток аспарагиновой кислоты утрачивает отрицательный заряд только в сильнокислой среде, при рН 3. Остаток основной аминокислоты аргинина, напротив, теряет положительный заряд при рН 13 — в сильнощелочной среде. В щелочной среде, при рН 11, заряжается фенольный гидроксил тирозина, а при рН 10 то же самое происходит с сульфгидрильной группой цистеина. Большой интерес вызывает гистидин, радикал которого включает в себя имидазольный цикл: последний приобретает положительный заряд при рН 6, т.е. в физиологических условиях. Иными словами, взаимные превращения заряженной и незаряженной форм остатков гистидина происходят в организме постоянно. Эта легкость перехода определяет каталитическую активность остатков гистидина: данная аминокислота, в частности, входит в состав активных центров ряда ферментов, таких как нуклеазы.
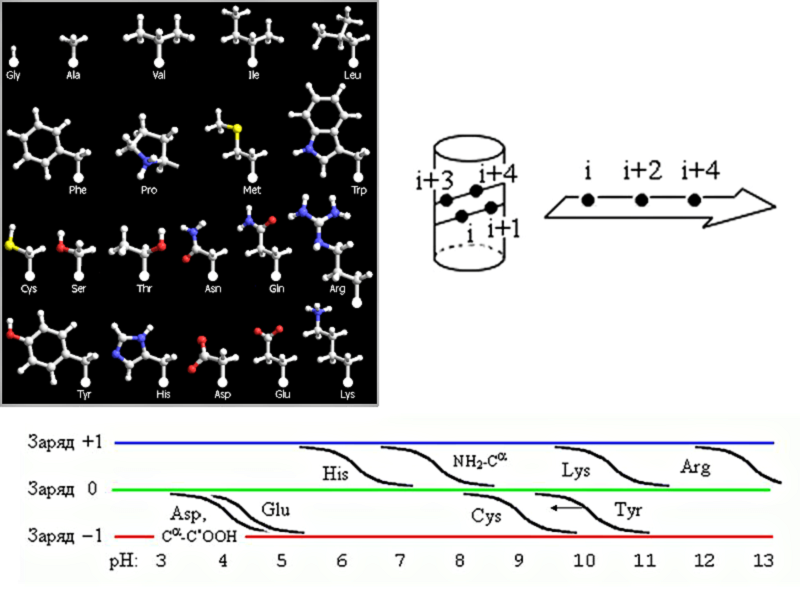
Рисунок 12. Многообразие структур и свойств боковых радикалов аминокислот в составе белков. Вверху слева: боковые цепи двадцати стандартных аминокислотных остатков. Вверху справа: боковые группы, которые (если все они неполярные) могут формировать единые гидрофобные поверхности на α-спиралях и на β-структурных участках. Аналогичные сочетания полярных групп в цепи приводят к образованию гидрофильных областей на противоположных поверхностях α-спиралей и β-тяжей. Внизу: заряженность ионизуемых боковых групп, а также N-конца пептидной цепи (NH2—Cα) и ее С-конца (Cα—C’OOH) при разных рН.
Двойная Тройная спираль
Как уже сказано выше, двойную спираль ДНК никому представлять не нужно. Тройная спираль коллагена значительно менее узнаваема, причем незаслуженно, ведь коллаген — главный белок организма хордовых животных (и человека), из него состоят соединительные ткани.
Коллаген отличает бедный аминокислотный состав: в нем отсутствуют ароматические аминокислоты, зато он обогащен глицином и пролином. Аминокислотная последовательность полипептидных цепей коллагена также необычна: аминокислоты чередуются в правильном порядке; каждым третьим остатком является глицин. Каждая цепочка коллагена закручена в особую левую спираль (напомню, что α-спираль почти всегда правая), а вместе цепочки скручиваются в правую тройную («коллагеновую») суперспираль (рис. 13).
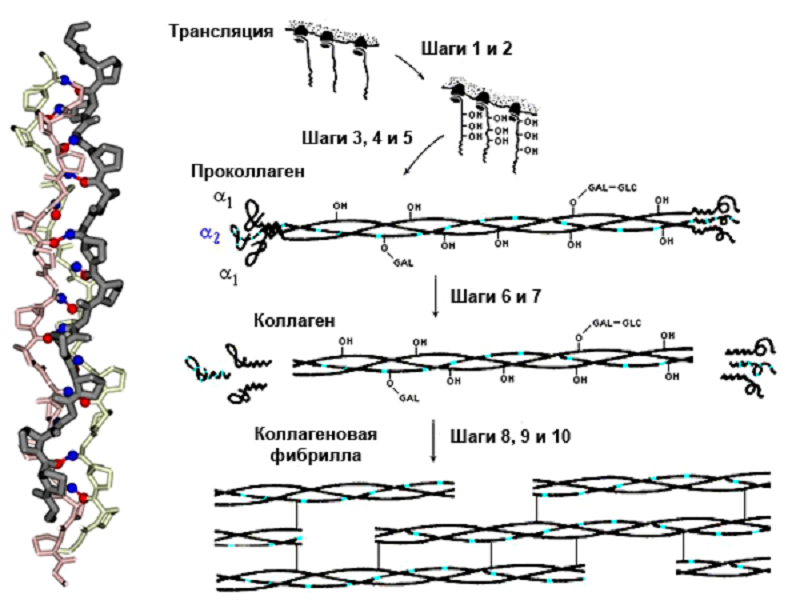
Рисунок 13. Модель суперспирали коллагена и ее формирование. Слева: модель для последовательности (глицин–пролин–пролин)n. Каждая цепь выделена своим цветом. Отмечены завязывающие водородные связи Н-атомы NH-групп глицина (синим) и О-атомы СО-групп первого пролина тройки Gly–Pro–Pro (красным). При этом Gly цепи «1» завязывает связь с цепью «2», а Pro — с цепью «3» и т.д. Завиваясь вокруг двух других, каждая цепь коллагена образует правую суперспираль. «Супер» — потому что на более мелком масштабе, на масштабе конформаций отдельных остатков, коллагеновая цепь уже образует спираль типа poly(Pro)II (эта «микроспираль» — левая); ее можно проследить по направлению пролиновых колец.
Справа: образование коллагена in vivo. Шаг 1. Биосинтез про- α1-цепей и про- α2-цепей (по 1300 остатков в каждой) в пропорции 2:1. Шаг 2. Гидроксилирование некоторых остатков Pro и Lys. Шаг 3. Присоединение сахаров (GLC-GAL) к гидроксилированным остаткам. Шаг 4. Образование тримера и S-S-связей на его концах. Шаг 5. Образование тройной спирали в середине проколлагена. Шаг 6. Секреция проколлагена во внеклеточное пространство. Шаг 7. Отщепление глобулярных частей. Шаги 8–10. Спонтанное образование фибрилл из тройных суперспиралей, окончательная модификация аминокислотных остатков и образование ковалентных сшивок модифицированных остатков коллагеновых цепей.
На этом особенности коллагена не кончаются. Некоторые остатки пролина и лизина в его составе гидроксилированы (3-гидроксипролин, 4-гидроксипролин, 5-гидроксилизин) и образуют дополнительные водородные связи, стабилизирующие и упрочняющие белковую фибриллу. Еще бόльшие возможности для формирования водородных связей создает то, что ряд остатков гликозилирован по гидроксильным группам, а некоторые гидроксилы гидроксилизина окислены до кетогруппы.
Гидроксилирование аминокислотных остатков коллагена невозможно в отсутствии аскорбиновой кислоты (витамина С). Поэтому при недостатке данного витамина в пище человека и животных, неспособных к самостоятельному биосинтезу аскорбиновой кислоты, развивается тяжелое заболевание — цинга. При цинге в организме синтезируется аномальный коллаген, лишенный прочности. Соответственно, соединительные ткани становятся очень хрупкими — разрушаются дёсны, прикосновение к телу вызывает боль и гематому. Питание фруктами, богатыми аскорбиновой кислотой, быстро устраняет симптомы цинги. Следует подчеркнуть, что причиной этих симптомов является отсутствие характерной для нормального коллагена системы водородных связей, образуемой остатками гидроксиаминокислот.
Энергетический ландшафт
Выше неоднократно говорилось о том, что нативная конформация биополимеров энергетически наиболее выгодна, и молекула в стандартных для себя условиях стремится принять именно ее. Чтобы убедиться в этом, достаточно взглянуть на карту энергетического ландшафта макромолекулы (рис. 14). Самая глубокая «впадина» на ней соответствует нативной конформации (энергетический минимум), а самые высокие «горные пики», понятно, принадлежат самым невыгодным, напряженным структурам, принимать которые молекула избегает. Обращает на себя внимание то, что соответствующий нативной конформации глобальный минимум отделен от остальных впадин широким пространством — «энергетической щелью». Это затрудняет спонтанный переход макромолекулы из нативной конформации в какую-либо другую, тоже энергетически выгодную [12]. Надо сказать, что в данном правиле есть исключения — функции ряда биополимеров связаны с переходом из одной конформации в другую, у них и энергетический ландшафт другой [14]. Но такие исключения только подтверждают общее правило.
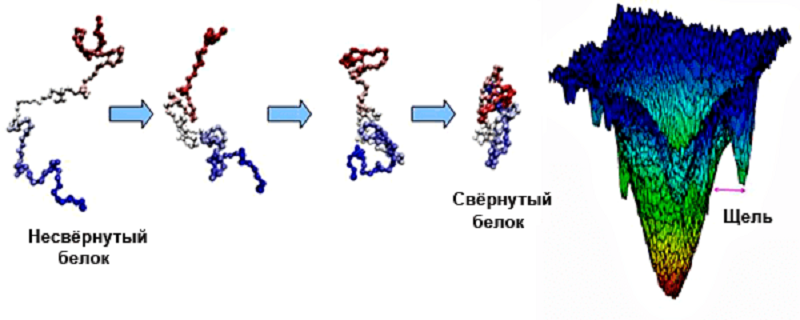
Рисунок 14. Самосборка третичной структуры белка. Слева: один из возможных путей последовательного сворачивания белка. Все промежуточные состояния имеют высокую свободную энергию и потому не накапливаются при сворачивании и не могут наблюдаться непосредственно. Справа: схематическое изображение энергетического ландшафта белковой цепи. (На рисунке мы можем изобразить только две координаты, описывающих конформацию белковой цепи, тогда как реальная конформация описывается сотнями координат.) Широкая щель между глобальным энергетическим минимумом и прочими энергетическими минимумами необходима для того, чтобы стабильная укладка цепи разрушалась только путем термодинамического перехода типа «всё-или-ничего»; это обеспечивает надежность функционирования белка — по принципу «всё-или-ничего», как у электрической лампочки.
Тем не менее спонтанная правильная укладка биополимера наблюдается далеко не всегда. Например, приготовление яичницы есть ни что иное, как тепловая денатурация яичного белка. Но никто до сих пор не наблюдал, чтобы, остывая, яичница ренатурировала обратно в сырое яйцо. Причиной этому служит неупорядоченное взаимодействие между собой полипептидных цепей, их сплетение в единый клубок. Такого рода стабилизация денатурированного состояния наблюдается и в живой ткани, скажем, при том же самом термическом воздействии. Эволюция предусмотрела решение и этой проблемы, создав так называемые белки теплового шока. Эти агенты названы так потому, что интенсивно вырабатываются в организме при термических ожогах. Их задача — помочь денатурированным макромолекулам вернуть нативную структуру. Белки теплового шока еще называют шаперонами, т.е. «няньками». Для них характерно наличие вместительной полости, в которую помещаются фрагменты денатурированных молекул и где создаются оптимальные условия для правильной укладки цепей. Таким образом, функция шаперонов сводится к устранению стерических препятствий на пути самопроизвольной ренатурации биополимеров.
Не только белки, но и углеводы
До сих пор речь шла фактически только о двух классах биополимеров — белках и нуклеиновых кислотах. Но есть и третий большой класс — полисахариды, которых мы традиционно упустили из вида.
Молекулярные биологи всегда относились к полисахаридам с некоторым пренебрежением, как к грубой субстанции. Дескать, нуклеиновые кислоты — это интересный объект исследования, они — носитель генетической информации. Белки тоже интересны, к ним относятся почти все ферменты. А полисахариды всего-навсего энергетический запас, топливо живого организма или строительный материал, не более. Разумеется, данный подход неверен и постепенно изживает себя. Теперь мы знаем, что полисахариды и их производные (в частности, протеогликаны) играют ключевую роль в регуляции клеточной деятельности. Например, рецепторы клеточной поверхности представляют собой разветвленные молекулы полисахаридной природы, а роль полисахаридов клеточных стенок растений в регуляции жизнедеятельности самого растения еще только начала выясняться, хотя уже получены интереснейшие данные.
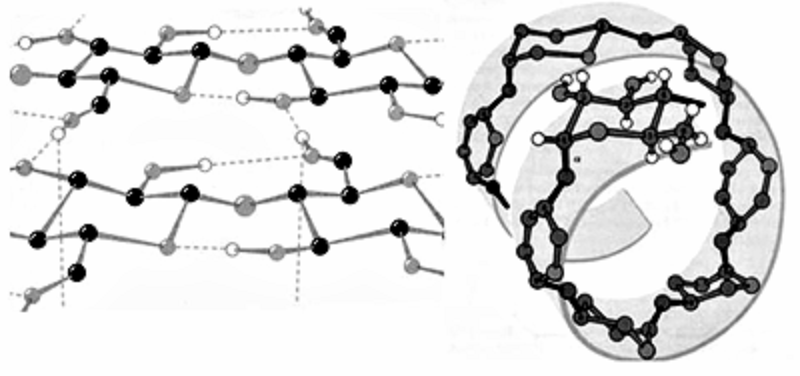
Рисунок 15. Водородные связи в полисахаридах. Слева: в целлюлозе соседние остатки глюкозы повернуты на 180°, что позволяет им образовать две Н-связи. Это делает невозможным перемещение остатков друг относительно друга, и молекула целлюлозы представляет собой жесткую, негнущуюся нить. Такие нити образуют водородные связи между собой, формируя микрофибриллы, которые объединяются в фибриллы — жгуты с высокой механической прочностью. Справа: другая конфигурация связей между мономерами в амилозе приводит к тому, что водородные связи образуются между остатками глюкозы, находящимися в цепи далеко друг от друга. Поэтому амилоза образует спиральные структуры, в которых на один виток приходится 6 остатков глюкозы, т.е. водородными связями соединены первый и шестой остатки, второй и седьмой, третий и восьмой и т.д.
Нас же интересует роль слабых взаимодействий, которая у полисахаридов проявляется, пожалуй, даже сильнее, чем у других биополимеров. С первого взгляда ясно, что хлопковая вата и картофельный крахмал не одно и то же, хотя химическое строение целлюлозы и амилозы (неразветвленной фракции крахмала) очень сходное. Оба вещества представляют собой (1→4)-D-глюканы — гомополимеры, состоящие из остатков D-глюкозы в форме пиранозных циклов, соединенных друг с другом гликозидными связями в положениях 1 и 4 (рис. 15). Разница в том, что амилоза — это α-(1→4)-D-глюкан (в ней остатки глюкозы не повернуты относительно друг друга), а целлюлоза — β-(1→4)-D-глюкан (в ней каждый остаток глюкозы повернут на 180° относительно двух своих соседей). В результате макромолекулы целлюлозы оказываются выпрямленными и образуют прочную сеть водородных связей как между собой, так и внутри каждой макромолекулы. Пучок таких макромолекул образует фибриллу. Внутри фибриллы макромолекулы упакованы настолько плотно и упорядоченно, что формируют кристаллическую структуру, редкую для полимеров. Фибриллы целлюлозы по механической прочности приближаются к стали и инертны до такой степени, что выдерживают действие уксусно-азотного реактива (горячей смеси азотной и уксусной кислот). Вот почему целлюлоза выполняет в растениях опорные, механические функции. Она является каркасом клеточных стенок растений, фактически их скелетом. Очень сходное строение имеет хитин — азотистый полисахарид клеточных стенок грибов и наружного скелета многих беспозвоночных животных.
Амилоза структурирована иначе. Ее макромолекулы имеют форму широкой спирали, на каждый виток которой приходится шесть глюкозных остатков. Каждый остаток связан водородной связью с шестым от себя «собратом». Спираль имеет вместительную внутреннюю полость, в которую могут проникать комплексообразователи (например, молекулы йода, образующего с крахмалом комплекс синего цвета). Такая структура делает амилозу рыхлой и непрочной. В отличие от целлюлозы она легко растворяется в воде, образуя вязкий клейстер, и не менее легко гидролизуется. Поэтому в растениях амилоза вместе с разветвленным амилопектином играет роль резервного полисахарида — хранилища глюкозы.
Итак, все приведенные в статье данные свидетельствуют о колоссальной роли, которую играют слабые взаимодействия в живом организме. Статья не претендует на научную новизну: самое главное, что уже известные факты рассмотрены в ней с несколько нетривиальной точки зрения. Можно лишь напомнить о том, что уже прозвучало в начале — слабые связи в значительно большей степени годятся на роль рычагов управления молекулярной машиной, чем ковалентные. А то, что они столь широко представлены в живых системах и несут столько полезных функций, лишь подчеркивает гениальность Природы. Надеюсь, что прозвучавшие в этой статье сведения заинтересуют и тех, кто занимается созданием искусственных молекулярных машин: следует помнить о том, что мир един, живой и неживой природой управляют одни и те же законы. Не стоим ли мы у истока новой науки — молекулярной бионики — кто знает?
Литература
- Раздвинувший границы химии;
- Изучение эволюции белков уточнило механизм действия противоопухолевого лекарства иматиниб;
- На заре молекулярной графики;
- Изваяние невидимого;
- Румянцев Е.В., Антина Е.В., Чистяков Ю.В. Нуклеиновые кислоты. Из: Химические основы жизни: методическое пособие к лекционному курсу. Иваново: ИГхту, 2003. — 80 с. ISBN 5-230-01590-Х;
- У истоков генетического кода: родственные души;
- Инге-Вечтомов С.Г. Введение в молекулярную генетику. М.: Высшая школа, 1983. — 343 с.;
- Номенклатурный работник стереохимии;
- Липкин В.М. Проблема белка. М.: Наука, 1995. — Т.1. — 496 с.;
- Финкельштейн А. В., Птицын О. Б. Физика белка: Курс лекций с цветными и стереоскопическими иллюстрациями и задачами. М.: КДУ, 2005 — 456 с.;
- Новые успехи в предсказании пространственной структуры белков;
- Торжество компьютерных методов: предсказание строения белков;
- Физическая водобоязнь;
- Молекулярная поверхность: что в облике тебе моём?;
- Одна последовательность — одна структура: был ли Анфинсен неправ?.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚




