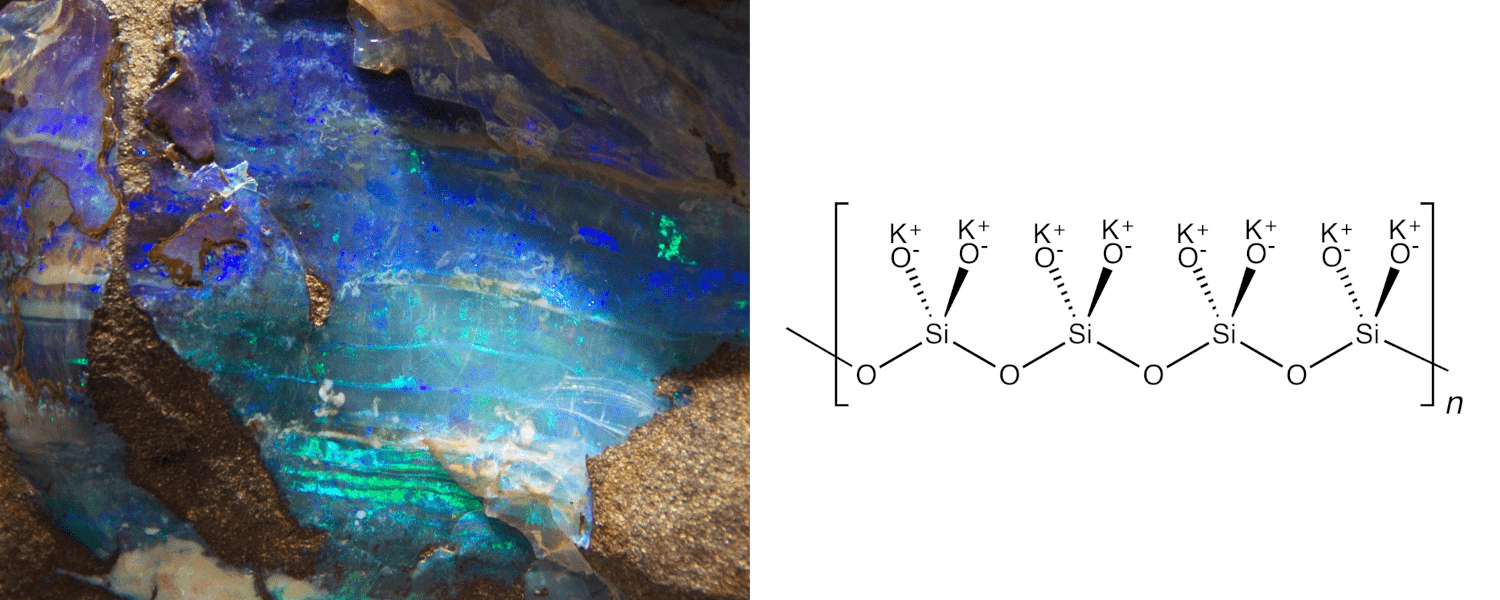Биодеградация на переднем крае науки
18 января 2024
Биодеградация на переднем крае науки
- 885
- 0
- 1
Биодеградация как природное явление протекает сама по себе, без всякого вмешательства человека. Но когда человек осознал пользу этого явления, он, как и положено человеку, создал технологию, которая в ряде случаев может увеличивать эффективность биодеградации многократно. Фактически получился резонанс двух природных явлений — совершеннейшего микробного метаболизма и мощнейшего человеческого разума. На фото представлен самый мощный промышленный ферментер в мире, построенный в Китае компанией Calysseo. Он вмещает 20 000 тонн культуральной среды! Ферментер создан для производства микробного белка, но его можно применять и для создания микробных биопрепаратов с целью биоремедиации загрязнений. Сейчас Calysseo занята строительством ферментера на 100 000 тонн в Саудовской Аравии. К работе этот исполин должен приступить в конце 2026 года.
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Каждый год я планирую, что очередная статья, посвященная биодеградации, будет последней. И тем не менее, всегда накапливается новый материал, которым хочется поделиться с читателями. Причина этого заключается, по-видимому, в том, что тема попала «в струю», и практический интерес к ней возрос. Как и раньше, я стараюсь делать акцент на самые необычные и интересные примеры биодеградации, несколько оставляя в стороне их практическую значимость, — потому что именно они находятся на переднем крае науки. Некоторые примеры настолько экзотичны, что даже термин «биодеградация» к ним применим только формально. И далеко не все связаны с защитой окружающей среды, с которой биодеградация ассоциируется в первую очередь.
Конкурс «Био/Мол/Текст»-2023/2024
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2023/2024.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

Партнер номинации — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Тихие труженики
Приспособляемость микробов к условиям окружающей среды удивительна. Ни одна другая группа живых организмов не может сравниться с ними. Бактерии обитают в источниках с температурой воды 120 ℃, в охладителях ядерных реакторов и на дне океанов. Выдерживают они и пребывание в космическом пространстве, и перегрузку в сотни тысяч g [1]. Немногим отстают от них споры грибов. Эти примеры никого не оставляют равнодушными, о них много говорят и пишут.
На первый взгляд, причина такой удивительной живучести микробов кажется парадоксальной. Она кроется в их уязвимости. Микробы, в отличие от животных, не могут уйти из опасной зоны. Их размеры малы, а способность к передвижению ограничена. Но из всех живых организмов именно микробы обладают самым быстрым темпом смены поколений. И, соответственно, самой быстрой эволюцией, открывающей почти неограниченные адаптивные возможности. Вот и приспосабливаются.
Мне как исследователю, изучающему процессы микробиологической очистки, ближе примеры устойчивости микроорганизмов к химическим загрязнителям. Неспроста экологи относят бактерии и грибы к группе редуцентов — с латыни это слово переводится как «те, кто разлагает». К этой же группе относят ряд низших животных — например, дождевых червей, которых иногда тоже применяют для биодеградации. До сих пор ведутся споры, относить ли к редуцентам некоторые виды бесхлорофилльных растений, таких как подъельник (Monotropa) (рис. 1).

Рисунок 1. Подъельник обыкновенный, или вертляница (Monotropa hypopitys) — цветковое растение, лишенное хлорофилла и неспособное к фотосинтезу. Произрастает в лесах Северного полушария. В симбиозе с почвенными грибами (и, возможно, корнями деревьев) подъельник разлагает отмершую органику, т.е., является сапротрофом. Это одно из тех редких растений, которые заняли экологическую нишу редуцентов.
На практике
Биосфера планеты Земля до сих пор остается уникальным явлением. В других уголках космоса жизнь до сих пор не обнаружена, даже в самых примитивных формах. В конечном итоге биосфера породила человека и созданную им цивилизацию. В прошедшем столетии было принято противопоставлять природу и сотворенную нами, людьми, культуру. Но теперь мы приходим к мнению, что этот подход неверный. Все существующее во Вселенной является ее частью. Все появилось из существовавшего когда-то протовещества. Биосфера — это мощнейшая биогеохимическая сила нашей планеты, с ней связан уникальный состав атмосферы Земли, на 21% состоящей из кислорода, производство триллионов тонн органического вещества, которое вообще-то в окислительной атмосфере существовать не должно.
По академику В.И. Вернадскому, биосфера состоит из биокосного вещества, содержит минеральный и органический компонент и богатейший видовой состав организмов, заселивших всю поверхность планеты вплоть до самых неблагоприятных для жизни районов. Разумеется, биосфера не просуществовала бы почти 4 миллиарда лет без присущей ей способности к самоочищению, которое является залогом благополучного существования на планете каждого живого существа, в том числе и людей. Разумеется, свойства поверхности земного шара обусловлены богатейшим видовым составом биоты — в первую очередь, микробиоты. Мы еще очень далеки от полного описания видового состава микроорганизмов. Еще меньше информации собрано о метаболических путях микробов. Однако, нет сомнений в многообразии последних. Разнообразие микробов и их метаболизма как раз и обусловливает способность почв, вод и даже атмосферы к самоочищению от соединений разнообразных свойств и структур. Например, искусственных полимеров [2], которые традиционно рассматриваются как сложный объект для биодеструкторов.
Читая мои работы [3–9], читатель может легко впасть в заблуждение, решив, что биодеградация — это очень просто. Что можно спокойно бросать на землю пластиковые стаканы и пакеты, и через небольшой промежуток времени они исчезнут навсегда. В действительности, биодеградация всегда эффективна на глобальном уровне, в масштабах земного шара и во временные отрезки в миллионы лет. Но на локальном уровне нескольких замусоренных квадратных метров она может совершенно не проявиться. Просто эволюция не подхватит изменения, коснувшиеся живых организмов на столь ограниченной территории за столь ограниченное время. Поэтому, сколько бы примеров биологической деструкции не узнала наука, задача бережного отношения к природе со стороны людей отнюдь не снимается.
Примером территорий, не оправившихся после вмешательства человека даже спустя сто с лишним лет, могут являться так называемые беллигеративные ландшафты, оставшиеся после боевых действий, особенно ожесточенных в ХХ веке (рис. 2). В последнее время политологи все чаще в один голос заявляют, что мир находится на пороге новой Мировой войны. Очевидно, что эта война, если (не приведи Господь Бог) случится, по размаху и последствиям превзойдет Вторую Мировую — крупнейшую в прошедшей Истории. Страшно представить, к каким последствиям не только для населения Земли, но и для биосферы, самой жизни, она приведет.

Рисунок 2. Беллигеративный пейзаж в окрестностях маленького французского городка Верден. Этот населенный пункт стал известен на весь мир и вошел в историю во время Верденского сражения 1916 года — крупнейшей битвы Первой мировой войны. Почвенный покров на этой территории полностью уничтожен, а грунт настолько отравлен металлами из корпусов артиллерийских снарядов, что растительный покров не восстановился даже спустя сто с лишним лет.
«Элементы»
Экологический ликбез
Так часто бывает в жизни, когда о самом важном сообщаешь в конце. Вот уже девятая по счету моя статья в «Биомолекуле», восьмая, посвященная биодеградации. И только сейчас я подхожу к разъяснению основных понятий — азов, с которых, вообще-то, следовало начинать свое повествование. Разумеется, антропогенные загрязнения почвы, воды и воздуха имеют фатальные последствия.
- Загрязнитель
- любой природный или антропогенный агент, попадающий в окружающую природную среду в количествах, превышающих фоновые значения и вызывающий тем самым ее загрязнение (также загрязнителем именуют и источник загрязнения, например, завод или полигон ТБО). При этом «мерой» загрязнения данным агентом среды является степень отклонения от фоновых значений данного агента. Согласно этой (широкой) трактовке любой новый для среды агент (даже если он не токсичен по отношению к биоте) рассматривается как загрязнитель. В узком смысле «загрязнитель» — это физический, химический или биологический компонент, попавший в среду техногенным путем и оказывающий вредное токсическое действие на биоту (живые организмы).
Виды загрязнителей:
- Загрязняющее вещество — химическое вещество, присутствующее в окружающей среде в количествах, превышающих фоновые значения.
- Физические загрязнители — загрязнители, созданные различными физическими полями (электромагнитное излучение, шум, радиоактивное излучение).
- Биологические загрязнители — биологические виды (в том числе микроорганизмы), не характерные для данного биогеоценоза или находящиеся там в излишних, превышающих обычные, количествах.
- Техногенные (антропогенные) загрязнители — агенты загрязнения, созданные человеком.
- Природные (естественные) загрязнители — агенты загрязнения, имеющие природное происхождение.
- Загрязняющее вещество (также поллютант) — один из видов загрязнителей, любое химическое вещество или соединение, которое находится в объекте окружающей природной среды в количествах, превышающих фоновые значения и вызывающие тем самым химическое загрязнение.
Существуют загрязняющие вещества природного происхождения — попадающие в природную среду в результате естественных процессов (пример — загрязнение прилегающих территорий пеплом при извержении вулкана); — и антропогенного происхождения. По характеру загрязняющие вещества делятся на: первичные (поступившие в окружающую среду непосредственно из источников загрязнения) и вторичные, образующиеся из первичных в результате биогенных и абиогенных трансформаций. Наиболее распространенные антропогенные загрязнители:
- в атмосфере — кислые газы (диоксид углерода, диоксид серы, оксиды азота), взвешенные частицы (сажа, аэрозоли кислот и соединений тяжелых металлов), органические соединения, в том числе формирующие фотохимический смог и разрушающие озоновый слой атмосферы, пары нефтепродуктов.
- в гидросфере — растворимые соли тяжелых металлов, органические соединения, нефтепродукты, разогретые сточные воды из охладителей, вызывающие тепловое загрязнение.
- в литосфере (особенно в ее верхнем плодородном слое — почве, который нас более всего интересует) — соли тяжелых металлов, нефтепродукты. Следует отличать инертные вещества (например, стекло), вызывающие лишь механическое загрязнение почв, но не оказывающие токсическое воздействие.
- в биосфере наиболее опасными поллютантами являются ксенобиотики, то есть вещества, не входящие в естественный обмен веществ в организме. Среди них встречаются суперэкотоксиканты, из которых наиболее известны диоксины [10]. Следует особо отметить, что вычленить биосферу из других сред земного шара невозможно. Живое вещество неотделимо от окружающего его органического и минерального компонентов.
Специфика почвенного покрова состоит в том, что он по своей природе является сорбентом и может удерживать загрязнители длительное время. С одной стороны, это снижает токсическое воздействие загрязнителей; с другой — продлевает их воздействие [11]. Поскольку почва является твердой, неподвижной средой, в ней (в отличие от водной и воздушной сред) почти невозможно перемешивание и разбавление загрязнителей.
Водная и, особенно, воздушная среды, напротив, способствуют переносу загрязнителей на большие расстояния. Но при этом происходит разбавление и снижение вреда от них. Эффекты противоположной направленности своеобразным образом компенсируют друг друга.
Любая отрава по плечу
Пестициды — соединения и их смеси, применяемые для борьбы с сельскохозяйственными вредителями (грызуны, насекомые, моллюски, клещи, круглые черви), сорными растениями и болезнями растений — в первую очередь, вызываемыми фитопатогенными грибами. Соответственно, по спектру действия пестициды подразделяют на инсектициды, родентициды (зооциды), акарициды, моллюскоциды, нематоциды, гербициды, альгициды, фунгициды, слимициды и т.д. Бактерициды и вируциды формально не относятся к пестицидам, хотя близки к ним по характеру воздействия. Биоциды — вещества, токсичные для любых форм жизни, и в настоящее время также к пестицидам не относятся. Все пестициды объединяет высокая биологическая активность, токсичность. Однако, по химическому строению это совершенно различные вещества. Спектр действия пестицидов также очень разнообразен. Соответственно, пути расщепления пестицидов, отвечающие за них ферменты и микроорганизмы, тоже очень многообразны. В силу характера применения, пестициды чаще всего вносятся именно в почвы. И обезвреживаются, главным образом, почвенной микробиотой.
Для окружающей среды пестициды представляют особую угрозу, потому что эта группа веществ изначально создана для борьбы с живыми организмами. В почве они подавляют жизнедеятельность микроорганизмов, растений и беспозвоночных. Ряд пестицидов и их метаболитов, которые могут быть еще опаснее, чем исходные вещества, накапливается в растениях и поступает в пищевую цепочку. При этом виды, находящиеся на вершине пищевой пирамиды — человек и высшие хищники (рис. 3А), — страдают от применения пестицидов значительно больше, чем организмы, против которых изначально направлено их применение.
До недавнего времени была очень распространена точка зрения, что пестициды галогенароматической природы (например, ДДТ (1,1,1-трихлор-2,2-бис (4-хлорфенил) этан)) не разлагаются в окружающей среде и накапливаются в тканях живых организмов даже в тысячах километров от мест применения. Теперь распространяется альтернативная версия, что обнаруженный в жировой ткани животных «ДДТ» — это, на самом деле, близкие ему по строению природные галогенароматические метаболиты, продуцируемые, например, морскими бактериями, живущими в симбиозе с губками. Это может косвенно свидетельствовать о том, что ДДТ и близкие ему пестициды обезвреживаются в окружающей среде намного быстрее и эффективнее, чем предполагалось до сих пор. А также хорошо объясняет, почему «следы ДДТ» находят именно в морских организмах, никак не контактирующих с районами, где применяются пестициды [12] (рис. 3Б).
В статье [5] я рассказывал про удивительные метаболические превращения неприродных веществ, в результате которых вырабатываются другие неприродные вещества. Например, гербицид сульфометуронметил становится пищевой добавкой сахарином. На самом деле, такие примеры далеко не единичны.
Карбендазим — фунгицидный препарат, служащий для защиты культурных растений от фитопатогенных грибков. Вещество это в природе неизвестно и является продуктом промышленного синтеза. Однако, подобно большинству фунгицидов, карбендазим не влияет на рост представителей другой крупнейшей группы микробов — бактерий. Для них он практически нетоксичен, а культура Rhodococcus sp. CX-1 разлагает его путями, характерными для всех ароматических соединений — через катехин и муконаты. Но самое интересное заключается в том, что это не встречающееся в природе вещество образуется как промежуточный продукт бактериальной биодеградации двух других синтетических фунгицидов — беномила и тиофанат-метила [13], [14] (рис. 4)! Причем, во втором случае бензимидазольный фрагмент молекулы формируется в процессе метаболизма.
Конечно, все три фунгицида изначально имеют структурное сходство, и превращение один в другой само по себе не должно сильно удивлять. Но такие примеры наводят на мысль, что образование одних ксенобиотиков из других под контролем ферментных систем живых клеток в природе не редкость, а вполне обыденное явление. Просто за его изучение всерьез никто не брался. А изучать надо не из праздного любопытства. Не зная путей метаболизма того или иного биологически активного вещества, мы не можем точно оценить его влияние на организм или окружающую среду.
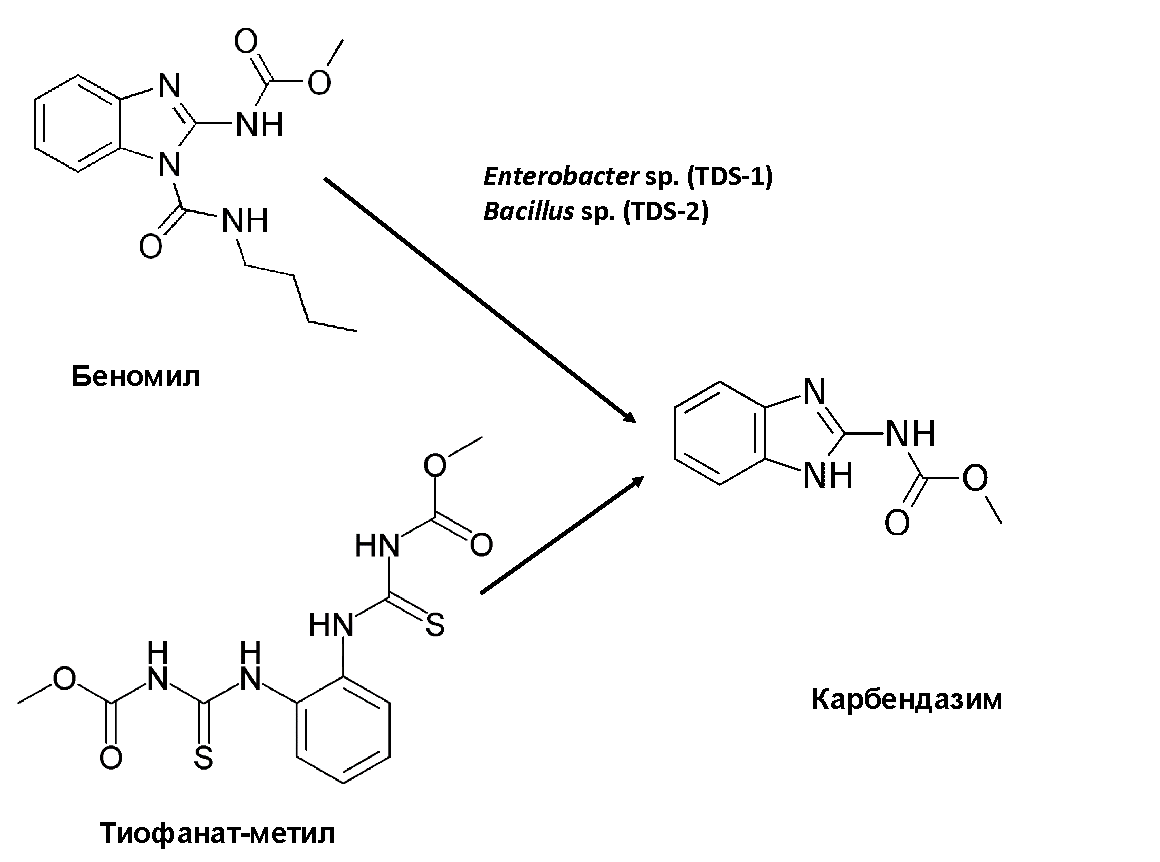
Рисунок 4. Синтетический фунгицид карбендазим образуется в качестве метаболита других ароматических фунгицидов — беномила и тиофанат-метила.
рисунок автора
Микробы испаряют металл
Формально тяжелыми металлами являются все металлы, плотность которых в г/см3 выше плотности железа. Как правило, это элементы с высокими порядковыми номерами, и им присуща высокая токсичность. Экологи и биохимики вкладывают в определение «тяжелый металл» несколько другой смысл. Это переходные металлы, катионы которых являются мягкими кислотами Льюиса и имеют высокое сродство к тиольным (сульфгидрильным) группам –SH. Соответственно, они легко связываются с тиольными группами белков и подавляют их активность. Это придает тяжелым металлам высокую токсичность и способность надолго задерживаться, аккумулироваться в организме.
В отличие от пестицидов, абсолютное большинство тяжелых металлов имеет природное происхождение — за исключением сверхтяжелых и сильнорадиоактивных элементов, синтезированных путем ядерных реакций. В почву они проникают как из природных месторождений, так и в результате деятельности человека (например, сжигания топлива с добавками тетраэтилсвинца, коррозии металлических сплавов). Однако в природе тяжелые металлы встречаются в виде руд (как правило, сульфидных) или самородков — в формах, малоопасных для окружающей среды. Человек превращает их в более биодоступные и опасные формы — водорастворимые соли и комплексы, жирорастворимые металлорганические вещества.
Некоторые особо опасные металлы и металлоиды могут образовывать летучие алкилированные соединения. Человеку они давно известны. Например, тетраэтилсвинец [4] длительное время использовался в качестве присадки к топливам, а какодиловая (диметиларсиновая) кислота в позапрошлом веке применялась в качестве пестицида. Подобные соединения обладают высочайшей токсичностью — приятный, похожий на эфирный запах некоторых из них не должен вводить в заблуждение. Собственно, поэтому они вышли из употребления. Но микроорганизмы их синтезируют! Свинец, ртуть, мышьяк, сурьму, кадмий, олово, селен, теллур, таллий метаногенные микробы Methanobacterium formicicum, Methanosarcina barkeri, Methanobacterium thermoautotrophicum превращают в летучие метильные производные, которые испаряются в атмосферу [15], [16] (рис. 5). Донором метильных групп служит аминокислота метионин в составе микробных клеток. Цель микробов очевидна — они очищают свою среду обитания, совершенно не заботясь о чистоте атмосферы. Тем не менее, биометилирование является одной из основных угроз, связанных с загрязнениями тяжелыми металлами.
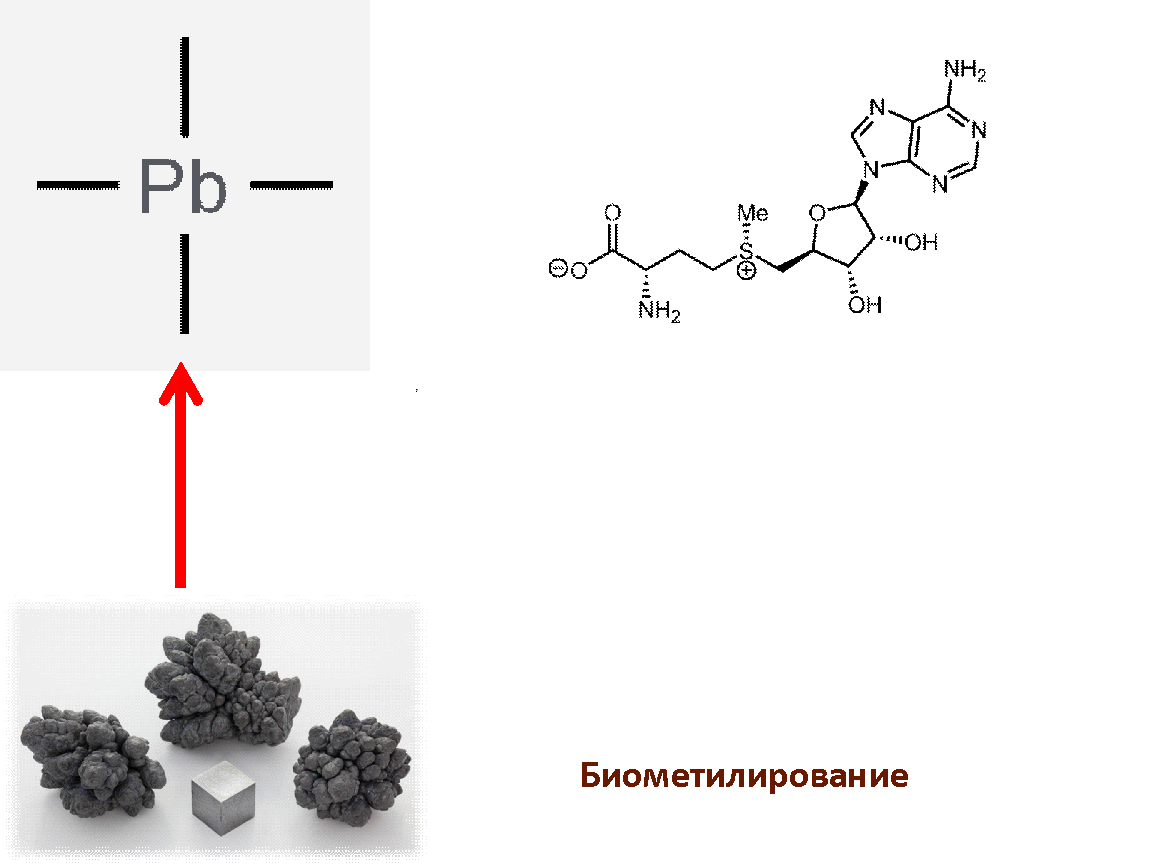
Рисунок 5. Биометилирование тяжелых металлов. Результатом микробного метаболизма тяжелых металлов (олово, свинец, ртуть, мышьяк) могут стать еще более токсичные летучие соединения. Например, такие как какодиловая кислота или тетраметилсвинец.
рисунок автора
Настоящие экстремалы
Радионуклиды по характеру загрязнений очень близки к тяжелым металлам, и в большинстве своем относятся к ним. Радиоактивные изотопы — атомы с неустойчивыми ядрами, претерпевающими спонтанный распад — есть у всех химических элементов. Элементы технеций, прометий и все элементы тяжелее свинца состоят исключительно из радиоактивных изотопов. Периоды полураспада радионуклидов могут составлять от десятков наносекунд (актиний-217) до 2·1019 лет (висмут-209: этот период полураспада на девять порядков превышает возраст Вселенной). Чем меньше период полураспада изотопа, тем выше его радиоактивность и опасность для окружающей среды. При распаде ядра атомов излучают α-частицы (ядра атомов гелия-4) (актиноиды, радий, радон), либо β-частицы (электроны) (углерод-14, йод-131). Значительно реже испускается γ-излучение — электромагнитное излучение очень высоких энергий (кобальт-60). Иногда радиоактивный распад сопровождается формированием ядер элементов, более тяжелых, чем гелий (кластерный распад) (барий-114 распадается с образованием углерода-12). Высокие энергии этих частиц позволяют им повреждать молекулы биополимеров и даже вызывать распад (радиолиз) молекул воды, в том числе, входящей в состав живых клеток и тканей.
Наибольшую опасность представляют короткоживущие изотопы с периодом полураспада менее 10 суток. Они постоянно присутствуют в природе, входя в радиоактивные ряды. Однако, природные короткоживущие радионуклиды не накапливаются и присутствуют в почве в следовых концентрациях, в равновесии между образованием и распадом. В результате деятельности человека — например, испытаний ядерного оружия или аварий ядерных реакторов — короткоживущие изотопы с сильной радиоактивностью могут поступать в окружающую среду (в том числе, почву) в высоких концентрациях. Примером может служить йод-131.
В статье [7] я уже демонстрировал один пример биодеградации радиоактивного материала — раствора соли урана в трибутилфосфате, которым этот самый уран экстрагируют. Но этот пример не единственный. Есть и другие примеры, в чем-то даже более удивительные.
Природный уран более чем на 99% состоит из слаборадиоактивного изотопа 238U, который нельзя использовать в качестве ядерного топлива. В атомной энергетике и ядерном оружии применяется 235U, которого в природном уране менее 1%. Чтобы получить уран-235, проводят процедуру обогащения. При этом образуется большое количество малоценного обедненного урана. Уран — очень тяжелый металл, его плотность почти втрое выше плотности железа. А радиоактивность обедненного урана низкая. Поэтому его применяют в тех отраслях, где требуются материалы с высокой плотностью — производстве танковой брони и бронебойных снарядов (рис. 6а), балансировочных грузов в кораблях и самолетах, роторов гироскопов, защиты от рентгеновских лучей.
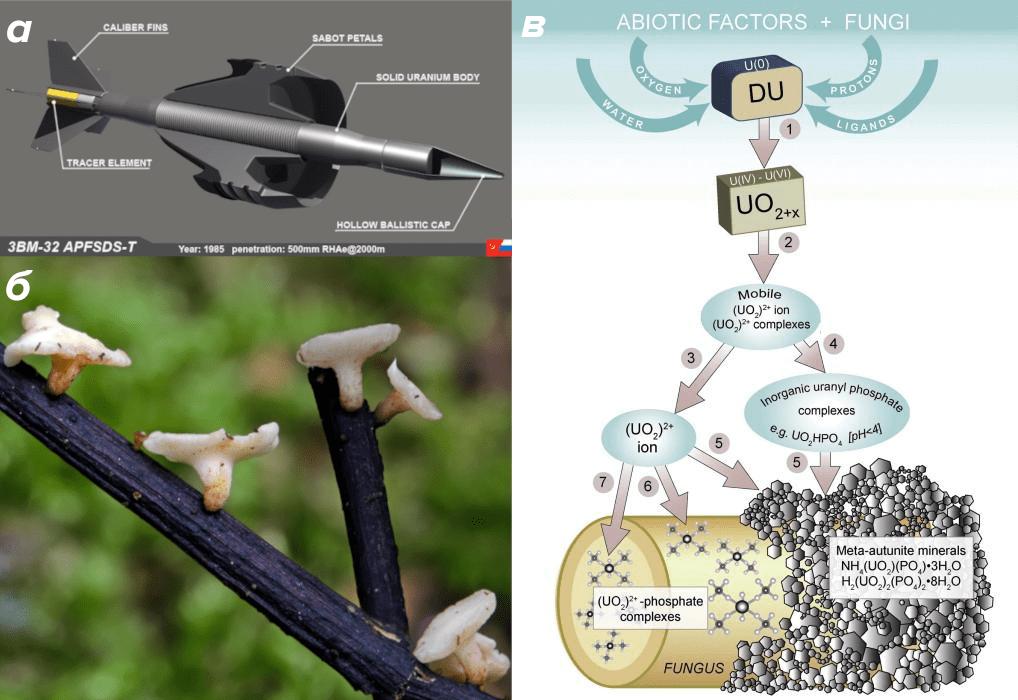
Рисунок 6. Даже уран не помеха. а — Бронебойный оперенный противотанковый подкалиберный снаряд БМ2 из обедненного урана. Грибы способны его обезвредить! б — Плодовые тела Hymenoscyphus albidus — близкого родственника гриба, обезвреживающего обедненный уран. в — Схема метаболизма обедненного урана грибами.
Но обедненный уран — металл не только очень ядовитый, но и обладающий радиоактивностью, пускай и слабой. Соответственно, он представляет большую угрозу для окружающей среды. Не может не вызывать удивление способность грибов Rhizopogon rubescens (гриб, внешне похожий на трюфель), Hymenoscyphus ericae (типичный гриб-редуцент, вызывающий гниение органических остатков) (рис. 6б) и Beauveria caledonica (гриб, паразитирующий на насекомых) разлагать металлический обедненный уран [17]. Поверхность урана, покрытая мицелием грибов, окисляется до оксидов IV и VI, которые далее в ряд стадий превращаются сначала в растворимые соли уранила, а затем в нерастворимые фосфаты уранила (рис. 6в) — вещества, нерастворимые в воде и химически инертные. Соответственно, их опасность для окружающей среды минимальна. То есть, продукты превращений обедненного урана грибами — просто идеальные кандидаты на роль захоронений ядерных отходов. А сами грибы продемонстрировали настоящее биохимическое чудо — выдержали двойной удар токсичности и радиации.
Главный поллютант
Нефть является природным ископаемым, сложной смесью органических соединений, преимущественно бедных кислородом и гидрофобных. Как правило, это черная вязкая жидкость, однако есть в ней и газообразные (попутный, природный газы), и твердые фракции (природные: озокерит, битум, горючие сланцы, асфальт; искусственные: нефтяной пек). По современным представлениям, нефть является продуктом глубокого анаэробного разложения живых организмов. Однако существуют теории и абиогенного происхождения нефти в результате реакции карбидов с водой в глубинах земной коры. Наряду с природным газом, нефть в настоящее время является наиболее интенсивно добываемым полезным ископаемым. Соответственно, загрязнения нефтью в результате ее утечек и разливов также приобретают глобальный характер.

Рисунок 7. Загрязнитель и спасение от него. а — Разлив нефти в Кувейте. б — Жидкий кислород в стакане. Жидкий и твердый кислород имеет небесно-голубой цвет. в — Формула молекулярного кислорода. Кислород необходим нам для дыхания, и значение этого вещества для современной биосферы трудно переоценить. Однако живые клетки используют его (особенно активные формы) для проведения множества химических превращений, в том числе, для детоксикации ксенобиотиков и токсинов — например, нефти и нефтепродуктов.
Нефть в природном состоянии практически не используется. В качестве топлива (главное применение нефти сегодня) применяются нефтепродукты — очищенные смеси насыщенных и ароматических углеводородов, получаемые путем фракционирования либо крекинга (разложения) нефти. К ним относятся бензин, керосин, соляровое масло, мазут. В меньших масштабах компоненты нефти применяются в качестве растворителей (петролейный эфир, уайт-спирит), химическом производстве (в основном, ненасыщенные углеводороды), биотехнологии — для получения биомассы микроорганизмов, питающихся нефтепродуктами.
Нефтепродукты в почву проникают после неполного сгорания в двигателях автомобилей или тракторов. Легкие, летучие фракции (бензин) оказывают наиболее сильное токсическое воздействие на почвенные организмы. Более тяжелые фракции из-за своей гидрофобности нарушают всасывание влаги корнями растений, дыхание путем диффузии у почвенных беспозвоночных, пропитывают шерсть и перья теплокровных и нарушают теплообмен. В загрязненной нефтью и нефтепродуктами почве содержание углерода возрастает. Однако этот углерод входит в состав соединений, с трудом подвергаемых микробной деструкции. Тем не менее, именно органическая природа нефти, состоящей практически целиком из биогенных элементов, позволяет осуществлять ее биодеградацию и эффективную биоремедиацию загрязненных участков.
Обычно ксенобиотики под влиянием ферментных систем микроорганизмов подвергаются деструкции до простейших соединений, таких как углекислый газ и вода. Следует подчеркнуть особо, что слово «обычно» на современной Земле означает «в аэробных условиях, в присутствии кислорода». Молекулярный кислород — это универсальный деструктор органических веществ, вплоть до самого сложного строения (рис. 7). Даже самые начальные этапы окисления веществ кислородом, как правило, приводят к снижению их токсичности через увеличение гидрофильности. Правда, не всегда. Некоторые вещества более токсичны в окисленном состоянии — нет правил без исключений.
Но биодеградация может протекать и в анаэробных условиях, хотя в целом такие бескислородные процессы медленные и малоэффективные. Но при этом жизнь в процессе эволюции создает очень необычные пути метаболизма, в которых достигается компромисс между необходимостью токсикант обезвредить и неспособностью разрушить его структуру.
Весьма необычен путь анаэробной деструкции циклогексана — нефтепродукта, токсичного промышленного растворителя и сырья в производстве капролактама. В аэробных условиях (в присутствии кислорода) микробы сравнительно легко окисляют циклогексан до безвредных веществ — об этом уже говорилось в статье [8]. В отсутствие кислорода сделать это труднее — как и большинство насыщенных углеводородов, циклогексан устойчив. Так как же его обезвредить? Из воды в озере Цвишенанер Меер в Нижней Саксонии (Германия) выделены анаэробные бактерии Geobacter sp. FRC-32, которые существуют в анаэробных условиях за счет анаммокс-процесса — превращают нитрат или нитрит аммония в газообразный азот. Про этот уникальный метаболический путь я уже рассказывал в статье [5]. Такой способ получения энергии сам по себе делает эту бактерию необычной. Но геобактер, к тому же, еще утилизируют незамещенный циклогексан. Часть его полностью окисляется с раскрытием цикла. Но обезвредить так весь циклогексан бактерия не может. Оставшееся вещество бактерия связывает, присоединяя его к фумаровой кислоте с образованием циклогексилянтарной кислоты (рис. 8). Далее через ряд стадий образуется циклогексилацетил-КоА, участвующий в биосинтезе жирных кислот. В результате образуются необычные жирные кислоты с циклогексильной группой на конце [18].
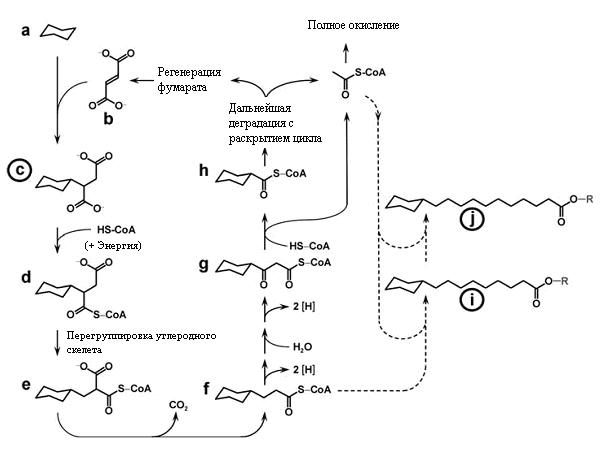
Рисунок 8. Анаэробный метаболизм циклогексана, приводящий к его иммобилизации в составе жирных кислот. Обведенные кружком буквы обозначают обнаруженные соединения. Циклогексан (a) активируется путем добавления к фумарату (b), давая циклогексилсукцинат (c), который затем может быть активирован до циклогексилсукцинил-КоА (d). Последний может подвергаться перегруппировке углеродного скелета в (циклогексилметил) малонил-КоА (е), который в результате де- или транскарбоксилирования приводит к циклогексилпропионил-КоА (f). Основная масса последних разлагается путем регулярного β-окисления через 3-оксо-3-циклогексилпропионил-CoA (g), циклогексилкарбоксил-CoA (h) и расщепление кольца с получением ацетил-CoA, а также нового фумарата для реакции активации. Некоторые циклогексилпропионил-CoA (f) могут вносить вклад в синтез клеточных жирных кислот путем добавления С2-звеньев с образованием 9-циклогексилнонаноата (i) и 11-циклогексилундеканоата (j).
[18] с изменениями
А в дальнейшем эти жирные кислоты могут включиться в состав микробных запасных полимеров — полигидроксиалканоатов, гранулы которых запасаются внутри клеток и не представляют для них вреда. Про полигидроксиалканоаты, их разнообразие, биосинтез и сферы применения очень подробно и обстоятельно рассказано в капитальном труде [19].
Биодеградация нефтей и нефтепродуктов в настоящее время настолько востребована на практике, что речь идет уже не о самих путях биотрансформации. Сейчас большое внимание уделяется различным вариантам этого процесса. Например, биодеградации в экстремальных условиях. Вот оно, настоящее раздолье для биохимии и генетики микроорганизмов! Казалось бы, способность питаться нефтепродуктами — само по себе неординарное явление. А что можно сказать, например, про микроорганизмы, делающие это в условиях Крайнего Севера? Или экстремального засоления почв? Может быть, они с других планет? Нет. Эти микробы, как и мы с вами, имеют земное происхождение. Просто о жизни на Земле мы еще далеко не все знаем, вот и удивляемся.
Статья [20] посвящена примерам биодеградации нефтепродуктов в экстремальных условиях (значения температуры, рН, солености, давления). Не стоит забывать о том, что присутствие в окружающей среде токсичных веществ — само по себе неблагоприятный фактор. То есть, микробы оказываются приспособленными по целому спектру экстремальных условий!
Еще недавно считалось, что биодеградация возможна только в интервале температур 20–40 ℃. Микробиологи называют эти условия «мезофильными». Но в реальности температура может быть гораздо ниже — скажем, у нас в России, прежде всего, в Сибири или за Полярным кругом. И что, в этих условиях биодеградация неприменима? Оказывается, применима. Пресловутая генная инженерия позволила переносить плазмиды с генами, отвечающими за биодеградацию, в бактерии-психрофилы, растущие в диапазоне температур 0–20 ℃ [21]. Это значит, что биодеградация, скажем, нефтепродуктов возможна и в Арктике, освоение которой стало в последние годы приоритетной задачей.
Одолеть непобедимого
Отходы пластиков появились в мире примерно в середине 50-х годов прошлого века. За последние 70 лет их объем вырос в несколько сотен тысяч раз и продолжает расти. Производство пластиковых изделий является одной из самых динамичных развивающихся отраслей и увеличивается в среднем на 5% в год. Сейчас в год производится около 400 миллионов тонн пластика, и, по прогнозам, к 2050 году его производство удвоится. Несколько миллионов тонн пластика ежегодно поступает на свалки и полигоны, которые оказывают резкое негативное влияние на окружающую среду и качество жизни, здоровье людей.
Пластик все больше и больше загрязняет нашу планету, потому что его производство сегодня многократно превосходит скорость биодеградации. Каждую минуту в наши океаны попадает количество пластиковых отходов, способное поместиться в кузов грузовика.

Рисунок 9. Пейзаж Большого тихоокеанского мусорного пятна.
Помимо этого, за последние 50 лет пластик стал самым популярным упаковочным материалом для пищевых продуктов. Он прочен, легок, презентабелен и относительно дешев. Он доминирует в разовой упаковке, сумках для покупок, готовых контейнерах и столовых приборах в ресторанах и кафе. Современный мир предпочитает пластиковую упаковку любой другой, спрос на нее растет.
Пластиковые отходы накапливаются на мусорных полигонах. В Тихом океане сформировалось устойчивое крупное скопление пластикового мусора — Большое Пластиковое Пятно (рис. 9). Самая большая угроза, связанная с пластиками, заключается в следующем. Под влиянием факторов среды пластиковые материалы крошатся, образуя вездесущие мельчайшие частицы, объединяемые названием «микропластик». Проблема потребления микропластика, остатки которого ученые обнаруживают в питьевой воде и тканях живых существ, радикальных решений не находит в связи с увеличением масштабов производства и потребления полимеров. Однако следует подчеркнуть важный момент. Пластики являются органическими веществами и состоят из тех же элементов, что и живые организмы. Это водород, углерод, азот, кислород, фосфор, сера, хлор. Соответственно, существует теоретическая возможность превращать пластики в природные соединения, усваиваемые живыми организмами. Эта возможность реализуется при использовании метода биодеградации.
Разумеется, создание эффективных методов разложения пластиковых отходов и возвращения их в природный круговорот веществ является приоритетной задачей, важность которой будет возрастать с каждым годом.
Надо сказать, что в целом микроорганизмы справляются с пластиками довольно успешно, хотя не настолько, чтобы останавливать рост интенсивно пополняемых мусорных полигонов. Тем не менее, среди этого класса отходов есть такие, для которых сама возможность биодеградации до последнего времени представлялась нереальной.
Перфторуглероды — это углеводороды, в которых все атомы водорода замещены атомами фтора. Эти довольно экзотические вещества в природе встречаются, главным образом, в вулканических газах. Свойства перфторуглеродов очень сходны со свойствами инертных газов. Их впору называть «органическими инертными газами». В частности, они химически инертны (не в пример молекулярному фтору, про который рассказывал в статье [8]!) и обладают очень слабыми ван-дер-ваальсовыми взаимодействиями, про которые я упоминал в [9]. Полимер политетрафторэтилен, известный как тефлон и фторопласт-4, является одним из самых химически стойких материалов. Он не горит, не взаимодействует с окислителями, кислотами и щелочами. Вступает в реакции только с реагентами экстремальной активности — такими как расплавленные щелочные металлы, фтор, трифторид хлора и дифторид ксенона. Кроме того, у него самая низкая среди всех материалов адгезия, поэтому тефлон скользкий на ощупь, и к нему ничто не прилипает. Он не смачивается жидкостями. В статье [9] я уже рассказывал про гидрофильные и гидрофобные вещества. Так вот, уникальность тефлона в том, что он гидрофобный и липофобный одновременно — его не смачивают ни вода, ни масла, ни бензин. Такое сочетание свойств позволило использовать тефлон в качестве антипригарных покрытий сковород, и это произвело настоящую революцию в кулинарии и ведении домашнего хозяйства.
Несложно представить, что на протяжении многих десятилетий бытовало мнение, что тефлон (равно как другие перфторуглероды — например, газообразные фреоны) не подвержены метаболизму. Однако в последнее время эта аксиома пошатнулась [22]. В статье, написанной нашими соотечественниками [23], сообщается, что обитающий в Японском море брюхоногий моллюск Littorina brevicola способен не только поедать, но и разлагать частицы микропластиков. Даже политетрафторэтилена! Воистину, живые клетки справляются с любыми трудностями, даже непреодолимыми. Подобные примеры вселяют надежду на то, что со временем наши океаны и планета в целом освободятся от пластиковых отходов. Новые вещества — это новый ресурс, который биосфера не сможет обойти вниманием.

Рисунок 10. К слову о тефлоне. а — Структурная формула перфтор-н-гептана, типичного представителя фторуглеродов. Это один из компонентов дыхательных жидкостей, способных заменять воздух, поскольку в перфторалканах отлично растворяется молекулярный кислород. Политетрафторэтилен является его высшим гомологом. б — Посуда с тефлоновым покрытием. Ее название «Тефаль» является производным от слов «тефлон» и «алюминий». в — ракушки морской улитки L. brevicola. г — Пластиковые бутылки намного удобнее стеклянных. Но утилизация старых бутылок это большая проблема. Один из способов — остроумные поделки для украшения клумб. д — Но есть способ лучше. Если хорошенько поработать над ферментом кутиназой, можно «научить» его гидролизовать ПЭТ до мономеров — терефталевой кислоты и этиленгликоля.
Но политетрафторэтилен используется не только в производстве кухонной посуды. Из него делают медицинские протезы (например, кровеносных сосудов), детали оборудования для работы в особо агрессивных средах. В статье [24] сообщается о том, что тефлоновые протезы подвергаются биодеградации даже в тканях человеческого организма, правда, исключительно медленной, на протяжении многих лет.
О том, насколько важна проблема утилизации пластикового мусора и каких высот достигли работы по биодеградации в мире, свидетельствуют, например, статьи [25–27], первая из которых опубликована в престижнейшем журнале Nature и посвящена ферментативному гидролизу полиэтилентерефталата до мономеров. Про «бутылочный пластик» ПЭТ я уже рассказывал в статье [5]. Авторский коллектив из Франции сравнил активность нескольких ферментов кутиназ, в норме гидролизующих кутин — растительный биополимер на основе длинноцепочечных оксижирных кислот.
Затем была задействована даже не наука — искусство белковой инженерии. Ученые создали фермент, устойчивый к температурам свыше 70 ℃, а самое главное, гидролизующий не кутин, а малопохожий на него ПЭТ. Я не буду подробно рассказывать, что они делали. Об этом в деталях рассказано на «Элементах», в новости «Генномодифицированный природный фермент эффективно разбирает пластик на кирпичики». Достаточно сказать, что была заменена аминокислотная последовательность активного центра фермента и гидрофобного участка связывания с субстратом с применением программ молекулярного докинга и анализом на компьютере нескольких сотен структур белка. Испытывались различные варианты повышения термостабильности фермента — создавались отсутствующие в исходном белке мостики с ионом кальция, дополнительные серные мостики и так далее. Фактически, авторы искусственно осуществили биологическую эволюцию, направленную на освоение нового пищевого субстрата. Но провели ее на несколько порядков быстрее, чем если бы она осуществлялась в естественных условиях. Эволюционнный отбор не обладает даром предвидения. А человек обладает. Это позволяет получать новые адаптированные организмы без большого числа промежуточных форм и эволюционных тупиков, столь характерных для естественного отбора.
А авторами работы [28] описан совсем необычный метаболический путь, осуществляемый генмодифицированной Escherichia coli MG1655 RARE. В нем терефталевая кислота, выделяющаяся при гидролизе ПЭТ, в ряд стадий превращается в ванилин — вкусовую добавку! В настоящее время ванилин получают из ряда природных ароматических соединений, таких как лигнин, эвгенол, куркумин, феруловая кислота. Микробиологическими методами ванилин можно получать и из глюкозы через шикиматный путь — об этом в публикации тоже упоминается. Также в статье подробно расписано, из каких микроорганизмов заимствованы гены, кодирующие фрагменты этого необычного пути — их не менее четырех. Таким образом, пластиковый отход, не разлагающийся в окружающей среде, можно биологическим методом напрямую превращать в пищевой продукт! Впрочем, на этом удивительном случае мне не нужно останавливаться подробно. Он уже представлен на страницах «Биомолекулы», в статье [29].
Подобные примеры удивительны, и порой кажется, что затраченные усилия не оправдывают результат. Просто оторванная от реальности наука ради науки. А мусорные полигоны продолжают расти. Но со временем таких примеров будет больше, а методы белковой инженерии станут рутиной. И именно они позволят очистить планету от рукотворных загрязнений.
Обходной маневр
Знакомство читателей с моими статьями может создать впечатление, что биодеградация — дело очень легкое и происходящее само по себе. Дескать, стоит только появиться на поверхности земного шара новому веществу, как тотчас появляется новый микроб, который это вещество утилизирует. Действительность, конечно, намного сложнее. «Тотчас» может занять несколько тысяч, а то и миллионов лет. Созданию штаммов, осуществляющих биодеградацию, способствует созданная человеком генная инженерия. Например, алкилбензойные кислоты (рис. 11б) с трудом поддаются микробному метаболизму. Дело в том, что промежуточными продуктами деградации этих ксенобиотиков являются алкилкатехины, а они, в свою очередь, ингибируют фермент 2,3-катехиндиоксигеназу — важное звено в метаболизме ароматических соединений. Ученые преодолели это препятствие, выращивая бактерии псевдомонады (рис. 11в, г), в норме расщепляющие бензойную кислоту (рис. 11а) в присутствии сильного мутагена. Некоторые из штаммов мутантов стали вырабатывать измененную 2,3-катехиндиоксигеназу, не ингибируемую алкилкатехинами, и без труда обезвреживать п-этилбензоат [24].
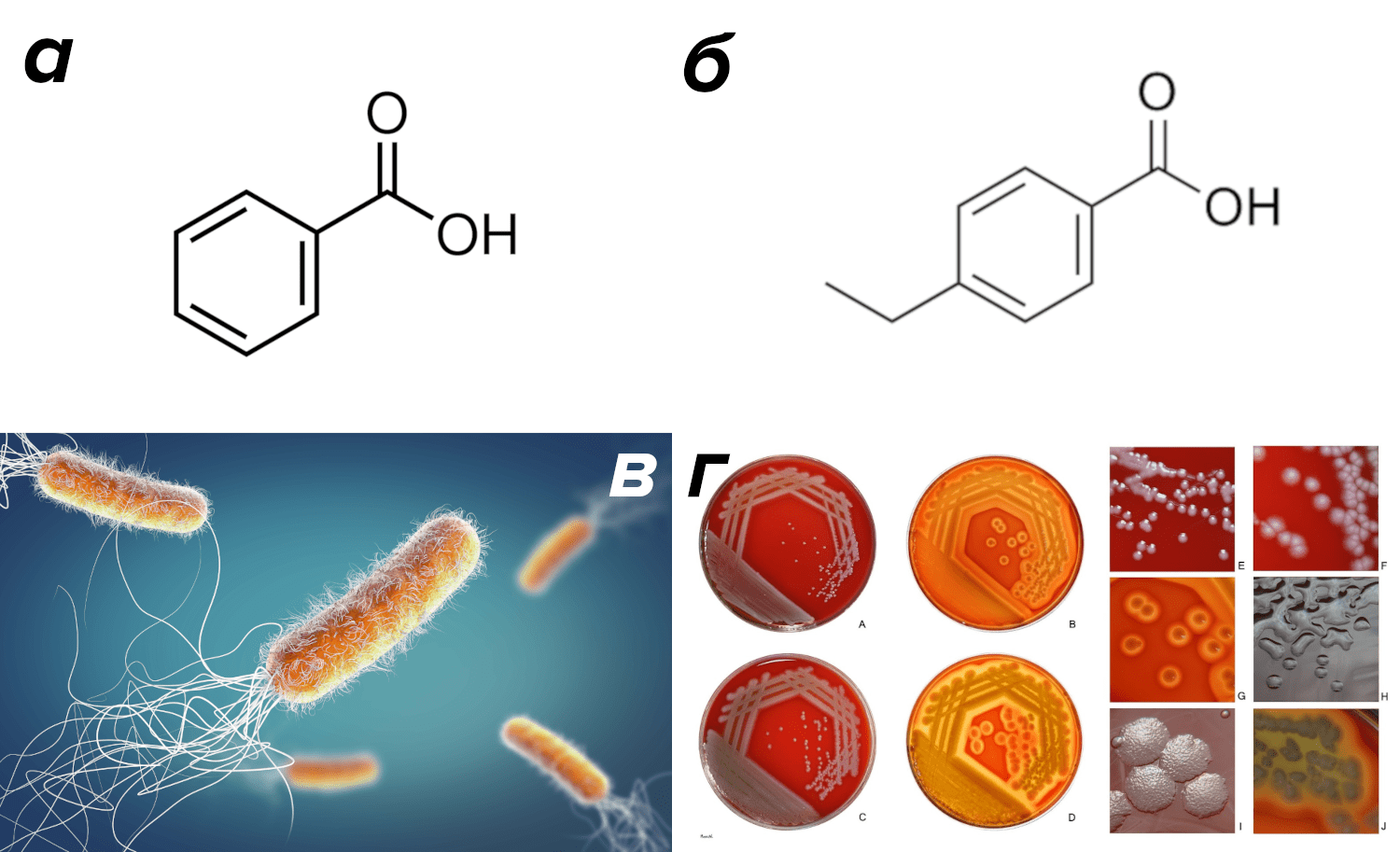
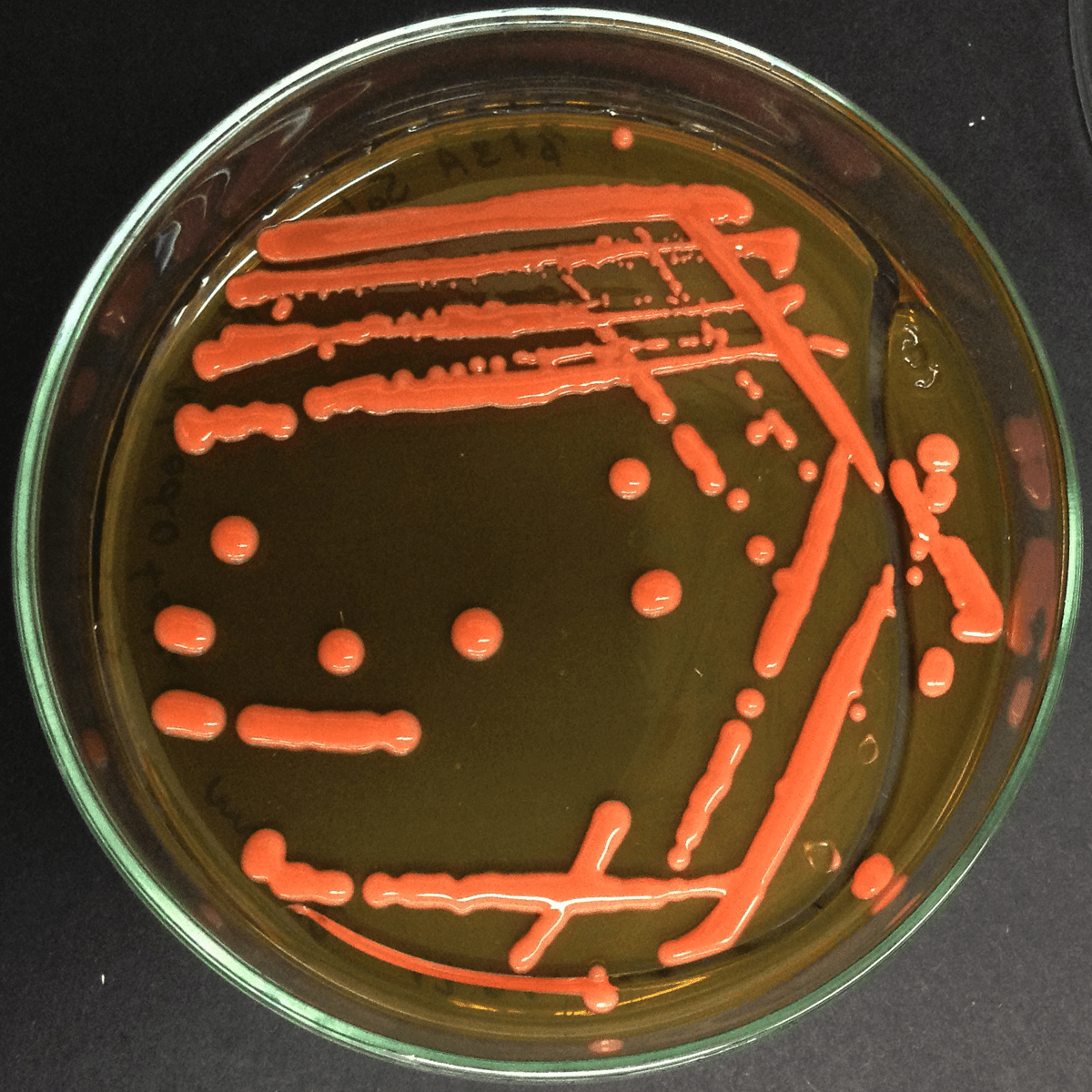
Рисунок 11. Обед из (алкил)бензойных кислот. а — Бензойная кислота, структурная формула. б — П-этилбензойная кислота — один из представителей алкилбензойных кислот, структурная формула. в — Бактерии синегнойные палочки (Pseudomonas aeruginosa), представители обширного рода псевдомонад. Пожалуй, именно Pseudomonas можно назвать «рабочими лошадками» биодеградации. В сообществах активных илов на них приходится около 70% популяции бактериального сообщества. И они способны обезвреживать широчайший спектр поллютантов. г — колонии синегнойной палочки на кровяном агаре.
Распространению в популяциях микробов способности к биодеградации очень способствует такое явление как горизонтальный перенос генов. Прокариотические организмы могут передавать свой наследственный материал не только привычным для нас образом — прямым потомкам, — но и отдаленным родственникам, представителям других штаммов и даже видов. Поэтому многие микробиологи считают понятие «вид» для бактерий условным. В результате, когда генетически модифицированные бактерии, обезвреживающие замещенные бензоаты, были внедрены в сообщество активного ила, то путем горизонтального переноса генов эта способность распространилась среди местной, автохтонной микрофлоры [30].
Двойная польза
В предыдущей статье [9] я рассказывал про то, как ученые «обучают» микробов синтезировать неприродные вещества. Например, бутадиен-1,3 или дивинил (рис. 12в) — основной мономер для синтетических каучуков (о них я также рассказывал в одной из предыдущих статей)). Казалось бы, есть ли смысл повторяться и снова говорить об этом? Тем более, что биотехнологическое производство дивинила пока еще не блещет рентабельностью — это вещество намного дешевле производить из природного газа с использованием катализаторов, этот крупнотоннажный синтез давно доведен до совершенства и остается единственным. Тем не менее, изыскания продолжаются.
В предыдущих статьях я неоднократно рассказывал про биодеградацию ароматических соединений с раскрытием бензольного кольца и образованием очень характерного метаболита — муконовой кислоты (рис. 12а, б). Если присмотреться к формуле этого соединения, то можно увидеть, что муконат — это готовая молекула дивинила, к которой симметрично «пришиты» две карбоксильные группы. Стало быть, есть возможность быстро синтезировать дивинил из муконата известной химикам органикам реакцией декарбоксилирования.
Но химикам-то реакция известна, и проведут они ее без труда. Биотехнологам намного сложнее. Ведь им надо ни много ни мало создать новые ферменты с активностью, не встречающейся в природе! Тем не менее, биотехнологии справились. Излишне говорить, что это биотехнологи из Японии, вооруженные самыми передовыми методами белковой и генной инженерии [1].
Кишечную палочку Escherichia coli (рис. 12д) они путем трансгенеза снабдили ферментом ферулоилдекарбоксилазой, в норме встречающейся у грибов (например, черных аспергиллов (Aspergillus niger) и пекарских дрожжей (Saccharomyces cerevisiae), рис. 12е), способной отщеплять молекулу углекислого газа от ненасыщенных ароматических кислот. Из растительного метаболита феруловой кислоты (рис. 12г) этот фермент образует 4-винилгваякол, обладающий сильным запахом гвоздики и придающий неповторимый аромат некоторым немецким сортам пива. Разумеется, активный центр ферулоилдекарбоксилазы содержит аминокислоты с радикалами, способными «прилипать» к ароматическому ядру молекул субстрата. Подобные процессы на основе гидрофобных взаимодействий описаны в моей статье [31]. Такими аминокислотами являются треонин в положении 395, тирозин 394, аланин 331 и изолейцин 187. Все вместе они удерживают молекулу ароматической кислоты в активном центре, пока другие аминокислотные остатки — глутаминовая кислота 282 и аргинин 173 — отрывают от нее карбоксильную группу.
Японским ученым удалось заменить треонин 395 на гидрофильный глутамин, а тирозин 394 на гистидин, остаток которого обладает мощной каталитической активностью. В результате активный центр фермента полностью утратил способность «отлавливать» гидрофобные ароматические молекулы, зато приобрел новую — связывать и отрывать вторую карбоксильную группу, расположенную напротив первой. То есть, превратился в совершенно новый фермент цис, цис-муконоилдекарбоксилазу с новой активностью, до сих пор не найденной в природе!
Здесь, конечно, напрашивается сравнение с Левшой, подковавшим блоху. Для нас же важен результат этих тончайших экспериментов. Получилась бактерия, способная к биодеградации ароматических веществ (например, бензола, до муконовой кислоты — их естественного метаболита). А далее декарбоксилировать муконовую кислоту до бутадиена — не встречающегося в природе (по крайней мере, не обнаруженного) ценного сырья в производстве каучуков. То есть, одновременно решать две разнонаправленные задачи — обезвреживать опасный ядовитый поллютант и синтезировать ценный продукт.
Правда, пока еще только в теории. В работе японцев кишечная палочка бензол не обезвреживала, а синтезировала ароматический катехин шикиматным путем из глюкозы. Тем не менее, половина задачи — биосинтез дивинила — уже реально решена. Вторую половину решить в принципе можно, поскольку катехин является прямым метаболитом фенола и бензола.
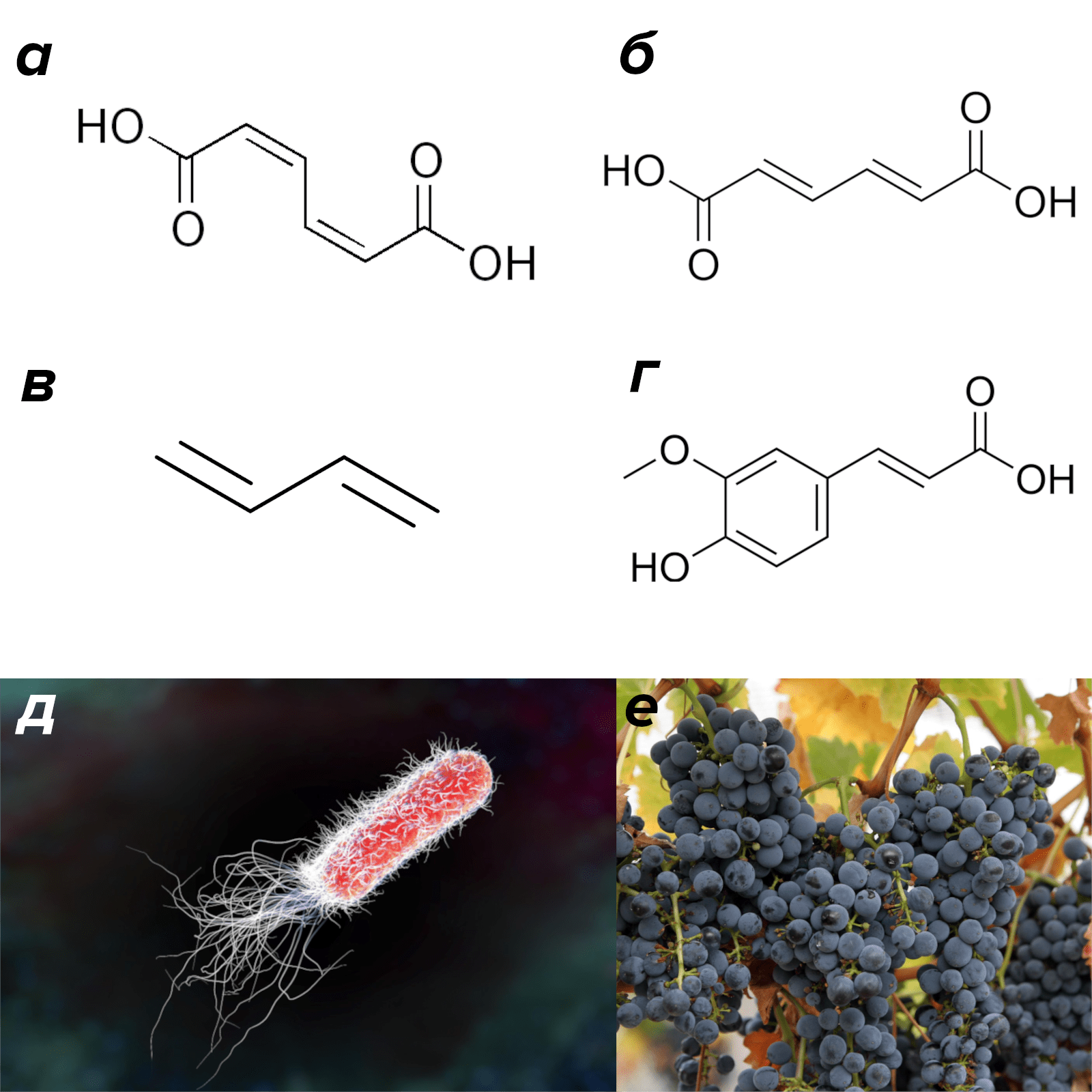
Рисунок 12. Загрязнитель — в полезный продукт. Сверху: Структурные формулы муконовой кислоты: а — цис, цис-изомер, б — транс, транс-. в — Бутадиен-1,3 или дивинил. г — Феруловая кислота. д — Кишечная палочка — самый известный и подробно изученный представитель кишечного микробиома человека. е — Ягоды культурного винограда (Vitis vinifera) покрыты налетом из воска, в котором живут дикие штаммы Saccharomyces cerevisiae — этот вид включает расы винных, пивных и пекарских дрожжей, с глубокой древности и по настоящую пору играющих важнейшую роль в жизни и экономике людей. Только с помощью этих «волшебных» микроорганизмов можно осуществлять выпечку хлеба и других пищевых продуктов из теста, приготовление вина, пива, большинства крепких алкогольных напитков, а в ряде стран и производство технического этилового спирта. А в наше время штаммы S. cerevisiae стали важным объектом научных исследований.
Киборги на страже чистоты
Когда речь заходит о биодеградации поллютантов, ученые и инженеры очень часто, сознательно или нет, противопоставляют биологическую очистку другим методам — химическим, механическим и физическим. Часто приходится слышать довольно типичную фразу: «биодеградация по сравнению с традиционными методами очистки имеет ряд преимуществ». Или наоборот, недостатков. А всегда ли уместно подобное противопоставление? Ведь методы и научные дисциплины «в чистом виде» присутствуют только у нас в голове. Человеческий разум стремится разбить реальность на фрагменты и расставить по полочкам. Природные же явления и процессы почти всегда носят смешанный характер. Это, между прочим, касается и биодеградации.
Исследователи все чаще стали обращать внимание на так называемые нанобиогибриды — агломераты из живых клеток, чаще микробных, и минеральных частиц нанометрового размера. Все-таки, недавний бум нанотехнологий не мог обойти биологию стороной. В оригинальной статье [32] коллектив авторов из Национального университета Ирландии исследовал биодеградацию красителей, в частности, метилового оранжевого, гибридным агломератом из гриба Aspergillus niger (рис. 13в) и частиц сульфида цинка ZnS (рис. 13г). Это вещество известно как природный минерал цинковая обманка или сфалерит и является известным люминофором — способно отдавать поглощенную энергию в форме видимого света. Во времена черно-белого телевидения сульфид цинка широко применялся в кинескопах и люминесцентных лампах. Кроме того, это вещество обладает свойствами полупроводника. В настоящее время сфалерит в виде наночастиц нередко применяется в качестве катализатора — при облучении ультрафиолетом он становится очень активным.
Авторы из Ирландии работали с двумя формами сульфида цинка — полученным чисто химическим путем и путем биосинтеза анаэробными сульфидогенными бактериями (различаются размером частиц и каталитической активностью). По наблюдениям, клетки грибов и кристаллики сульфида цинка, оказавшись вместе в культуральной среде, формируют агломераты за счет электростатического притяжения. Получается такой своеобразный микроб-киборг (рис. 13д), в котором живой и неорганический компонент дополняют друг друга. Как и положено киборгу из фантастических фильмов, это создание оказалось более эффективным, чем гриб и минерал по отдельности. По крайней мере, если речь заходит о биодеградации.
Авторов статьи в первую очередь интересует биодеградация органических красителей. На примере искуственно созданного (неприродного) метилоранжа (краситель метиловый оранжевый, который часто используют в лабораториях в качестве индикатора рН; рис. 13а, б) они показали, что грибок киборг, вооруженный наночастицами сфалерита, при освещении ультрафиолетом обесцвечивает и разлагает красители намного эффективнее, чем просто минерал или просто грибок (рис. 13е). Ферментативная активность и свойства люминофора, аккумулирующего и отдающего энергию света, значительно усиливают действие друг друга. В статье приведен и список продуктов химических превращений метилоранжа. Надо отметить, что это вещество относится к группе диазосоединений, которые отличаются яркой и глубокой окраской (входящая в состав их молекул диазогруппа –N=N– является хроматофором — поглощает видимый свет), но при этом токсичны и обладают канцерогенными свойствами. Их удаление из окружающей среды является важной задачей.
В конце своей весьма интересной статьи авторы приводят целую таблицу примеров биодеградации самых разных веществ при помощи грибков и наночастиц — сульфида и селенида кадмия, сульфида олова, фосфида индия, металлического золота, кобальта, двуокиси титана, оксида железа. А лично у меня при ее чтении возникла мысль, что подобные «киборги» из клеток и минеральных частиц обязательно должны встречаться и в природе. В конце концов, все, изобретенное человеком, природа создала еще раньше. Возможно, какие-то виды грибов вообще не обходятся без минерального довеска, способного «прокачать» мощь их метаболизма. Но их еще предстоит обнаружить.
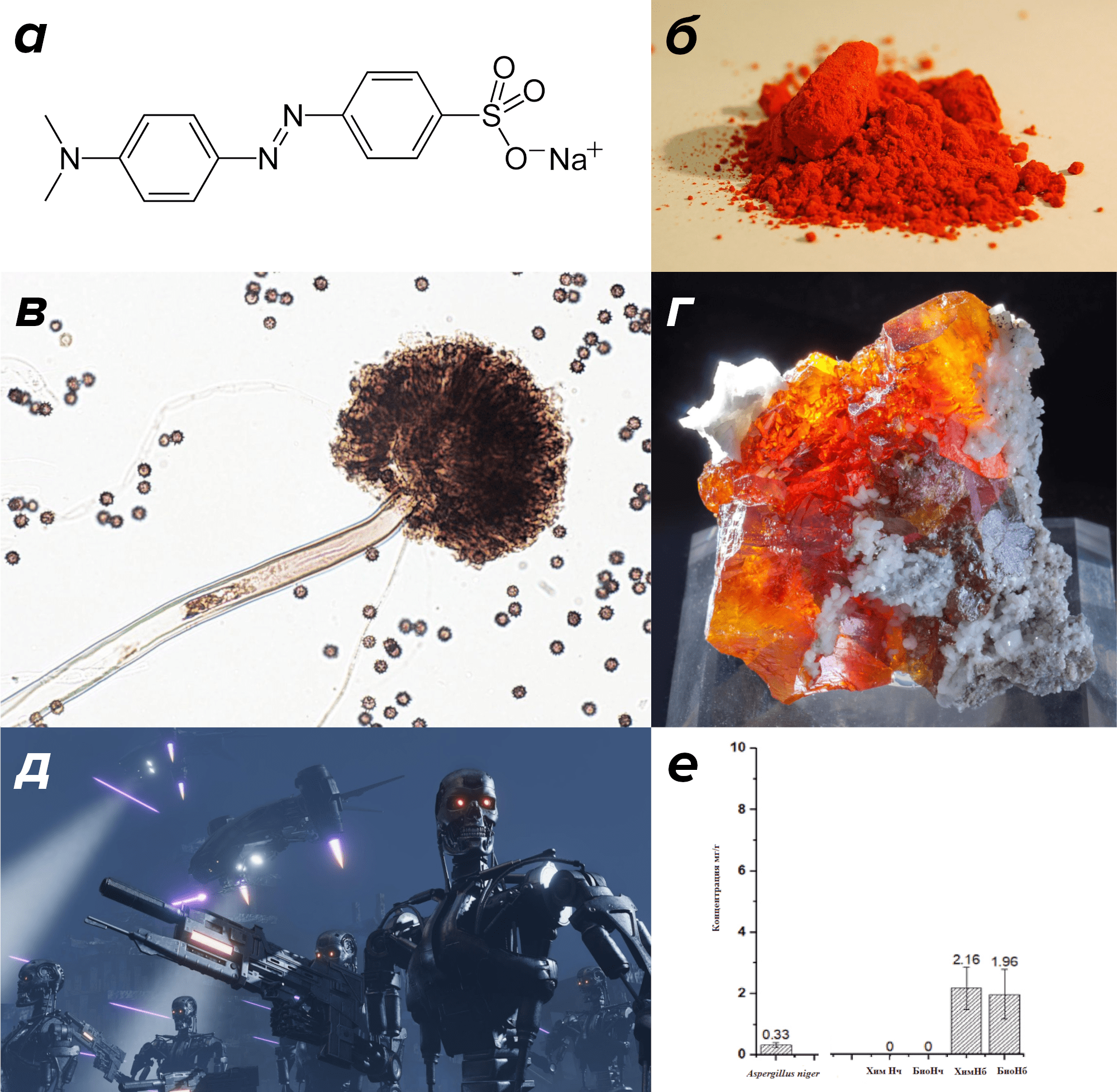
Рисунок 13. Живой организм и минерал отлично дополняют друг друга. Сверху: Краситель метиловый оранжевый: а — структурная формула и б — внешний вид вещества. в — Конидиеносец и споры-конидии черного аспергилла в световом микроскопе. Его диаметр около 40 мкм. г — Минерал сфалерит имеет такое многообразие форм, что его часто путают с другими минералами. Собственно, поэтому его называют «обманкой». Некоторые разновидности камня очень красивы и даже используются в производстве бижутерии, дешевых ювелирных украшений. д — Киборги, оказывается, способны бороться не только с людьми, но и с загрязнениями окружающей среды. е — Эффективность разложения метилоранжа биогибридами черного аспергилла и минерала сфалерита. Хим Нч — наночастицы сфалерита, полученные химическим путем. БиоНч — наночастицы, полученные при помощи бактерий. Нб — соответствующие нанобиогибриды.
Microbe Wiki, Vsegda-pomnim.com, «Дзен», диаграмма из статьи [32] с изменениями
Все дороги ведут к глицерину
Смысл биодеградации любого токсичного или плохо усваиваемого вещества состоит в том, чтобы превращать его в легкоусваиваемые и безвредные соединения. Однако некоторые пути метаболизма, скорее, отражают эстетику, чем практическую полезность. Хотя полезность, выражающаяся в обезвреживании токсиканта, безусловно, присутствует в любом случае. Примеры таких красивых превращений я уже приводил ранее, на примере биосинтеза фолиевой кислоты из анилина, аспарагина из цианида, фруктозы из формальдегида, тирозина из фенола. Кстати, в главе, посвященной формальдегиду, я рассказывал о том, что один из путей его превращений — присоединение к пятиуглеродному сахару ксилулозо-5-фосфату с образованием короткоживущего интермедиата — шестиуглеродного сахара (вероятно, тагатозо-6-фосфата, или сорбозо-6-фосфата, более точную информацию я, к сожалению, не встретил). Который, не покидая активного центра фермента, распадается в нем до двух простейших трехуглеродных сахаров — глицеральдегида и дигидроксиацетона. Этот метаболический путь осуществляется ферментом дигидроксиацетонсинтазой (также именуемым формальдегидтранскетолазой) и характерен для метилотрофных дрожжей, например, Candida boidinii.
Бросается в глаза сходство активности этого фермента и знаменитого рубиско — рибулозобисфосфаткарбоксилазы [33], которая содержится в хлоропластах растений и также синтезирует шестиуглеродный сахар из пятиуглеродного путем присоединения одноуглеродной молекулы. Правда, не формальдегида, а углекислого газа — это кульминационная стадия процесса фотосинтеза. Сам рубиско, между прочим, считается самым распространенным белком в биосфере, и одним из наиболее важных. Авторы из Китая [34] утверждают, что им удалось получить трансгенный табак (рис. 14), вырабатывающий дигидроксиацетонсинтазу дрожжей и очищающий воздух от формальдегида. Факт, безусловно, потрясающе интересный, но мы отвлеклись.

Рисунок 14. Табак культурный (Nicotiana tabacum). Это растение заслужило немало проклятий из-за тяги людей к курению. Но, оказывается, трансгенный табак может приносить пользу, очищая воздух от формальдегида.
«Дзен»
Любой, кто мало-мальски знаком с биохимией, знает, что ближайшим по структуре к трехуглеродным сахарам устойчивым веществом является глицерин — трехатомный спирт пропантриол. Глицерофосфат образуется в живых клетках непосредственно из дигидроксиацетонфосфата, который, в свою очередь, при изомеризации D-глицеральдегид-3-фосфата [35]. Конечно, глицерин — не единственный продукт превращений трехуглеродных сахаров, играющих одну из ключевых ролей в биохимии. И тем не менее, он очень важен. Глицерин в виде сложных эфиров с жирными кислотами входит в состав жиров и фосфолипидов, а также некоторых биополимеров клеточных стенок, таких как гидрофобный кутин у растений, тейхоевые кислоты, составляющие до 75% массы клеточных стенок у бактерий микрококков. Он же может метаболизироваться в сахара (например, глюкозу в процессе глюконеогенеза), аминокислоты, пировиноградную кислоту. Глицерин является компонентом сладких и полусладких вин, образуется в них в результате неполного сбраживания глюкозы (именно он придает сладкий вкус). Сложный эфир глицерина и азотной кислоты — нитроглицерин — является мощной взрывчаткой, на основе которой изготавливают динамит и пироксилин. А также лекарственным средством, эффективно расширяющим коронарные сосуды сердца.
Уникальная амфибия сибирский углозуб (Salamandrella keyserlingii), приспособленный жить в условиях вечной мерзлоты Сибири, Камчатского края, Чукотки и Севера Европейской России, переносит морозы до −55 ℃ благодаря глицерину, который накапливает зимой до 37% от массы печени (рис. 15, справа). Смеси глицерина с водой замерзают при намного более низких температурах, чем оба вещества в чистом виде, и поэтому обладают свойствами антифризов. Очевидно, что это вещество в связанном виде содержится во всех живых организмах и в естественных концентрациях практически безвредно для них. Это позволяет использовать глицерин в качестве компонента практически всех кремов, косметических и увлажняющих средств, туалетного мыла. То есть, превращение ядовитого формальдегида в глицерин означает его полную детоксикацию, причем в одну стадию.

Рисунок 15. Глицерин как биологический антифриз. Слева: Упрощенная схема метаболического превращения трихлорпропана в глицерин. Не показаны промежуточные метаболиты 2,3-дихлор-н-пропанол (после трихлорпропана) и хлорпропиленгликоль (после эпихлоргидрина). Справа: Углозуб сибирский, саламандра длиной около 12 см. Входит в Красную книгу и выживает в вечной мерзлоте Северо-Восточной Евразии благодаря… глицерину!
химическая схема автора и «Животные Красной книги России»

Рисунок 16. Биодеградация хлорорганических соединений сопровождается выделением хлорид-ионов. Первый продукт расщепления это соляная кислота, которая в окружающей среде со временем нейтрализуется. Хлор в природе накапливается в виде стабильных и нетоксичных соединений, таких как хлористый натрий (галит, поваренная соль), сильвин и сильвинит (хлористый калий KCl, часто вместе с NaCl), бишофит (хлористый магний MgCl2), каинит и карналлит (смешанные хлориды и сульфаты магния и калия), хлорапатит (смешанная соль хлорид — фосфат кальция Ca5(PO4)3Cl). Справа: Формула поваренной соли — фрагмент ионной кристаллической решетки.
Но вот что интересно. Существует органический растворитель 1,2,3-трихлорпропан, молекулярная структура которого практически повторяет структуру глицерина — только гидроксильные группы замещены атомами хлора. В принципе, его даже можно получать из глицерина и в лабораторных условиях наверняка получают, хотя в промышленности используются более доступные и дешевые методы хлорирования пропана и пропилена. Наверно, излишне говорить, что подобно большинству органических растворителей (в особенности, содержащих в составе хлор!), трихлорпропан сильно ядовит и обладает канцерогенными свойствами. Трихлорпропан используют как обезжиривающее средство, для снятия красок и лаков. Он прекрасно растворяет гидрофобные вещества. Также он является фунгицидом.
И вот меня заинтересовал вопрос, могут ли микробы метаболизировать трихлорпропан в глицерин? То есть, замещать все атомы хлора на гидроксильные группы, сохраняя без изменений углеродный скелет молекулы? Стал наугад искать в сети и… Нашел статьи авторов из Чехии, в которых представлен созданный искусственно метаболический путь, ведущий от трихлорпропана к глицерину [5], [36] (рис.15, слева). Осуществляет его генмодифицированный штамм Agrobacterium radiobacter AD1. Промежуточными продуктами, как и следовало ожидать, являются хлорированные спирты, которые легко отщепляют атомы хлора и превращаются в трехчленные гетероциклы оксираны. Про простейший оксиран, окись этилена, я уже рассказывал в работе [5]. Безусловно, путь не только имеет практическую полезность, превращая ядовитую жидкость в пребиотик, но и восхищает изяществом.
Здесь следует остановиться еще на одном моменте. Одним из промежуточных продуктов представленного метаболического пути является эпихлоргидрин (хлорметилоксиран) — важное сырье для производства эпоксидных смол. Собственно, трихлорпропан обычно получают в качестве побочного продукта производства эпихлоргидрина. Значит, глицерин является, в том числе, продуктом биодеградации эпихлоргидрина [37]! А заодно эпоксидных смол, образующихся при реакции эпихлоргидрина и бисфенолов — такие смолы входят в состав широко применяемых в быту эпоксидных клеев [38], [39].
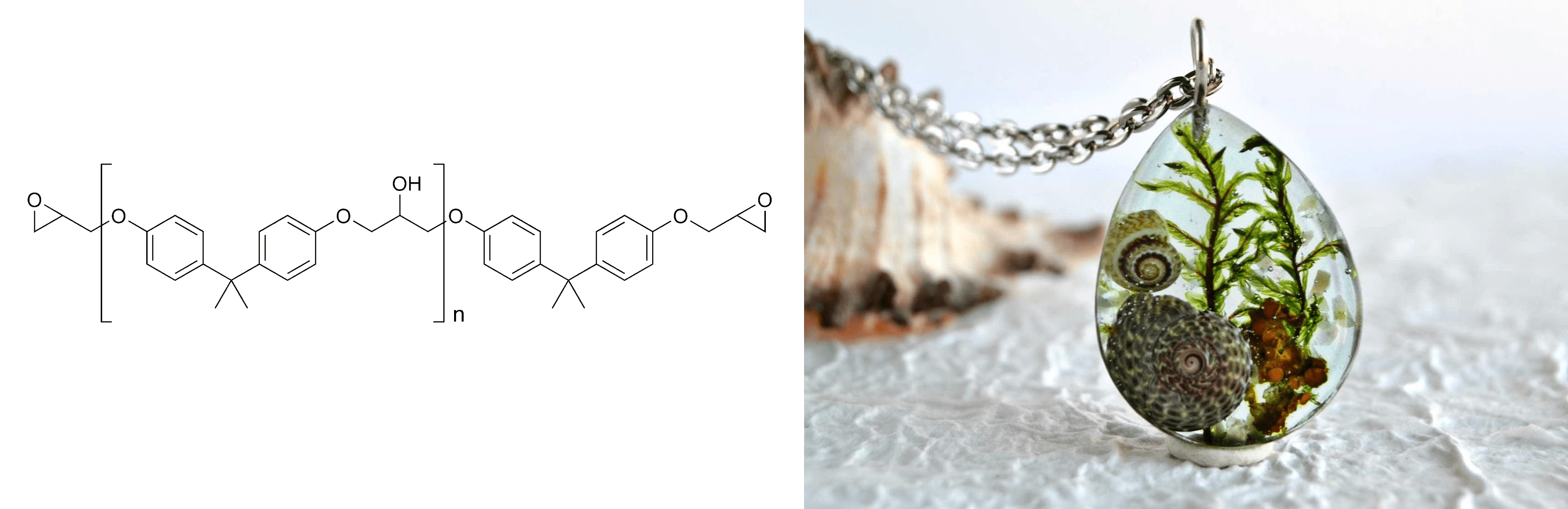
Рисунок 17. Всё про «эпоксидку». Слева: Структурная формула эпоксидной смолы. В данном случае, это самая распространенная ее марка — сополимер эпихлоргидрина и бисфенола А. Низкомолекулярные олигомеры представляют собой вязкие жидкости с очень сильной адгезией. На их основе готовят широко востребованные эпоксидные клеи. Высокомолекулярные смолы представляют собой твердые прозрачные стекловидные массы. Справа: Ими часто заливают биологические препараты для долгого хранения. Застывая, смола формирует капсулу, защищающую образец от внешних воздействий. Залитые эпоксидной смолой растения, раковинки и насекомых часто используют в качестве украшений.
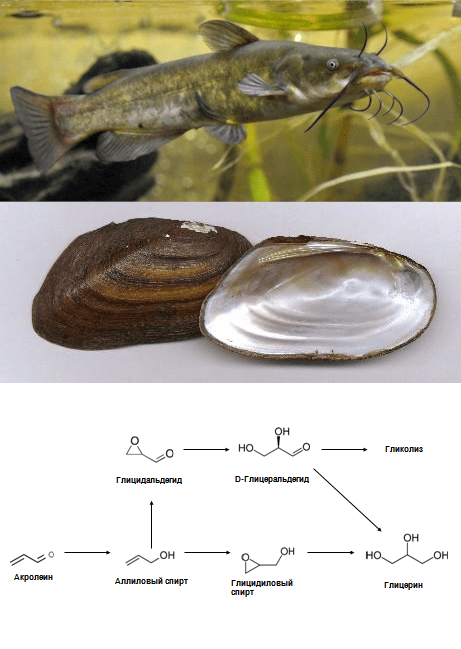
Рисунок 18. Жизнь против огня. Пиролиз превращает глицерин в акролеин, а живые организмы наоборот. Сверху: Канальный сом Ictalurus punctatus. В центре: Створки раковины мидии Elliptio complanata. Это представители американской фауны. Впрочем, наши виды рыб и моллюсков, вероятно, также способны превращать акролеин в глицерин. Снизу: Метаболические пути акролеина.
SpinningPRO, Freshwater Molluscan Shells, рисунок автора по [40], [41]
Но глицерин является конечным продуктом биодеградации не только трихлорпропана. Токсичный лакриматор и гербицид акролеин, применявшийся в качестве химического оружия в Первую мировую войну, вступает в многообразные метаболические пути как у бактерий, так и в организме высших позвоночных. Наиболее интересен путь, в котором акролеин восстанавливается до аллилового спирта. Далее спирт окисляется по двойной связи до глицидола, а последний гидролизуется с раскрытием цикла до безвредного глицерина [40] (рис. 18). Но параллельно акролеин вступает в другие метаболические пути с образованием акриловой, пропионовой и пропиоловой кислот — во многом, этим определяется его токсическое действие. Этим путем акролеин обезвреживается в организме пресноводных рыб и беспозвоночных — раков и двустворчатых моллюсков. В статье [41] описано очень близкое, но отличное превращение акролеина — в печени млекопитающих он окисляется до глицидальдегида, который далее гидролизуется до глицеральдегида. Последний вступает в гликолитический путь и усваивается организмом. Любопытно, что впервые люди познакомились с акролеином, образующимся при пиролизе сала, жиров и растительных масел во время прожаривания пищи. Именно он в составе дыма раздражает глаза и дыхательные пути. То есть, превращение акролеина в глицерин — метаболический путь, обратный превращению глицерина в акролеин при пиролизе!
Подытоживая сказанное, приходим к выводу, что глицерин является конечным продуктом превращений как минимум пяти токсикантов, причем совершенно различных по структуре и свойствам — формальдегида, акролеина, эпихлоргидрина, трихлорпропана и эпоксидных смол. А если учесть, что в настоящее время изучаются новые перспективные полимеры на основе глицерина [42], это количество в будущем может возрасти и дальше.
Биодеградация или биовыщелачивание?
У знакомого с моими работами читателя может сложиться впечатление, что биодеградация — это очень узкое направление, решающее исключительно проблемы защиты окружающей среды. И никакое многообразие конкретных примеров не меняет это положение дел. Но так ли это?
Действительно, биодеградация — явление слишком широкое и многообразное, чтобы служить только одной цели. Мы прекрасно знаем, что любые природные явления оказывают множество воздействий на человека. И биодеградация не исключение. Кстати, даже терминология многообразна. В одной из статей [8] мы уже познакомились с частным случаем биодеградации — явлением биокоррозии металлов и строительных материалов. Теперь познакомимся с биовыщелачиванием.
Как известно, жизнь стремится занять все доступное пространство и использовать все доступные ресурсы. А на поверхности нашей планеты самым доступным ресурсом является сама земная кора, сложенная разнообразными минеральными породами и содержащая в своем составе все биогенные элементы. Но как их использовать? В нашем сознании горная порода ассоциируется с чем-то очень прочным и неприступным. С твердыней. Но на практике невидимые глазом микробы интенсивно разрушают горные породы, принимают активное участие в их выветривании. Огромная группа силикатных бактерий извлекают из минералов металлы (например, марганец из граната, о чем я уже рассказывал в прошлогодней статье [9]). Другие — солюбилизаторы фосфатов — переводят в растворимую форму фосфатные минералы, в обычных условиях практически нерастворимые в воде [43]. Тем самым, снабжают биосферу ценнейшим элементом фосфором. Ведь дефицит фосфора обусловлен как раз низкой растворимостью большинства его солей, и, как следствие, низкой биологической доступностью. А вовсе не редкостью данного элемента.
Для живых организмов, населяющих аридные зоны нашей планеты, стратегически важным ресурсом является вода, которую они извлекают буквально из любых источников. Включая даже такой труднодоступный, как кристаллогидраты. Растения и цианобактерии, произрастающие в пустыне Атакама на севере Чили — одной из самых засушливых точек земного шара, — способны извлекать воду из кристаллической решетки минерала гипса CaSO4·2H2O, превращая его в безводный сульфат кальция — минерал ангидрит, и вызывая фазовый переход [44], [45]. Гипс содержит до 20,8% воды и является важным ее запасом в засушливых условиях (рис. 19В, Г, Д).
Как правило, микроорганизмы подвергают минерал химическому воздействию. Самый простой и эффективный способ — образование кислот, растворяющих минерал. Скажем, солюбилизирующие фосфат бактерии или грибы выделяют щавелевую кислоту, и ценные фосфаты в минерале замещаются малоценными с биологической точки зрения оксалатами [43]. Другая стратегия — выработка сидерофоров, эффективных комплексообразователей с ионами переходных металлов — например, двухвалентного железа, необходимого живым организмам.
Таким образом, живая природа эффективно использует литосферу как источник сырья. Но ведь человек тоже испокон веков добывает полезные ископаемые для своих нужд, и интенсивность добычи возрастает с каждым годом. Есть ли возможность использовать микроорганизмы для этой цели? Конечно есть. Растворяя минерал, микробы извлекают из него не только нужное для себя, а все, что в нем содержится. Например, я встретил работы, в которых минералы сподумен и лепидолит подвергали микробиологической обработке — грибами черными аспергиллами, дрожжами, бактериями — и извлекали ценный металл литий [46], [47] (рис. 19А, Б).
Литий применяется в производстве аккумуляторов, и цена на него резко подскочила вверх в последние годы. Соответственно, вырос интерес к его добыче. Современные методы извлечения этого элемента из руд уже неэффективны, и ведется поиск новых. Среди них — биологический метод, получивший название «биовыщелачивания руд». И хотя литий, в отличие от своих ближайших соседей по Периодической таблице — натрия и калия, — практически не используется живыми организмами, и более того, токсичен для них даже в низких дозировках, тем не менее, он извлекается из минералов при биовыщелачивании. И это облегчает его добычу человеком.
Таким образом, в широком смысле биодеградация — это не только защита окружающей среды от токсичных поллютантов, но и переработка полезных ископаемых. А дальнейшее развитие биотехнологии наверняка откроет для нее массу новых и неожиданных применений.
Биодеградация с человеческим лицом
В своих статьях я, кажется, исходил биодеградацию вдоль и поперек. При этом выяснилось, что в ней участвуют представители практически всех таксономических групп живых организмов — от бактерий до коров. Безусловно, закономерен вопрос: человек (Homo sapiens sapiens) может осуществлять биодеградацию? Вопрос с подвохом. Потому, что, разумеется, людей никто не заставит обезвреживать токсины в организме. Вообще, эксперименты на людях, слава Богу, запрещены.
Поэтому вопрос следует перефразировать. Можно ли создать, скажем, съедобную полимерную упаковку для пищевых продуктов? Чтобы съедать их вместе с упаковкой. Тогда проблема загрязнения окружающей среды решится сама собой!

Рисунок 20. В ближайшем будущем можно будет кушать сладости вместе с оберткой!
Оказывается, это возможно. Коллектив исследователей из Индии разработал пищевую пленку на основе природных пищевых веществ — крахмала и растительного масла [49] (рис. 20). По виду и свойствам она мало отличается от привычной нам полиэтиленовой пленки. Но ее можно есть! Это, конечно, сенсация. Но только по причине того, что данный пример — первый. Мне кажется, со временем таких съедобных и безвредных для окружающей среды материалов станет много и они будут чем-то совсем привычным.
Безусловно, уместно вспомнить хирургические нити из поликапролактона, которые по прошествию времени сами растворяются в тканях человека. О них я уже рассказывал ранее [8].
Здесь мы подошли к развилке, соединяющей биодеградацию с другим, принципиально противоположным подходом к защите окружающей среды. Можно акцентировать внимание не на создании микробов, разлагающих все на свете, а на разработке материалов, легко разлагающихся в окружающей среде. Например, повсеместно заменять полиэтиленовые пленки на пленки из биоразлагаемых полимеров полигидроксиалканоатов. Или вернуться к старой доброй бумаге из целлюлозы. Для ее производства больше не понадобится вырубать леса — с производством целлюлозы высокого качества прекрасно справляются некоторые бактерии.
Существуют ли неприродные вещества?
В своих предыдущих статьях я много писал о том, что разнообразие биологической химии намного больше, чем мы привыкли думать. Просто сила инерции нашего мышления не поспевает за развитием аналитического оборудования, позволяющего находить в живых организмах все новые соединения, содержащиеся, возможно, в исключительно малых концентрациях.
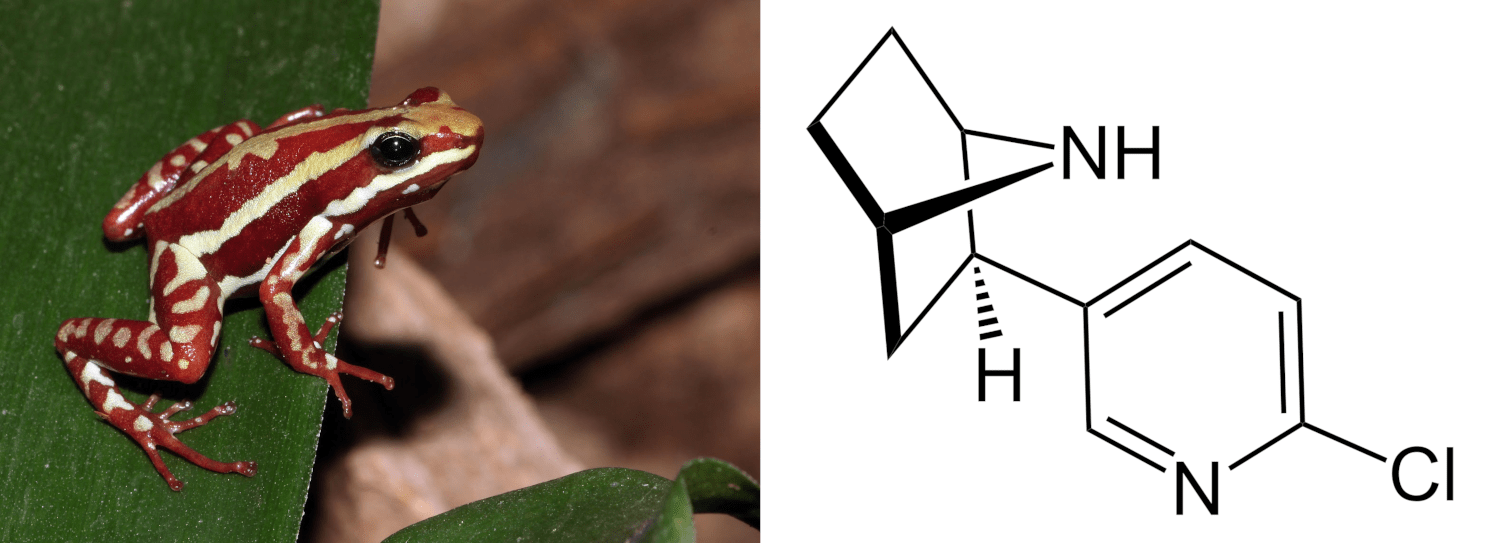
Например, когда в 1974 году из кожных покровов сильно ядовитой южноамериканской лягушки франтоватого древолаза Epipedobates tricolor был выделен алкалоид, позже названный эпибатидином (рис. 21А), исследователи вначале усомнились в правильности интерпретации результатов анализа. Решили, что произошло загрязнение образца. Слишком неожиданной оказалась его структура. Ведь эпибатидин до сих пор является единственным известным природным хлорпиридином [50]! Это ядовитое соединение, взаимодействующее с никотиновыми и мускариновыми рецепторами. Исследования показали, что эпибатидин оказывает наркотическое действие, близкое к действию кокаина. Болеутоляющее действие эпибатидина в 200 раз сильнее, чем у морфина. Однако его токсичность намного выше, что делает применение эпибатидина крайне опасным.
Специфика лягушек древолазов в том, что они не синтезируют яды сами, а получают их (или, что более вероятно, их менее токсичные предшественники) с пищей — определенными насекомыми и клещами. Эти беспозвоночные, вероятно, получают их из пищевых растений или симбиотической микрофлоры. С другой стороны, индейцы — коренные жители Южной и Центральной Америки — обрабатывают ядом лягушек стрелы и дротики. То есть, ядовитые соединения проходят долгий и не до конца изученный путь.
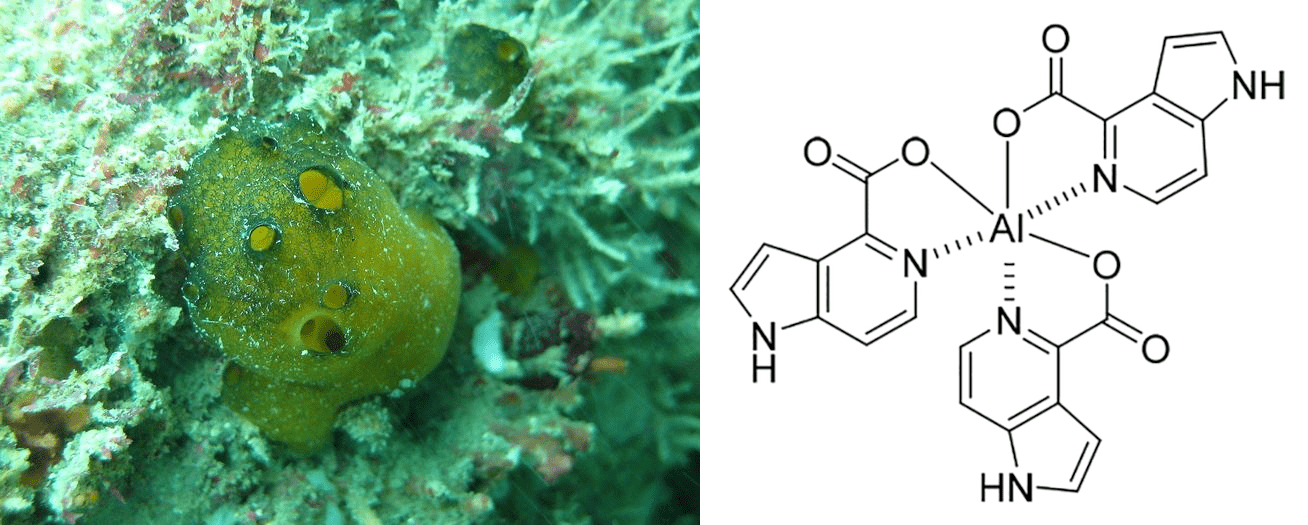
Губка Guitarra fimbriata, произрастающая у побережья Курильских островов, содержит уникальные метаболиты гвитаррины А–Е, представляющие собой алкалоиды редкой 5-азаиндольной природы (рис. 21Б). А также алюминумгвитаррин А (комплекс Al3+ с гвитаррином А [51]), относящийся к редчайшим веществам биологической природы, содержащим в своем составе алюминий. Судя по тому, что этот комплекс формируется спонтанно, а концентрация ионов алюминия в воде исключительно мала (он хорошо растворяется только в сильнокислой среде), у лиганда исключительно высокое сродство к Al3+. Гвитаррины являются ингибиторами бактериальных щелочных фосфатаз и, вероятно, защищают свои губки от инфекций, вызываемых морскими бактериями [52]. Кстати, соли алюминия тоже обладают антимикробной активностью и до недавнего времени их добавляли в дезодоранты (позже стали исключать из-за высокой токсичности). О свойствах алюминумгвитаррина известно мало, но, возможно, это вещество наносит по патогенным бактериям двойной удар за счет совместного антибактериального действия металла и лигандов.
А морская губка Placospongia sp., произрастающая в Корейском проливе, продуцирует необычный метаболит фосфойодин А, молекула которого содержит сразу три экзотические для живой природы типа групп — фосфонатную, две ацетиленовые и атом йода [53] (рис. 21В). Каждая из этих групп по отдельности редко встречается в биологических веществах. А сочетание всех трех делает фосфойодин поистине уникальной молекулой — настоящим биохимическим шедевром.
Другой любопытный пример — драгоценный камень опал (рис. 21Г). Именно от него пошел термин «опалесценция», и не зря. Некоторые камни обладают удивительной игрой и переливами красок. По своей природе опал — это водный раствор поликремниевой кислоты состава SiO2·nH2O: жидкость, но настолько вязкая, что ведет себя как аморфное твердое вещество. Опалы надо регулярно погружать в воду, чтобы они впитывали ее; иначе они высохнут и растрескаются. Но при избыточной влажности они набухают и теряют привлекательность — вот такое капризное украшение.
На сайте «Элементы» 1 апреля 2016 года вышла статья про то, что ученые получили мутантное растение резуховидку, накапливающее в лепестках цветков силикаты в таком количестве, что цветок превращается в кусочек опала. В готовое ювелирное украшение! Жаль, что статья оказалась первоапрельской шуткой. Впрочем, самые удачные шутки, как известно, те, которые без обмана. И здесь сказана правда, хотя в преувеличенном, гротескном виде. Живые организмы, особенно растения, действительно накапливают силикаты, а некоторые формируют опалы. Существует даже определение «биогенные опалы». Правда, внешне они мало привлекательны, но по химической природе самые настоящие. Близкий к опалам минерал формирует панцири диатомовых водорослей — пожалуй, крупнейшим «специалистам по кремнию» среди живых существ [54] (рис. 21Д).
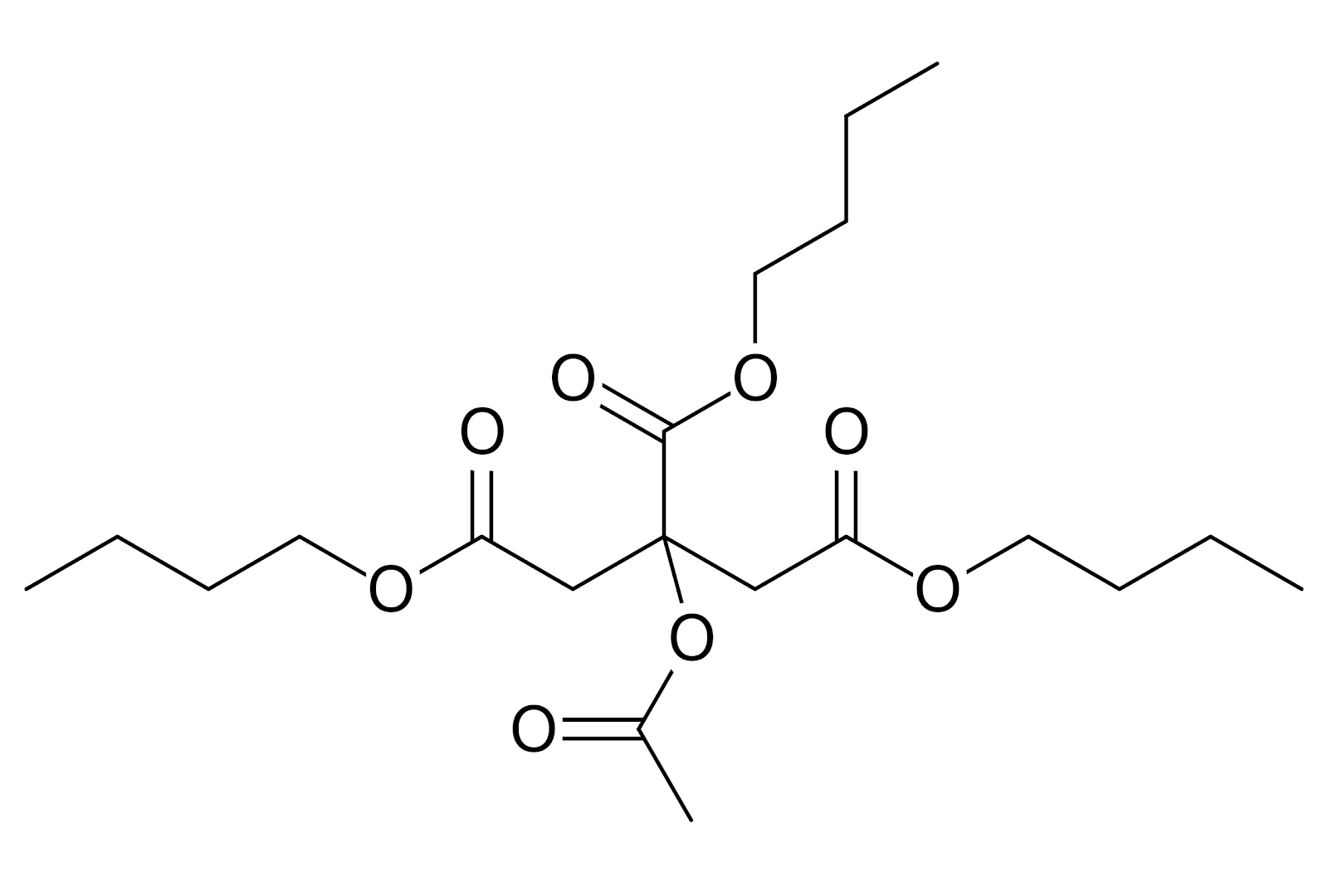
Но человек не только постоянно открывает новые природные вещества. В последние годы методами генных манипуляций люди создают промышленные штаммы микробов, производящие вещества, которые ранее создавались только химическим синтезом. То есть, мы сами обогащаем природную химию. Примером может послужить О-ацетилтри-н-бутил-цитрат — малотоксичный нелетучий растворитель, используемый в качестве пластификатора и входящий в состав лаков для ногтей (рис. 21Е). Все предшественники этой молекулы — лимонная и уксусная кислоты и спирт н-бутанол — известны в природе (рис. 21Ж и З). Последний является продуктом ацетоно-бутанолового брожения, а кислоты вообще являются ключевыми звеньями метаболизма. Казалось бы, синтезировать такую молекулу живой клетке — раз плюнуть. Тем не менее, информации о нахождении ацетилтрибутилцитрата в природе я не нашел. Видимо, живым клеткам это вещество не сильно нужно, и тратить на него ценный цитрат жалко.
Это конечно, вовсе не значит, что таких организмов в природе нет и не было. Но можно сказать однозначно — они редки и не попадались исследователям. Возможно, неоднократно появлялись в истории Земли, а затем исчезали. Во всяком случае, сходные с трибутилацетилцитратом соединения вырабатываются живыми организмами для химической коммуникации в качестве феромонов.
Зато я встретил китайский патент [55], в котором описывается процесс ферментативного синтеза предшественника растворителя трибутилцитрата из лимонной кислоты и бутанола при помощи липаз. В принципе, можно получить и искомый ацетилтрибутилцитрат, если обработать трибутилцитрат, полученный ферментативным путем, специально подобранной ацетилтрансферазой.
Заключение
Перечисленные примеры, на первый взгляд, связаны между собой очень слабо. Тем не менее, это отдельные мазки из огромной картины нашей биосферы, наводненной непрестанно идущими процессами метаболизма. И эта крошечная выборка из общего многообразия свидетельствует о том, что биологическая химия охватывает химию в целом. Каждый класс веществ в ней представлен. И есть уверенность в том, что дальнейшее совершенствование приборного парка позволит обнаружить в живых организмах и те классы веществ, которые в них до сих пор не найдены. Пускай это будут следовые концентрации или даже продукты превращений крайне нестабильных промежуточных продуктов. Соответственно, живые организмы способны воздействовать на практически любые вещества. Чего стоит пример с тефлоном, который долгое время считался абсолютно не подверженным метаболическим превращениям. Но в последние годы поступают доказательства того, что даже он им подвергается.
Мы недооценивали возможности биосферы. И с этим нужно считаться. Принесет ли нам это осознание больше благ или зол? Покажет будущее. По горячим следам правильные выводы не сделать. Одно можно прогнозировать наверняка. В будущем роль биотехнологии будет возрастать, и она в той или иной степени охватит всю созданную человеком технологию в целом. И принесет людям новые, невиданные до сих пор возможности. Но, как и любая технология, биотехнология не сделает людей счастливыми. Счастье люди должны создавать для себя и друг друга сами. Любые технические приемы, даже с приставкой «био», не решают проблему счастья, а только предоставляют новые возможности для этого.
Литература
- Yutaro Mori, Shuhei Noda, Tomokazu Shirai, Akihiko Kondo. (2021). Direct 1,3-butadiene biosynthesis in Escherichia coli via a tailored ferulic acid decarboxylase mutant. Nat Commun. 12;
- Michael Thomas Zumstein, Arno Schintlmeister, Taylor Frederick Nelson, Rebekka Baumgartner, Dagmar Woebken, et. al. (2018). Biodegradation of synthetic polymers in soils: Tracking carbon into CO 2 and microbial biomass. Sci. Adv. 4;
- Биодеградация белого фосфора: как яд стал удобрением;
- Биодеградация ксенобиотиков как самозащита природы;
- Являются ли ксенобиотики ксенобиотиками? Одна из сторон разнообразия природных соединений;
- Раздумья о природной и неприродной химии;
- Биодеградация: что в ней удивительного?;
- От биодеградации к сюрпризам биохимии;
- Многоликая биодеградация;
- Биологический энциклопедический словарь / Ред. М.С. Гиляров // Советская энциклопедия, 1989. — 864 с.;
- Белюченко И.С. Экология в терминах и понятиях // Краснодар: Изд КубГАУ, 2000. — 496 с.;
- Фролов Ю.М. (2007). ДДТ возвращается. Наука и жизнь. 7, с. 52;
- Mariusz Cycoń, Marcin Wójcik, Zofia Piotrowska-Seget. (2011). Biodegradation kinetics of the benzimidazole fungicide thiophanate-methyl by bacteria isolated from loamy sand soil. Biodegradation. 22, 573-583;
- Zhengnan Long, Xiuguo Wang, Yingjun Wang, Huawei Dai, Changhao Li, et. al. (2021). Characterization of a novel carbendazim-degrading strain Rhodococcus sp. CX-1 revealed by genome and transcriptome analyses. Science of The Total Environment. 754, 142137;
- William R. Cullen. (2014). Chemical Mechanism of Arsenic Biomethylation. Chem. Res. Toxicol. 27, 457-461;
- Geoffrey Michael Gadd. (2010). Metals, minerals and microbes: geomicrobiology and bioremediation. Microbiology. 156, 609-643;
- Marina Fomina, John M. Charnock, Stephen Hillier, Rebeca Alvarez, Francis Livens, Geoffrey M. Gadd. (2008). Role of fungi in the biogeochemical fate of depleted uranium. Current Biology. 18, R375-R377;
- Florin Musat, Heinz Wilkes, Astrid Behrends, Dagmar Woebken, Friedrich Widdel. (2010). Microbial nitrate-dependent cyclohexane degradation coupled with anaerobic ammonium oxidation. ISME J. 4, 1290-1301;
- Акименко В.К. Полигидроксиалканоаты микроорганизмов: поиск природных и конструирование рекомбинантных штаммов-продуцентов, биосинтез, использование // Институт биохимии и физиологии микроорганизмов им. Г.К. Скрябина РАН. М.: ТиРу, 2015. — 284 с.;
- R. Margesin, F. Schinner. (2001). Biodegradation and bioremediation of hydrocarbons in extreme environments. Applied Microbiology and Biotechnology. 56, 650-663;
- R J Kolenc, W E Inniss, B R Glick, C W Robinson, C I Mayfield. (1988). Transfer and expression of mesophilic plasmid-mediated degradative capacity in a psychrotrophic bacterium. Appl Environ Microbiol. 54, 638-641;
- Lawrence P. Wackett. (2021). Why Is the Biodegradation of Polyfluorinated Compounds So Rare?. mSphere. 6;
- Vyacheslav S. Odintsov, Alexander A. Karpenko, Maxim A. Karpenko. (2022). Degradation of micro-nano-sized polytetrafluoroethylene and acrylic fluorinated copolymer particles in the periwinkle digestive tract. Environ Sci Pollut Res. 30, 25972-25980;
- I. Flessenkämper, K.-M. Müller. (2004). Biodegradation einer PTFE-Prothese. Zentralbl Chir. 126, 151-156;
- V. Tournier, C. M. Topham, A. Gilles, B. David, C. Folgoas, et. al. (2020). An engineered PET depolymerase to break down and recycle plastic bottles. Nature. 580, 216-219;
- Åsa M. Ronkvist, Wenchun Xie, Wenhua Lu, Richard A. Gross. (2009). Cutinase-Catalyzed Hydrolysis of Poly(ethylene terephthalate). Macromolecules. 42, 5128-5138;
- Sintawee Sulaiman, Dong-Ju You, Eiko Kanaya, Yuichi Koga, Shigenori Kanaya. (2014). Crystal Structure and Thermodynamic and Kinetic Stability of Metagenome-Derived LC-Cutinase. Biochemistry. 53, 1858-1869;
- Joanna C. Sadler, Stephen Wallace. (2021). Microbial synthesis of vanillin from waste poly(ethylene terephthalate). Green Chem. 23, 4665-4672;
- Ванильные мечты о пластике;
- Juan L. Ramos, Alain Wasserfallen, Keith Rose, Kenneth N. Timmis. (1987). Redesigning Metabolic Routes: Manipulation of TOL Plasmid Pathway for Catabolism of Alkylbenzoates. Science. 235, 593-596;
- Роль слабых взаимодействий в биополимерах;
- Uddandarao Priyanka, Piet N.L. Lens. (2022). Light driven Aspergillus niger-ZnS nanobiohybrids for degradation of methyl orange. Chemosphere. 298, 134162;
- Волонтер фотосинтеза;
- Su-Qin Xiao, Zhen Sun, Sha-Sha Wang, Jing Zhang, Kun-Zhi Li, Li-Mei Chen. (2012). Overexpressions of dihydroxyacetone synthase and dihydroxyacetone kinase in chloroplasts install a novel photosynthetic HCHO-assimilation pathway in transgenic tobacco using modified Gateway entry vectors. Acta Physiol Plant. 34, 1975-1985;
- Yosuke Koga, Hiroyuki Morii. (2007). Biosynthesis of Ether-Type Polar Lipids in Archaea and Evolutionary Considerations. Microbiol Mol Biol Rev. 71, 97-120;
- Ghufrana Samin, Martina Pavlova, M. Irfan Arif, Christiaan P. Postema, Jiri Damborsky, Dick B. Janssen. (2014). A Pseudomonas putida Strain Genetically Engineered for 1,2,3-Trichloropropane Bioremediation. Appl Environ Microbiol. 80, 5467-5476;
- A. J. Van Den Wijngaard, D. B. Janssen, B. Witholt. (1989). Degradation of Epichlorohydrin and Halohydrins by Bacterial Cultures Isolated from Freshwater Sediment. Microbiology. 135, 2199-2208;
- Noam Eliaz, Eliora Ron, Michael Gozin, Sara Younger, Dvora Biran, Noam Tal. (2018). Microbial Degradation of Epoxy. Materials. 11, 2123;
- Anila Bello, Yalong Xue, Dhimiter Bello. (2021). Urinary biomonitoring of occupational exposures to Bisphenol A Diglycidyl Ether (BADGE) – based epoxy resins among construction painters in metal structure coating. Environment International. 156, 106632;
- Adrian J. Nordone, Timothy A. Dotson, Martin F. Kovacs, Rebecca Doane, Ron C Biever. (1998). Metabolism of [14C]acrolein (Magnacide H® herbicide): Nature and magnitude of residues in freshwater fish and shellfish. Enviro Toxic and Chemistry. 17, 276-281;
- O Faroon, N Roney, J Taylor, A Ashizawa, MH Lumpkin, DJ Plewak. (2008). Acrolein health effects. Toxicol Ind Health. 24, 447-490;
- Shailja Goyal, Nacú B Hernández, Eric W Cochran. (2021). An update on the future prospects of glycerol polymers. Polymer International. 70, 911-917;
- Xia Kang, Laszlo Csetenyi, Geoffrey Michael Gadd. (2020). Monazite transformation into Ce‐ and La‐containing oxalates by Aspergillus niger. Environmental Microbiology. 22, 1635-1648;
- Wei Huang, Emine Ertekin, Taifeng Wang, Luz Cruz, Micah Dailey, et. al. (2020). Mechanism of water extraction from gypsum rock by desert colonizing microorganisms. Proc Natl Acad Sci USA. 117, 10681-10687;
- Adrián Escudero, Sara Palacio, Fernando T. Maestre, Arantzazu L. Luzuriaga. (2015). Plant life on gypsum: a review of its multiple facets. Biological Reviews. 90, 1-18;
- Marcinčáková R., Mražíková A., Velgosová O., Kaduková J., Vojtko M., Holub M. The Influence of Spore Age of Aspergillus Niger on Lithium Dissolution from Lepidolite // Inżynieria Mineralna. 2014. Vol. 15. No.2. P. 211-216;
- I. Rezza, E. Salinas, V. Calvente, D. Benuzzi, M.I. Sanz de Tosetti. (1997). Extraction of lithium from spodumene by bioleaching. Letters in Applied Microbiology. 25, 172-176;
- Бактерии из камней Атакамы готовы покорять Марс;
- Subhas C. Shit, Pathik M. Shah. (2014). Edible Polymers: Challenges and Opportunities. Journal of Polymers. 2014, 1-13;
- Bahare Salehi, Simona Sestito, Simona Rapposelli, Gregorio Peron, Daniela Calina, et. al. (2018). Epibatidine: A Promising Natural Alkaloid in Health. Biomolecules. 9, 6;
- Alla G. Guzii, Tatyana N. Makarieva, Vladimir A. Denisenko, Andrey V. Gerasimenko, Anatoly A. Udovenko, et. al. (2019). Guitarrins A–E and Aluminumguitarrin A: 5-Azaindoles from the Northwestern Pacific Marine Sponge Guitarra fimbriata. J. Nat. Prod. 82, 1704-1709;
- Yong Hu, Siling Chen, Fang Yang, Shuai Dong. (2021). Marine Indole Alkaloids—Isolation, Structure and Bioactivities. Marine Drugs. 19, 658;
- Hiyoung Kim, Jungwook Chin, Hyukjae Choi, Kyungryul Baek, Tae-Gu Lee, et. al. (2013). Phosphoiodyns A and B, Unique Phosphorus-Containing Iodinated Polyacetylenes from a Korean Sponge Placospongia sp.. Org. Lett. 15, 100-103;
- Andrea K. Wallace, Nicolas Chanut, Christopher A. Voigt. (2020). Silica Nanostructures Produced Using Diatom Peptides with Designed Post‐Translational Modifications. Adv Funct Materials. 30;
- The preparation method of a kind of tributyl citrate // Patent CN104529774B. China. 2016. 6p. (In Chinese).;
- Cases I., de Lorenzo V. (2005). Genetically modified organisms for the environment: stories of success and failure and what we have learned from them. International Microbiology. 8, 213–222;
- Pabulo Henrique Rampelotto. (2010). Resistance of Microorganisms to Extreme Environmental Conditions and Its Contribution to Astrobiology. Sustainability. 2, 1602-1623;
- K Nüsslein, D Maris, K Timmis, D F Dwyer. (1992). Expression and transfer of engineered catabolic pathways harbored by Pseudomonas spp. introduced into activated sludge microcosms. Appl Environ Microbiol. 58, 3380-3386;
- Pavel Dvorak, Sarka Bidmanova, Jiri Damborsky, Zbynek Prokop. (2014). Immobilized Synthetic Pathway for Biodegradation of Toxic Recalcitrant Pollutant 1,2,3-Trichloropropane. Environ. Sci. Technol. 48, 6859-6866.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚