Мозг под наблюдением: путеводитель по методам нейровизуализации
15 мая 2026
Мозг под наблюдением: путеводитель по методам нейровизуализации
- 1496
- 0
- 3
Мозг не открывается сразу и целиком. Каждый метод — это отдельный разговор: один спрашивает о сосудах, другой — о тканях, третий — об активности нейронов. Врач за экраном — не просто наблюдатель, а переводчик между физическими сигналами и клинической реальностью.
Рисунок в полном размере.
иллюстрация Елены Беловой
-
Автор
-
Редакторы
-
Рецензенты
-
Иллюстратор
Темы
Долгое время головной мозг оставался «черным ящиком»: изучать его если и приходилось, то посмертно или на операции; но видеть, что в нем происходит в реальном времени, не было никакой возможности. Все изменилось, когда новые открытия в области физики пришли в медицину: сегодня нейровизуализация — это не один инструмент, а целый арсенал технологий, каждая из которых смотрит на мозг под своим углом: через плотность тканей, магнитные свойства протонов водорода или сосудистый отклик на нейронную активность. Во второй статье спецпроекта «Медицинские нейротехнологии» мы разбираем, как устроена лучевая диагностика мозга, на каких принципах основана, какие имеет возможности и где применяется. А в финале поговорим, как искусственный интеллект и радиомика переводят медицинское изображение из картинки в массив данных, открывая доступ к закономерностям, невидимым человеческому глазу.
Медицинские нейротехнологии
В этом спецпроекте мы расскажем об инструментальной диагностике и лечении неврологических заболеваний, объединяя фундаментальную науку, клиническую практику и передовые тенденции в неврологии. Спецпроект дополняет цикл статей по нейрофармакологии, переходя от молекулярных основ заболеваний нервной системы к реалиям современной медицины и практическим подходам к диагностике и лечению.


Партнеры спецпроекта — Фонд развития отечественной науки, техники и медицины (ФРОНТМЕД), Российский центр неврологии и нейронаук
Головной мозг — самый защищенный орган человеческого тела. Он укрыт черепом, окружен цереброспинальной жидкостью, отгорожен от крови особым барьером [1]. И все же именно он остается одним из самых уязвимых: инсульт, опухоль, травма, нейродегенерация — любое из этих состояний способно за короткое время изменить личность, речь, движение или сознание человека. Долгое время врачи могли лишь наблюдать за последствиями — и догадываться о причинах. Мозг оставался закрытым. Чтобы понять, как устроена эта система в норме, читайте наш «Ликбез по ЦНС» [2] — здесь же речь пойдет о том, как современная медицина научилась заглядывать внутрь без скальпеля.
- Нейровизуализация —
- это совокупность диагностических методов, позволяющих неинвазивно получать изображения нервных структур, быстро и точно диагностировать острые и хронические неврологические патологии, определять жизнеспособность тканей, предполагать механизмы заболевания, помогая клиницисту определить оптимальную тактику лечения.
Но важно не только уметь «читать» изображения мозга, но и выбрать наилучший способ визуализации. Допустим, пациент поступает в приемное отделение с внезапной слабостью в правой руке и нарушением речи. Врач подозревает инсульт. Время идет на минуты. Какой метод выбрать: компьютерную томографию или магнитно-резонансную? Как оценить проходимость сосудистого русла и исключить разрыв аневризмы? А если у пациента подозрение на опухоль? Опасения подтвердились — и впереди нейрохирургическая операция; но как еще до операции определить, где расположена опухоль относительно центра речи?
В каждом из этих случаев врач выбирает метод визуализации в зависимости от конкретной клинической задачи, а не собственных предпочтений — это мы обсудим ниже. Врачи не всегда понимали, как именно визуализировать мозг человека для постановки диагноза или выбора лечения. В первой статье спецпроекта «Мозговой штурм: краткая история медицинских нейротехнологий» мы подробно рассмотрели, как ученые и врачи по крупицам собирали информацию, иногда по воле случая: наблюдая за пациентами, получившими ранения или травмы [3]. Однако до середины XX столетия все эти данные получали либо посмертно, либо в условиях инвазивного вмешательства. Мозг оставался в значительной степени «черным ящиком»: мы могли видеть его структуру в моменте, но не в динамике; последствия повреждения, но не процесс работы.
Методы нейровизуализации получили импульс во второй половине XX века, когда физические открытия начали проникать в медицину. Компьютерная томография (КТ), основанная на рентгеновском излучении, впервые позволила получать послойные изображения мозга без хирургического вмешательства [4], [5]. Магнитно-резонансная томография (МРТ) выросла из фундаментальных исследований магнитных свойств ядер атомов, а спустя десятилетия была адаптирована для получения изображений внутренних органов [6]. А уже в 1990 году группа Сэйдзи Огавы показала, что МРТ способна регистрировать изменения оксигенации крови, связанные с нейрональной активностью. Так появилась функциональная МРТ (фМРТ) — метод, позволивший наблюдать работу мозга in vivo [7].
Визуализация головного мозга на сегодняшний день — целый спектр технологий, основанных на разных физических принципах: от рентгеновского излучения до явления ядерного магнитного резонанса. Каждая показывает свою сторону реальности: структуру и плотность тканей, сосудистую анатомию и кровоток, функциональную активность. «Биомолекула» кратко уже обозревала часть из этих технологий («12 методов в картинках: нейробиология» [8]), но настало время рассказать о современных и актуальных методах нейровизуализации подробнее.
В этой статье мы разберем физические принципы основных нейровизуализационных методик, их клинические возможности и ограничения, а также обсудим, почему выбор метода всегда является компромиссом между скоростью, контрастностью, безопасностью и диагностической точностью.
Магнитно-резонансная томография (МРТ): громкий способ видеть мозг
Для начала давайте попытаемся понять, как устроен МР-томограф. Снаружи это просто большая труба с отверстием посередине: наверняка многим приходилось бывать в ней и слышать причудливые звуки МРТ. Внутри этой конструкции скрыты четыре системы, каждая из которых решает свою задачу (рис. 1).
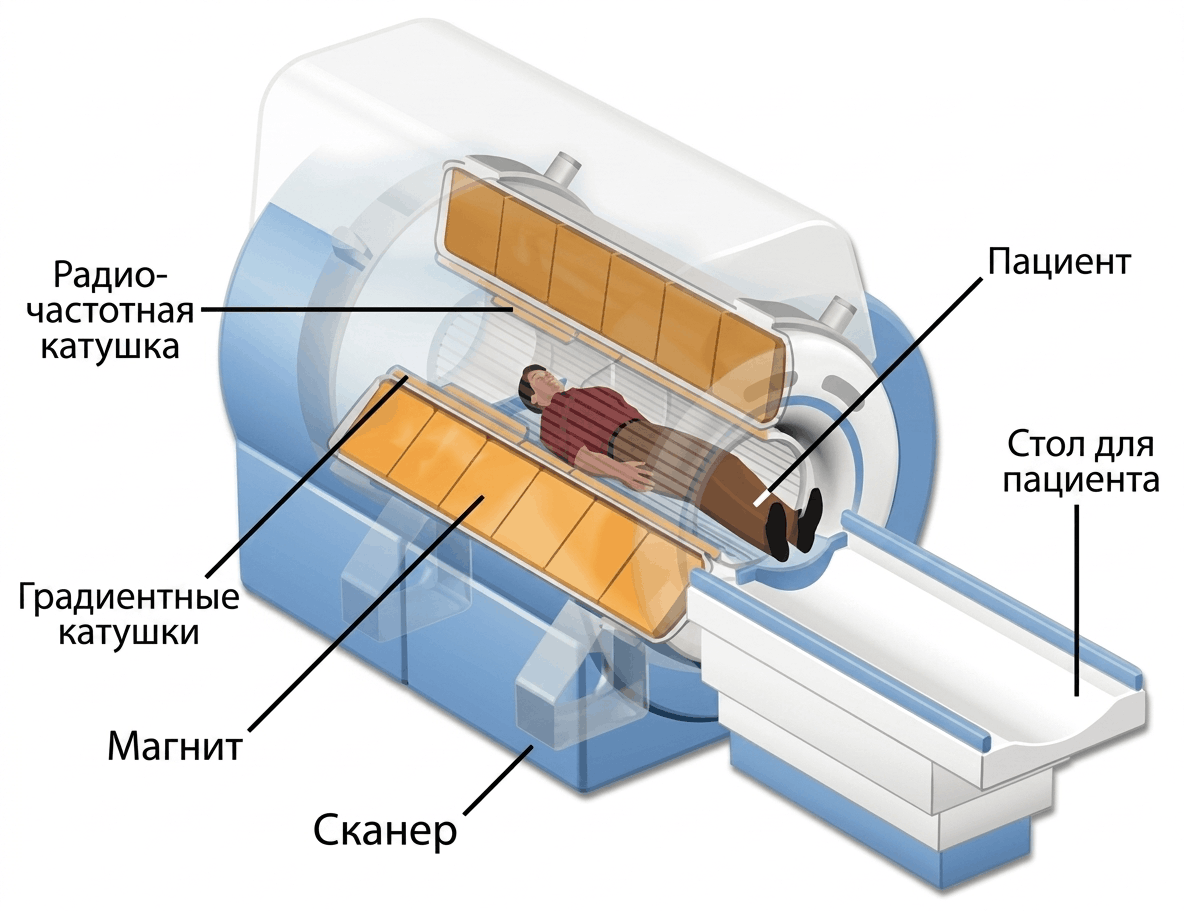
Рисунок 1. Устройство МР-томографа. Магнит современных томографов создает поле с магнитной индукцией 1,5–3,0 Тесла, что в десятки тысяч раз сильнее, чем у Земли. Чтобы поддерживать такую мощь, катушки магнита охлаждаются жидким гелием до температур, близких к абсолютному нулю, переходя в режим сверхпроводимости — состояние, при котором электрический ток циркулирует без какого-либо сопротивления и потерь. Градиентные катушки создают точно рассчитанные изменения магнитного поля в трех направлениях пространства (именно они, переключая токи и изменяя магнитное поле, отвечают за тот характерный громкий стук, жужжание и щелканье, которые слышны лежащему внутри аппарата пациенту). Радиочастотные катушки делятся на два типа. Передающие катушки посылают в тело пациента радиоволны строго определенной частоты (63,8 МГц для аппаратов с полем 1,5 Тесла и 127,7 МГц для трехтесловых систем), чтобы вывести протоны водорода из равновесия. Приемные катушки улавливают ответный сигнал, который протоны испускают, возвращаясь обратно. Наконец, всем этим оркестром дирижирует компьютерная система. Она синхронизирует работу магнита, градиентных и радиочастотных катушек, собирает поступающие данные и с помощью математических алгоритмов превращает поток сигналов в изображение, которое врач видит на экране [9].
[10], с изменениями
В основе МРТ лежит явление ядерного магнитного резонанса, о котором мы говорили в связи с биомолекулярной ЯМР-спектроскопией: «12 методов в картинках: структурная биология» [11] и «Сверхпроводящие магниты и рецепторы биомембран: Лаборатория биомолекулярной ЯМР-спектроскопии ИБХ РАН» [12]. Чтобы понять, как это работает, представим протоны (ядра атома водорода: в человеческом теле их триллионы триллионов, ведь мы на ~60% состоим из воды) крошечными магнитными стрелками, прямо как в компасе. В обычных условиях они ориентированы хаотично, но стоит поместить человека в сильное магнитное поле томографа, как картина меняется: стрелки выстраиваются вдоль линий его напряженности (рис. 2). Затем в дело вступает радиочастотный (РЧ) импульс — строго на той частоте, на которую «настроены» протоны. Импульс выбивает протоны из равновесия, заставляя их отклониться. Это явление называется резонансом: так камертон начинает звучать в ответ на ноту той же высоты. Отклонение протонов от исходного положения происходит на определенный угол переворота (flip angle). Его величина зависит от мощности и длительности импульса: классический импульс на 90° полностью переводит намагниченность в поперечную плоскость, тогда как в последовательностях градиентного эха используются также малые углы — от 5° до 40°, — что позволяет значительно ускорить сканирование. Когда же импульс выключается, протоны возвращаются в исходное положение, и именно в это время испускают слабый электромагнитный сигнал, который улавливают приемные катушки томографа [13].
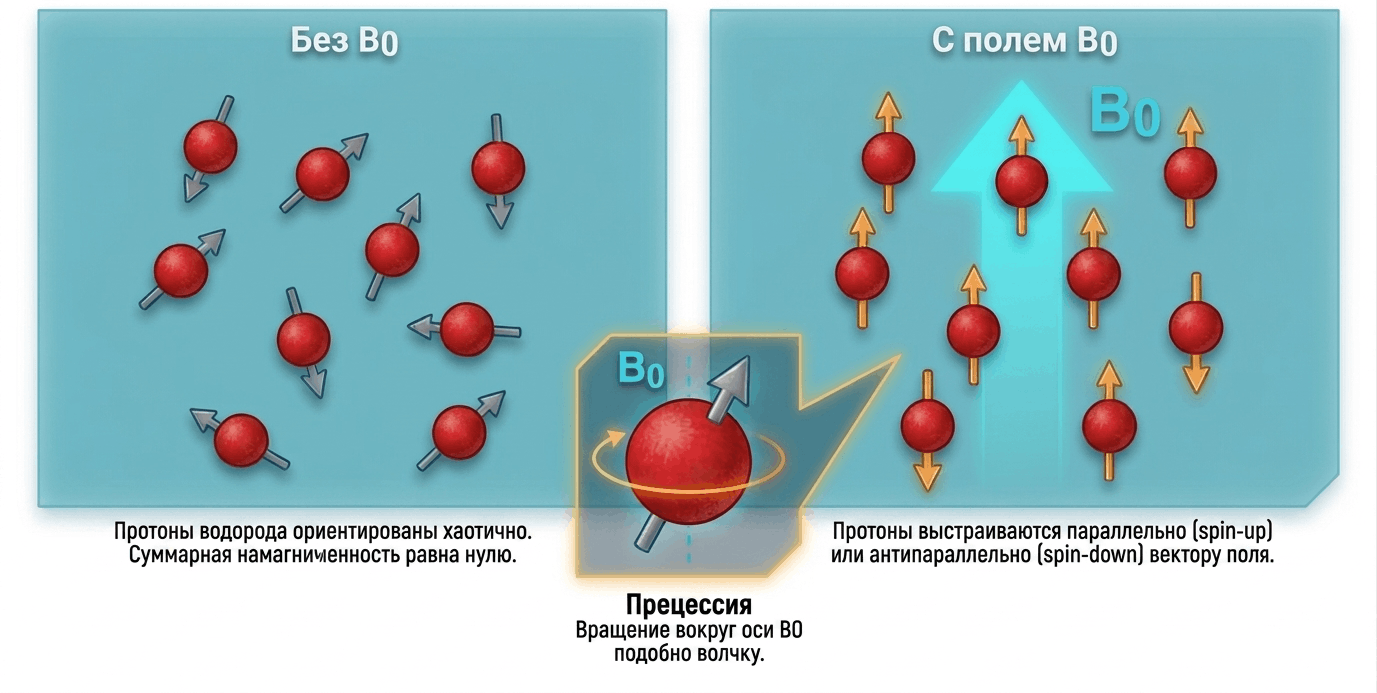
Рисунок 2. Поведение протонов водорода во внешнем магнитном поле B0. Слева: Хаотичная ориентация магнитных моментов в отсутствие внешнего поля. Справа: Выстраивание спинов вдоль или напротив вектора B0 с возникновением прецессии.
изображение сгенерировано Notebook LM по промпту автора статьи
Возвращение протонов в равновесное состояние происходит не в мгновение ока — это постепенный процесс, реализующийся сразу по трем независимым механизмам: T1- и T2-релаксацией (соответственно, спин-решеточной и спин-спиновой) (рис. 3), а также спадом свободной индукции (FID, Free Induction Decay), описываемым константой T2*.
- T2* —
- ускоренная версия T2-релаксации: помимо взаимодействий между самими протонами, в ней дополнительную роль играют неоднородности внешнего магнитного поля.
Именно FID лежит в основе последовательностей градиентного эха — наиболее быстрых из применяемых в клинической МРТ. В отличие от спинового эха, где второй РЧ-импульс (180°) компенсирует эти неоднородности, градиентное эхо их не устраняет — и потому чувствительно к отклонениям поля томографа от идеальной однородности, а также к локальным искажениям поля, создаваемым такими веществами, как дезоксигемоглобин, продукты распада крови и отложения железа [14].
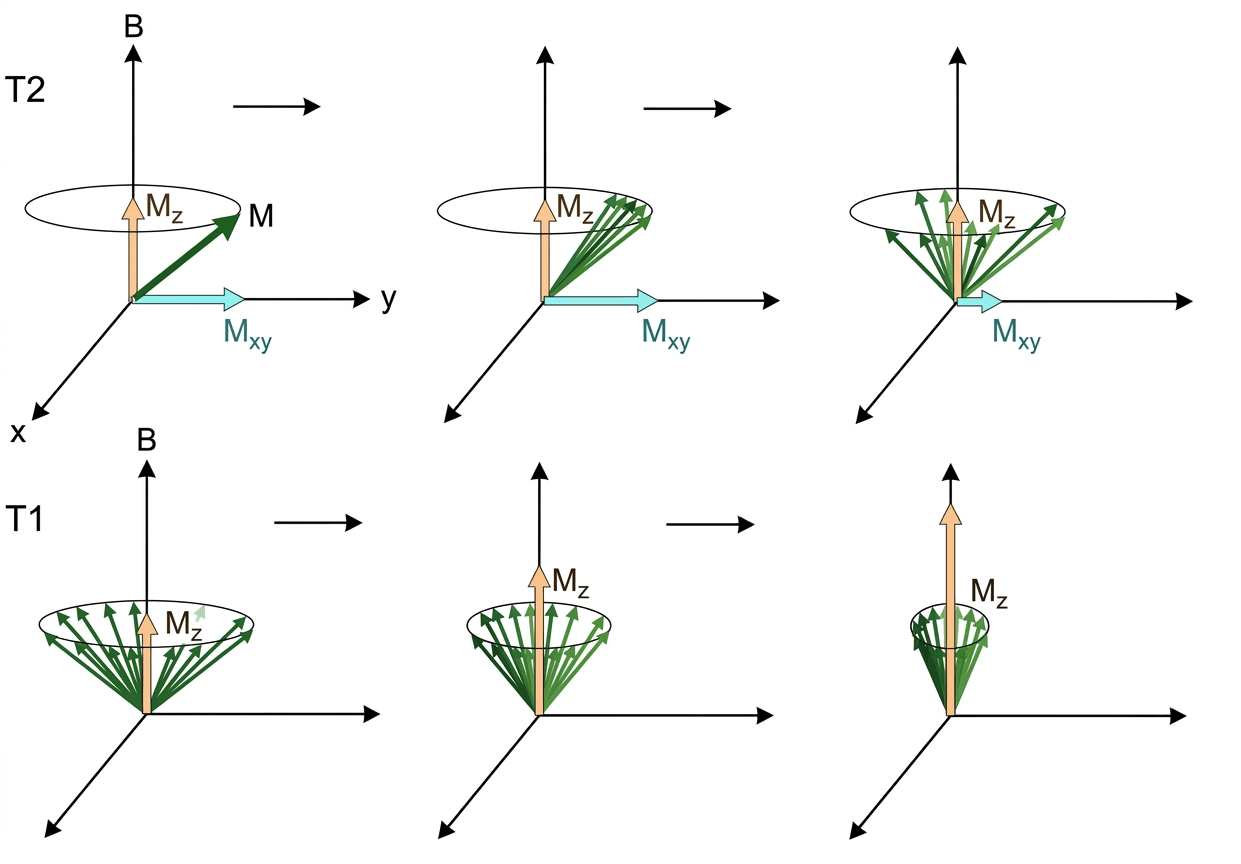
Рисунок 3. Процессы релаксации в МРТ: T2 и T1. Ряд T2 (поперечная релаксация, или спин-спиновая) демонстрирует «расфазировку» спинов. Со временем индивидуальные магнитные моменты разбегаются в плоскости XY, и суммарный вектор Mxy исчезает. Здесь энергия никуда не уходит, но протоны, поначалу прецессирующие синхронно, начинают «сбиваться с ритма» из-за взаимных магнитных взаимодействий. Это похоже на хор, в котором певцы постепенно перестают попадать в такт друг другу: голоса не исчезают, но стройное звучание теряется. Ряд T1 (продольная релаксация, или спин-решеточная) демонстрирует восстановление намагниченности вдоль основной оси Z. Вектор Mz постепенно возвращается к своему исходному состоянию. Возбужденные протоны постепенно отдают накопленную энергию окружающим молекулам ткани — той самой «решетке» — и восстанавливают намагниченность вдоль основного поля. Можно представить это как раскачанный маятник, который постепенно успокаивается, передавая энергию опоре.
Прецессия в МРТ — это вращение магнитных моментов протонов водорода вокруг оси внешнего магнитного поля, напоминающее движение волчка. Частота этого вращения называется Ларморовой частотой и прямо пропорциональна силе поля.
МРТ не фотографирует мозг, а «прислушивается» к тому, как по-разному ткани возвращаются в равновесие после возбуждения. Протоны в жировой ткани, сером веществе, ликворе делают это с разной скоростью — и именно эти различия превращаются в контраст на изображении. Ликвор, практически лишенный макромолекул, медленно теряет фазовую согласованность и медленно восстанавливает намагниченность — его T1 и T2 длинные. Белое вещество, богатое миелином, ведет себя иначе: липиды ограничивают подвижность молекул воды, и оба времени релаксации оказываются короткими.
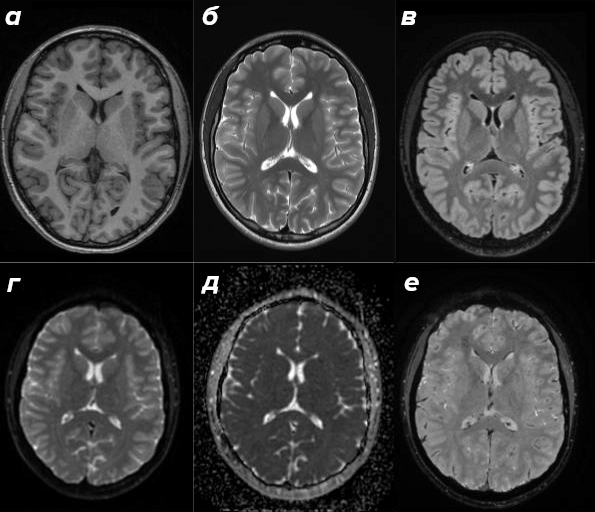
Контрастность изображения определяется тем, какой из этих механизмов оператор выведет на первый план. Для этого в его распоряжении — временны́е параметры последовательности (TR и TE), величина угла переворота, наличие инвертирующих РЧ-импульсов и выбор типа последовательности: спиновое или градиентное эхо. Варьируя их сочетание, оператор настраивает чувствительность метода к конкретным тканевым свойствам: в зависимости от химического состава, содержания воды, липидов и парамагнитных веществ анатомические структуры и патологические изменения отображаются с различной интенсивностью в градациях серого. Так, ликвор и патологический отек выглядят яркими на T2-взвешенных изображениях, тогда как миелинизированное белое вещество — на T1-взвешенных [15]. Каждая такая настройка — это отдельный режим сканирования со своим диагностическим вопросом, и стандартное МРТ-исследование головного мозга всегда включает несколько таких режимов: только вместе они складываются в полноценную диагностическую картину (рис. 4).
- TR (Time of Repetition) —
- временной интервал между последовательными радиочастотными импульсами, примененными к одному и тому же срезу.
- TE (Echo Time) —
- интервал времени от радиочастотного импульса до пика регистрируемого сигнала (эхо).
-
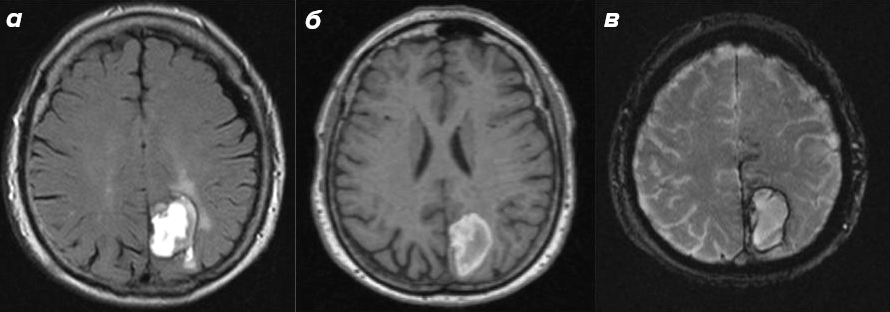
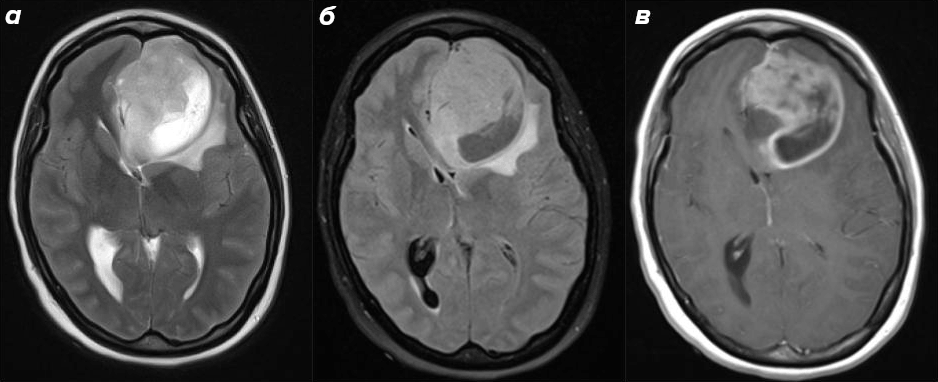
T1-взвешенные изображения (Т1-ВИ) — анатомический «атлас» мозга. Они хорошо показывают серое и белое вещество, жировую ткань, причем серое вещество выглядит «серым», белое — «белым», а ликвор — темным. При подозрении на опухоль, инфекцию или острый очаг демиелинизации к протоколу добавляется контрастное усиление: пациенту внутривенно вводят препарат на основе гадолиния и получают T1-ВИ, аналогичные таковым до введения контрастного вещества. Там, где гематоэнцефалический барьер нарушен, происходит накопление контраста — очаг патологии буквально «подсвечивается» на изображении [16].
-
T2-взвешенные изображения (T2-ВИ) используются для поиска патологии: там, где есть структурные изменения ткани головного мозга, интенсивность МР-сигнала повышается, из-за чего он получается более «светлым». По сути Т2-режим — «детектор» патологических изменений в нейровизуализации, указывающий на то, где именно стоит искать проблему. В этом режиме серое вещество головного мозга выглядит светлее белого вещества, ликвор также светлый.
-
T2 FLAIR — это T2 с применением метода инверсии-восстановления (IR). Его логика проста: если перед основной последовательностью подать специальный инверсионный импульс и точно подобрать паузу до следующего возбуждения, сигнал от свободной жидкости «обнулится» (т. е. ликвор, в отличие от T2-ВИ, станет темным), и на первый план выйдут патологические изменения, которые иначе терялись бы на ярком фоне ликвора. Убирая «шумный» фон, этот метод делает еще больший акцент на патологии [17].
-
Диффузионно-взвешенная МРТ (ДВИ; DWI) регистрирует броуновское движение молекул воды в тканях. Там, где при инсульте из-за цитостатического отека клетки набухают, движение воды по межклеточному пространству затрудняется — диффузия ограничивается, что ДВИ подмечает уже в первые часы после появления симптомов, когда другие методы еще слепы. Этот же принцип помогает выявлять опухоли с высокой клеточностью и абсцессы головного мозга с вязким содержимым в центре без какого-либо контрастного усиления [18], [19].
-
SWI (susceptibility-weighted imaging; изображения, взвешенные по магнитной восприимчивости) — режим, чувствительный к магнитным неоднородностям тканей. Дезоксигемоглобин, продукты распада крови, отложения железа локально искажают магнитное поле, что улавливает и усиливает SWI. Так артефакт преобразуется в диагностическую методику, особенно ценную при черепно-мозговых травмах, нейродегенеративных заболеваниях и кровоизлияниях [20].
Как из сигнала получается изображение
Представьте, что вы оказались в огромном темном зале, где одновременно играют тысячи музыкантов. Вы слышите общий звук, но не можете понять, кто именно играет у левой стены, а кто у правой. Именно такая проблема стоит перед томографом: все протоны в магнитном поле резонируют на одной и той же частоте, и сами по себе не сообщают, откуда в головном мозге пришел сигнал. Решение этой задачи потребовало изящного физического трюка.
Градиенты: пространство, закодированное в частоте
Чтобы «привязать» каждый сигнал к конкретной точке в пространстве, в томографе используются градиентные катушки, управляющие искажениями магнитного поля. Благодаря этому протоны в разных частях тела оказываются в полях разной напряженности — а значит, резонируют на слегка разных частотах. Частота становится своеобразным «адресом». Это и есть ключевой принцип пространственного кодирования МРТ. Процесс разворачивается в три последовательных шага по числу пространственных измерений (рис. 5).
-
Выбор среза. Прежде чем получить изображение, нужно выбрать, какой именно срез тела мы хотим увидеть. Для этого включается градиент вдоль оси Z (допустим, от головы к ногам). Теперь каждый горизонтальный слой тела находится в поле немного иной напряженности, а значит, имеет свою резонансную частоту. РЧ-импульс подается строго на одну частоту и возбуждает протоны только в одном тонком слое ткани, толщиной от долей миллиметра до нескольких миллиметров. Все остальные срезы «молчат».
-
Частотное кодирование. Теперь сигналы протонов внутри выбранного среза нужно «положить» на второе измерение (например, ось X). Для этого включается второй градиент, действующий вдоль этого направления. Теперь протоны, лежащие левее, прецессируют чуть медленнее, а правее — чуть быстрее. Их сигналы, записанные одновременно, складываются в сложную «мелодию». Разложив этот суммарный сигнал с помощью преобразования Фурье, можно определить вклад каждой точки вдоль оси X.
-
Фазовое кодирование. С третьей осью — осталась Y — все несколько сложнее. Здесь нельзя просто включить градиент «навсегда»: одновременное частотное кодирование двух измерений нельзя однозначно декодировать. Поэтому поступают иначе: Y-градиент включается кратковременно — ровно настолько, чтобы протоны в разных точках по этому направлению накопили разный фазовый сдвиг (оказались в разных «стадиях» своего колебательного цикла). После выключения градиента протоны снова прецессируют с одинаковой частотой, но теперь каждый со своим «клеймом» фазы, которое сохраняется в сигнале. Этот шаг повторяется многократно с разными амплитудами градиента, чтобы закодировать информацию о всех позициях вдоль оси Y [14].
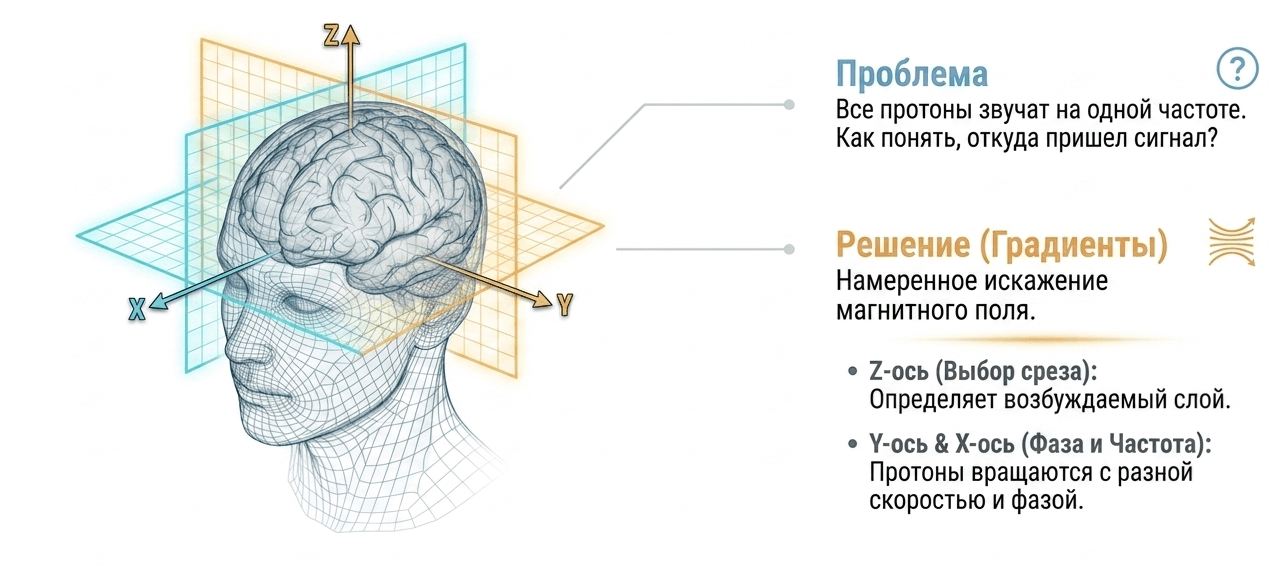
Рисунок 5. Пространственное кодирование в МРТ: отвечают магнитные градиенты. Наложение градиентов по осям X, Y и Z позволяет локализовать сигнал от конкретных областей мозга, изменяя частоту и фазу вращения протонов.
изображение сгенерировано Notebook LM по промпту автора статьи
K-пространство: архив данных перед финальной сборкой
Собранные за время сканирования сигналы не превращаются сразу в изображение. Они собираются в специальном математическом k-пространстве (от англ. k-space). Это не анатомическая карта мозга, а своего рода «частотный архив»: каждая строка в нем соответствует отдельному шагу фазового кодирования и содержит информацию о пространственных частотах изображения (рис. 6) [14].
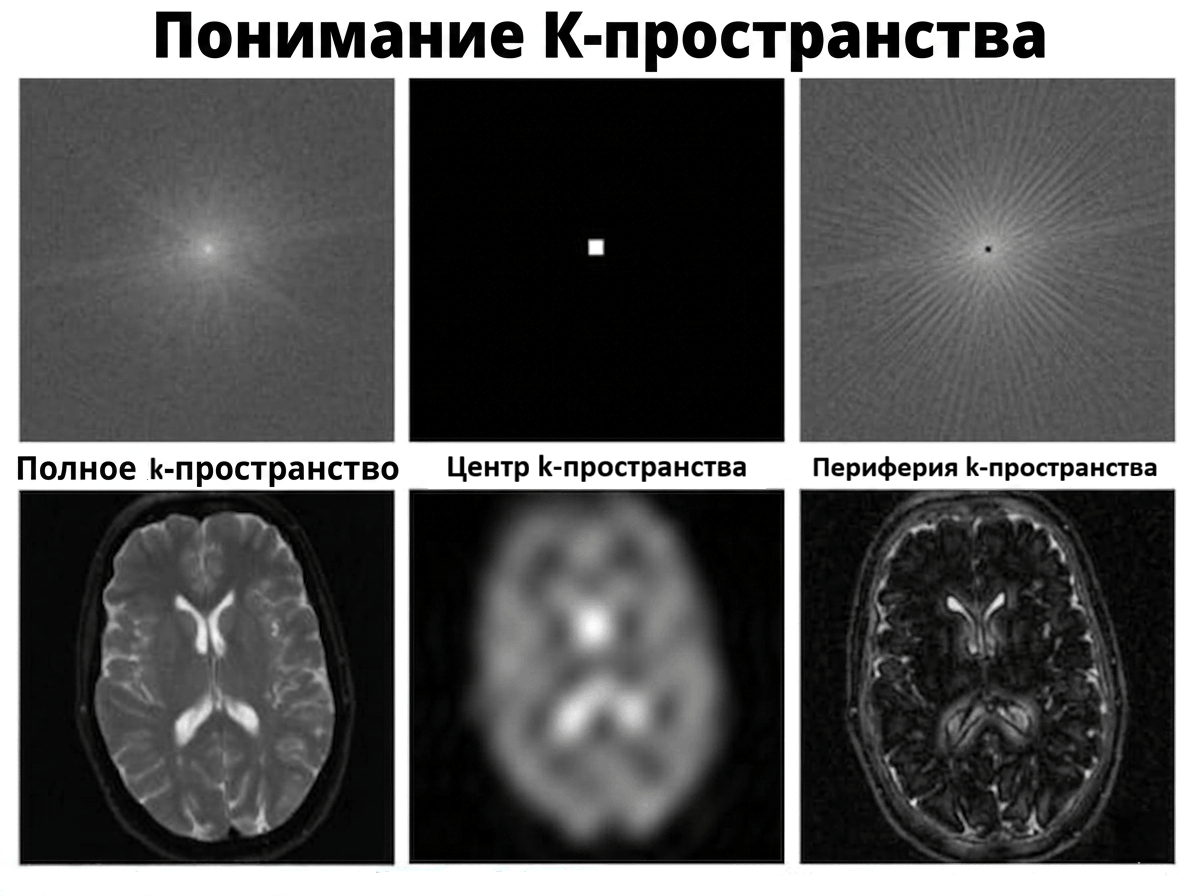
Рисунок 6. Роль k-пространства в формировании МРТ-изображения. Центральная часть (низкие частоты): отвечает за общую контрастность и основные формы (картинка яркая, но размытая). Периферия (высокие частоты): отвечает за детализацию, границы и четкость (картинка темная, видны только контуры). Именно поэтому, если в эксперименте заполнить только центральные строки k-пространства, изображение получится размытым, но узнаваемым, крайние же строки добавляют резкость.
Oncology & Medical Physics, c изменениями
Когда все данные собраны, к k-пространству применяется обратное преобразование Фурье — математическая операция, которая декодирует частотно-фазовую информацию и восстанавливает изображение в реальных координатах. Каждому элементу изображения (вокселю — трехмерному аналогу пикселя) соответствует конкретная точка в мозге с определенной интенсивностью МР-сигнала.
Сильные стороны и слепые пятна диагностических возможностей МРТ
Что МРТ умеет лучше всего
Главное достоинство МРТ — исключительная контрастность мягких тканей. Там, где компьютерная томография (КТ) видит почти однородную серую массу, МРТ четко дифференцирует серое и белое вещество головного мозга, определяет очаговые изменения размером в несколько миллиметров, опухолевые образования и зоны отека. Это стало возможным благодаря чувствительности к молекулярному окружению протонов воды, а оно в разных тканях принципиально различается.
Не менее важна мультипланарность: МРТ позволяет получать изображения в любой плоскости: аксиальной, сагиттальной или коронарной. Современные 3D-последовательности и вовсе позволяют после одного сканирования реконструировать срезы в произвольной проекции.
Принципиально важно и то, что в МРТ нет ионизирующего излучения. Это делает метод безопасным для пациентов, которым необходимы повторные исследования в динамике, а также для детей и беременных женщин при отсутствии индивидуальных противопоказаний. Именно поэтому МРТ стала методом выбора в педиатрической нейрорадиологии и при наблюдении за хроническими заболеваниями — например, рассеянным склерозом [21], где количество исследований на протяжении жизни может исчисляться десятками.
Наконец, МРТ отличается обилием диагностических режимов. Помимо распространенных сценариев вроде определения острого инсульта по ДВИ или микрокровоизлияний по SWI, существуют дополнительные методики, такие как МР-спектроскопия, которая позволяет оценить метаболический профиль опухоли без биопсии, или МР-трактография, отражающая целостность проводящих путей головного мозга. Каждый из этих режимов отвечает на свой клинический вопрос, а затем именно совокупность ответов формирует полную диагностическую картину.
Где проходят границы МРТ
При всех достоинствах у метода есть реальные и принципиальные ограничения, которые важно понимать как врачу, так и пациенту:
-
Время исследования. Стандартный протокол МРТ головного мозга занимает в среднем 20–30 минут; расширенный с применением дополнительных режимов сканирования или контрастирования может превысить и час. Это создает сразу несколько проблем. Во-первых, пациент длительное время должен сохранять неподвижность: даже миллиметровое смещение головы во время сканирования приводит к двигательным артефактам, которые размывают изображение и могут имитировать или маскировать патологию. Во-вторых, в неотложной ситуации (например, при подозрении на острое кровоизлияние или тяжелую травму) даже 30 минут могут оказаться непозволительной роскошью. В таких случаях именно КТ, выполняемая за секунды, остается первичным методом диагностики.
-
Противопоказания, связанные с магнитным полем. Мощное постоянное магнитное поле томографа — не абстрактная физическая характеристика, а реальный фактор риска для здоровья, а порой и жизни пациентов с некоторыми имплантами. Кардиостимуляторы и имплантируемые кардиовертеры-дефибрилляторы старых моделей могут изменять режим работы или выходить из строя под воздействием магнитного поля; металлические хирургические клипсы способны смещаться; кохлеарные импланты повреждаться. Сегодня существуют МР-совместимые версии большинства таких устройств, однако перед исследованием необходимо документальное подтверждение совместимости: устного заверения пациента будет недостаточно. Отдельную проблему представляет клаустрофобия: замкнутое пространство тоннеля томографа переносится тяжело примерно каждым десятым пациентом, что иногда требует седации или использования томографов открытого типа, состоящих из двух горизонтальных магнитных плит (сверху и снизу), между которыми находится пациент, при этом боковые стороны остаются полностью открытыми [22].
-
Слабые стороны при визуализации костей и кальцификатов. МРТ плохо «видит» кортикальную кость и кальцинаты, так как они содержат мало свободной воды и потому дают крайне слабый сигнал. Для оценки переломов, костных эрозий, кальцифицированных структур и мелких кальцинатов КТ остается значительно более информативным методом. Это же касается и легочной ткани, насыщенной воздухом, поэтому МРТ в пульмонологии применяется значительно реже, чем КТ.
-
Стоимость и доступность. МР-томограф — технически сложное и дорогостоящее оборудование. Стоимость современного клинического аппарата составляет от нескольких десятков до нескольких сотен миллионов рублей, а его эксплуатация требует регулярной дозаправки криогенами для охлаждения сверхпроводящих магнитов, специально подготовленного помещения и квалифицированного персонала. В результате МРТ куда менее доступна, чем КТ, особенно в небольших больницах и отдаленных районах.
Рентгеновское излучение и математика: как работает КТ
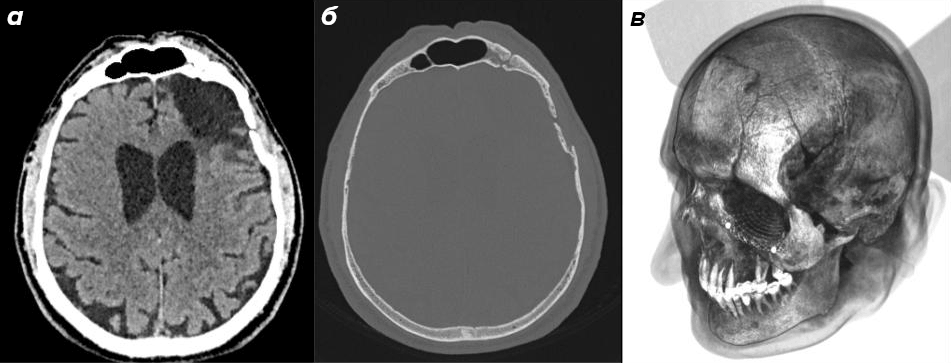
До появления компьютерной томографии (КТ) врач, желавший заглянуть внутрь черепа без хирургического вмешательства, располагал крайне скудным арсеналом. Обычный рентгеновский снимок дает плоское суммарное изображение: все структуры, лежащие на пути луча, накладываются друг на друга, и мягкие ткани мозга практически не различаются на фоне костей черепа (рис. 7).
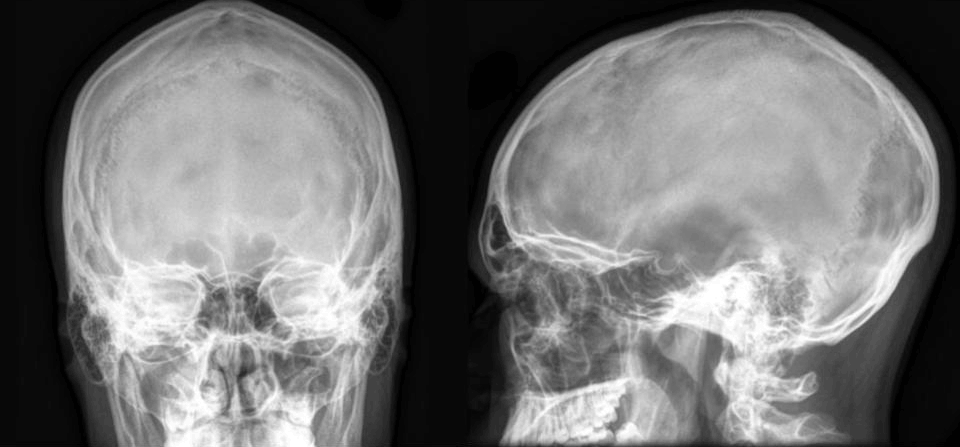
Рисунок 7. Рентгенографическое изображение черепа без патологии в прямой и боковой проекции.
Революция произошла в начале 1970-х годов. Британский инженер Годфри Хаунсфилд из компании EMI предложил принципиально иной подход: если сделать не один снимок, а сотни под разными углами, а затем математически обработать этот массив, можно восстановить распределение поглощающей способности тканей в каждой точке среза. Независимо от него южноафриканский и американский физик Аллан Кормак еще в 1960-х годах разработал математический аппарат для такой реконструкции, не подозревая, что его теория вскоре найдет прямое клиническое применение. В 1979 году оба ученых были удостоены Нобелевской премии по физиологии и медицине: редкий случай, когда награда за вклад в медицину досталась инженеру и физику.
Первый клинический КТ-сканер был установлен в лондонской больнице Аткинсон Морли в 1971 году и предназначался исключительно для исследования головного мозга. Время получения одного среза составляло около 4–5 минут, а полная реконструкция изображения — несколько часов. Сегодня современный мультидетекторный томограф с многорядными детекторами сканирует весь мозг менее чем за 5 секунд.
Внешне КТ-аппарат напоминает большое кольцо, которое называют гентри (от англ. gantry), в центре которого находится стол для пациента. Но внутри этого кольца скрыта сложная механическая и электронная система (рис. 8), просвечивающая движущегося на столе пациента веерными пучками рентгеновских лучей и восстанавливающая объемное изображение рентгеновской плотности тканей тела — технически, тело представляется набором вокселей (как и в МРТ — трехмерных аналогов пикселей).
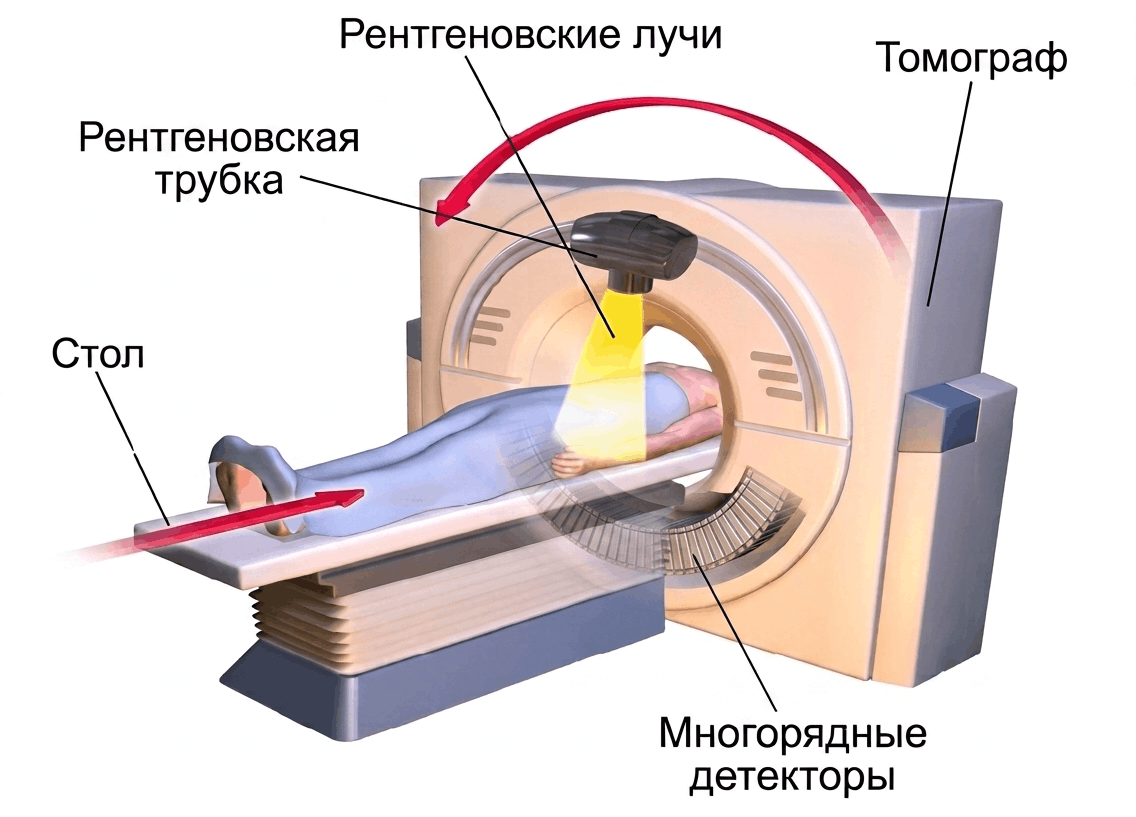
Рисунок 8. Строение компьютерного томографа. На вращающемся кольце внутри гентри закреплена рентгеновская трубка. Веерный пучок генерируемых ей рентгеновских лучей проходит сквозь тело пациента, ослабляясь за счет поглощения; а затем регистрируется детекторами (расположенные напротив трубки ряды сцинтилляторов и ионизационных камер). Ключевое техническое решение современных компьютерных томографов — спиральное сканирование. Стол с пациентом непрерывно движется сквозь гентри, пока рентгеновская трубка вращается вокруг него. В результате траектория пучка относительно тела описывает спираль. Это позволяет сканировать большие объемы — например, весь головной мозг или всю грудную клетку — за единственный задержанный вдох, без пропусков между срезами и с возможностью последующей реконструкции в любой плоскости. Полученные детекторами данные — это не готовое изображение, а источник информации о степени поглощения рентгеновского излучения различными тканями организма. Чтобы получить анатомическое изображение, компьютер применяет алгоритм реконструкции, чаще всего метод обратного проецирования с фильтрацией (filtered back projection, FBP) или более современный итерационный подход. В итоге каждому вокселю присваивается числовое значение, отражающее локальную рентгеновскую плотность ткани [23].
Wikimedia Commons, с изменениями
Единицы Хаунсфилда: универсальный язык плотности
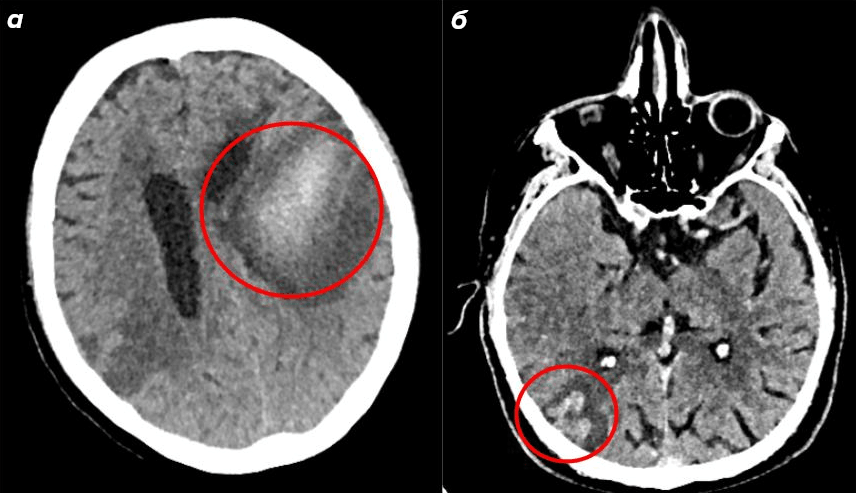
Числовые значения, которые получает каждый воксель, выражаются в единицах Хаунсфилда (HU) — шкале, нормированной относительно воды. Логика шкалы проста: вода принята за точку отсчета (0 HU), воздух — за нижний предел (−1000 HU). Все остальное располагается между этими полюсами и выше (рис. 9). Эта шкала — не просто техническая условность, а мощный диагностический инструмент. Зная, что свежая кровь поглощает рентгеновское излучение значительно сильнее, чем вещество мозга, рентгенолог безошибочно распознает острую гематому по характерной гиперденсной (светлой) зоне даже без контрастного усиления. Аналогично, снижение плотности в зоне ишемии ниже нормальных значений для мозговой ткани указывает на цитостатический отек и гибель клеток [23].
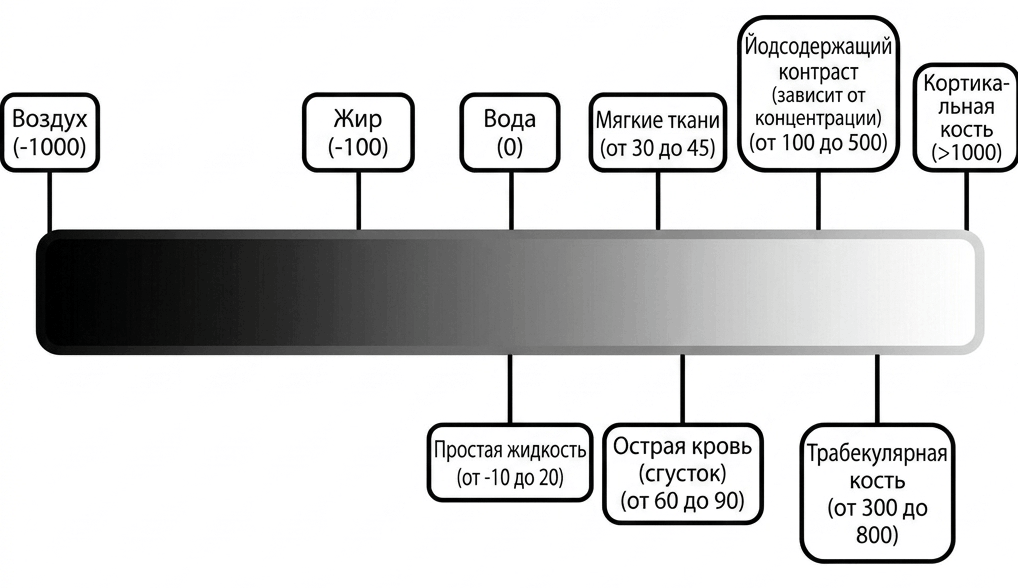
Рисунок 9. Упрощенная шкала Хаунсфилда (HU) и соответствующие показатели плотности различных тканей и веществ в компьютерной томографии.
Hounsfield scale (diagram) | Radiology Case | Radiopaedia, с изменениями
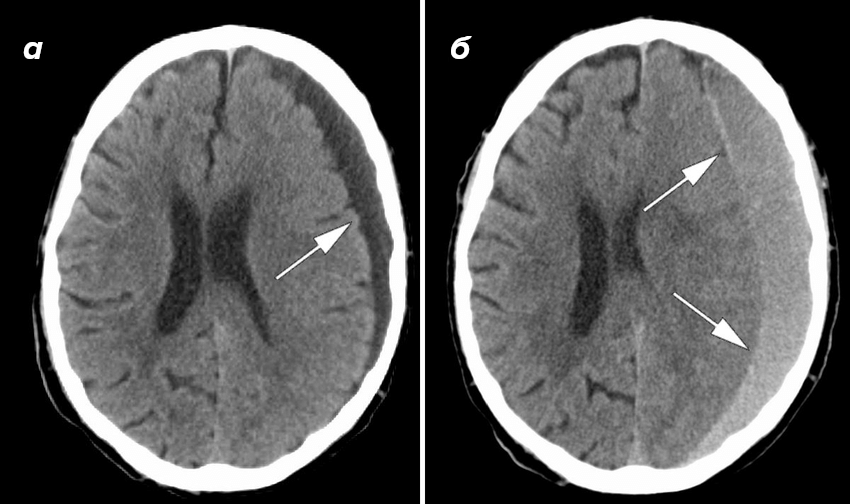
Поскольку диапазон HU широк, а человеческий глаз различает лишь около 30–40 оттенков серого, в практике используется понятие «окна», то есть диапазона отображаемых значений. Рентгенолог, оценивающий ткань мозга, выставляет узкое окно (примерно от 0 до +80 HU), которое позволяет сконцентрироваться на структурах в нужном диапазоне плотностей. Для анализа костей окно сдвигается вверх и расширяется. Одно и то же исходное изображение, просмотренное в разных окнах, дает принципиально разную диагностическую информацию (рис. 10).
Почему КТ незаменима в экстренной диагностике
Главное преимущество КТ перед МРТ — скорость. Современный томограф сканирует головной мозг за несколько секунд, а с учетом укладки пациента и реконструкции изображений весь процесс занимает не более 10–15 минут. В условиях, когда счет идет на минуты (например, при инсульте, черепно-мозговой травме, разрыве аневризмы), это критически важно.
КТ исключительно хорошо визуализирует именно то, что чаще всего угрожает жизни в остром периоде: свежую кровь (высокая плотность гемоглобина делает гематомы ярко-белыми на нативных изображениях), переломы костей черепа и смещение срединных структур мозга. Именно поэтому КТ без контраста остается первым и обязательным исследованием при любом подозрении на острое внутричерепное кровоизлияние в соответствии со всеми международными клиническими руководствами [25].
Дополнительные практические преимущества: возможность обследования пациентов с металлическими имплантами и кардиостимуляторами, а также реанимационных пациентов на аппарате искусственной вентиляции легких и с другим оборудованием, которое часто несовместимо с МРТ или требует дополнительных технических решений.
Цена за скорость: ограничения КТ
Главный недостаток метода — ионизирующее излучение. Эффективная доза при КТ головного мозга составляет около 1–2 мЗв, что сопоставимо с несколькими месяцами естественного фонового облучения; при этом рекомендуемые безопасные дозы облучения для населения составляют 1 мЗв в год, с допустимым кратковременным увеличением до 5 мЗв [26]. Поэтому для разового исследования у взрослого пациента это приемлемо, однако при необходимости повторных исследований, особенно у детей, у которых ткани более радиочувствительны, доза суммируется, и ее нужно учитывать. Именно поэтому в радиологии действует принцип ALARA (As Low As Reasonably Achievable), означающий, что доза должна быть настолько низкой, насколько это достижимо без потери диагностической информации.
Второй существенный недостаток — низкая контрастность мягких тканей по сравнению с МРТ. Серое и белое вещество мозга различаются на КТ примерно на 10 HU, что уже на пределе разрешения метода. КТ может пропустить раннюю ишемию, очаги демиелинизации, небольшие опухоли. Кроме того, задняя черепная ямка на КТ страдает от артефактов жесткости луча, то есть искажений, возникающих из-за неравномерного поглощения рентгеновского излучения костями основания черепа, что дополнительно снижает качество изображений в этой области.
Принцип выбора: не что сильнее, а что нужнее
Осознание как возможностей, так и ограничений КТ и МРТ позволяет сформулировать ключевой принцип клинической нейровизуализации: не существует универсального диагностического метода, но зато существует метод, оптимальный для конкретной задачи. МРТ — мощный инструмент, но не «золотой стандарт» для всех ситуаций. При остром кровоизлиянии и костной травме КТ быстрее и точнее. При оценке мягких тканей, ранней ишемии и демиелинизации МРТ остается вне конкуренции. А нередко оба метода применяются последовательно, дополняя друг друга: КТ для того, чтобы быстро исключить угрожающую жизни патологию, МРТ — чтобы детально охарактеризовать изменения и спланировать лечение.
Ультразвук на службе у мозга
Когда речь заходит о методах визуализации головного мозга, первыми на ум приходят МРТ и КТ, которые мы рассмотрели выше — громоздкие, дорогостоящие, стационарные аппараты. Ультразвук на этом фоне выглядит скромно: портативный датчик, гель на коже, черно-белая картинка на экране. Именно поэтому многие недооценивают его диагностический потенциал в неврологии — и напрасно, ведь в ряде клинических ситуаций УЗИ незаменимо.
В основе ультразвуковой диагностики лежит эффект эхолокации: датчик генерирует короткие импульсы высокочастотных звуковых волн (от 1 до 20 МГц, что значительно выше порога человеческого слуха), которые проникают в ткани и отражаются на границах структур с разным акустическим сопротивлением. Отраженные эхо-сигналы регистрируются тем же датчиком, по времени их возврата и амплитуде компьютер восстанавливает изображение. Чем выше частота волн, тем лучше пространственное разрешение, но тем меньше глубина проникновения: высокочастотные датчики (10–20 МГц) видят поверхностные структуры в деталях, низкочастотные (1–3 МГц) проникают глубже, но получают изображения с меньшей четкостью.
Главная проблема применения ультразвука в визуализации головного мозга — плотная костная ткань. Кость обладает высоким акустическим сопротивлением и практически полностью отражает ультразвуковые волны, создавая «акустическую тень» за собой. Черепная коробка, надежно защищающая мозг от механических повреждений, становится серьезным препятствием для УЗИ. Это ограничение во многом определяет, где и как ультразвук применяется в неврологии: либо через «акустические окна» (места, где кость тонка или отсутствует), либо интраоперационно, когда хирург уже открыл доступ к мозгу.
Нейросонография новорожденных: закрывающееся окно возможностей
Природа сама предоставила идеальное акустическое окно — большой родничок новорожденного. Этот неокостеневший участок черепа в первые месяцы жизни остается открытым, и через него ультразвуковой датчик получает прямой доступ к мозгу без каких-либо костных помех.
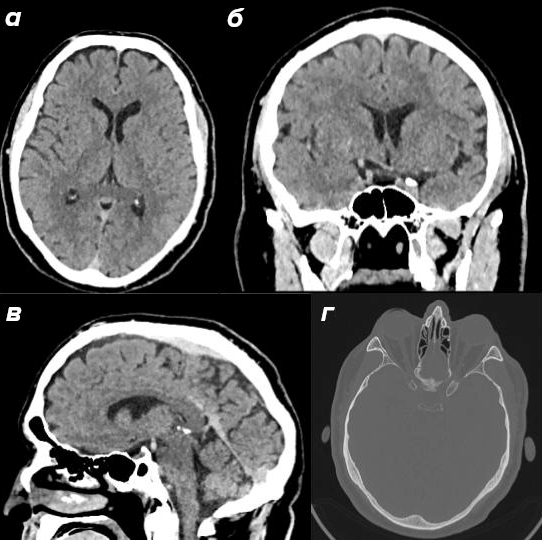
Нейросонография (НСГ) стала стандартным скрининговым методом в неонатологии. Она позволяет у постели ребенка, без транспортировки в отделение лучевой диагностики, без седации и малейшей лучевой нагрузки оценить основные структуры мозга новорожденного (рис. 11). Метод особенно ценен в отделениях реанимации новорожденных, где любое перемещение крайне недоношенного ребенка сопряжено с риском.
Диапазон выявляемых патологий весьма широк. Внутрижелудочковые кровоизлияния — одно из наиболее грозных осложнений недоношенности — на НСГ выглядят как гиперэхогенные (яркие) зоны в области сосудистых сплетений, нередко с затеканием крови в желудочки мозга. Перивентрикулярная лейкомаляция в связи с ишемическим поражением белого вещества вокруг желудочков на ранней стадии проявляется повышением эхогенности, а на поздней — формированием кистозных полостей, отчетливо видимых при ультразвуковом исследовании [27].
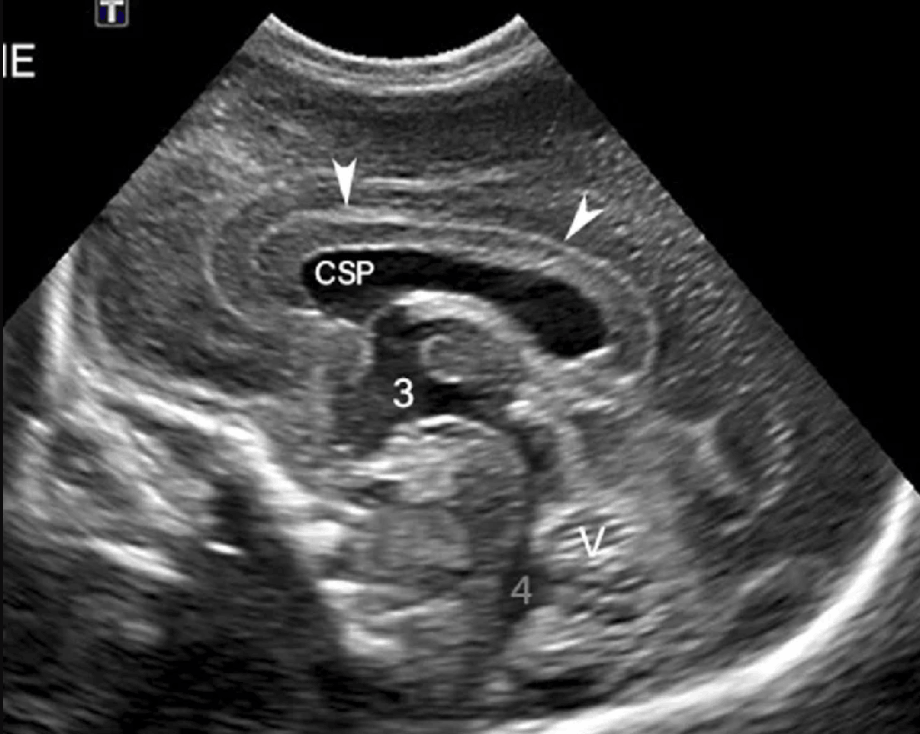
Рисунок 11. Ультразвуковое исследование головы новорожденного (в норме) в сагиттальной плоскости по срединной линии. Эхонегативная полость прозрачной перегородки (CSP) продолжается кзади как полость Верге, а далее кзади и книзу — как полость промежуточного паруса. Она располагается под мозолистым телом (указано наконечниками стрелок). 3 — третий желудочек; 4 — четвертый желудочек; V — червь мозжечка.
Кроме того, НСГ позволяет оценивать размеры желудочков в динамике, что критически важно при гидроцефалии, когда нарастание вентрикуломегалии требует своевременного дренирования. Ребенка можно сканировать ежедневно и не беспокоиться о накопленной дозе излучения.
Ограничение метода в детской неврологии столь же очевидно, как и его достоинство: родничок закрывается. Обычно это происходит к 12–18 месяцам жизни, после чего нейросонография через большой родничок уже невозможна. В дальнейшем для исследования мозга ребенка потребуются МРТ или КТ.
Транскраниальная допплерография: кровоток в реальном времени
Даже у взрослого человека с полностью сформировавшимся черепом ультразвук не теряет диагностической ценности. Транскраниальная допплерография (ТКДГ) применяет не анатомическую визуализацию, а эффект Доплера: оценка изменения частоты ультразвуковых волн, отраженных от движущихся объектов (в данном случае — эритроцитов в мозговых артериях).
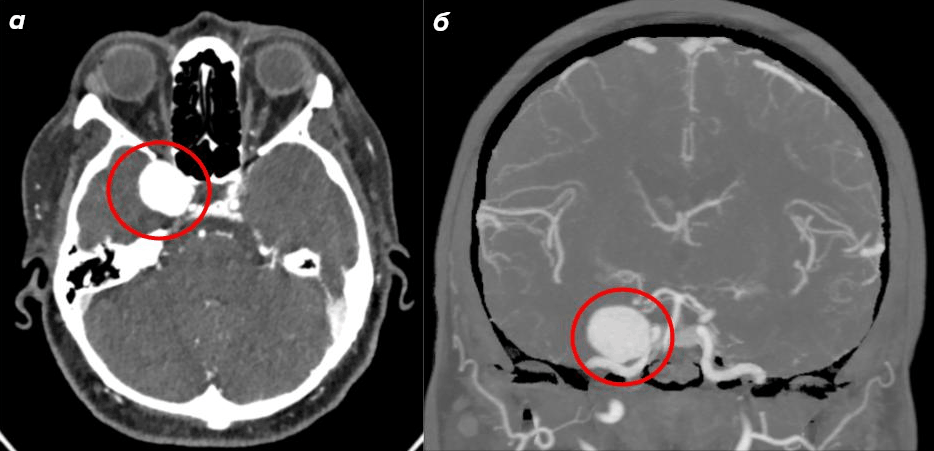
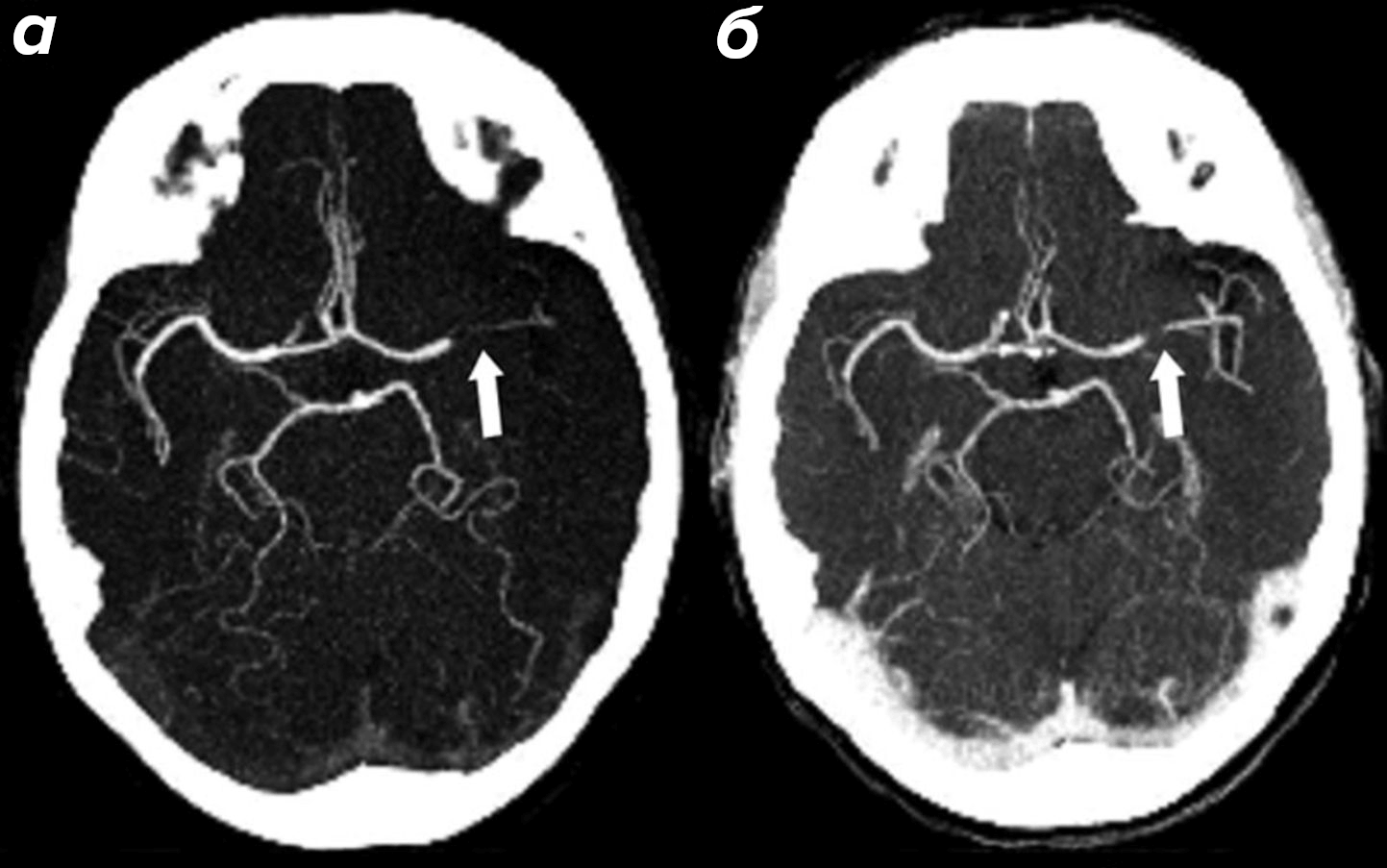
Принцип прост: если источник звука и его отражатель передвигаются относительно друг друга, частота отраженного сигнала изменяется пропорционально скорости движения. Зная эту разницу частот, можно вычислить скорость кровотока в сосуде. Для проведения исследования используют относительно низкие частоты (2 МГц), которые способны проникать через истонченные участки черепа — акустические окна (рис. 12).
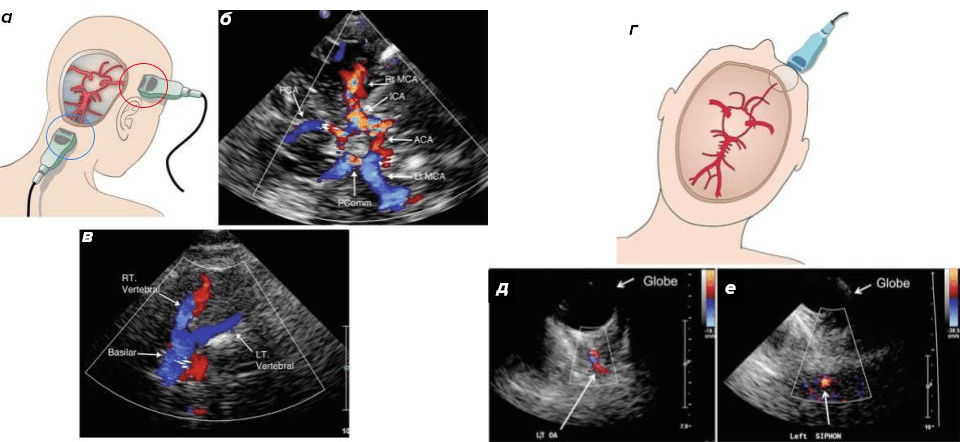
Рисунок 12. Транскраниальная допплерография: основные доступы и визуализируемые артерии.
а: синий круг — трансфораминальный доступ (датчик устанавливается по срединной линии ниже затылочного бугра); красный круг — транстемпоральный доступ (датчик располагается на височной кости либо над скуловой дугой кпереди от наружного слухового прохода, либо чуть более кзади, над мочкой уха).
г — трансорбитальный доступ (датчик прикладывается поверх закрытого века) для допплеровского УЗИ внутричерепных сосудов.
б — цветовое допплеровское картирование (ЦДК), полученное через транстемпоральное окно: отображает кровоток в виллизиевом круге.
в — ЦДК, полученное через трансфораминальное окно: показывает сосуды заднего круга кровообращения.
д, е — ЦДК-изображения, полученные через транстемпоральное окно: демонстрируют кровоток в проходимой левой глазной артерии (д) и сифоне левой сонной артерии (е).
[30], с изменениями
Клиническое применение ТКДГ многообразно. При стенозе внутричерепных артерий скорость кровотока в суженном сегменте резко возрастает точно так же, как ускоряется поток воды в сдавленном шланге. Это позволяет выявлять гемодинамически значимые стенозы и оценивать их тяжесть. При вазоспазме после субарахноидального кровоизлияния — опасного осложнения разрыва аневризмы, при котором артерии спазмируются и мозг страдает от ишемии, — ТКДГ позволяет ежедневно контролировать скорость кровотока и своевременно диагностировать нарастание спазма.
Один из важнейших сценариев применения ТКДГ — верификация смерти мозга. При прекращении мозгового кровообращения ТКДГ фиксирует характерный паттерн: реверберирующий кровоток или полное отсутствие сигнала. В ряде стран этот критерий включен в официальные протоколы констатации смерти мозга.
Наконец, ТКДГ с микроэмболодетекцией позволяет выявлять циркулирующие микроэмболы в мозговых артериях: крошечные пузырьки газа или фрагменты тромбов, дающие характерные высокоинтенсивные сигналы на фоне нормального допплеровского спектра. Это особенно важно при контроле эффективности антитромботической терапии и мониторинге пациентов во время кардиохирургических операций с искусственным кровообращением [29].
Дуплексное сканирование брахиоцефальных артерий: ворота к мозгу
Если ТКДГ смотрит внутрь черепа, то дуплексное сканирование исследует магистральные артерии шеи (сонные и позвоночные), по которым кровь поступает к мозгу (рис. 13). Метод сочетает В-режим (двумерное анатомическое изображение) с цветовым допплеровским картированием (визуализация кровотока в цвете) и спектральным доплером (количественная оценка скоростей).
В В-режиме отчетливо видна стенка сонной артерии: ее слои, толщина, наличие атеросклеротических бляшек. Толщина комплекса интима-медиа (КИМ), то есть суммарная толщина внутренней и средней оболочек артерии, является признанным маркером субклинического атеросклероза и сердечно-сосудистого риска: увеличение КИМ на каждые 0,1 мм ассоциировано с возрастанием риска инсульта примерно на 18% [31].
Бляшки — основная находка при дуплексном сканировании у пациентов с цереброваскулярной патологией. Метод позволяет оценить их эхоструктуру (однородная или гетерогенная, мягкая или кальцинированная), поверхность (гладкая или изъязвленная), степень стеноза в процентах от просвета артерии. Мягкие, гетерогенные, изъязвленные («нестабильные») бляшки ассоциированы с повышенным риском эмболии и инсульта даже при умеренной степени стеноза. Именно поэтому не только степень стеноза, но и морфология бляшки влияет на выбор тактики лечения: консервативная терапия, каротидная эндартерэктомия или стентирование [32].
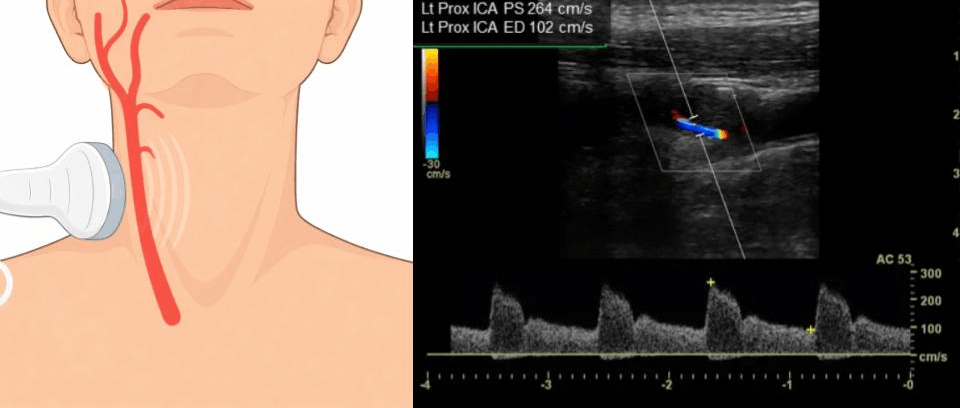
Рисунок 13. Дуплексное сканирование пациента со стенозом сонной артерии. В проксимальном отделе правой внутренней сонной артерии (ВСА) выявлена крупная гомогенная бляшка с локальным повышением скорости кровотока на фоне стеноза >70%.
Интраоперационный ультразвук: навигация в глубине мозга
Отдельную и весьма практически значимую нишу занимает интраоперационная нейросонография (ИОУЗИ). Когда нейрохирург вскрывает черепную коробку и обнажает поверхность мозга, костный барьер исчезает, поэтому и ультразвуковой датчик, стерильно упакованный, можно приложить прямо к мозговой ткани.
В этих условиях ультразвук демонстрирует свои уникальные преимущества перед другими интраоперационными методами. Он позволяет в реальном времени визуализировать опухоль относительно окружающих структур и непрерывно контролировать ход ее удаления. МРТ-навигация, с которой нейрохирурги работают в современных операционных, опирается на данные, полученные до операции; по мере удаления опухоли и перераспределения мозговой ткани эти данные постепенно устаревают — возникает феномен «сдвига мозга» (brain shift), который может смещать анатомические ориентиры на несколько миллиметров. Интраоперационный ультразвук обновляет картину в реальном времени и позволяет хирургу видеть актуальное расположение остатков опухоли [34].
Особенно ценно ИОУЗИ с контрастным усилением (contrast-enhanced intraoperative ultrasound, CE-IOUS): после внутривенного введения микропузырьковых контрастных агентов опухолевая ткань с нарушенным гематоэнцефалическим барьером явно проступает на фоне нормального мозга. Это позволяет точно определять границы опухоли и выявлять ее остатки после, казалось бы, полного удаления — и тут же расширить зону резекции (рис. 14) [35].
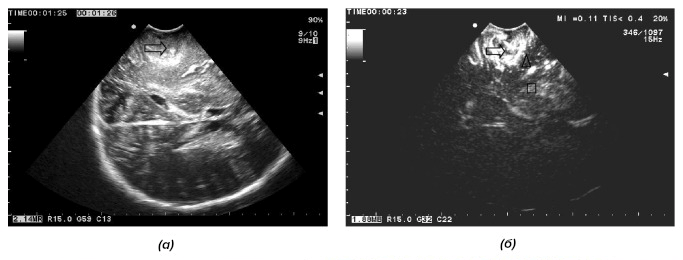
Рисунок 14. Интраоперационное ультразвуковое исследование (ИОУЗИ).
а — ИОУЗИ злокачественной глиомы: опухоль гиперэхогенна, имеет нечеткие границы и неоднородную внутреннюю эхо-структуру. Отек выражен отчетливо (стрелка указывает на опухоль).
б — ИОУЗИ с контрастом: эхо-сигнал от глиомы (стрелка) значительно усиливается; отек головного мозга (треугольник) — меньше; а нормальная ткань мозга (рамка) — еще меньше.
Сравнение с другими методами: где ультразвук выигрывает
Место УЗИ в нейровизуализации определяется не тем, что он видит лучше МРТ, ведь по детализации анатомии он значительно уступает; а тем, что он делает возможным то, что МРТ и КТ сделать не могут.
-
Портативность. Ультразвуковой аппарат можно привезти в реанимацию, операционную, приемный покой. Это критически важно для нестабильных пациентов, которых невозможно транспортировать в кабинет МРТ.
-
Мониторинг в реальном времени. Ни МРТ, ни КТ не позволяют наблюдать кровоток непрерывно в течение длительного времени.
-
Отсутствие лучевой нагрузки. Особенно ценно при многократных повторных исследованиях у новорожденных.
-
Интерактивность. Врач управляет датчиком в реальном времени, ориентируясь на клиническую ситуацию и немедленно получая ответ.
Таким образом, ультразвук в визуализации головного мозга — это не вчерашний день диагностики, вытесненный более современными методами, а живая и развивающаяся область, занимающая собственную, незаменимую нишу. Там, где МРТ требует неподвижности и времени, где КТ несет лучевую нагрузку, где любой другой метод невозможен у постели тяжелого больного — именно ультразвук остается глазами врача в самых сложных клинических ситуациях.
Ангиография: как увидеть сосуды мозга
Структурная МРТ показывает вещество мозга, КТ делает акцент на костях и свежей крови. Но ни тот ни другой метод не отвечают на вопрос, который нередко оказывается самым важным: что происходит внутри сосудов? Просвет артерии, скорость и характер кровотока, наличие тромба, аневризмы или патологического сплетения сосудов — все это требует отдельного класса методов, объединенных термином «ангиография».
Значимость этого вопроса трудно переоценить. Большинство острых неврологических катастроф (ишемический и геморрагический инсульт, разрыв аневризмы, тромбоз венозного синуса) непосредственно связаны с нарушением кровотока. Промедление с диагностикой в таких случаях означает гибель нейронов. Именно поэтому быстрая и точная визуализация сосудистого русла стала одним из ключевых направлений развития нейрорадиологии.
Сегодня под термином «ангиография» понимают три принципиально разных метода: КТ-ангиографию (КТА), МР-ангиографию (МРА) и цифровую субтракционную ангиографию (ЦСА). Каждый из них имеет свои преимущества и недостатки.
КТ-ангиография: скорость и детализация в экстренной ситуации
Болюсное контрастирование — это метод введения контрастного вещества в вену с высокой скоростью (2–7 мл/с) с помощью автоматического инжектора.
Современные мультидетекторные КТ позволяют получить трехмерную реконструкцию всего артериального круга мозга — от дуги аорты до дистальных ветвей средней мозговой артерии — за 5–10 секунд сканирования. Полученные объемные данные можно просматривать в любой плоскости, строить трехмерные реконструкции и виртуально «вращать» сосудистое дерево.
Именно скорость делает КТА незаменимой в экстренной ситуации. При подозрении на окклюзию крупной артерии — одну из самых опасных форм ишемического инсульта — КТА выполняется немедленно после нативной КТ и позволяет за минуты подтвердить или исключить тромбоз. КТА с успехом выявляет также стенозы магистральных артерий, аневризмы диаметром от 2–3 мм и артериовенозные мальформации, и широко используется при планировании как эндоваскулярных, так и открытых хирургических вмешательств (рис. 15) [37], [38].
Главные ограничения КТА — ионизирующее излучение и нефротоксичность йодсодержащих контрастных веществ. Последнее особенно актуально у пациентов с хронической болезнью почек. Кроме того, у пациентов с аллергической реакцией на йодсодержащий контраст в анамнезе необходимо использовать альтернативные методы диагностики или проводить премедикацию.
МР-ангиография: безопасность и возможность повторных исследований
МР-ангиография (МРА) —
семейство МРТ-методик, позволяющих визуализировать сосуды без ионизирующего излучения. Она может выполняться как с контрастным усилением (гадолиний-содержащие препараты), так и полностью без него. Именно бесконтрастные варианты представляют особый интерес.
Наиболее распространенная бесконтрастная методика — TOF (time-of-flight). Ее принцип основан на различии в магнитных свойствах движущейся крови и неподвижных тканей. В зоне сканирования статичные ткани получают многократные РЧ-импульсы и постепенно «насыщаются», то есть их сигнал угасает. Свежая ненасыщенная кровь, непрерывно притекающая в зону сканирования, дает яркий сигнал на фоне темного мозгового вещества, так что просвет сосудов буквально «светится» без использования какого-либо контраста.
Другая бесконтрастная методика — PC (phase-contrast) МРА — использует фазовые сдвиги перемещающихся протонов крови для создания изображения сосудов и даже количественной оценки скорости кровотока. Это позволяет не просто увидеть сосуд, но и измерить, с какой скоростью движется кровь, что особенно ценно при оценке гемодинамической значимости стеноза [40].
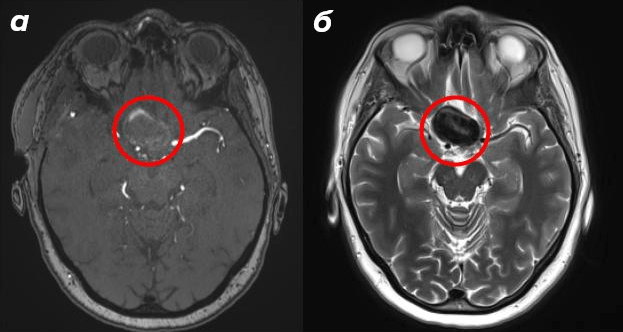
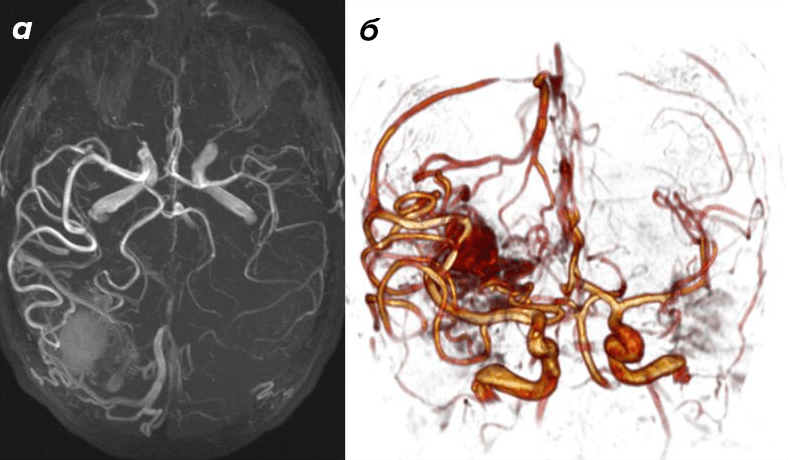
МРА позволяет надежно выявлять стенозы и окклюзии, интракраниальные аневризмы, артериовенозные мальформации и венозные тромбозы (рис. 16). Отсутствие лучевой нагрузки и возможность проведения без использования контрастного препарата делает ее методом выбора при динамическом наблюдении — например, для контроля за размером аневризмы после ее клипирования или для мониторинга стеноза в ходе консервативной терапии.
Вместе с тем МРА имеет и ограничения: метод чувствителен к турбулентному кровотоку. В зонах завихрений (у шейки аневризмы или при выраженном стенозе) сигнал от крови падает, что может имитировать более выраженное поражение, чем есть на самом деле. Пространственное разрешение МРА также уступает КТА и тем более ЦСА (см. ниже), что затрудняет визуализацию артерий диаметром менее 1 мм. Наконец, длительность МРА-исследования выше, чем КТА, что ограничивает ее применение в экстренных ситуациях.
Цифровая субтракционная ангиография: «золотой стандарт», за который нужно платить
Техника ЦСА такова: через пункцию бедренной или лучевой артерии под местной анестезией вводится катетер, который под рентгеновским контролем проводится в аорту, а затем в сонные или позвоночные артерии. В нужный момент через катетер вводится контрастное вещество, и аппарат выполняет серию быстрых рентгеновских снимков. Ключевой элемент технологии — субтракция: компьютер вычитает из изображения с контрастом «маску» (снимок, сделанный до его введения). В результате кости и мягкие ткани «исчезают», и остается только контрастированное сосудистое русло в мельчайших деталях [41].
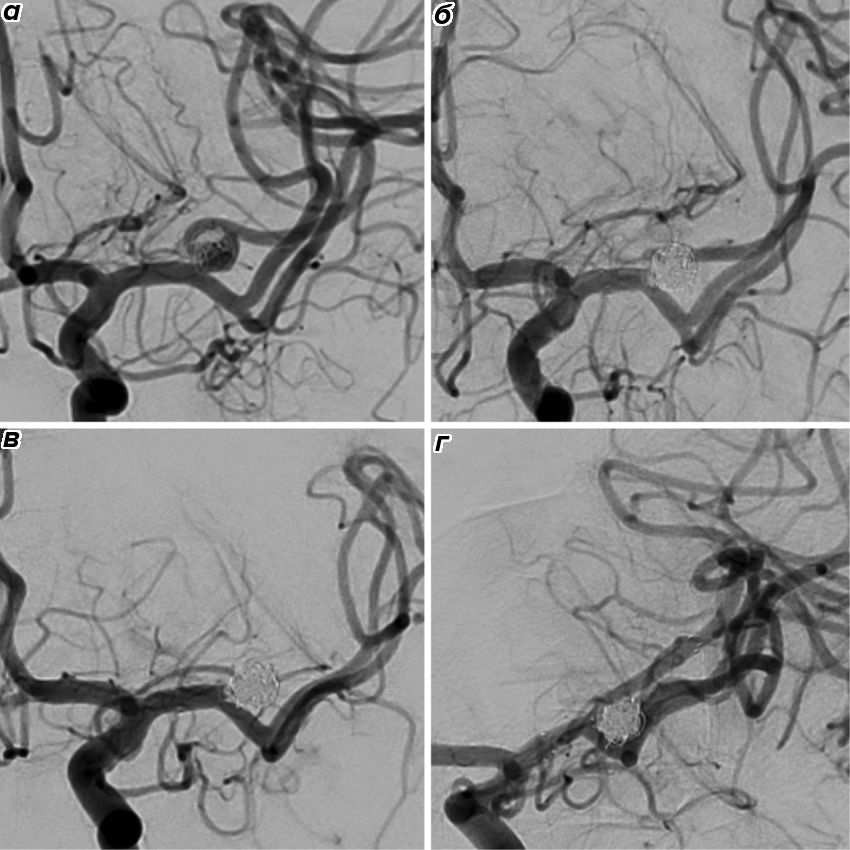
Пространственное разрешение ЦСА существенно превосходит КТА и МРА: четко видны сосуды диаметром менее 1 мм, можно оценивать точную форму и размер шейки аневризмы, анализировать архитектуру питающих и дренирующих сосудов артериовенозной мальформации. Не менее важно и временно́е разрешение. Снимая несколько кадров в секунду, ЦСА позволяет наблюдать движение контраста в реальном времени: видеть, как заполняется аневризма, как перераспределяется кровоток после вмешательства, есть ли ранний венозный сброс (рис. 17).
Но главное преимущество ЦСА — это возможность проведения немедленного лечебного вмешательства. Через тот же катетер, не меняя доступа, возможно эмболизировать аневризму, восстановить проходимость тромбированной артерии, провести химиоэмболизацию сосудистой мальформации или стентирование стенозированной артерии. Именно это делает ЦСА не просто диагностическим, а диагностически-терапевтическим методом.
Однако цена этой точности высока. ЦСА — инвазивная процедура со всеми вытекающими рисками: повреждение стенки артерии в месте пункции, диссекция сосуда при продвижении катетера, тромбоэмболические осложнения, включая инсульт. Это пусть и редкие, но реальные риски. По данным крупных исследований, частота всех неврологических осложнений ЦСА составляет около 0,7–2,6%, тогда как частота возникновения стойкого неврологического дефицита — около 0,1–0,4% [42]. Кроме того, процедура сопровождается значительной лучевой нагрузкой, введением йодсодержащего контраста и требует наблюдения пациента после процедуры.
Как выбрать метод: клиническая логика
Три метода ангиографии — это не конкурирующие технологии, а взаимодополняющие инструменты, каждый из которых оптимален в своей клинической ситуации (табл. 1). Практическая логика выбора выглядит так. При остром инсульте выбирают КТА: быстро, точно, достаточно для решения о тромбэктомии. При динамическом наблюдении за известной аневризмой или стенозом у молодого пациента — МРА: без излучения, можно повторять многократно. При сложной сосудистой патологии, неоднозначных результатах неинвазивных методов или необходимости эндоваскулярного вмешательства проводят ЦСА. Нередко методы используются последовательно: КТА или МРА ставят вопрос, ЦСА дает окончательный ответ, и, при необходимости, сразу же решает проблему.
|
КТА |
МРА |
ЦСА |
|
|---|---|---|---|
|
Скорость |
Секунды |
Минуты |
30–60 мин |
|
Инвазивность |
Нет |
Нет |
Да |
|
Излучение |
Да |
Нет |
Да |
|
Разрешение |
Высокое |
Среднее |
Максимальное |
|
Мелкие сосуды |
Хорошо |
Ограниченно |
Отлично |
|
Лечебный потенциал |
Нет |
Нет |
Да |
|
Повторные исследования |
Ограниченно |
Оптимально |
Ограниченно |
Функциональная МРТ: как увидеть работу мозга
Структурная МРТ по сути показывает, где и что находится, какого размера, какой формы, изменена ли ткань. Но мозг — это не статичный орган. Его смысл в непрерывной работе: нейроны генерируют потенциалы действия, синапсы передают сигналы, сети активируются и затихают. Структурный снимок фиксирует момент, но не процесс.
Функциональная МРТ (фМРТ) делает следующий шаг: она позволяет наблюдать за работающим мозгом, пусть и косвенно. Именно это превратило ее из инструмента фундаментальной науки в арсенале ученых в клинически значимый метод, без которого сегодня немыслима нейрохирургия, эпилептология и значительная часть нейронауки. Для проведения фМРТ уже недостаточно просто «положить» пациента в томограф: для такого исследования требуется целый арсенал специализированного оборудования и действий (рис. 18).
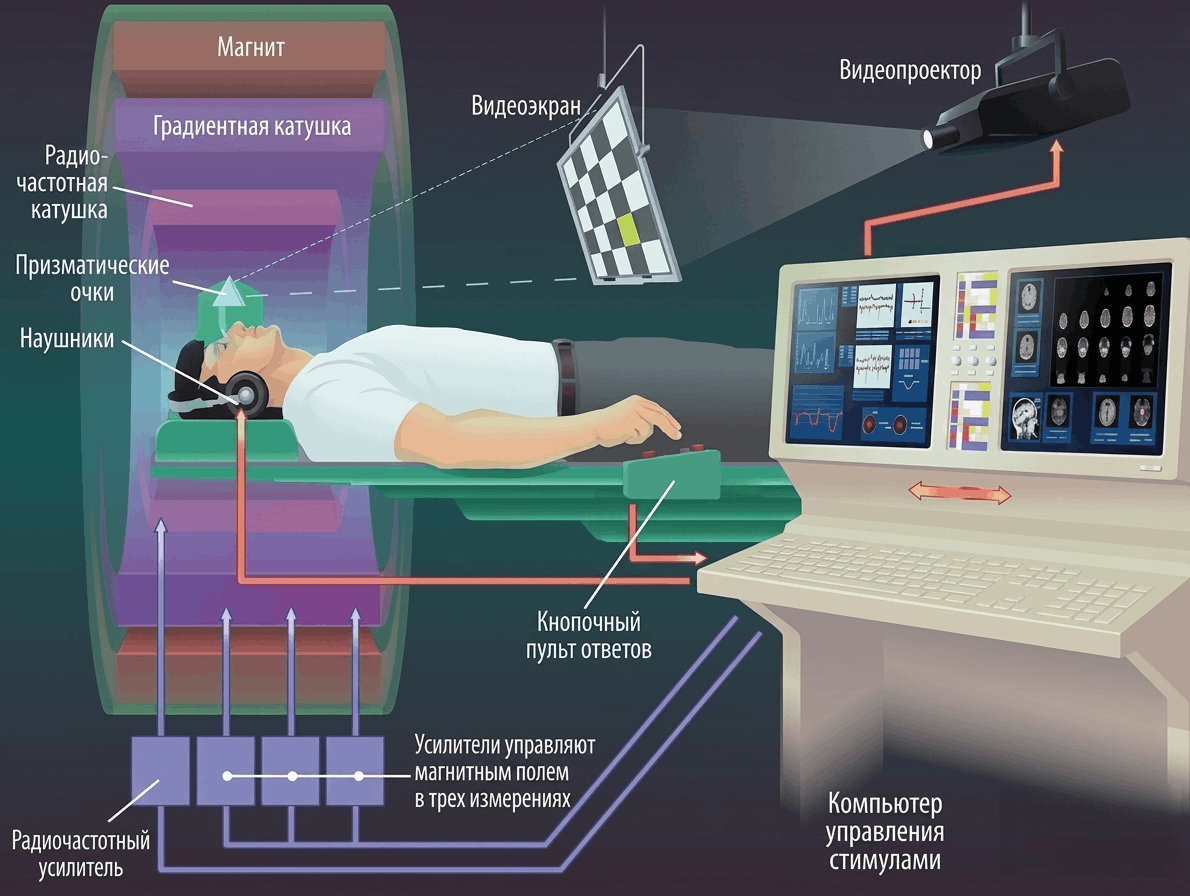
Рисунок 18. Комплекс оборудования, необходимого для проведения фМРТ-исследования. Основа всего — высокопольный МР-томограф с магнитной индукцией от 1,5 Тесла и выше: чем сильнее поле, тем отчетливее улавливаются тонкие изменения сигнала, связанные с нейрональной активностью. Если необходимо увидеть, как мозг решает когнитивную задачу или реагирует на раздражитель, понадобится еще и система предъявления стимулов: МР-совместимые видеоэкраны, специальные очки или зеркало, наушники и кнопочные пульты, с помощью которых испытуемый отвечает на вопросы или реагирует на сигналы, не покидая магнитного поля. Наконец, полученный массив данных требуют мощных вычислительных станций и специализированного программного обеспечения, без которых превратить «сырые» изображения в осмысленные карты активации попросту не получится.
fMRI data analysis with FSL, с изменениями
Физика BOLD-сигнала: почему кровь «знает» о мыслях
В основе фМРТ лежит принцип BOLD-контраста (англ. Blood Oxygenation Level Dependent — контраст, зависящий от уровня оксигенации крови), а чтобы понять его, нужно вспомнить несколько фактов о крови и магнетизме.
Гемоглобин существует в двух формах. Насыщенный кислородом оксигемоглобин практически не влияет на магнитное поле. А вот «отдавший» кислород дезоксигемоглобин обладает выраженными парамагнитными свойствами: он создает локальные неоднородности магнитного поля, которые ускоряют потерю фазовой согласованности протонов и тем самым снижают МР-сигнал (рис. 19).
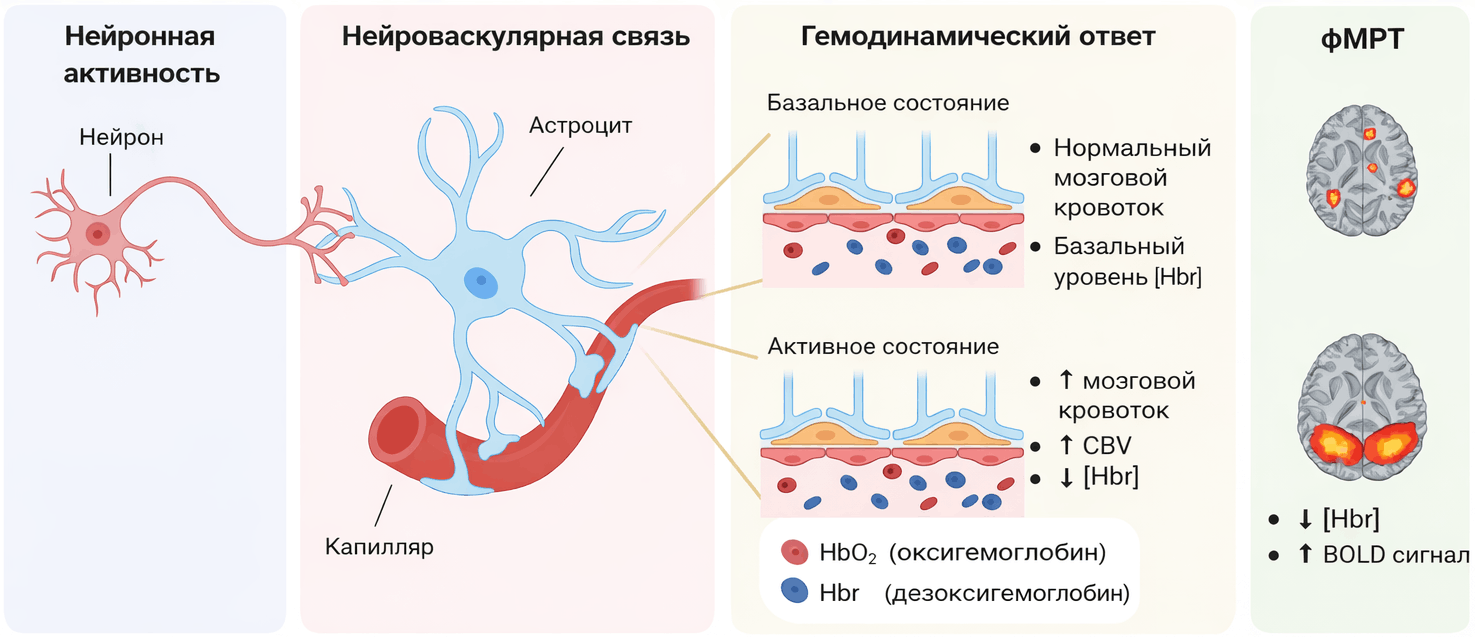
Рисунок 19. Нейронные и сосудистые компоненты, влияющие на BOLD-сигнал фМРТ. Когда группа нейронов активируется, ее энергетические потребности резко возрастают, на что мозг отвечает увеличением локального кровотока. Причем реакция оказывается избыточной: приток насыщенной кислородом крови превышает реальное потребление кислорода нейронами. В результате концентрация дезоксигемоглобина в капиллярах активной зоны снижается, неоднородности поля уменьшаются, а локальный МР-сигнал растет. Именно это изменение сигнала и регистрирует фМРТ.
Alice Giubergia | BioRender, с изменениями
Важно понимать: фМРТ измеряет не электрическую активность нейронов напрямую, а нейроваскулярный ответ — сосудистую реакцию на нейронную активность. Между электрическим разрядом нейрона и пиком BOLD-сигнала проходит 4–6 секунд, поскольку сосудам необходимо время, чтобы отреагировать. Такая задержка, описываемая функцией гемодинамического отклика (hemodynamic response function, HRF), накладывает принципиальные ограничения на временно́е разрешение метода: фМРТ видит, где активирован мозг, с точностью до миллиметров; и когда именно — но с точностью лишь до секунд. Для сравнения: ЭЭГ регистрирует электрическую активность с точностью до миллисекунд, но практически не способна локализовать ее источник в глубоких структурах мозга. Таким образом, фМРТ и ЭЭГ не конкурируют, а дополняют друг друга [45].
фМРТ с парадигмами: мозг на задании
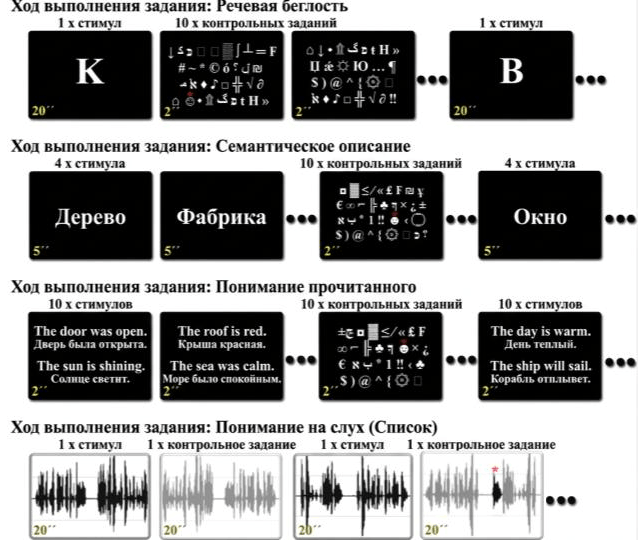
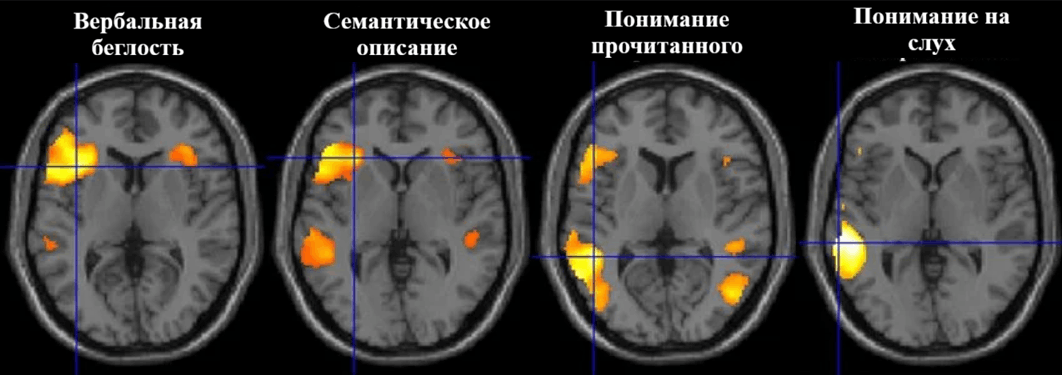
Первый и наиболее интуитивно понятный подход — фМРТ с парадигмами (task-based fMRI). Логика заключается в том, что мы просим пациента выполнить задание, активирующее интересующую нас зону мозга, а затем сравниваем сигнал во время выполнения с сигналом в контрольном состоянии. Разница и есть «карта активации». Парадигмами называют типы задач, которые выполняет пациент: моторные, речевые, сенсорные или когнитивные.
На практике это может выглядеть так: пациент поочередно сжимает кулак и расслабляет руку (моторная парадигма), а врач видит активацию первичной моторной коры. Если пациент произносит вслух слова (речевая парадигма), то активируются зоны Брока и Вернике, и так далее. Действие из той или иной парадигмы освещает свой функциональный ландшафт (рис. 20).
Дизайн парадигм для максимизации точности исследования — отдельное искусство. Классическим считается блочный подход: пациент поочередно выполняет задание и отдыхает блоками по 20–30 секунд, что дает устойчивый и воспроизводимый сигнал. Но иногда используют событийный дизайн. В таком случае стимулы предъявляются по одному с разными интервалами, что позволяет разделять ответы на отдельные события и изучать более тонкие когнитивные процессы, но требует более сложного статистического анализа.
Главным клиническим применением фМРТ с парадигмами стало предоперационное картирование. Перед удалением опухоли, расположенной вблизи функционально значимых зон, нейрохирург должен знать, где именно проходит граница между пораженной тканью и корой, обеспечивающей речь или движение. фМРТ позволяет неинвазивно нанести эти зоны на карту и спланировать доступ так, чтобы максимально радикально удалить опухоль, минимизировав риск послеоперационного неврологического дефицита [46].
Ограничения метода тесно связаны с его природой. Он требует сотрудничества пациента: человек должен понимать задание, удерживать внимание, выполнять команды. При этом выполнение нужной парадигмы не всегда физически осуществимо — например, пациент с афазией не может выполнять речевые задания; пациент с парезом испытывает трудности со сжатием кулака; а человек с выраженной тревогой скорее всего не справится с тем, чтобы сохранять неподвижность. Дополнительную сложность вносит нейропластичность: при опухолях и других объемных поражениях функциональные зоны могут смещаться или реорганизовываться относительно их типичной локализации — и тогда стандартные атласы головного мозга оказываются ненадежным ориентиром при планировании операции [47].
фМРТ покоя: неспокойное спокойствие
Второй подход кажется парадоксальным: пациент ничего не делает — просто лежит с закрытыми глазами, стараясь ни о чем не думать. И тем не менее именно этот режим открыл один из самых неожиданных феноменов современной нейронауки.
В 1995 году группа Бхарата Бисвала обнаружила, что в состоянии покоя BOLD-сигнал в разных отделах мозга синхронно колеблется на низких частотах (0,01–0,1 Гц). Причем синхронными оказались именно те области, которые анатомически и функционально связаны между собой. Левая и правая моторная кора пульсирует в унисон, хотя пациент не совершает никаких движений. То же наблюдается с зонами зрения, слуха, речи. Это открытие положило начало концепции функциональных нейронных сетей покоя (resting-state networks, RSN), или функциональной коннективности головного мозга [49].
Наиболее изученная из них — сеть пассивного режима работы мозга (default mode network, DMN). Она активна именно тогда, когда человек не занят внешней задачей, включает медиальную префронтальную и заднюю поясную кору, угловую извилину. Считается, что DMN связана с самореференцией, планированием будущего и извлечением эпизодических воспоминаний. При болезни Альцгеймера эта сеть одной из первых теряет связность, а ведь ее нарушения на фМРТ покоя можно обнаружить за годы до появления клинических симптомов (с одним важным уточнением — речь пока идет о групповых различиях в исследованиях, а не о диагностическом инструменте для отдельного пациента) [50].
Помимо DMN, описаны десятки других сетей: сенсомоторная, зрительная, сеть выявления значимости, центральная исполнительная сеть и другие (рис. 21). Нарушения их связности характерны для шизофрении, депрессии, аутизма, СДВГ и становятся предметом активных исследований как потенциальные биомаркеры этих состояний.
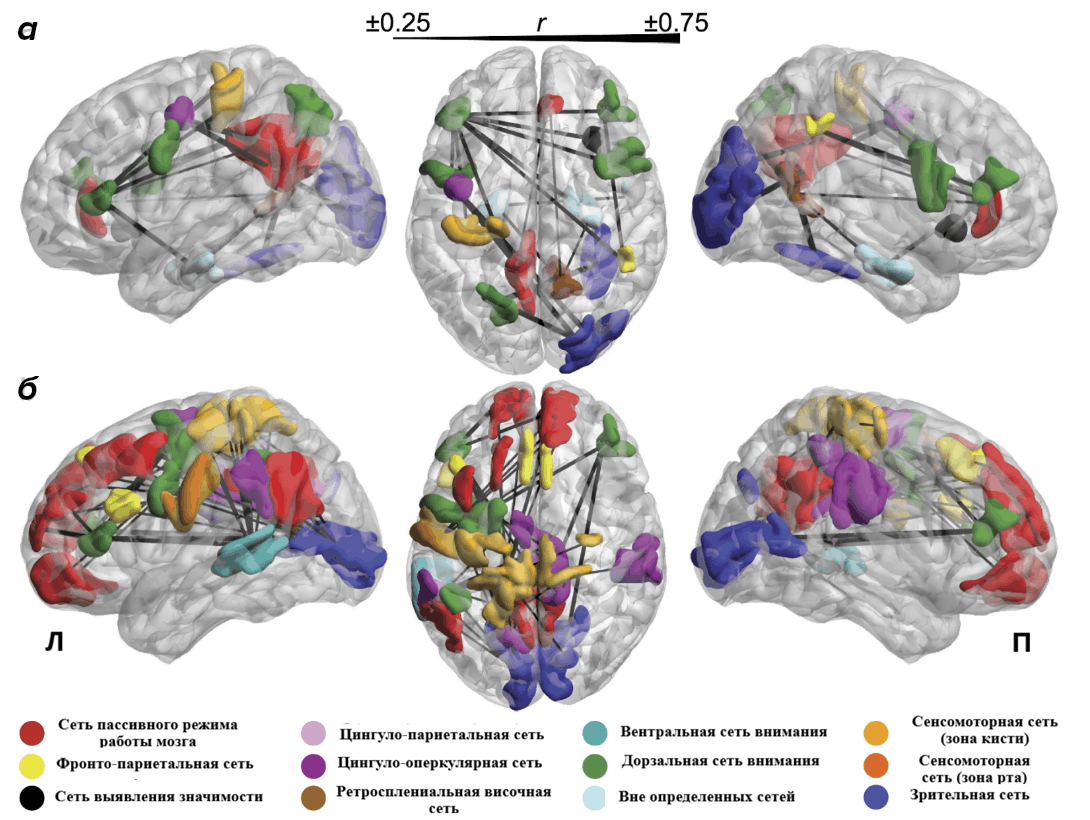
Рисунок 21. Функциональные сети мозга, связанные с индивидуальными различиями в интеллекте человека. а — сети, в которых более высокая функциональная коннективность коррелировала с более высоким интеллектом. б — сети, в которых более низкая функциональная коннективность (т. е. снижение положительных корреляций и/или усиление антикорреляций) коррелировала с более высоким интеллектом.
Ключевое практическое достоинство фМРТ покоя — независимость от активного участия пациента. Именно поэтому метод применим там, где фМРТ с парадигмами невозможна: у детей раннего возраста, пациентов с афазией, нарушением сознания или тяжелыми когнитивными расстройствами. В нейрохирургии фМРТ покоя начинает использоваться как альтернатива или дополнение к функциональному картированию с парадигмами, особенно когда пациент не способен выполнить задание.
Обратной стороной метода является сложность интерпретации результатов. Нет четкого стимула, нет контрольного состояния, а следовательно нет однозначной связи между наблюдаемыми колебаниями и конкретными когнитивными процессами. Результат существенно зависит от того, что именно делает пациент в сканере (думает, засыпает, двигает глазами), от алгоритмов предобработки данных и от статистических порогов. Воспроизводимость результатов между разными исследовательскими группами и на разных аппаратах остается предметом активной дискуссии.
Клиническое применение и ограничения фМРТ: между картой активации и диагнозом
Долгое время фМРТ оставалась преимущественно исследовательским инструментом из-за сложностей в обработке и интерпретации, что было серьезным барьером для перехода в повседневную клиническую практику. Однако сегодня граница между лабораторией и клиникой постепенно стирается. Во многом это стало возможным благодаря появлению стандартизированных конвейеров обработки данных, которые автоматизируют рутинные этапы предобработки и существенно снижают зависимость результата от квалификации оператора. Параллельно развиваются методы машинного обучения, позволяющие выявлять клинически значимые паттерны активности и коннективности там, где традиционный статистический анализ давал неоднозначные результаты. Наконец, рост вычислительных мощностей сократил время обработки с часов до минут, сделав метод практически применимым в предоперационной подготовке. Все это позволяет фМРТ находить уже вполне конкретное применение в нейрохирургии, неврологии и психиатрии.
Нейрохирургия: удалить опухоль, сохранив речь
Выше мы уже упомянули, что предоперационное картирование функционально значимых зон мозга стало основным применением фМРТ, имеющим в том числе хорошее клиническое обоснование. Когда опухоль располагается вблизи областей, ответственных за движение, речь или чувствительность, хирург оказывается перед непростой задачей: удалить патологический очаг максимально полно, не повредив при этом то, что делает пациента собой — способность говорить, двигаться, понимать речь.
Дело в том, что анатомия мозга при всей схожести внутри группы обладает и довольно выраженными индивидуальными чертами: у разных людей речевые зоны могут смещаться, а опухоль способна и вовсе вытеснить функцию в соседние области, и никакой стандартизированный атлас головного мозга этого не покажет. Полученные карты активации интегрируются в системы нейронавигации, которые в режиме реального времени помогают хирургу ориентироваться во время операции. Это позволяет максимально безопасно подойти к опухоли, снизить риск послеоперационного неврологического дефицита и при необходимости расширить объем резекции там, где без такой карты хирург был бы вынужден отступить [63].
Неврология: нейропластичность под наблюдением
В неврологической практике фМРТ используется прежде всего как инструмент для изучения и мониторинга того, как мозг перестраивается после повреждения. После инсульта, черепно-мозговой травмы или нейрохирургической операции мозг способен частично перераспределять функции: здоровые области берут на себя работу поврежденных. Этот процесс, называемый нейропластичностью, можно наблюдать в динамике с помощью повторных фМРТ-исследований, оценивая, как меняются карты активации по мере восстановления пациента, какие сети перестраиваются и насколько эта перестройка коррелирует с клиническим улучшением [64].
Особую область применения представляют пациенты с нарушениями сознания: в вегетативном состоянии или состоянии минимального сознания. Классические клинические методы оценки сознания основаны на наблюдении за поведением, но некоторые пациенты могут осознавать происходящее вокруг них, не имея возможности это продемонстрировать. Исследования показали, что часть таких пациентов способна произвольно модулировать активность мозга в ответ на инструкции, например, представлять навигацию по знакомому дому, что регистрируется с помощью фМРТ даже при полном отсутствии внешних поведенческих реакций. Это не только меняет диагностическую оценку, но и ставит глубокие этические вопросы о принятии медицинских решений в отношении таких пациентов [65], [66].
Психиатрия: увидеть депрессию и не только
В психиатрии фМРТ пока остается преимущественно исследовательским инструментом, однако масштаб накопленных данных уже позволяет говорить о наличии устойчивых закономерностей. При депрессии стабильно выявляется гиперактивность медиальной префронтальной коры и нарушения коннективности внутри сети пассивного режима работы. Эти две структуры связаны с руминацией и самореференциальным мышлением. При шизофрении обнаруживается дезинтеграция связей между префронтальной корой и лимбическими структурами, а также нарушения в сетях, обеспечивающих предсказание и обработку ошибок. При расстройствах аутистического спектра фМРТ выявляет атипичные паттерны коннективности в социально-когнитивных сетях. Однако здесь важно сделать принципиальную оговорку: несмотря на воспроизводимость этих закономерностей на уровне групп, их диагностическая ценность на уровне индивидуума остается ограниченной. фМРТ-данные пациентов столь разнообразны, что ни один из выявленных паттернов пока не достиг порога клинической применимости в качестве самостоятельного диагностического биомаркера. Именно поэтому фМРТ в психиатрии на сегодняшний день следует рассматривать как инструмент, помогающий понять механизм заболевания и, возможно, разработать новые терапевтические мишени, но не способный полноценно заменить клиническую диагностику [67], [68].
Отдельного упоминания заслуживает фармакологическая фМРТ — подход, в котором стимулом служит не выполнение задания, а ответ на фармакологический препарат. Регистрируя BOLD-ответ на введение конкретной молекулы, исследователи могут картировать зоны мозга, чувствительные к ее действию, и изучать механизмы действия антидепрессантов, антипсихотиков, противоэпилептических средств и экспериментальных соединений. Это открывает возможности для персонализации терапии и прогнозирования ответа на лечение еще до его начала [69].
Вместе с тем необходимо учитывать принципиальные ограничения метода. Напомним, что BOLD-сигнал остается косвенным показателем: он отражает сосудистую, а не нейрональную активность — следовательно, любые патологии сосудов или изменения метаболизма могут искажать его интерпретацию. В то же время статистические пороги и выбор алгоритмов существенно влияют на конечный результат, — а это означает, что карта активации всегда является результатом не только физических измерений, но и методологических решений исследователя.
Функциональная МРТ позволила нейронауке перейти от вопроса «где?» к вопросу «как?», от структуры к локализации функций и изучению сетевой организации мозга. Но, как и любой метод, она показывает лишь часть картины — ту, которую позволяет увидеть физика явления и математика анализа.
Сравнение методов визуализации
Ни один из методов нейровизуализации не обладает абсолютным превосходством над остальными — каждый имеет свои сильные стороны и недостатки, которые мы успели рассмотреть ранее. Представленные ниже сравнительные таблицы 2 и 3 систематизируют эту информацию, помогая ориентироваться в многообразии доступных инструментов.
|
Метод |
Физ. принцип |
РГ-излучение |
Скорость |
Инвазивность |
Контраст |
Преимущества |
Ограничения |
Преимущественное применение |
|---|---|---|---|---|---|---|---|---|
|
КТ |
Рентгеновское излучение, послойная реконструкция |
Да, |
★★★★★ |
Нет (в/в катетер при контрастировании) |
Йодсодержащий / нет |
Скорость; кровь, кость, кальций; совместимость с металлическими имплантатами; широкая доступность |
Лучевая нагрузка; слабый контраст мягких тканей; артефакты задней черепной ямки |
Острое кровоизлияние, ЧМТ, переломы, экстренный скрининг |
|
МРТ |
Ядерный магнитный резонанс |
Нет |
★★☆☆☆ |
Нет (в/в катетер при контрастировании) |
Гадолинийсодержащий / нет |
Наилучший контраст мягких тканей; семейство режимов (DWI, SWI, FLAIR, и т.д.); нет излучения; мультипланарность |
Длительность; клаустрофобия; несовместимые имплантаты; стоимость; артефакты движения |
Опухоли, демиелинизация, ранняя ишемия, нейродегенерация, предоперационное планирование |
|
фМРТ |
BOLD-контраст (оксигенация крови) |
Нет |
★☆☆☆☆ |
Нет |
Нет |
Картирование функциональных зон и сетей мозга |
Косвенный сигнал (нейроваскулярный ответ); артефакты движения; сложная обработка; требует участия пациента |
Предоперационное картирование речи и моторики, нейронаука, групповые психиатрические исследования |
|
НСГ |
УЗИ через большой родничок |
Нет |
★★★★★ |
Нет |
Нет |
Портативность; прикроватная диагностика; нет излучения; повторяемость без ограничений |
Только при открытом родничке (до ~18 мес); ограниченная анатомическая детализация |
ВЖК у недоношенных, гидроцефалия, перивентрикулярная лейкомаляция |
|
ИОУЗИ |
УЗИ, датчик на поверхность мозга |
Нет |
★★★★★ |
Да |
Нет / микропузырьки |
Актуальная навигация без «сдвига мозга»; выявление остатков опухоли непосредственно в ходе операции |
Требует открытого хирургического доступа; уступает МРТ по анатомическому разрешению |
Интраоперационный контроль резекции опухолей, уточнение границ удаления |
Таблица в полном размере.
|
Метод |
Физ. принцип |
Излучение |
Скорость |
Инвазивность |
Контраст |
Ключевые преимущества |
Ключевые ограничения |
|---|---|---|---|---|---|---|---|
|
КТА |
Рентгеновское излучение |
Да, |
★★★★★ |
Нет |
Йодсодержащий (обязателен) |
Максимальная скорость; 3D-реконструкция артериального дерева; высокое пространственное разрешение; широкая доступность |
Ионизирующее излучение; нефротоксичность контраста; риск аллергической реакции на йод |
|
МРА |
МРТ (TOF, PC) |
Нет |
★★★☆☆ |
Нет |
Гадолинийсодержащий / нет |
Нет ионизирующего излучения; бесконтрастные варианты (TOF,PC); безопасны для повторных и динамических исследований |
Чувствительность к турбулентному кровотоку; хуже визуализирует мелкие дистальные сосуды; длиннее КТА |
|
ЦСА |
Рентген + катетерный контраст + субтракция фона |
Да, |
★★☆☆☆ |
Да |
Йодсодержащий (обязателен) |
Наивысшее пространственное и временно́е разрешение; визуализация сосудов <1 мм; диагностика и эндоваскулярное лечение в одной процедуре |
Инвазивность; риск неврологических осложнений; высокая лучевая нагрузка; требует специализированной операционной и обученного персонала |
|
ТКДГ |
Эффект Доплера, низкие частоты (2 МГц) через акустическое окно черепа |
Нет |
★★★★★ |
Нет |
Нет / микропузырьки |
Непрерывный мониторинг кровотока в реальном времени; детекция микроэмболов; верификация смерти мозга; портативность |
Отсутствие акустического окна у 10–15% пациентов; нет анатомического изображения — только скорость потока |
|
Дуплекс БЦА |
B-режим УЗИ + цветовой доплер |
Нет |
★★★★☆ |
Нет |
Нет |
Морфология и структура бляшки; толщина комплекса интима-медиа (КИМ); оценка скорости кровотока; нет излучения; низкая стоимость |
Только экстракраниальные сосуды; не визуализирует интракраниальные артерии; результат зависит от опыта оператора |
Таблица в полном размере.
Искусственный интеллект в нейровизуализации: от изображения к данным
Почему рентгенология стала полигоном для ИИ
Когда в середине 2010-х годов алгоритмы глубокого обучения начали демонстрировать впечатляющие результаты в распознавании изображений , медицинское сообщество закономерно задалось вопросом: а что, если применить эти технологии к диагностическим снимкам?
Подробнее о методах компьютерного зрения мы писали в статьях «Глаза прогресса: как глубокое обучение помогает видеть невидимое для человека» [70] и «Смена подходов в компьютерном зрении: как ИИ открывал клетку заново» [71].
Рентгенология оказалась идеальной стартовой площадкой. Каждый КТ-срез — это матрица чисел, где каждое значение соответствует рентгеновской плотности конкретного вокселя, а каждый МРТ-скан — это набор интенсивностей сигнала. Для алгоритма машинного обучения разницы между фотографией кошки и аксиальным срезом мозга по существу нет. В обоих случаях на вход дается матрица чисел, на выходе получается классификация или сегментация значений [72].
Но у рентгенологии есть еще одно критическое преимущество: стандартизация и масштаб данных. С 1990-х годов медицинские изображения хранятся в формате DICOM (Digital Imaging and Communications in Medicine) — универсальном стандарте, который обеспечивает совместимость между аппаратами разных производителей и больницами разных стран. Крупные радиологические архивы содержат миллионы размеченных исследований, что стало идеальной библиотекой данных для глубокого машинного обучения. Там, где другие медицинские специальности только начинают собирать структурированные базы данных, рентгенология уже накапливала их десятилетиями [73].
Радиомика: то, что глаз не видит
Автоматизация рутинной диагностики — лишь первый уровень применения ИИ в нейровизуализации. Значительно более амбициозное направление — радиомика, суть которой состоит в извлечении из медицинских изображений количественной информации недоступной человеческому глазу [79]. Основы метода разобраны в статье «Увидеть то, что неподвластно глазу: как радиомика помогает врачам в диагностике опухолей» [80], а прочитав «Как аэрофотосъемка связана с медицинскими снимками, большими данными и ИИ?» [81] можно ознакомиться с конкретными примерами клинического применения радиомики, ее ограничениями и способами их преодоления. Сейчас же вспомним основные моменты. Радиомический анализ работает в несколько шагов (рис. 24). Ярким примером радиомики в действии является алгоритм, способный предсказывать молекулярный профиль глиомы (наличие мутации IDH1/2, коделецию 1p/19q, метилирование промотора MGMT) по МР-изображениям, без хирургической биопсии. Эти молекулярные маркеры критически важны для выбора терапии, но их определение требует инвазивного вмешательства [82].
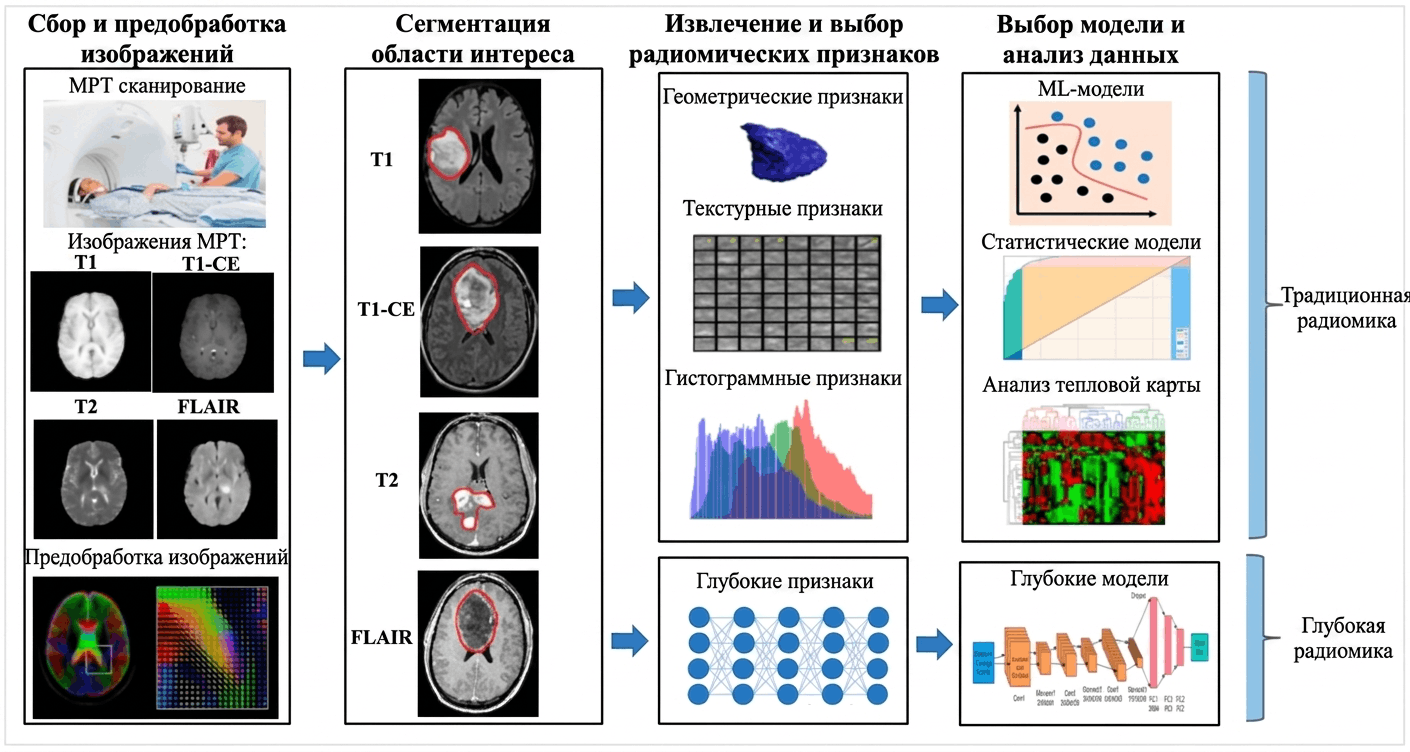
Рисунок 24. Этапы радиомического анализа для характеристики поражений головного мозга: от получения медицинских изображений до построения прогностических моделей. Сначала выполняется сегментация интересующей области любым из способов: вручную, полу- или полностью автоматически с помощью нейросети. Затем из очерченной области извлекается набор количественных признаков, при этом их число может достигать нескольких сотен и даже тысяч на одно изображение. Эти признаки условно делятся на несколько групп. Признаки формы описывают геометрию объекта: сферичность, компактность, соотношение осей, характер контуров. Признаки первого порядка характеризуют статистику интенсивностей: среднее значение, дисперсию, асимметрию гистограммы. Признаки второго порядка текстурные: они описывают пространственные взаимоотношения между вокселями, степень неоднородности ткани (матрицы GLCM, GLRLM и другие). Признаки высших порядков получают после применения математических фильтров, которые выделяют паттерны на разных пространственных масштабах. Наконец, «глубокая радиомика»— признаки, извлекаемые глубокими нейросетями автоматически, без ручного определения: они часто не имеют интуитивной интерпретации, но могут нести наибольшую прогностическую ценность. Из полученного массива методами статистического анализа и отбора признаков выделяется наиболее информативное подмножество. На его основе строится модель, способная предсказывать клинически значимые характеристики.
[83], с изменениями
Ограничения и нерешенные проблемы
При всем потенциале радиомика и ИИ в нейровизуализации сталкиваются с рядом серьезных вызовов, которые пока не позволяют говорить о повсеместном клиническом внедрении.
-
Воспроизводимость. Радиомические признаки чувствительны к параметрам сканирования: протокол МРТ, мощность магнита, производитель аппарата, толщина среза… все это влияет на числовые значения признаков. Модель, обученная на данных одного центра с одним протоколом, может давать принципиально иные результаты при применении в другом центре. Это так называемая проблема внешней валидации. Именно ее отсутствие является ахиллесовой пятой большинства публикаций в области радиомики. Исследований, где модель разрабатывается на данных одного центра и независимо проверяется на данных другого, остается меньшинство [82].
-
Переобучение. Когда число извлекаемых признаков (сотни и тысячи) значительно превышает число пациентов в выборке (нередко несколько десятков), модель рискует «запомнить» особенности конкретной обучающей выборки вместо того, чтобы выявить реальные биологические закономерности. Такая модель показывает высокую точность на обучающих данных, но — резко теряет ее на новых пациентах [85].
-
«Черный ящик». Глубокие нейросети принимают решения на основе паттернов, которые крайне сложно интерпретировать содержательно. Алгоритм может безошибочно классифицировать опухоль, но не может объяснить, какие биологические процессы стоят за выделенными им признаками. Это создает серьезное препятствие для клинического доверия: врач, принимающий решение о лечении, обоснованно хочет понимать логику системы, которой доверяет [86].
-
Регуляторные и этические вопросы. Внедрение ИИ-систем в клиническую практику требует четкого определения ответственности: кто несет юридическую ответственность за ошибочный диагноз, поставленный с участием алгоритма? Как обеспечить защиту персональных данных при обучении моделей на больших архивах изображений? Эти вопросы активно обсуждаются регуляторными органами по всему миру, и единого готового решения пока нет [87].
ИИ как дополнительный инструмент, а не замена врача-рентгенолога
Дискуссия о том, заменит ли ИИ врача-рентгенолога, возникла практически сразу. Сегодня большинство специалистов склоняются к более взвешенной позиции: ИИ не заменяет рентгенолога, а меняет характер его работы. Рутинные задачи, такие как первичный просмотр исследований, измерения анатомических структур или выявление очевидной патологии, алгоритмы выполняют быстрее и с сопоставимой точностью. Это освобождает врача для более сложной аналитической работы: сопоставления данных разных методов, клинической интерпретации неоднозначных диагностических случаев, взаимодействия с клиницистами. Система ИИ становится инструментом «второго мнения», не заменяя суждение врача, а снижая вероятность того, что патология будет пропущена из-за усталости, высокой нагрузки или простой невнимательности.
Таким образом, если первые этапы развития нейровизуализации позволили увидеть структуру мозга, а затем и его функцию, то ИИ и радиомика открывают следующий диагностический уровень — количественный анализ скрытых закономерностей, недоступных невооруженному взгляду. Это не революция, а эволюция инструментария: каждое новое поколение методов не вытесняет предыдущее, а добавляет новое измерение к нашему пониманию.
Заключение: нейровизуализация как диалог с мозгом, а не готовый ответ
Еще сто лет назад врач, столкнувшийся с пациентом с неврологическим дефицитом, располагал крайне ограниченным арсеналом. Мозг оставался органом, о внутреннем устройстве которого можно было судить лишь косвенно — по симптомам или посмертно на вскрытии.
Сегодня за несколько часов можно получить послойные изображения мозга с субмиллиметровым разрешением, оценить кровоток в сосуде, порой диаметром менее миллиметра, увидеть, какие зоны коры активируются при счете или произнесении слов, измерить диффузию молекул воды вдоль нервных волокон, а потенциально и извлечь из изображения сотни количественных признаков, невидимых человеческому глазу.
Каждая диагностическая методика, рассмотренная в этой статье, приближает нас к пониманию головного мозга, но при всем технологическом прогрессе один принцип остается неизменным — универсального метода диагностики в нейровизуализации не существует.
Каждый инструмент — это компромисс. КТ быстра, но использует рентгеновское излучение и плохо дифференцирует мягкие ткани. МРТ детализирована, но требует больше времени и противопоказана при некоторых металлических имплантах. ЦСА крайне точна, но инвазивна. фМРТ показывает работу мозга, но регистрирует не нейронную активность, а ее сосудистый отклик. Радиомика извлекает скрытые признаки, но страдает от проблем воспроизводимости и интерпретируемости.
Выбор метода остается клиническим решением, требующим от врача хорошего понимания всех аспектов: заболевания, анамнеза пациента, противопоказаний и диагностических вопросов, на которые необходимо найти ответы. Технология предоставляет возможности, а клиническое мышление определяет, какую из них использовать.
Будущее области, по всей видимости, связано не столько с появлением принципиально новых физических методов, сколько с интеграцией уже существующих. Структурные, функциональные, метаболические и молекулярные данные, собранные в единую цифровую модель состояния мозга конкретного пациента, способны дать несравнимо больше, чем каждый метод по отдельности.
Параллельно развивается сверхвысокопольная МРТ: томографы с магнитной индукцией 7 Тесла и выше, уже одобренные для клинического применения, позволяют визуализировать структуры, недоступные стандартным 1,5–3 Тл аппаратам. К таким структурам относятся отдельные корковые слои, мелкие сосуды, ядра таламуса. Это открывает новые возможности в диагностике эпилепсии, рассеянного склероза и нейродегенеративных заболеваний (рис. 25).
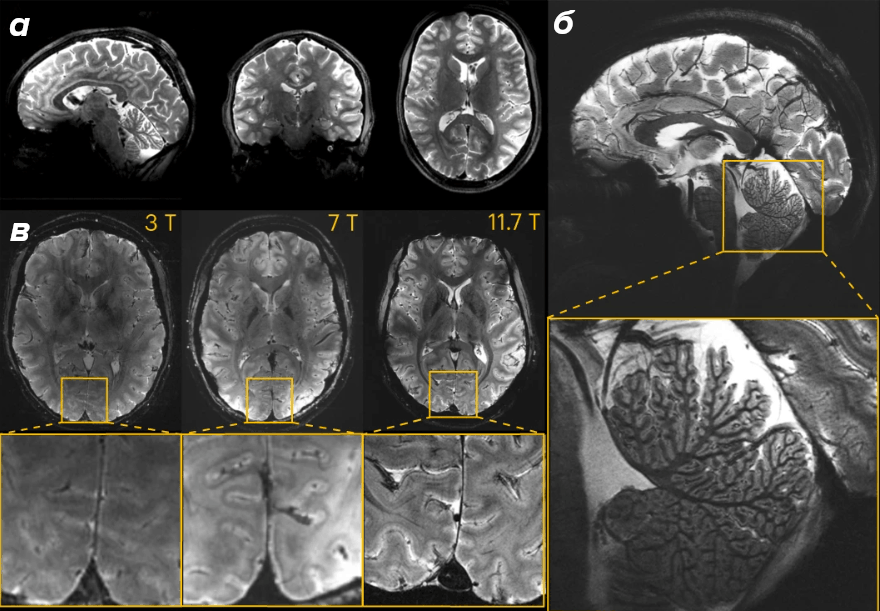
Рисунок 25. Визуализация головного мозга при сканировании на сверхвысокопольных МР-томографах.
а — 3D T2-ВИ на томографе 11,7 Тл с высокой гомогенностью магнитного поля, достигнутой во всем объеме головного мозга.
б — T2-ВИ сагиттальный срез на томографе 11,7 Тл.
в — Т2-ВИ аксиальные срезы, полученные на МР-томографах 3 Тл (слева), 7 Тл (в центре) и 11,7 Тл (справа).
[88], с изменениями
Наконец, развитие ИИ-ассистированного анализа обещает сократить разрыв между исследовательскими возможностями и рутинной клинической практикой: методы, требующие сегодня часов ручной обработки данных, буквально завтра будут выполняться автоматически и становиться частью стандартного диагностического заключения.
Итак, сегодня мы узнали, что нейровизуализация — это не просто способ «увидеть» головной мозг, это еще и язык, на котором современная медицина разговаривает с одной из самых сложных систем человеческого организма. И как любой язык, она требует понимания ее грамматики, ограничений и области применения.
До встречи в новых статьях спецпроекта «Медицинские нейротехнологии»!
Литература
- Blood-brain barrier. Связующее между двумя мирами — кровеносной и центральной нервной системами;
- Ликбез по ЦНС;
- Мозговой штурм: краткая история медицинских нейротехнологий;
- G. N. Hounsfield. (1973). Computerized transverse axial scanning (tomography): Part 1. Description of system. BJR. 46, 1016–1022;
- James Ambrose. (1973). Computerized transverse axial scanning (tomography): Part 2. Clinical application. BJR. 46, 1023–1047;
- William G. Bradley. (1984). Magnetic Resonance Imaging Of The Central Nervous System. Neurological Research. 6, 91–106;
- S Ogawa, T M Lee, A R Kay, D W Tank. (1990). Brain magnetic resonance imaging with contrast dependent on blood oxygenation.. Proc. Natl. Acad. Sci. U.S.A. 87, 9868–9872;
- 12 методов в картинках: нейробиология;
- Suraj D. Serai, Mai-Lan Ho, Maddy Artunduaga, Sherwin S. Chan, Govind B. Chavhan. (2021). Components of a magnetic resonance imaging system and their relationship to safety and image quality. Pediatr Radiol. 51, 716–723;
- Student, M.Sc. Medical Engineering, College of Engineering, Al-Nahrain University, Baghdad, Iraq., Hassanain Ali Lafta Mossa. (2012). Planning And Designing Of Magnetic Resonance Imaging (MRI) Facilities In Baghdads’ Hospitals. JFET. 7, 1–10;
- 12 методов в картинках: структурная биология;
- Сверхпроводящие магниты и рецепторы биомембран: Лаборатория биомолекулярной ЯМР-спектроскопии ИБХ РАН;
- Sean C.L. Deoni. (2011). Magnetic Resonance Relaxation and Quantitative Measurement in the Brain. Methods in Molecular Biology. 65–108;
- John P Ridgway. (2010). Cardiovascular magnetic resonance physics for clinicians: part I. Journal of Cardiovascular Magnetic Resonance. 12, 71;
- McRobbie D.W., Moore E.A., Graves M.J., Prince M.R. MRI from Picture to Proton (3rd Edition). Cambridge: Cambridge University Press, 2017. — 259 p.;
- Val M. Runge, Lawrence R. Muroff, John W. Wells. (1997). Principles of contrast enhancement in the evaluation of brain diseases: An overview. Magnetic Resonance Imaging. 7, 5–13;
- Kates R., Atkinson D., Brant-Zawadzki M. (1996). Fluid-attenuated inversion recovery (FLAIR): clinical prospectus of current and future applications. Top. Magn. Reson. Imaging. 8, 389–396;
- Gregory W. Albers. (1998). Diffusion-weighted MRI for evaluation of acute stroke. Neurology. 51;
- Shih-Chin Chang, Ping-Hong Lai, Wei-Liang Chen, Hsu-Huei Weng, Jih-Tsun Ho, et. al. (2002). Diffusion-weighted MRI features of brain abscess and cystic or necrotic brain tumors. Clinical Imaging. 26, 227–236;
- Saifeng Liu, Sagar Buch, Yongsheng Chen, Hyun‐Seok Choi, Yongming Dai, et. al. (2017). Susceptibility‐weighted imaging: current status and future directions. NMR in Biomedicine. 30;
- Рассеянный склероз: иммунная система против мозга;
- Ivan Pedrosa, David A. Altman, Jonathan R. Dillman, Michael N. Hoff, Alexander M. McKinney, et. al. (2025). American College of Radiology Manual on MR Safety: 2024 Update and Revisions. Radiology. 315;
- L. W. Goldman. (2007). Principles of CT and CT Technology. Journal of Nuclear Medicine Technology. 35, 115–128;
- Rafael García Carretero. (2017). Reoccurrence of Bleeding of a Chronic Subdural Haematoma Following a Fall. The Journal of Critical Care Medicine. 3, 118–119;
- Steven M. Greenberg, Wendy C. Ziai, Charlotte Cordonnier, Dar Dowlatshahi, Brandon Francis, et. al. (2022). 2022 Guideline for the Management of Patients With Spontaneous Intracerebral Hemorrhage: A Guideline From the American Heart Association/American Stroke Association. Stroke. 53;
- The 2007 Recommendations of the International Commission on Radiological Protection. ICRP publication 103. Ann ICRP. 37, 1–332;
- Abigail Locke, Sangam Kanekar. (2022). Imaging of Premature Infants. Clinics in Perinatology. 49, 641–655;
- Vijetha V. Maller, Harris L. Cohen. (2019). Neonatal Head Ultrasound. Ultrasound Quarterly. 35, 202–211;
- Robert H. Bonow, Christopher C. Young, David I. Bass, Anne Moore, Michael R. Levitt. (2019). Transcranial Doppler ultrasonography in neurological surgery and neurocritical care. Neurosurgical Focus. 47, E2;
- Jonathan D. Kirsch, Mahan Mathur, Michele H. Johnson, Gunabushanam Gowthaman, Leslie M. Scoutt. (2013). Advances in Transcranial Doppler US: Imaging Ahead. RadioGraphics. 33, E1-E14;
- M. W. Lorenz, H. S. Markus, M. L. Bots, M. Rosvall, M. Sitzer. (2007). Prediction of Clinical Cardiovascular Events With Carotid Intima-Media Thickness: A Systematic Review and Meta-Analysis. Circulation. 115, 459–467;
- N. El-Barghouty, A. Nicolaides, V. Bahal, G. Geroulakos, A. Androulakis. (1996). The identification of the high risk carotid plaque. European Journal of Vascular and Endovascular Surgery. 11, 470–478;
- Siddharth Bhattacharjee, Richa D. Jain, Lokesh Bathala, Anuradha HK, Vijay K. Sharma. (2022). Pictorial Essay of Cervical Duplex Ultrasonography. pocus. 7, 245–252;
- Ji Shi, Ye Zhang, Bing Yao, Peixin Sun, Yuanyuan Hao, et. al. (2021). Application of Multiparametric Intraoperative Ultrasound in Glioma Surgery. BioMed Research International. 2021;
- Shu-Qing Yu, Ji-Sheng Wang, Si-Yuan Chen, Xiang-Ming Liu, Yan Li, et. al. (2015). Diagnostic Significance of Intraoperative Ultrasound Contrast in Evaluating the Resection Degree of Brain Glioma By Transmission Electron Microscopic Examination. Chinese Medical Journal. 128, 186–190;
- Ling-Gang Cheng, Wen He, Hong-Xia Zhang, Qian Song, Bin Ning, et. al. (2017). Corrigendum to “Intraoperative Contrast Enhanced Ultrasound Evaluates the Grade of Glioma”. BioMed Research International. 2017, 1–1;
- Bijoy K Menon, Johanna Maria Ospel, Ryan A McTaggart, Raul G Nogueira, Andrew M Demchuk, et. al. (2021). Imaging criteria across pivotal randomized controlled trials for late window thrombectomy patient selection. J NeuroIntervent Surg. 13, 985–989;
- Jan Menke, Jörg Larsen, Kai Kallenberg. (2011). Diagnosing cerebral aneurysms by computed tomographic angiography: Meta‐analysis. Annals of Neurology. 69, 646–654;
- Alex M. Mortimer, Ewan Simpson, Marcus D. Bradley, Shelley A. Renowden. (2013). Computed Tomography Angiography in Hyperacute Ischemic Stroke. Stroke. 44, 1480–1488;
- Özkan Özsarlak, Johan W. Van Goethem, Menno Maes, Paul M. Parizel. (2004). MR angiography of the intracranial vessels: technical aspects and clinical applications. Neuroradiology. 46, 955–972;
- Shirin Shaban, Bella Huasen, Abilash Haridas, Murray Killingsworth, John Worthington, et. al. (2022). Digital subtraction angiography in cerebrovascular disease: current practice and perspectives on diagnosis, acute treatment and prognosis. Acta Neurol Belg. 122, 763–780;
- Timothy J. Kaufmann, John Huston, Jay N. Mandrekar, Cathy D. Schleck, Kent R. Thielen, David F. Kallmes. (2007). Complications of Diagnostic Cerebral Angiography: Evaluation of 19 826 Consecutive Patients1. Radiology. 243, 812–819;
- Lukas Goertz, Michael Artur Smyk, Eberhard Siebert, Bernd Turowski, Jan Borggrefe, et. al. (2021). Low-Profile Laser-Cut Stents for Endovascular Treatment of Intracranial Aneurysms. Clin Neuroradiol. 31, 107–115;
- AaronSong Chuan Foo, SuLone Lim, Bengt Karlsson, TsengTsai Yeo. (2016). Spontaneous obliteration highlights the dynamic nature of cerebral arteriovenous malformations: A case report and review of the literature. Surg Neurol Int. 7, 45;
- C.J. Gauthier, A.P. Fan. (2019). BOLD signal physiology: Models and applications. NeuroImage. 187, 116–127;
- Nader Sanai, Mitchel S. Berger. (2010). Intraoperative stimulation techniques for functional pathway preservation and glioma resection. FOC. 28, E1;
- S. Cirillo, M. Caulo, V. Pieri, A. Falini, A. Castellano. (2019). Role of Functional Imaging Techniques to Assess Motor and Language Cortical Plasticity in Glioma Patients: A Systematic Review. Neural Plasticity. 2019, 1–16;
- Vasileios Kokkinos, Panagiotis Selviaridis, Ioannis Seimenis. (2021). Feasibility, Contrast Sensitivity and Network Specificity of Language fMRI in Presurgical Evaluation for Epilepsy and Brain Tumor Surgery. Brain Topogr. 34, 511–524;
- M.H. Lee, C.D. Smyser, J.S. Shimony. (2013). Resting-State fMRI: A Review of Methods and Clinical Applications. AJNR Am J Neuroradiol. 34, 1866–1872;
- Yvette I. Sheline, Marcus E. Raichle. (2013). Resting State Functional Connectivity in Preclinical Alzheimer’s Disease. Biological Psychiatry. 74, 340–347;
- Luke J. Hearne, Jason B. Mattingley, Luca Cocchi. (2016). Functional brain networks related to individual differences in human intelligence at rest. Sci Rep. 6;
- Jonathan D. Power, Bradley L. Schlaggar, Steven E. Petersen. (2015). Recent progress and outstanding issues in motion correction in resting state fMRI. NeuroImage. 105, 536–551;
- A.C. Evans, D.L. Collins, S.R. Mills, E.D. Brown, R.L. Kelly, T.M. Peters. (). 3D statistical neuroanatomical models from 305 MRI volumes. 1993 IEEE Conference Record Nuclear Science Symposium and Medical Imaging Conference. 1813–1817;
- Oscar Esteban, Christopher J. Markiewicz, Ross W. Blair, Craig A. Moodie, A. Ilkay Isik, et. al. (2019). fMRIPrep: a robust preprocessing pipeline for functional MRI. Nat Methods. 16, 111–116;
- K. J. Friston, A. P. Holmes, K. J. Worsley, J.‐P. Poline, C. D. Frith, R. S. J. Frackowiak. (1994). Statistical parametric maps in functional imaging: A general linear approach. Human Brain Mapping. 2, 189–210;
- K. J. Friston, P. Jezzard, R. Turner. (1994). Analysis of functional MRI time‐series. Human Brain Mapping. 1, 153–171;
- Anders Eklund, Thomas E. Nichols, Hans Knutsson. (2016). Cluster failure: Why fMRI inferences for spatial extent have inflated false-positive rates. Proc. Natl. Acad. Sci. U.S.A. 113, 7900–7905;
- Bharat Biswal, F. Zerrin Yetkin, Victor M. Haughton, James S. Hyde. (1995). Functional connectivity in the motor cortex of resting human brain using echo‐planar mri. Magnetic Resonance in Med. 34, 537–541;
- Rasmus M. Birn, Kevin Murphy, Peter A. Bandettini. (2008). The effect of respiration variations on independent component analysis results of resting state functional connectivity. Human Brain Mapping. 29, 740–750;
- Christian F Beckmann, Marilena DeLuca, Joseph T Devlin, Stephen M Smith. (2005). Investigations into resting-state connectivity using independent component analysis. Phil. Trans. R. Soc. B. 360, 1001–1013;
- Rotem Botvinik-Nezer, Felix Holzmeister, Colin F. Camerer, Anna Dreber, Juergen Huber, et. al. (2020). Variability in the analysis of a single neuroimaging dataset by many teams. Nature. 582, 84–88;
- José M. Soares, Ricardo Magalhães, Pedro S. Moreira, Alexandre Sousa, Edward Ganz, et. al. (2016). A Hitchhiker's Guide to Functional Magnetic Resonance Imaging. Front. Neurosci. 10;
- S. Dimou, R. A. Battisti, D. F. Hermens, J. Lagopoulos. (2013). A systematic review of functional magnetic resonance imaging and diffusion tensor imaging modalities used in presurgical planning of brain tumour resection. Neurosurg Rev. 36, 205–214;
- Nick S Ward. (2004). Functional reorganization of the cerebral motor system after stroke. Current Opinion in Neurology. 17, 725–730;
- Adrian M. Owen, Martin R. Coleman, Melanie Boly, Matthew H. Davis, Steven Laureys, John D. Pickard. (2006). Detecting Awareness in the Vegetative State. Science. 313, 1402–1402;
- Martin M. Monti, Audrey Vanhaudenhuyse, Martin R. Coleman, Melanie Boly, John D. Pickard, et. al. (2010). Willful Modulation of Brain Activity in Disorders of Consciousness. N Engl J Med. 362, 579–589;
- Mingrui Xia, Tianmei Si, Xiaoyi Sun, Qing Ma, Bangshan Liu, et. al. (2019). Reproducibility of functional brain alterations in major depressive disorder: Evidence from a multisite resting-state functional MRI study with 1,434 individuals. NeuroImage. 189, 700–714;
- Alan Anticevic, Michael W. Cole, John D. Murray, Philip R. Corlett, Xiao-Jing Wang, John H. Krystal. (2012). The role of default network deactivation in cognition and disease. Trends in Cognitive Sciences. 16, 584–592;
- Brian Knutson, Sasha E. B. Gibbs. (2007). Linking nucleus accumbens dopamine and blood oxygenation. Psychopharmacology. 191, 813–822;
- Глаза прогресса: как глубокое обучение помогает видеть невидимое для человека;
- Смена подходов в компьютерном зрении: Как ИИ открывал клетку заново;
- Geert Litjens, Thijs Kooi, Babak Ehteshami Bejnordi, Arnaud Arindra Adiyoso Setio, Francesco Ciompi, et. al. (2017). A survey on deep learning in medical image analysis. Medical Image Analysis. 42, 60–88;
- Martin J. Willemink, Wojciech A. Koszek, Cailin Hardell, Jie Wu, Dominik Fleischmann, et. al. (2020). Preparing Medical Imaging Data for Machine Learning. Radiology. 295, 4–15;
- Olaf Ronneberger, Philipp Fischer, Thomas Brox. (2015). U-Net: Convolutional Networks for Biomedical Image Segmentation. Lecture Notes in Computer Science. 234–241;
- Dosovitskiy A., Beyer L., Kolesnikov A., Weissenborn D., Zhai X., Unterthiner T. et al. (2021). An Image is Worth 16x16 Words: Transformers for Image Recognition at Scale. arXiv;
- Aohan Liu, Yuchen Guo, Jinhao Lyu, Jing Xie, Feng Xu, et. al. (2023). Automatic intracranial abnormality detection and localization in head CT scans by learning from free-text reports. Cell Reports Medicine. 4, 101164;
- Mohammad R. Arbabshirani, Brandon K. Fornwalt, Gino J. Mongelluzzo, Jonathan D. Suever, Brandon D. Geise, et. al. (2018). Advanced machine learning in action: identification of intracranial hemorrhage on computed tomography scans of the head with clinical workflow integration. npj Digital Med. 1;
- Guangming Zhu, Bin Jiang, Liz Tong, Yuan Xie, Greg Zaharchuk, Max Wintermark. (2019). Applications of Deep Learning to Neuro-Imaging Techniques. Front. Neurol. 10;
- Philippe Lambin, Emmanuel Rios-Velazquez, Ralph Leijenaar, Sara Carvalho, Ruud G.P.M. van Stiphout, et. al. (2012). Radiomics: Extracting more information from medical images using advanced feature analysis. European Journal of Cancer. 48, 441–446;
- Увидеть то, что неподвластно глазу: как радиомика помогает врачам в диагностике опухолей;
- Как аэрофотосъемка связана с медицинскими снимками, большими данными и ИИ?;
- Ran Ren, Anjun Zhu, Yaxi Li, Huli Liu, Guo Huang, et. al. (2025). Federated radiomics analysis of preoperative MRI across institutions: toward integrated glioma segmentation and molecular subtyping. Front. Radiol. 5;
- Biswajit Jena, Sanjay Saxena, Gopal Krishna Nayak, Antonella Balestrieri, Neha Gupta, et. al. (2022). Brain Tumor Characterization Using Radiogenomics in Artificial Intelligence Framework. Cancers. 14, 4052;
- Xueqing Peng, Shuyi Yang, Lingxiao Zhou, Yu Mei, Lili Shi, et. al. (2022). Repeatability and Reproducibility of Computed Tomography Radiomics for Pulmonary Nodules. Invest Radiol. 57, 242–253;
- Olivier Morin, Martin Vallières, Arthur Jochems, Henry C. Woodruff, Gilmer Valdes, et. al. (2018). A Deep Look Into the Future of Quantitative Imaging in Oncology: A Statement of Working Principles and Proposal for Change. International Journal of Radiation OncologyBiologyPhysics. 102, 1074–1082;
- Eric J. Topol. (2019). High-performance medicine: the convergence of human and artificial intelligence. Nat Med. 25, 44–56;
- Danton S. Char, Nigam H. Shah, David Magnus. (2018). Implementing Machine Learning in Health Care — Addressing Ethical Challenges. N Engl J Med. 378, 981–983;
- Nicolas Boulant, Franck Mauconduit, Vincent Gras, Alexis Amadon, Caroline Le Ster, et. al. (2024). In vivo imaging of the human brain with the Iseult 11.7-T MRI scanner. Nat Methods. 21, 2013–2016.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚