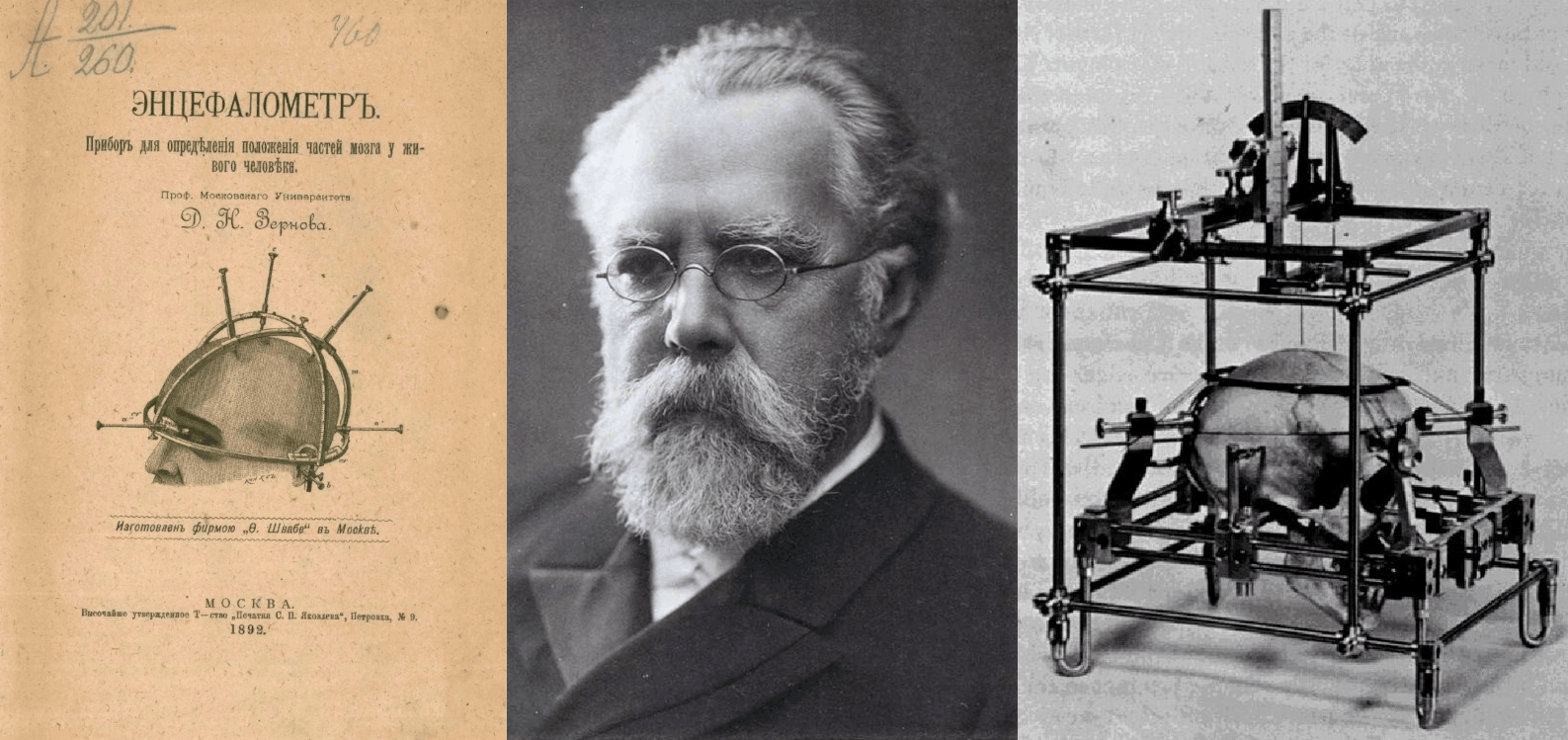Мозговой штурм: краткая история медицинских нейротехнологий
03 апреля 2026
Мозговой штурм: краткая история медицинских нейротехнологий
- 1141
- 0
- 2
История изучения мозга напоминает притчу о слоне: множество ученых и врачей пытаются разными методами с разных сторон понять, как работает этот сложный орган.
иллюстрация Елены Беловой
-
Автор
-
Редакторы
-
Рецензенты
-
Иллюстратор
Темы
Человеческий мозг похож на сложный многоярусный лабиринт, окруженный плотным куполом черепа. Научный штурм крепости разума начался в 16 веке и продолжается до сих пор — ученые строят лестницу все более изощренных технологий, позволяющих заглянуть за «крепостную стену». Однако даже самые современные подходы не дают исчерпывающего ответа, как устроен наш мозг. В первой статье спецпроекта «Медицинские нейротехнологии» мы раскроем историю изучения мозга от средних веков до наших дней: вместе пройдем путь от пыльных анатомических атласов до функциональной магнитно-резонансной томографии и фокусированного ультразвука и заглянем в недалекое будущее.
Медицинские нейротехнологии
В этом спецпроекте мы расскажем об инструментальной диагностике и лечении неврологических заболеваний, объединяя фундаментальную науку, клиническую практику и передовые тенденции в неврологии. Спецпроект дополняет цикл статей по нейрофармакологии, переходя от молекулярных основ заболеваний нервной системы к реалиям современной медицины и практическим подходам к диагностике и лечению.


Партнеры спецпроекта — Фонд развития отечественной науки, техники и медицины (ФРОНТМЕД), Российский центр неврологии и нейронаук
Высшим отличием человека является упорство в преодолении самых жестоких препятствий.
— Людвиг ван Бетховен
С самых древних времен находились желающие заглянуть внутрь черепной коробки, как в ящик Пандоры. Однако на протяжении тысячелетий представления о субстрате разума были фрагментарными и непоследовательными: еще в пятом тысячелетии до н.э. люди делали трепанацию — следы выскабливания отверстий обнаружены на 10% черепов каменного века, особенно среди взрослых мужчин [1]. Возможно, первобытные люди догадывались, что трепанация может облегчить головную боль и предотвратить нарушение сознания после травмы головы — хотя реальна и версия чисто ритуальных трепанаций.
В V веке до н.э. древнегреческий философ Алкмеон Кротонский предположил, что субстратом разума является мозг, но его идеи были отвергнуты Аристотелем, полагающим, что вместилище сознания — сердце; зато поддержаны школами Платона и Гиппократа в виде концепции энцефалоцентризма. Античные философы и врачи располагали только умозрительными заключениями об устройстве и функциях головного мозга, основанными на его размерах, плотности и температуре. Они не отделяли головной мозг от остального тела, не разрезали его и не разделяли на отдельные составляющие [2].
Фундамент представлений об анатомии человеческого мозга заложен римским врачом Галеном во II веке н.э. Тогда посмертное вскрытие человека было под запретом, поэтому Гален «подпольно» изучал случайные находки человеческих тел, либо мозг животных. Гален описал часть мозговых структур (например, мозжечок, желудочки мозга и черепно-мозговые нервы) [3], однако его внимание было сосредоточено не на мозговом веществе, а на мозговых желудочках. Отсутствие систематического доступа к человеческим мозгам привело к большому количеству «белых пятен» и ошибок.
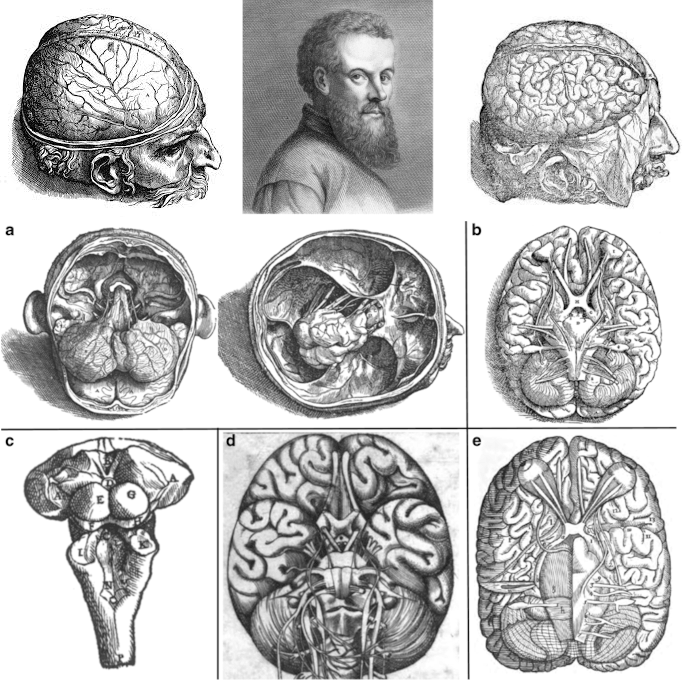
В XVI веке мифологическое мировоззрение уступило место научному познанию реальности. Технологии — как совокупность методов и инструментов — стали продолжением пытливой человеческой мысли. Эпоха Возрождения подарила миру гениев искусства, мастеров ремесла, основателей наук: все они были объединены стремлением постичь законы мироздания, включая устройство мозга (рис. 1), о чем мы дальше вам и расскажем.
- Энцефалоцентризм —
- философская концепция, согласно которой нашим телом управляет именно мозг, формирующий чувства, движения и мысли.
- Нейротехнологии
- объединяют научные методы и инструменты, позволяющие изучать, моделировать или изменять строение и функции элементов нервной системы. Медицинские нейротехнологии используются для диагностики и лечения заболеваний нервной системы. В знак начала этого спецпроекта предлагаем вам взглянуть на историю развития нейротехнологий (рис. 1) и их современную классификацию (рис. 6).
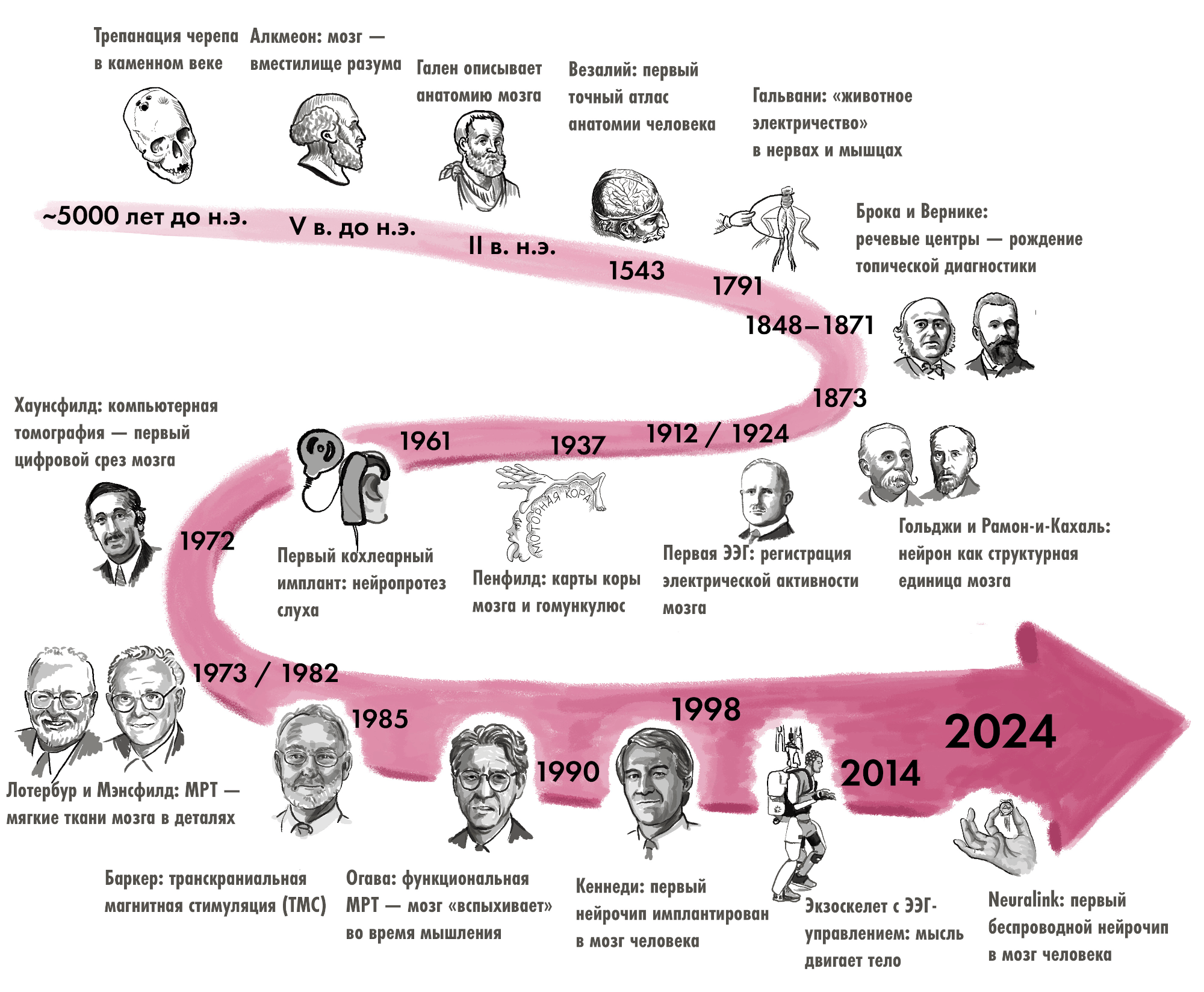
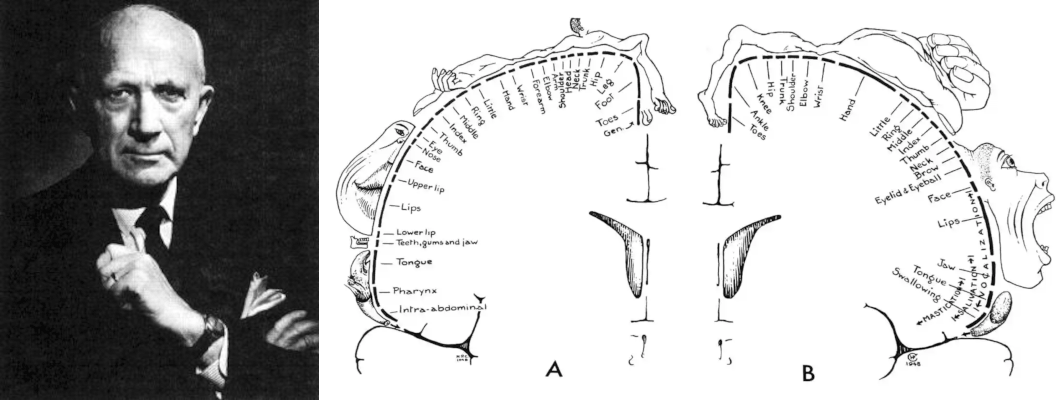
Рисунок 1. Основные вехи в долгой истории нейротехнологий. ~5000 лет до н.э.: Следы трепанации обнаружены на 10% черепов каменного века, преимущественно у взрослых мужчин. V в. до н.э.: Древнегреческий философ Алкмеон Кротонский первым выдвинул идею, что мозг — субстрат разума и ощущений. II в. н.э.: Римский врач Гален систематизировал знания об анатомии мозга, описав мозжечок, желудочки и черепно-мозговые нервы. 1543: Андреас Везалий опубликовал «De Humani Corporis Fabrica» — первый достоверный атлас анатомии человека, основанный на реальных вскрытиях. Раздел о мозге исправил множество ошибок Галена. 1791: Луиджи Гальвани в экспериментах с лягушачьими лапками доказал, что нервы и мышцы проводят электрический ток. Открытие «животного электричества» заложило основу всей нейрофизиологии. 1848–1871: В 1861 г. Поль Брока выявил моторный центр речи в левой лобной доле. В 1871 г. Карл Вернике описал сенсорный центр в левой височной доле. 1873: Камилло Гольджи открыл «черный метод» окраски нейронов нитратом серебра. Сантьяго Рамон-и-Кахаль доказал, что нейроны — отдельные клетки, а не единая сеть. 1895: Вильгельм Конрад Рентген открыл рентгеновское излучение. Уже через год врачи использовали рентгенографию черепа для диагностики переломов и инородных тел. 1912 / 1924: В 1912 г. советский физиолог В.В. Правдич-Неминский впервые зарегистрировал ЭЭГ с черепа собаки. В 1924–1929 гг. немецкий психиатр Ганс Бергер записал ЭЭГ человека, открыв эпоху функциональной диагностики мозга. 1927: Португальский невролог Антониу Эгаш Мониш разработал метод введения йодсодержащего контраста в мозговые сосуды (церебральная ангиография). 1937: Нейрохирург Уайлдер Пенфилд составил детальные карты функциональных зон коры и изобрел «гомункулюса» — модельного человечка, демонстрирующего непропорциональность функционального представительства частей тела в коре больших полушарий. 1948: Норберт Винер постулировал, что живой организм и машина используют одни принципы обратной связи и электрической передачи информации. Это концептуально открыло путь к нейроинтерфейсам. 1961: Уильям Хаус и Джон Дойл имплантировали первые электроды в улитку двух глухих пациентов. Это первый в истории нейропротез, восстанавливающий утраченное чувство через прямую электрическую стимуляцию нерва. 1972: Годфри Хаунсфилд и Аллан Кормак разработали компьютерный томограф. Началась эра нейровизуализации. 1973 / 1982: Пол Лотербур предложил использовать ЯМР для построения изображений (1973). Питер Мэнсфилд усовершенствовал алгоритмы. С 1982 г. начато коммерческое производство МР-томографов. 1985: Энтони Баркер с коллегами разработал метод транскраниальной магнитной стимуляции. 1990: Японский биофизик Сэйдзи Огава открыл принцип BOLD-контраста (зависимость МР-сигнала от насыщения гемоглобина кислородом). Это стало основой функциональной МРТ. 1998: Невролог Филипп Кеннеди имплантировал первый нейрочип в мозг парализованного пациента Джонни Рэя. Началась эра инвазивных нейроинтерфейсов «мозг–компьютер». 2014: На открытии ЧМ по футболу в Рио-де-Жанейро парализованный Джулиано Пинто ударил по мячу с помощью экзоскелета, управляемого ЭЭГ-сигналами с поверхности головы. 2024: В январе 2024 г. компания Neuralink Илона Маска имплантировала первый беспроводной нейрочип пациенту Ноланду Арбо. К 2026 г. чип использует 21 человек.
Иллюстрация Елены Беловой
Патологоанатомическое исследование мозга: открыл, увидел, сохранил
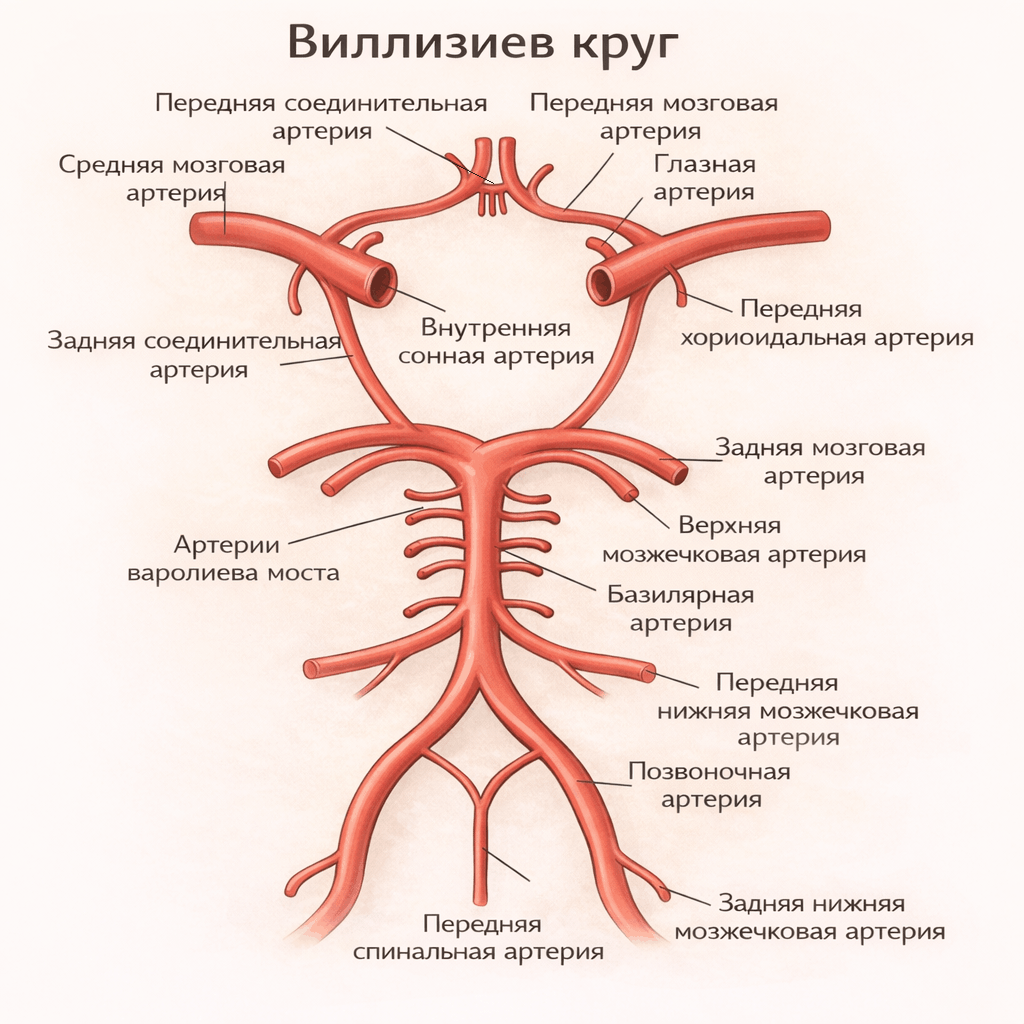
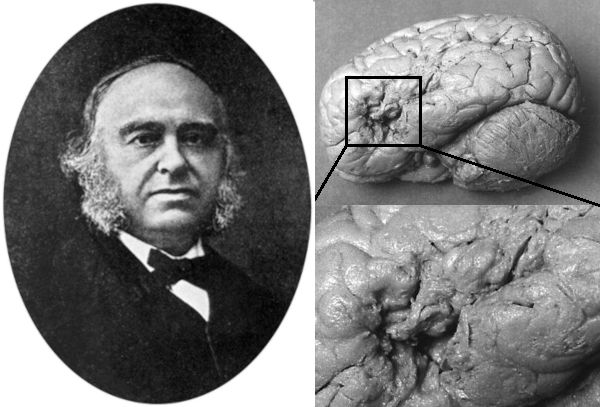
В 1559 году на рыцарском турнире во Франции разыгралась трагедия, давшая мощный импульс наукам о мозге. Граф Монтгомери нанес королю Генриху II удар, от которого тот скончался после зрительных галлюцинаций и паралича . Расследовать причину смерти поручили хирургу Амбруазу Паре, отвергшему прижигание ран кипящим маслом, и врачу Андреасу Везалию, создавшему достоверный атлас анатомии человеческого тела [4]. Вместе они впервые провели вскрытие черепа с патологоанатомическим исследованием мозга, то есть сопоставляя жалобы короля с обнаруженными при вскрытии повреждениями. Врачи описали субдуральную гематому (скопление крови под твердой мозговой оболочкой) и участки «раздавленных» затылочных долей головного мозга; определили их как причину галлюцинаций короля; а их зарисовки дополнили анатомические атласы (рис. 2А) [5]. К 1664 году, по результатам регулярных патологоанатомических исследований, английский врач Томас Уиллис создал еще более детальный атлас анатомии головного мозга (рис. 2Б), где обратил внимание на варианты нормального строения сосудистого анастомоза у основания мозга, названного в его честь виллизиевым кругом (рис. 2В) [6].
Этот и другие интересные факты более подробно рассказаны в книге «100 рассказов из истории медицины», рецензию на которую можно прочитать на «Биомолекуле» [7].
Подробнее об анатомии головного мозга можно почитать в разделе статьи от «Биомолекулы» «Ликбез по ЦНС: Анатомия мозга» [8].
- Патологоанатомическое исследование (аутопсия) —
- процедура посмертного анатомического исследования тела, в том числе внутренних органов, с целью установления причин заболеваний и смерти. В свою очередь, биопсия — прижизненный забор клеток или тканей с диагностической или исследовательской целью.
В 16–17 веках по всей Европе создавались анатомические музеи, такие как Кунсткамера в Санкт-Петербурге, для демонстрации просвещенной публике примеров искусной техники анатомического препарирования и консервации (рис. 3) [9]. Развитие практик холодной и сухой консервации мозга позволили к 19 веку создавать коллекции срезов; в России основоположником этого направления стал хирург Н.И. Пирогов [10]. Мозговые срезы в трех перпендикулярных плоскостях уточнили представления о взаимном расположении мозговых структур и легли в основу развития топической диагностики, стереотаксической нейрохирургии и нейровизуализации, о которых мы еще расскажем.

Рисунок 3. Препарат головного мозга (А), созданный голландским анатомом Фредериком Рюйшем (Б) и хранящийся в Кунсткамере. В 17 веке места, где проводились анатомические демонстрации, называли музеями, а препарирование человеческого тела считалось искусством. Ф. Рюйш одним из первых озаботился проблемой консервации мозговых тканей. Он делал инъекции смеси на основе сульфида ртути в мозговые сосуды, что и позволило коллекции Кунсткамеры сохраниться до настоящего времени.
Социально-политические потрясения ХХ века привели к формированию современных этических и правовых норм, регулирующих использование посмертных образцов мозга человека для научных целей. С тех пор в большинстве стран, в том числе в России, это возможно только при наличии прижизненного согласия донора или, в юридически разрешенных случаях, с согласия родственников. Сохранившиеся «банки мозга» стали систематизировать и накапливать материал в соответствии с международными стандартами. Образцы сопровождаются анамнестическими данными (чем болел владелец, как лечился, какой вел образ жизни), данными клинических наблюдений, генетического профилирования и нейровизуализации. Банки мозга ведут просветительскую деятельность о необходимости этически регулируемого донорства, разработки стандартов пробоподготовки и хранения образцов.
С развитием методов прижизненного изучения головного мозга (нейровизуализация и электрофизиология, о которых будет рассказано далее) актуальность изучения посмертных образцов мозговой ткани снизилась, но ненадолго — к началу XXI века стало очевидно, что многие социально-значимые заболевания нервной системы (такие как болезни Альцгеймера и Паркинсона) нуждаются в изучении мозговой ткани на молекулярно-генетическом уровне для разработки лечения. Такие исследования проводятся на материале, полученном при вскрытии или прижизненной биопсии. Доступность биопсийного материала повышается с развитием нейрохирургических методов [7].
В связи с ограниченным доступом к головному мозгу человека, ученые продолжают изучать нервную систему в норме и при патологии на животных моделях . На алтарь нейронаук было положено великое множество «братьев наших меньших» — улиток, кальмаров [11], рыб [12], лягушек [13], крыс [14], кошек, кроликов, собак, шимпанзе [15] и т.д.
Переходите по ссылкам на статьи спецпроекта «Биомолекулы» «12 модельных организмов», где мы подробно рассказали, какие бывают животные модели и как ученые работают с ними: от дизайна этичных экспериментов до возможных ограничений по экстраполяции результатов на человека.
Топическая диагностика: поиск функций на карте мозга
В 17–18 веке в западной медицине сформировался патологоанатомический подход к изучению заболеваний. Врачи наблюдали за состоянием своих пациентов, ассоциируя прижизненные проявления болезни с изменениями органов, обнаруженными посмертно. Оказалось, что характер нарушений мышления, движения и восприятия сильно зависит от «топики» (от греч. τόπος — «место»), т.е. локализации патологических изменений в различных участках головного и спинного мозга.
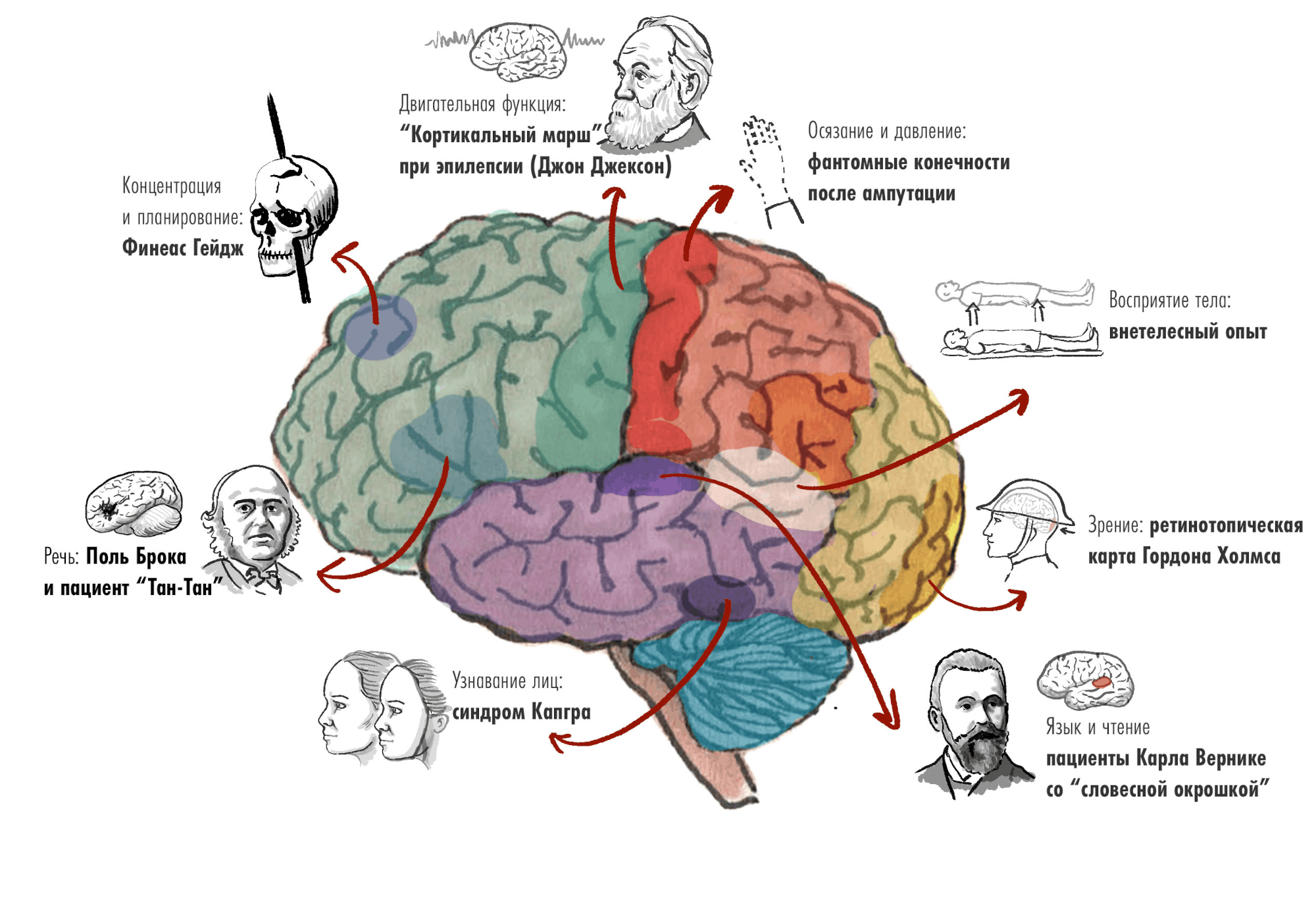
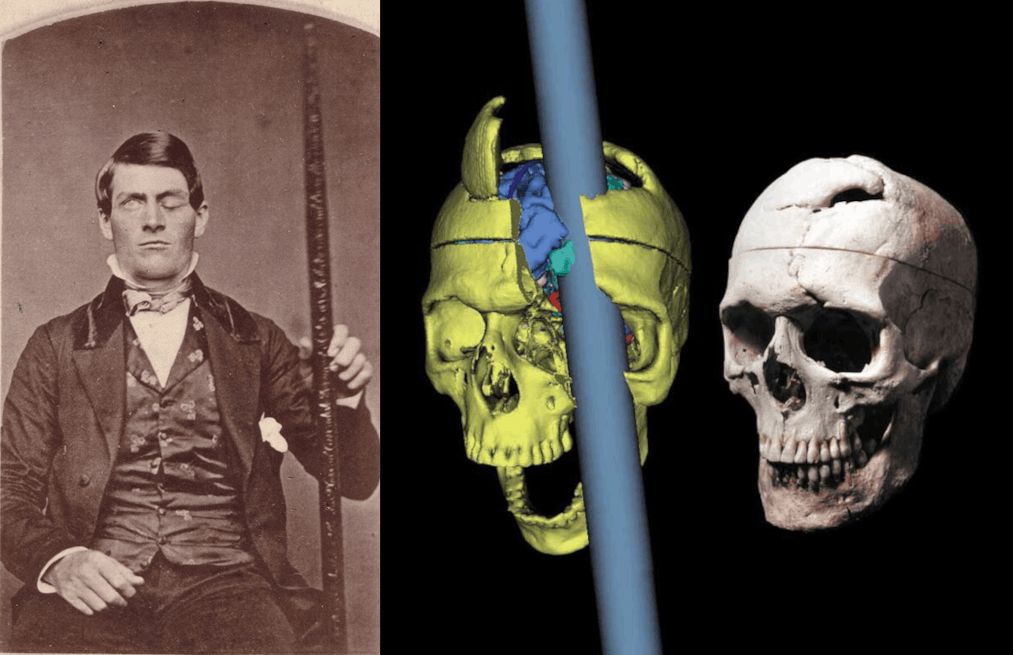
Накапливались случаи пациентов, благодаря которым анатомические атласы головного мозга дополнялись функциональными зонами (рис. 4А). В 1848 г. американский рабочий Финеас Гейдж попал в аварию на железной дороге — металлический лом пронзил его лобные доли; характер строителя из ответственного и добропорядочного превратился в импульсивный и неуправляемый (рис.4Б). Так врачи пришли к важному выводу, что лобные доли головного мозга отвечают за проявление воли, формирование нашего «Я», моральных качеств, принципов и убеждений [16], [17]. В 1861 году французский врач Поль Брока, исследуя мозг пациента по прозвищу «Тан-Тан» (способного произносить лишь этот слог), обнаружил повреждения в левой лобной доле, которую обозначил моторным центром речи [18]. А спустя 10 лет немецкий психиатр Карл Вернике описал обратный случай: пациент говорил бегло, но речь превращалась в бессмысленный поток слов — все дело было в повреждении сенсорного центра речи в левой височной доле. Ученые осознали: язык — это не единая «способность души», а система взаимосвязанных корковых зон и проводящих путей головного мозга [19] (рис. 4В) .
Увлекательные истории о пациентах с необычными симптомами при поражении различных отделов головного мозга можно найти в книге индийского невролога В. Рамачандрана «Мозг рассказывает». Ну а классика подобного чтения — «Человек, который принял жену за шляпу» Оливера Сакса.
В 19 веке определение зоны повреждения нервной системы по совокупности внешних проявлений болезни, названное топической диагностикой, способствовало обособлению неврологии как отдельной врачебной дисциплины, нацеленной на лечении заболеваний нервной системы. Большую роль в этом сыграл французский врач Жан Мартен Шарко, которого называют «отцом неврологии». С 1862 г. под его руководством в клинике Сальпетриер детально сопоставлялись клинические проявления рассеянного склероза, болезни Паркинсона, хореи с посмертными находками в головном мозге (рис. 4Г) [20].
Когда ученые нанесли на «карту мозга» различные функциональные зоны, созрел вопрос: насколько распределение этих зон отличается между людьми и могут ли нервные контуры с разными функциями «поменять квалификацию» и заменить друг друга (например, в случае обширного повреждения мозга)? В августе 1881 г. на VII Международном медицинском конгрессе в Лондоне состоялись нешуточные дебаты между двумя физиологами: немцем Фридрихом Гольцем и англичанином Дэвидом Ферье [21]. Гольц демонстрировал собак с обширными удалениями коры головного мозга: животные, несмотря на массивные повреждения, сохраняли нормальные движения и поведение. В ответ Ферье показывал макак с небольшими очагами поражения, у которых возникали одинаковые отклонения (функциональные дефициты).
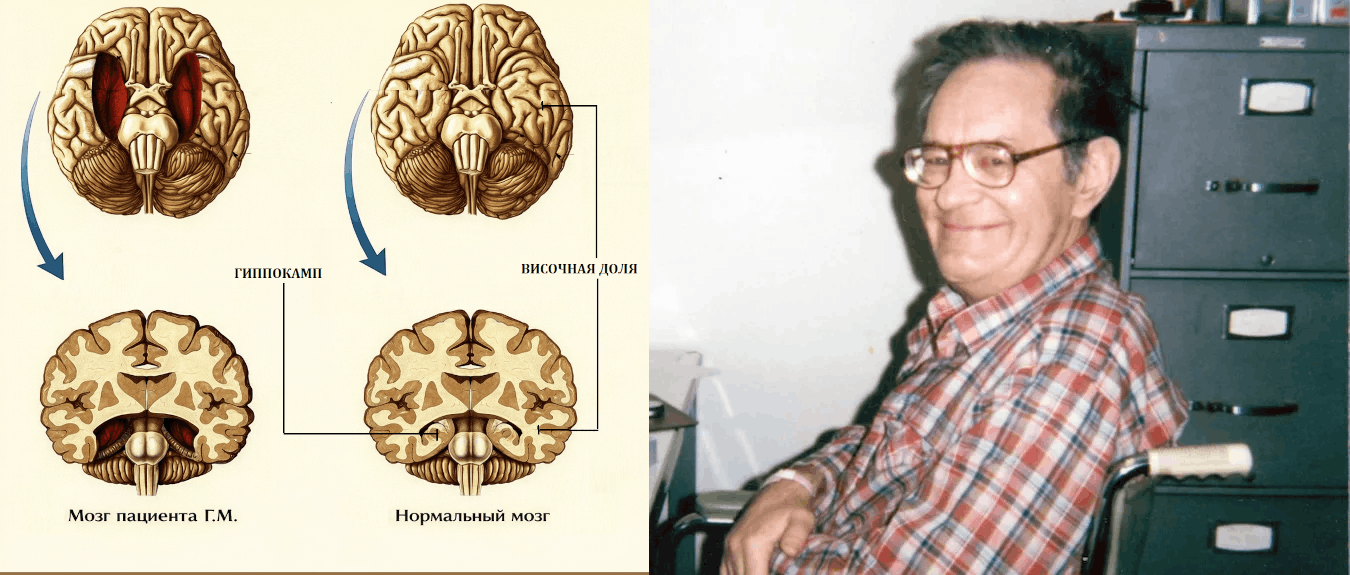
К концу XIX века оказалось, что истина находится посередине: некоторые функциональные зоны мозга действительно имеют строгую и ограниченную в размерах локализацию, в то время как другие нервные контуры распределены по нескольким участкам мозга и связаны друг с другом, что создает условия для нейропластичности. Это подтверждается в некоторых случаях хорошего восстановления пациентов после инсультов, операций и травм. Залогом «успеха» в таких случаях является более молодой возраст, отсутствие обширных повреждений, хронического стресса и вредных привычек, а также активные и грамотные восстановительные мероприятия, чтобы мозг «заново научился» нарушенным функциям. Самый яркий пример нейропластичности — это люди с утратой одного из полушарий головного мозга в детском возрасте, которые ведут нормальную жизнь, учатся, работают и создают семьи (рис. 5) [22].
- Нейропластичность —
- адаптивная способность нервных контуров к изменению структуры и выполняемых функций в условиях меняющейся окружающей среды (новый опыт, обучение, повреждение и т.п.).
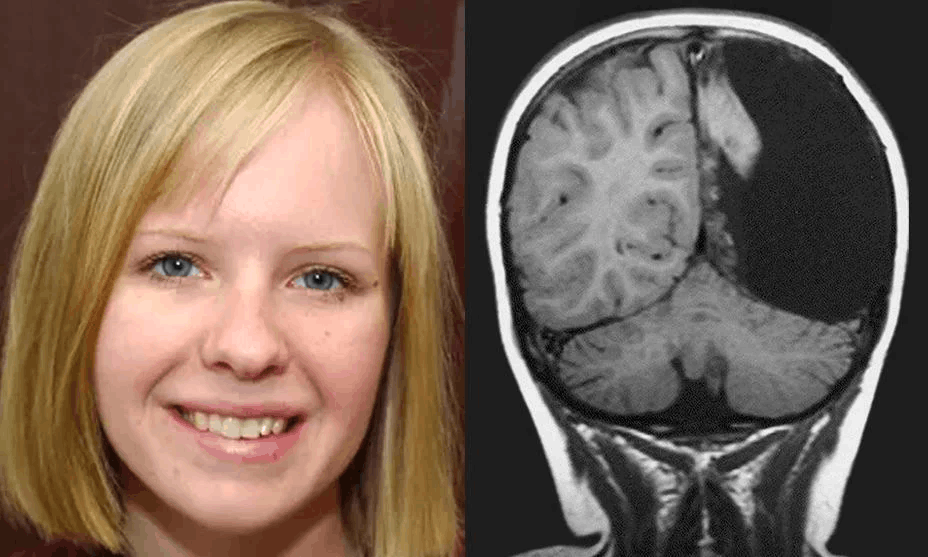
Рисунок 5. Головной мозг 7-летней девочки Кристины Сэнтхаус, которой удалили правое большое полушарие головного мозга из-за энцефалита Расмуссена — прогрессирующей воспалительной дегенерации головного мозга, сопровождающейся эпилептическими приступами (у Кристины было до 150 эпиприступов в день). После операции девочка могла говорить на двух языках и нормально передвигалась, в последствии получила высшее образование, создала семью и купила дом.
Несмотря на многообразие появившихся современных медицинских нейротехнологий (рис. 6), о которых мы расскажем в следующих разделах, клинический метод и топическая диагностика остаются незаменимыми инструментами неврологов. Они являются основой грамотной маршрутизации неврологического больного. Невролог может подойти к постели больного, оценить движения, чувствительность и координацию — это позволяет быстро и точно ограничить «зону поиска» патологических изменений и ускоряет последующую диагностику с использованием более специфичных и высокотехнологичных методов, таких как МРТ или ЭЭГ. Также топическая диагностика заложила основы для других методов, таких как стереотаксическая нейрохирургия, нейронавигация и нейромодуляция.
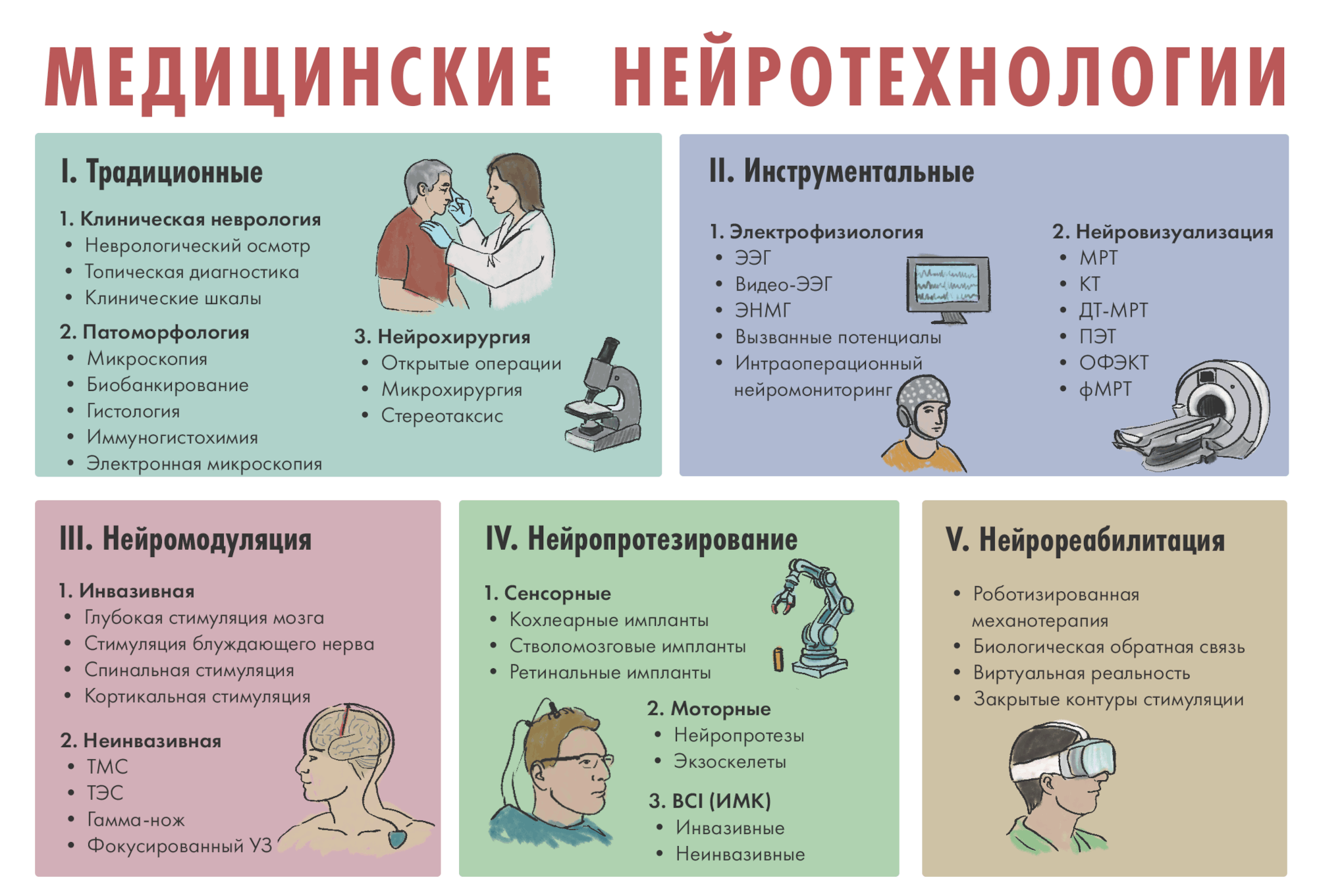
Рисунок 6. Все многообразие современных медицинских нейротехнологий можно разделить на диагностические и терапевтические. Традиционные подходы в неврологии и нейрохирургии не теряют актуальности — они не только заложили основы для развития других методов, но и стали основой грамотной маршрутизации пациента. Инструментальные методы повысили скорость и качество диагностики и лечения неврологических больных, сделали их более комфортными и персонализированными, т.е. учитывающими индивидуальные особенности строения нервной системы. Открылся доступ к наблюдению за живым мозгом в режиме реального времени — это стимулировало научное сообщество к разработке методов управляемого «вмешательства» в действующие нервные контуры. Так появились разнообразные методы нейромодуляцяции, нейропротезирования и нейрореабилитации. Потенциал многих из современных нейротехнологий еще только предстоит раскрыть в полной мере.
Иллюстрация Елены Беловой
Микроскопия мозга: от «черного метода» Гольджи до светящихся нейронов
Изучение головного мозга «невооруженным глазом» постепенно дополнили исследованиями срезов мозговой ткани на микроскопическом уровне. Начиная с XVII века совершенствовались методы микроскопии и окраски тканевых срезов, которые стали источником фундаментальных знаний о мозге. Под увеличительными стеклами нервная ткань предстала клубком спутанных нитей. В 1858 г. выдающийся немецкий гистолог Рудольф Вирхов ввел термин нейроглия (γλία с греч. — «клей») для обозначения бесструктурной ткани, удерживающей «нервные тельца», как клей. В 1873 году итальянский ученый Камилло Гольджи, работая со срезами совиного мозга, случайно пролил на них раствор нитрата серебра — на препарате проявились черные силуэты отдельных клеток с отростками. Так родился знаменитый «черный метод» Гольджи [23] — универсальный способ окраски, позволивший описать «нервные тельца» разных размеров и формы, подразделить их отростки на длинные аксоны и ветвящиеся дендриты, а также установить, что нейроглия тоже состоит из отдельных клеток. Однако автор сделал из открытия неверный вывод: он решил, что все клетки в мозге слиты в единую непрерывную сеть.
Очень подробно различные виды микроскопии и их использование рассмотрены в статье [24] другого нашего культового спецпроекта «12 методов».
Приблизился к истине научный соперник Гольджи, итальянец Сантьяго Рамон-и-Кахаль. Он продолжил окрашивать срезы нитратом серебра, но установил, что нервные клетки не слиты в единую сеть, а разделены промежутками. Его последователь, Чарльз Шеррингтон, сумел подтвердить гипотезу о наличии особых контактов между нервными клетками (в 1897 г. они были названы синапсами). В 1891 г. немецкий гистолог Генрих Вальдейер предложил назвать «элементарную единицу» нервной системы, состоящую из тела и отростков, нейроном (от греческого νεῦρον — «волокно», «жила»). В начале 20 века ученик Рамон-и-Кахаля Пио дель Рио-Ортега изобрел способы окраски нейроглии и создал первую морфологическую классификацию глиальных клеток .
Подробнее о роли микроскопии в развитии нейробиологии можно почитать в статье о С. Рамон-и-Кахале [25] и в серии «Нейробиология» [26] спецпроекта «12 методов».
ХХ век стал для неврологов периодом активных патоморфологических исследований мозга, т.е. ассоциации проявлений заболевания с изменениями нервной ткани на микроскопическом уровне. Это позволило перейти к поиску причин (этиология) и механизмов (патогенез) развития заболеваний на уровне клеток и тканей. Например, патоморфологические исследования выявили, что диагностическим признаком нейродегенеративных заболеваний является отложение патологических белковых агрегатов в веществе мозга (β-амилоида при болезни Альцгеймера, α-синуклеина при болезни Паркинсона, тау-белка при лобно-височной дегенерации), классифицировать опухоли мозга по происхождению [27].
- медицинская дисциплина, изучающая структурные изменения в клетках, тканях и органах, ассоциированные с заболеваниями.
- Этиология —
- раздел медицины, изучающий причины и условия возникновения болезней.
- Патогенез —
- механизм возникновения, развития и течения патологических процессов от молекулярных нарушений до сбоев в работе органов и организма в целом.
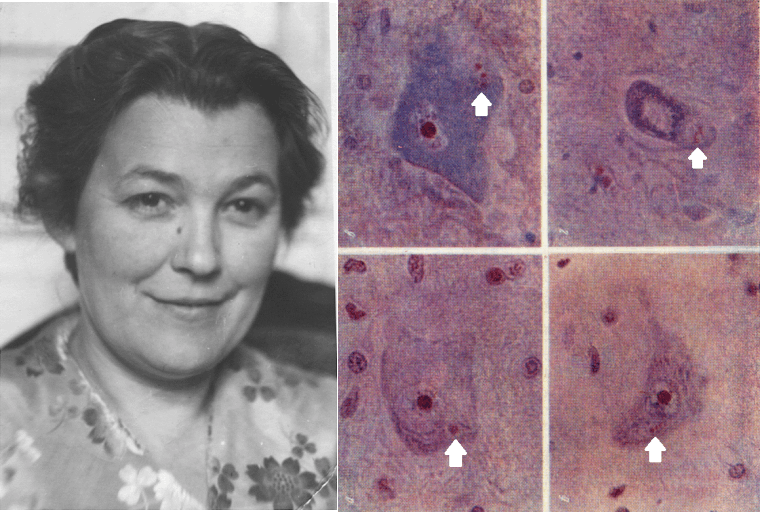
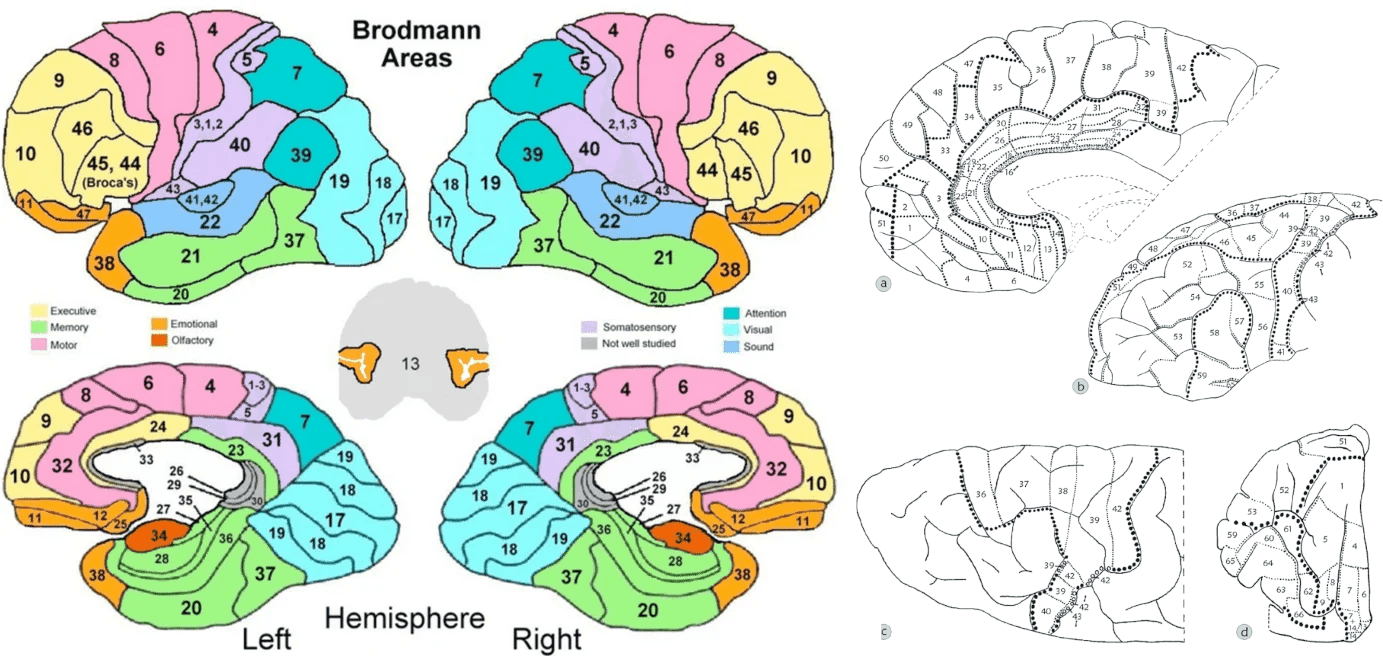
В СССР была сильная школа патоморфологии мозга — Татьяна Бунина из Института неврологии АМН СССР прославилась на весь мир, описав сложные молекулярные включения (тельца Буниной) в телах двигательных нейронов у пациентов с боковым амиотрофическим склерозом (рис. 7А) [28]. В этом же институте в послойных срезах были описаны характеристики мозговых сосудов разного калибра и их изменения при повышении артериального давления и атеросклерозе [29]. Микроскопия послойных тканевых срезов также повысила точность топической диагностики. Были описаны различия в строении слоев коры больших полушарий и мозжечка. Появились детальные карты «архитектуры» коры, основанные на гистологических различиях, такие как поля Бродмана и Фогта (рис. 7Б–В) [30].
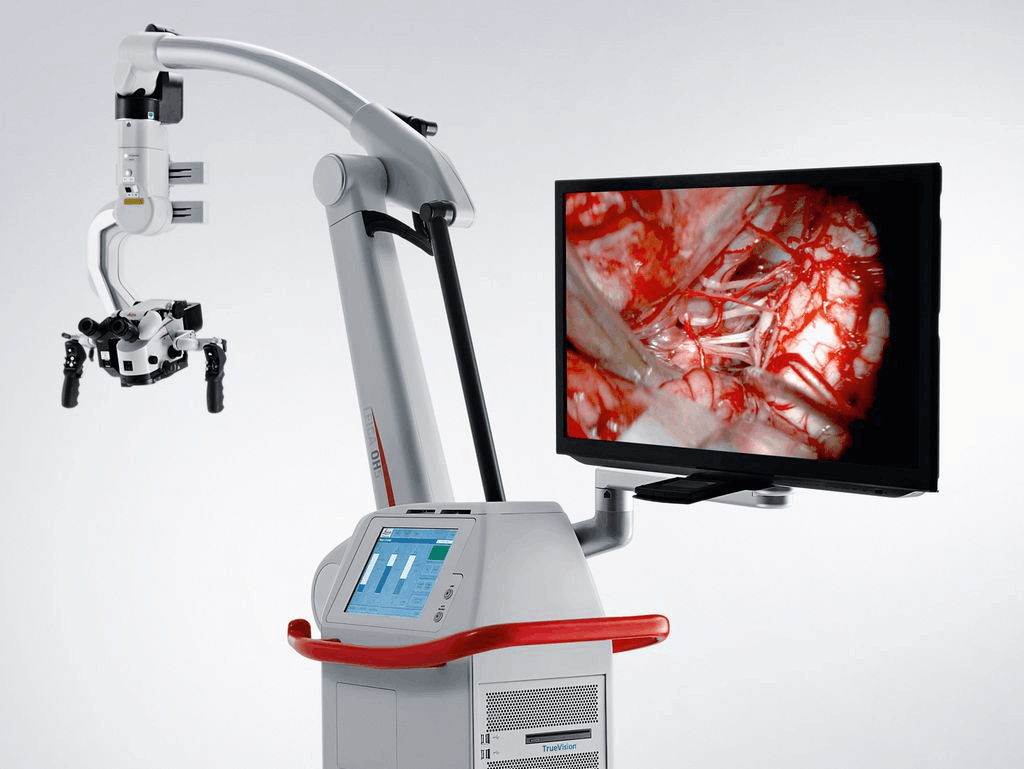
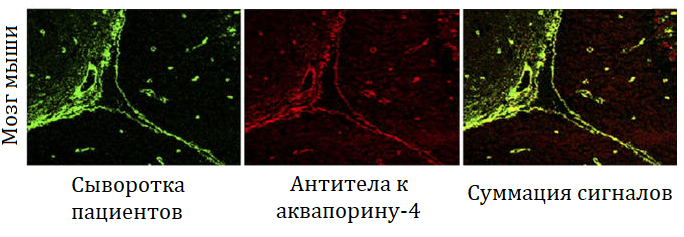
Микроскопия по сей день остается незаменимым инструментом диагностики и лечения нервных болезней. Разработаны нейрохирургические микроскопы, позволяющие выполнять тончайшие оперативные вмешательства (например, на периферических нервах, мозговых сосудах, при удалении аденом гипофиза) (рис. 8А). Нередко микроскопия со специальным гистологическим окрашиванием становится финальным диагностическим арбитром в постановке достоверного неврологического диагноза. Например, достоверную причину деменций устанавливают только при посмертном исследовании состава белковых агрегатов в ткани головного мозга, в то время как воспаление мелких сосудов головного мозга (васкулит) или опухоль нервной системы изучают и классифицируют прижизненно с помощью микроскопии биоптата (фрагмента нервной или сосудистой ткани, изъятого во время оперативного вмешательства). Иммуногистохимия и флуоресцентная микроскопия позволяют по характеру свечения мозгового среза определить, против каких молекул организм синтезирует специфические антитела при аутоиммунных заболеваниях нервной системы (рис. 8Б).
Природу иммунитета и аутоиммунных расстройств мы разбирали в статье «Иммунитет: борьба с чужими и… своими» [31] спецпроекта «Аутоиммунные заболевания», а в СП «Нейрофармакология» была публикация, посвященная конкретно проблемам нервной системы: «Аутоиммунные заболевания нервной системы: как сдержать нечаянное зло?» [32].
- Иммуногистохимия —
- высокоточный метод микроскопического исследования тканей, позволяющий специфически выявлять количество и расположение биомолекул-маркеров с помощью меченых антител. Подробно это было разобрано в статье «Иммунологические технологии» [33] спецпроекта «12 методов в картинках».
- Флуоресцентная микроскопия —
- метод световой микроскопии, позволяющий визуализировать отдельные структуры по испусканию света веществами-флуорофорами под воздействием света определенной длины волны. На «Биомолекуле» есть множество статей на тему флуоресценции, но начать можно со материала «Микроскопия» [24] все того же спецпроекта «12 методов в картинках».
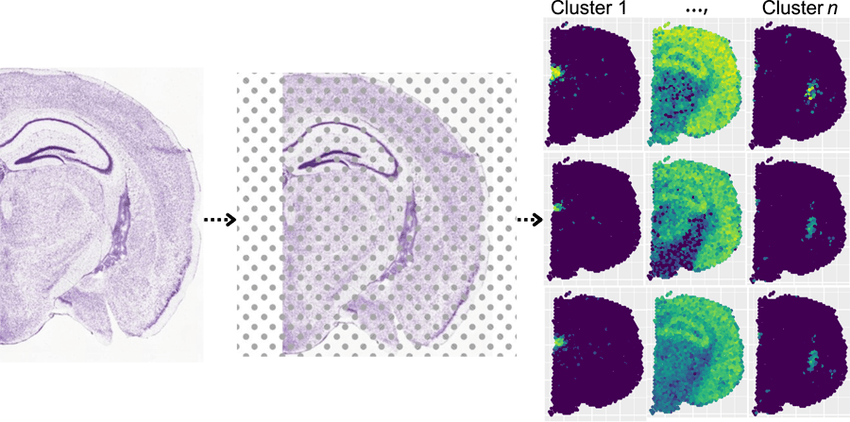
Сегодня гистологический срез можно превратить из статичной картинки в большую базу данных с помощью методов пространственной транскриптомики. Специальные приборы для РНК-секвенирования позволяют определить, какие гены активны в каждой конкретной клетке на срезе, сохранив ее пространственные координаты. Так исследователи получают новую информацию о патогенезе нервных болезней.
Электрофизиология: от «животного электричества» до диагностики состояния живого мозга
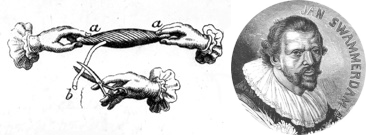
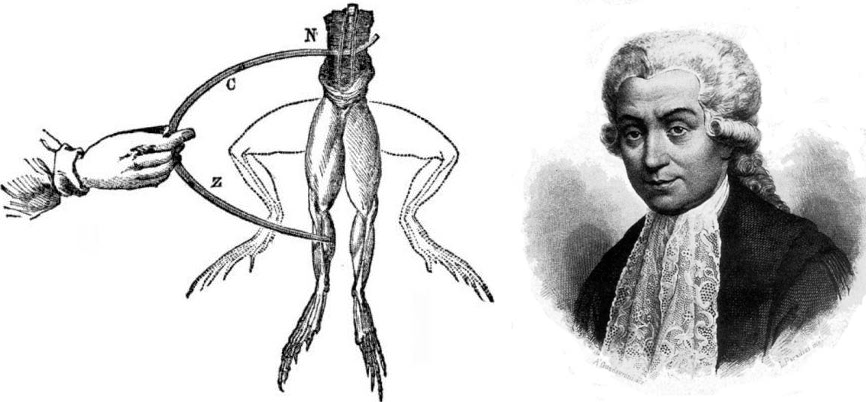
Еще со времен Галена ученые полагали, что мозг связан с телом и внешним миром с помощью чрезвычайно легкой жидкости — «психической пневмы». К началу XVIII века английские естествоиспытатели Исаак Ньютон и Стивен Гейлс предположили, что мозг «общается» с телом через «нити нервов» с помощью «энергии, действующей по поверхности, подобно электричеству». Началась массовая экспериментальная погоня за «животным электричеством» [36]. Открытия в этом направлении предвосхитил голландский биолог Ян Сваммердам: еще в 1664 году он препарировал бедренную мышцу лягушки, которая сокращалась при раздражении бедренного нерва (рис. 9А). В 1792 году Луиджи Гальвани в своем «Трактате о силах электричества при мышечном движении» обобщил известные на тот момент эксперименты с «оживлением» лапок мертвых лягушек при помощи тока [37]. Гальвани заключил, что нервы и мышцы способны проводить электричество (рис. 9Б).
В 1849 году немецкий физиолог Эмиль Дюбуа-Реймон заложил основы электрофизиологии, зарегистрировав два основных «электрических состояния» нейрона — потенциал покоя [38] и потенциал действия (рис. 9В) [39], [40]. С тех пор ученые в Европе и России находились в активном поиске эффективных способов регистрации электрической активности головного и спинного мозга, а также периферических нервных волокон. Кролики, кошки, собаки и шимпанзе подвергались различным операциям по удалению частей мозга и вживлению электродов в мозговую ткань: поведенческая активность, рефлекторные и вегетативные реакции сопоставлялись с зарегистрированными электрическими импульсами.
- Электрофизиология —
- раздел физиологии и клеточной биологии, изучающий электрические явления в живых организмах на молекулярном, клеточном, тканевом и организменном уровнях. Максимально подробно история изучения биоэлектричества — от лягушачьей лапки до ионных каналов — разобрана в книге Ф. Эшкрофт «Искра жизни».
- Потенциал покоя —
- это разность электрических потенциалов между внутренней и наружной сторонами мембраны невозбужденной клетки, обычно составляющая −55..−100 мВ. Идеально это явление разобрано в статье «Биомолекулы» «Формирование мембранного потенциала покоя» [38].
- Потенциал действия —
- кратковременное изменение (реверс) электрического потенциала на мембране возбудимой клетки (нервной, мышечной), служащее импульсом для передачи информации. Читайте: «От искры к пожару: как рождается и путешествует нервный импульс» [39].
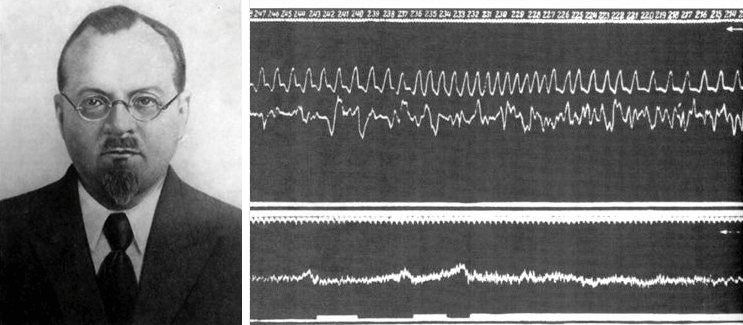
Научные изыскания на мозгах животных в конечном итоге привели к разработке универсального и безвредного способа регистрации суммарной электрической активности с поверхности черепа человека в режиме реального времени с помощью двух и более электродов. Сейчас этот метод известен как электроэнцефалография (ЭЭГ). Первая ЭЭГ была зарегистрирована с неповрежденного скальпа собаки в 1912 году «дедушкой ЭЭГ» — советским физиологом В.В. Правдич-Неминским (рис. 10А). А уже в 1929 году немецкий психиатр Ганс Бергер (которого называют «отцом ЭЭГ») опубликовал ЭЭГ-запись биоэлектрической активности с двух электродов, размещенных поверхности головы своего сына (рис. 10Б) [41].
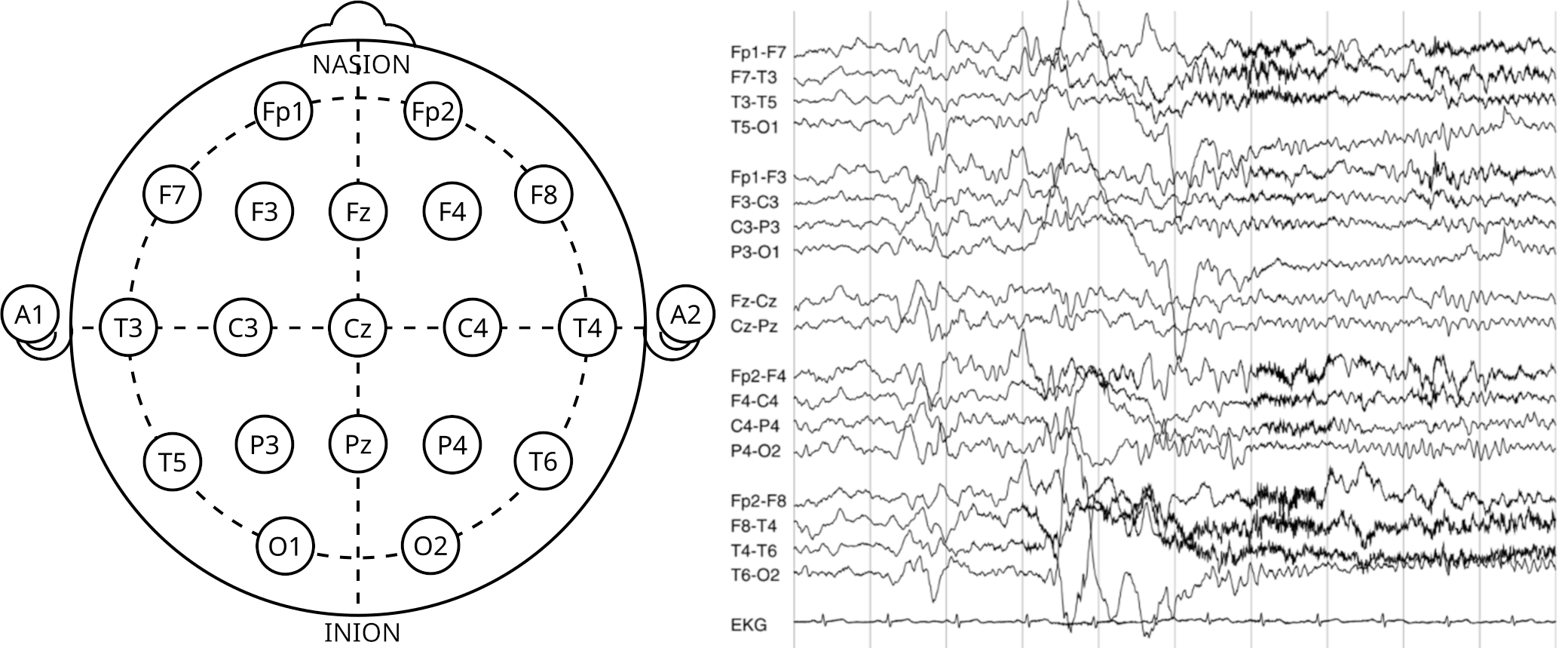
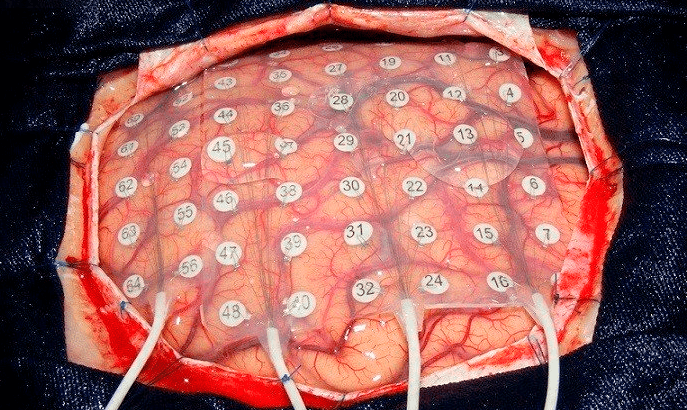
С появлением ЭЭГ в начале ХХ века началась эпоха функциональной диагностики в неврологии: врачи получили возможность «слышать голоса» миллиардов нейронов живого головного мозга в режиме реального времени. Современные ЭЭГ-установки могут регистрировать сигнал от сотен электродов с усилением и миллисекундным разрешением (рис. 10В), что позволяет отследить минимальные изменения электрической активности нервных контуров в динамике. Для лучшего «перевода» ЭЭГ совмещают с регистрацией электрической активности сердца (электрокардиография), мышц (электромиография) и видеорегистрацией (чем пациент занимается в период мониторинга).
- Функциональная диагностика —
- раздел медицины, направленный на динамическую оценку работы органов и систем организма при различных функциональных состояниях с помощью инструментальных методов.
- Электрокардиография (ЭКГ) —
- метод регистрации электрической активности сердца с поверхности тела.
- Электромиография —
- метод регистрации электрической активности скелетных мышц с помощью поверхностных электродов на поверхности тела или игольчатых электродов, погруженных в мышцу.
ЭЭГ сигнал очень достоверен, что играет важную роль в диагностике. Например, при обмороке или панической атаке ЭЭГ останется нормальной. И наоборот, эпилептиформная активность будет зарегистрирована, даже если у пациента нет внешних признаков эпилептического приступа (например, он просто лежит с закрытыми глазами). ЭЭГ-сигнал будет меняться при разном уровне сознания вплоть до глубокой комы, когда пациент никак не контактирует с внешним миром. ЭЭГ-сигнал исчезнет, если нейроны замолчали навсегда, поэтому ЭЭГ-протокол используется в установке факта смерти головного мозга. У некоторых неврологических заболеваний даже есть свой узнаваемый «ЭЭГ-почерк», а также существуют специфические ЭЭГ-сигналы для различных фаз сна, что используется в диагностике его нарушений для подбора эффективной терапии.
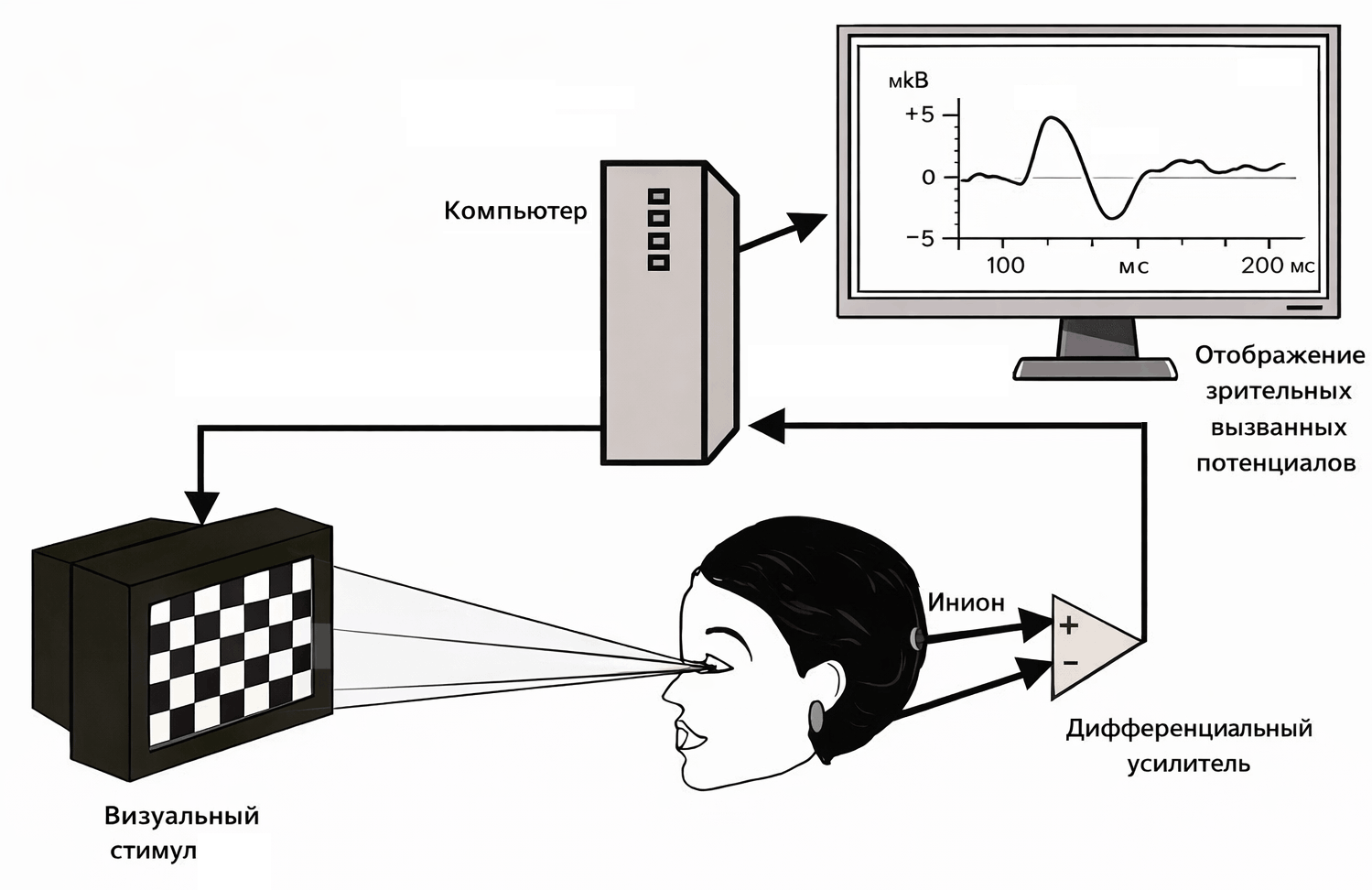
Разработка ЭЭГ-систем с множеством компактных электродов, а также математических алгоритмов обработки позволила вычленять из ЭЭГ-ритмов вызванные потенциалы — сверхслабые стереотипные ЭЭГ-изменения при воздействии раздражителей различной модальности или совершении действий. Рассчитываемый усредненный профиль вызванных потенциалов позволяет оценить работу зрительных, слуховых и двигательных нервных контуров по отдельности (рис. 10Д).
Нейромодуляция: вмешательство в нейронные дела
Ученые создали подробные анатомические атласы человеческого мозга, клиническим путем исследовали функции его поверхностных отделов, научились регистрировать электрическую активность нейронов. Однако ЭЭГ регистрирует лишь суммарную электрическую активность с поверхности головного мозга, т.е. преимущественно от корковых нейронов, ответственных за высшую нервную деятельность. А под корой скрыто много других нервных контуров, ответственных за движения, эмоции, биоритмы, регуляцию работы коры, переключение ее функциональных режимов.
В научном сообществе созрело два важных вопроса. Может ли электрическое воздействие на мозг извне помогать в диагностике и лечении его патологий? Можно ли безопасно воздействовать электричеством как на поверхностные, так и на глубокие структуры мозга, чтобы регулировать их функции? В поисках ответов на эти вопросы зародились методы нейромодуляции — внешнего воздействия на нервную ткань с целью коррекции их активности и функций.
- Нейромодуляция —
- целенаправленное изменение активности нервных контуров путем воздействия на определенные участки нервной системы для нормализации или оптимизации их функций.
Поверхностная нейромодуляция: от электрода до магнитной катушки
Первый опыт нейромодуляции был получен нейрохирургами на операционном столе, причем еще в 19 веке [42]: врачи спрашивали разрешения у пациентов во время операции с трепанацией черепа, чтобы влиять на активность нервных контуров, доступных для изучения с обнаженной поверхности головного мозга путем погружения стимулирующих электродов в живую мозговую ткань. Наиболее систематизированные и результативные исследования в этом направлении проводил американский нейрохирург Уайлдер Пенфилд, оперировавший пациентов с эпилепсией и опухолями [43]. Чтобы не отсечь жизнеспособную мозговую ткань при удалении патологических очагов, доктор Пенфилд вместе со своими коллегами Эдвином Болдри и Теодором Расмуссеном пробуждал пациентов от наркоза и использовал стимулирующие электроды с низким напряжением [44] (хорошо, что в головном мозге нет болевых рецепторов) — в ответ на раздражение отдельных участков коры больших полушарий пациенты начинали двигать конечностями, петь, плакать и смеяться. В результате к 1937 г. появились карты коркового представительства Пенфилда, которые используются до сих пор как нейрохирургами, так и учеными при разработке нейроинтерфейсов (рис. 11А-Б) [45].
Будить пациентов во время нейрохирургической операции также теперь не всегда обязательно, ведь врачи научились использовать методику интраоперационного нейромониторинга — в ответ на легкое раздражение мозговой ткани электродами регистрируются вызванные потенциалы, по амплитуде и задержке возникновения которых оценивается жизнеспособность нейронов в оперативном поле.
Современные неврологи тоже могут проводить поверхностную нейромодуляцию без помощи нейрохирургов. В 1985 г., благодаря работам научной группы Энтони Баркера, был разработан метод транскраниальной магнитной стимуляции (ТМС) [46] . Прикладывая магнитную катушку к поверхности головы, оператор стимулирует поверхностные нейроны посредством направленного магнитного поля (рис. 12). Эффект нейромодуляции зависит от частоты импульсов, формы катушки и точки ее приложения. ТМС позволяет изучать в динамике функциональные зоны коры больших полушарий без вскрытия черепа — например, отслеживать уменьшение зоны движения руки из-за гибели двигательных корковых нейронов при боковом амиотрофическом склерозе или инсульте. К настоящему времени разработаны протоколы терапевтической ТМС для лечения депрессии, мигрени, шума в ушах, болевого синдрома, а также лечения от зависимостей и восстановления после инсульта. Более подробно о методе ТМС будет рассказано в отдельной статье спецпроекта по медицинским нейротехнологиям.
- Интраоперационный нейромониторинг —
- регистрация и интерпретация биоэлектрических сигналов в режиме реального времени с целью контроля функциональной целостности структур нервной системы (головного и спинного мозга, черепных и периферических нервов) в ходе хирургического вмешательства.
- Транскраниальная магнитная стимуляция —
- неинвазивный диагностический и терапевтический метод стимуляции коры головного мозга при помощи коротких магнитных импульсов. Больше о таких методах можно прочесть в статье «Инструкция к перезагрузке мозга: неинвазивная нейромодуляция для лечения резистентной депрессии» [47].
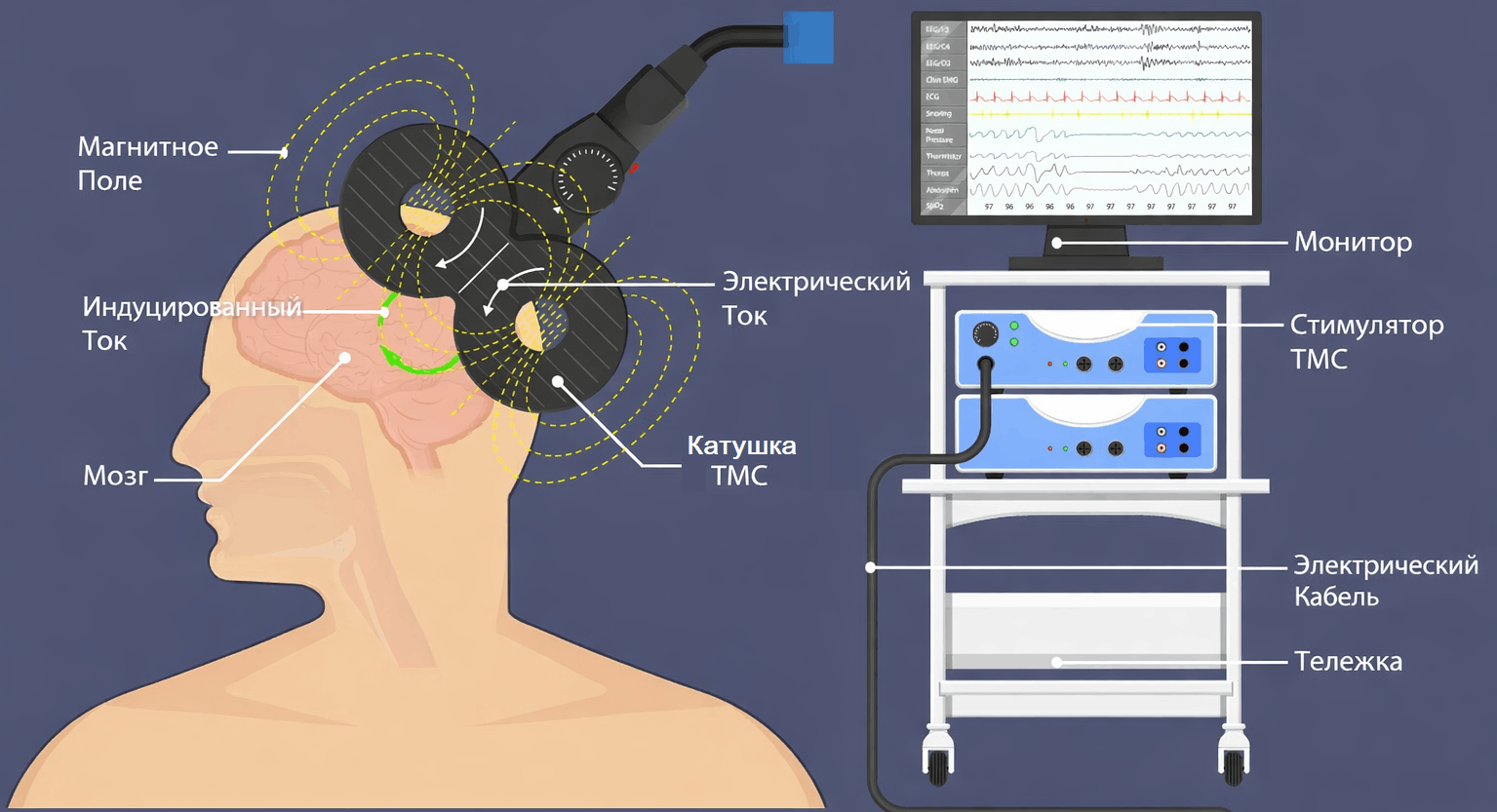
Рисунок 12. Принцип действия транскраниальной магнитной стимуляции (ТМС): генерация индуцированного электрического тока в поверхностных слоях головного мозга (прежде всего корковых нейронах) с помощью магнитной катушки. При диагностической ТМС оценивается амплитуда, время задержки и корковое представительство моторных вызванных потенциалов. При терапевтической ТМС производится ритмическая стимуляция различных отделов головного мозга с заданными частотными характеристиками.
Глубокая нейромодуляция: стереотаксис на животных моделях
Что же придало врачам смелости провести стимулирующие электроды вглубь человеческого мозга? Прежде всего, клиническая необходимость: к началу XX века неврологи накопили достаточно патоморфологических доказательств, что многие заболевания, вызывающие нарушения движений и эмоций, затрагивают глубокие структуры головного мозга (таламус, базальные ядра, лимбическую систему, ствол). Но как добраться к маленьким глубоким зонам с наименьшим риском повредить более поверхностные структуры живого мозга?
Элегантным решением проблемы стал стереотаксис — метод трехмерной навигации к глубоким отделам мозга. Первые исследования проводились на животных — фиксировали на поверхности головы жесткую конструкцию, относительно которой по анатомическим атласам рассчитывали координаты цели и необходимый вектор установки стимулирующих электродов (рис. 13А) [48].
- Стереотаксис —
- хирургический метод, позволяющий с высокой точностью (в милиметрах) провести инструмент (канюлю, электрод, луч) в глубоко расположенную целевую точку мозга по заранее рассчитанным трехмерным координатам.
В 1930-х швейцарский физиолог Вальтер Гесс использовал стереотаксические конструкции для стимуляции гипоталамуса кошек, что запускало ярость и оборонительные реакции (рис. 13Б) [49]. В 1950-х годах Джеймс Олдс и Питер Милнер обнаружили с помощью электростимуляции мозга крыс, что передние отделы гипоталамуса содержат «зоны удовольствия» (рис. 13В) [50]. А в 1960-х годах Хосе Дельгадо управлял поведением быка, дистанционно стимулируя электродом хвостатое ядро в составе базальных ядер (рис. 13Г) [51]. Все эти наблюдения расширили представления врачей о функциях глубоких структур головного мозга и легли в основу методов функциональной нейрохирургии, о которых будет рассказано далее.
Нейроинтерфейсы и нейропротезы: как компьютер говорит на языке нейронов
Нейрофизиология утвердила животное электричество как «язык общения» нейронов, а нейромодуляция доказала возможность управлять работой нервных контуров извне. В 1948 году «отец кибернетики» Норберт Винер постулировал, что живой организм и машина могут общаться на одном языке, так как используют электричество для передачи информации и принцип обратной связи для коррекции своих алгоритмов [52].
Это означало, что с помощью машин можно вернуть человеку утраченные функции — слух, зрение, способность говорить, ходить и управлять предметами. Нейропротезы восстанавливают электрический «канал связи» между мозговыми нейросетями и внешним миром. Например, чувствительные нейропротезы заменяют работу зрительных и слуховых рецепторов. Внешний раздражитель — свет или звук — переводится в электрический импульс, который по нервам уходят в мозг (рис. 14).
- Нейропротезы —
- устройства, замещающие утраченную функцию нервной системы через восстановление контакта с ее функционирующими элементами. Читайте также: «Что такое нейропротезирование? Это вредно?» [53].
При утрате слуха используют кохлеарный имплант. Внешний микрофон и процессор превращают звук в электрический код, а чип с электродами передает его на слуховую улитку и слуховой нерв. Особенно важны такие импланты для детей с врожденной глухотой: раннее отсутствие слуховой информации тормозит развитие речи и когнитивных функций. К сожалению, современные нейропротезы не способны восстановить вкус и обоняние, так как эти виды чувств имеют дело с молекулами вещества, а не физическими раздражителями.
До 80% информации об окружающем мире человек получает с помощью зрения, поэтому восстановлению утраченной зрительной функции уделяется повышенное внимание . Для зрительных нейропротезов используют камеры: изображение разбивается на пиксели, а дальше превращается в набор электрических импульсов. Эти импульсы подаются через чип из тончайших стимулирующих электродов на зрительную кору в затылочных долях больших полушарий. В результате человек может находить предметы, ориентироваться в пространстве, а иногда даже распознавать простые формы и крупные символы. Более «экзотические» нейропротезы передают информацию о пикселях с камеры на поверхность языка. На нем густая сеть нервных окончаний, и потому он хорошо «считывает» сложные паттерны стимуляции. Постепенно мозг учится «видеть языком» — сопоставлять чувство покалывания на языке с контурами предметов и расстоянием до них.
Подробнее о способах восстановления зрения читайте в статьях «Биомолекулы»: не только о технологиях нейропротезирования [54] и протезирования сетчатки [55], но и о белках-мишенях для таргетной терапии [56], возможностях генной терапии [57] и тактильной реабилитации незрячих пациентов [58].
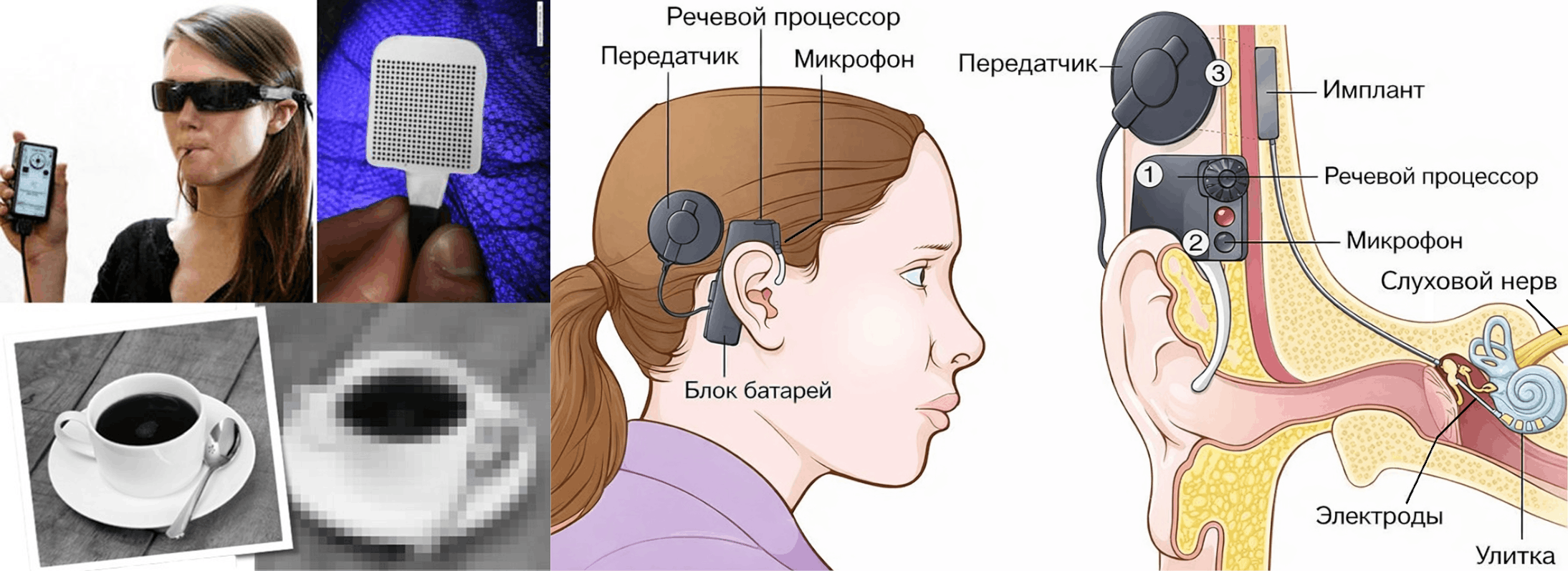
Рисунок 14. Примеры нейропротезов, восстанавливающих утраченную чувствительность. Слева: зрительный нейропротез, передающий информацию от видеокамеры на поверхность языка с помощью чипа из стимулирующих электродов. Справа: слуховой нейропротез (кохлеарный имплант), передающий информацию от микрофона на слуховую улитку.
Существует два основных принципа работы моторных нейропротезов, возвращающих способность к движению [59], [60]. Первый основан на электростимуляции собственных частей тела: если мозг посылает команду, но она не доходит до мышцы из-за травмы спинного мозга или периферического нерва, можно искусственным путем подать электрический импульс прямо на нервы или мышцы и заставить их действовать с нужной силой и в нужной последовательности. Второй подход стал возможен с разработкой нейроинтерфейсов, когда сигнал «намерения совершить действие» считывается с коры больших полушарий или с мышц и переводится в команду для внешнего устройства (внешние устройства, экзоскелет, «умные» приборы) (рис. 15А).
- Нейроинтерфейс «мозг-компьютер» —
- технология, превращающая биоэлектрическую активность мозга в цифровые команды управления внешними устройствами (компьютером, экзоскелетом, протезом), минуя естественные нервно-мышечные исполнительные пути. Мы уже рассказывали об этом: «Нейроинтерфейсы: как наука ставит людей на ноги» [61], «Киборги сегодня: нейрокомпьютерные технологии становятся неотъемлемой частью нашей жизни» [62] и «Нейроинтерфейсы и чтение мыслей. Способен ли «Призрак в доспехах» стать реальностью?» [63].
Первые опыты по обучению нейроинтерфейсов «мозг–компьютер» проводились в 90-х годах XX века на шимпанзе, а уже в 2014 году на Чемпионате мира по футболу в Рио-де-Жанейро человек с параличом ног Джулиано Пинто пнул мяч с помощью неинвазивного нейроинтерфейса: экзоскелет управлялся ЭЭГ-сигналами, зарегистрированными с накожных электродов на поверхности головы (рис. 15В). С тех пор экзоскелеты стали менее громоздкими и дорогими, уменьшилась задержка между намерением человека и исполнением команды. Также сейчас ведутся активные разработки коллективных нейроинтерфейсов, которые позволят людям читать мысли и намерения друг друга [65].
На рубеже ХХ и ХХI веков нашлись смельчаки, которые стали разрабатывать инвазивные нейроинтерфейсы на основе нейрочипов — множества маленьких электродов, имплантируемых в мозг и регистрирующих активность отдельных нейронов — однако они столкнулись с проблемой воспалительных реакций в мозге и инфекционных осложнений (рис. 16А). Ученые не одно десятилетие работали над проблемой биосовместимости имплантируемых электродов — начиная с разработки кремниевых электродов в конце 1960-х до концепции гибких электродов, приближающихся по механическим свойствам к нервной ткани в 2010-х.
В 2016 году Илон Маск анонсировал проект Neuralink . Ставка была сделана на очень тонкие гибкие «нити» толщиной в человеческий волос с множеством контактов, которые вводятся в кору роботизированной системой для управления различными гаджетами силой мысли (рис. 16Б). В конце января 2026 года Илон Маск отчитался, что за два года с момента начала тестирования технологии 21 человек уже использует нейрочип Neuralink в повседневной жизни — например, могут набирать на компьютере 40 слов в минуту.
Про Нейралинк «Биомолекула» уже писала: «Нейротехнологии Илона Маска» [67] и «Нейроинтерфейсы: как наука ставит людей на ноги» [61].
Нейровизуализация: слоеный пирог в черном ящике
Долгое время живой человеческий мозг оставался скрытым от глаз исследователя: о его состоянии приходилось судить по косвенным признакам (клинические проявления заболевания, электрическая активность). Исследовать мозг «наглядно» можно было только в результате посмертного вскрытия или на операционном столе после трепанации черепа. Такие условия значительно ограничивали изучение живого головного мозга, особенно всего, что было скрыто под извилинами коры больших полушарий. В решении этой проблемы на помощь пришли достижения физики и химии XX века.
- Нейровизуализация —
- совокупность методов, позволяющих бесконтактно получать детальные изображения структуры и картировать функции живых элементов нервной системы.
Первые атаки рентгеновскими лучами и ультразвуком отражены черепом
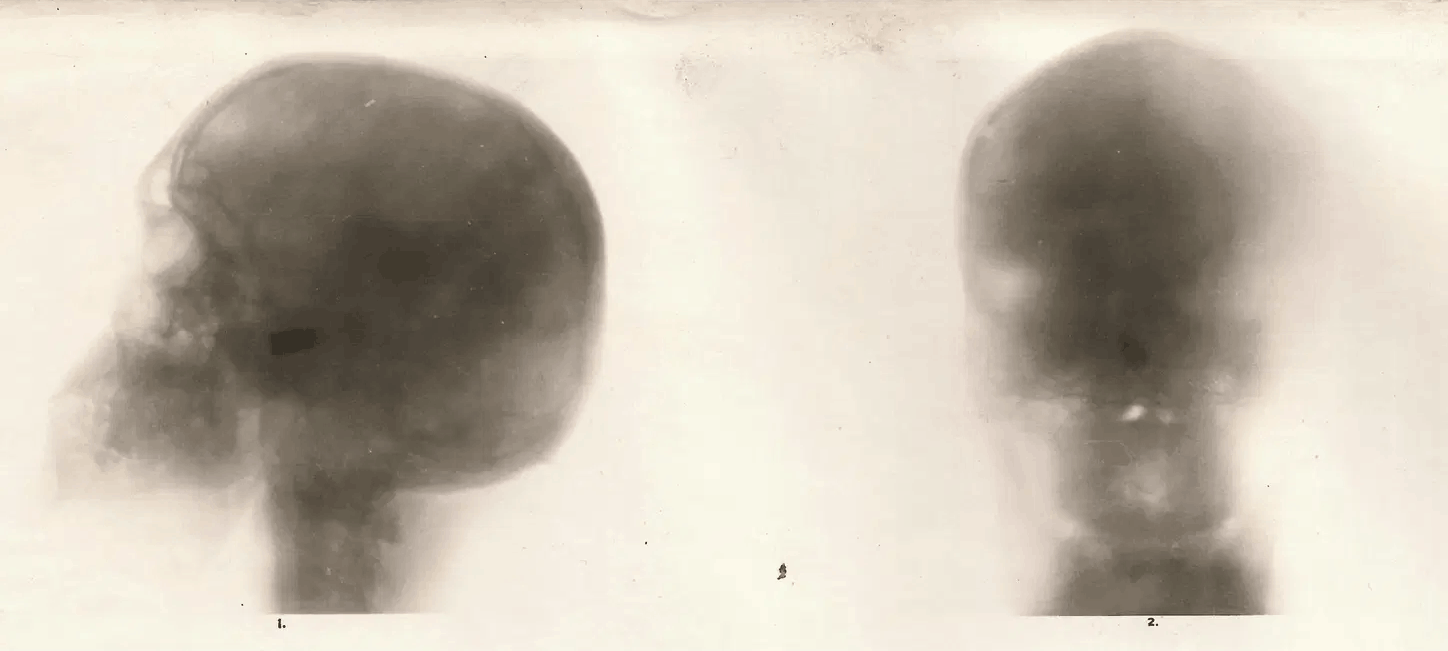
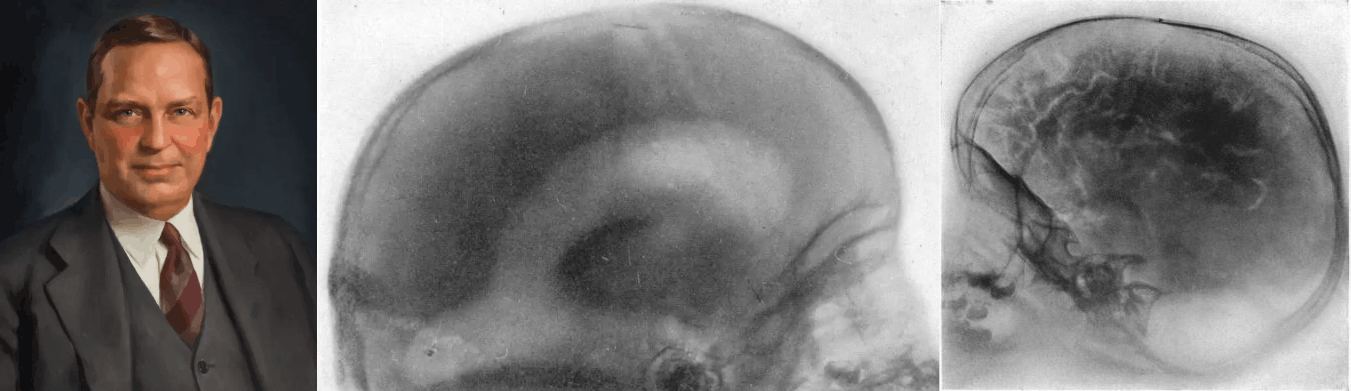
В 1895 году немецкий физик Вильгельм Конрад Рентген на две недели заперся в своей лаборатории, чтобы описать свойства случайно обнаруженных им X-лучей, названных впоследствии рентгеновскими. Излучение сильно поглощалось костной тканью, и уже год спустя врачи использовали рентгенографию черепа для диагностики переломов, смещений и инородных тел. В 1901 году В. Рентген был удостоен Нобелевской премии по физике, а в 1918 — в России создана первая рентгенологическая клиника. Однако небольшая доля рентгеновских лучей, проходящих через кости черепа, плохо поглощается цереброспинальной жидкостью и мозговыми тканями (рис. 17А). Чтобы хоть что-то рассмотреть внутри черепа, необходимо было придать мозговым структурам контраст. В 1918–19 гг. американский нейрохирург Уолтер Денди предложил для этого воздушное контрастирование (рис. 17Б). Через иглу-проводник воздух вводили в пространство с цереброспинальной жидкостью, омывающей спинной и головной мозг (туда несложно и безопасно попасть с помощью прокола в поясничной области — эта процедура называется люмбальной пункцией). Воздух контрастировал мозговые желудочки (вентрикулография) и субарахноидальные пространства вокруг мозга (пневмоэнцефалография). Однако процедура неизбежно сопровождалась сильной головной болью, поэтому требовала выдержки не только от врача, но и от пациента. Тем не менее, десятилетиями только эти методы позволяли приблизиться к визуализации мозга — к счастью, сейчас они не используются [68].
- Вентрикулография —
- рентгенологический метод визуализации желудочков мозга путем их прямого заполнения контрастным веществом (воздухом или йодсодержащим препаратом) через прокол в черепе.
- Пневмоэнцефалография —
- рентгенологический метод визуализации всех ликворных пространств мозга (желудочков и субарахноидального пространства) с помощью введения воздуха через поясничный прокол (люмбальную пункцию).
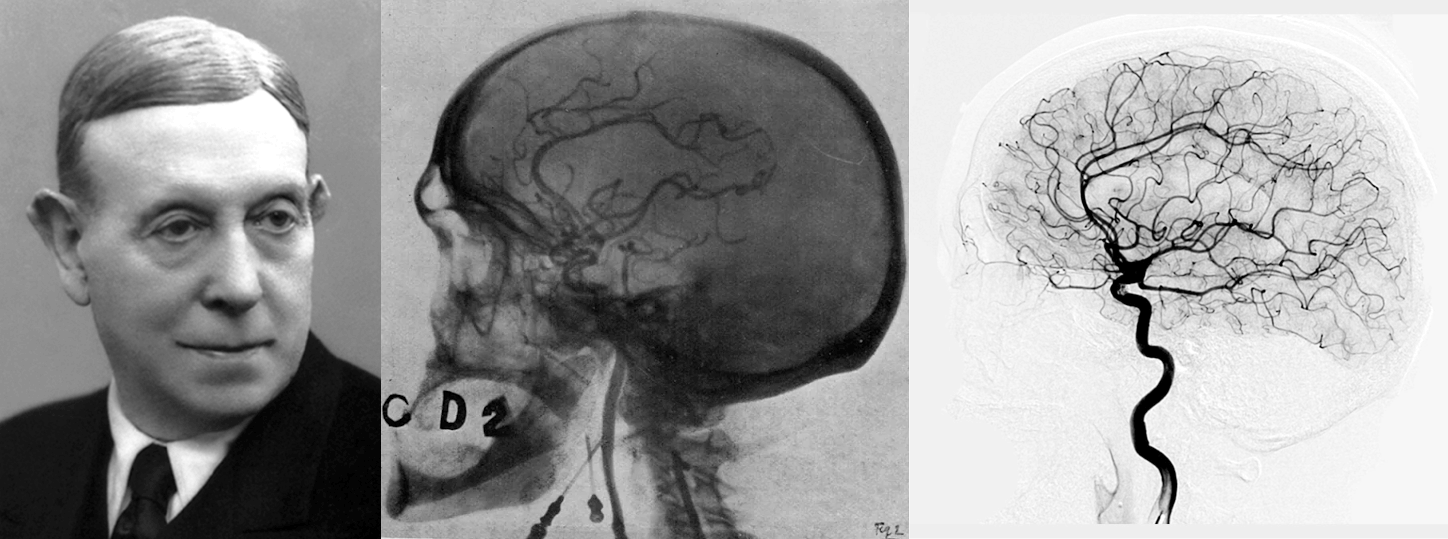
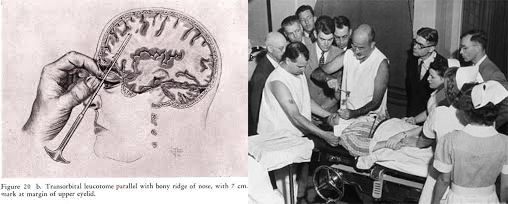
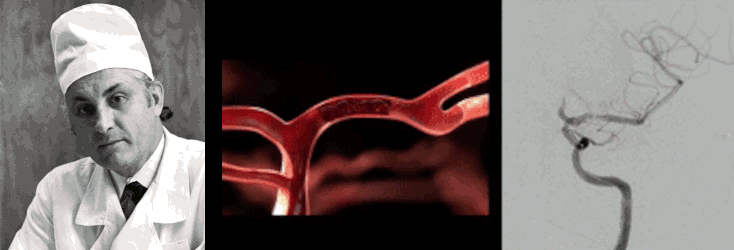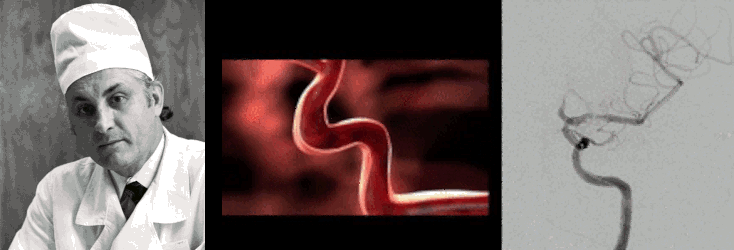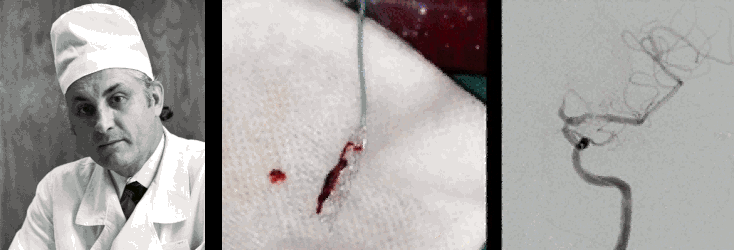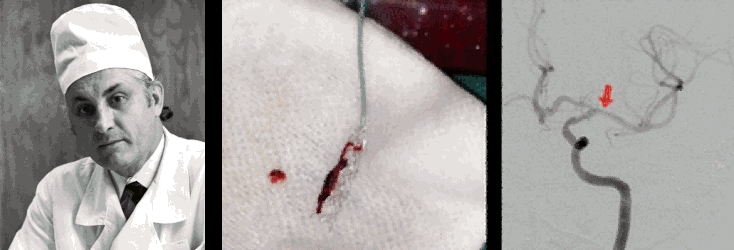
В 1927 году португальский невролог Антониу Эгаш Мониш предложил вводить йодсодержащее рентгеноконтрастное вещество в мозговые сосуды и разработал метод церебральной ангиографии, который до сих пор активно используют сосудистые нейрохирурги (рис. 17В) [69]. Однако Нобелевскую премию Мониш получил не за этот метод, а за разработку лоботомии — запрещенного в настоящий момент метода отсечения трактов лобных долей от остальных частей мозга у душевнобольных пациентов [70], о котором мы еще поговорим в следующей главе.
- Церебральная ангиография —
- рентгенологический метод визуализации просвета сосудов головного мозга высокого разрешения путем введения в артерии контрастного вещества (йодсодержащего препарата). Почитайте также о создателе метода и его противоположных по пользе изобретениях: «Эгаш Мониш: премия за убийство Макмерфи» [70].
- Лоботомия —
- запрещенный в настоящее время метод нейрохирургического вмешательства, при котором разрываются связи лобных долей больших полушарий с остальной частью головного мозга.
В 1942 году австрийский невролог Карл Теодор Дуссик предложил использовать ультразвук для диагностики заболеваний головного мозга — метод гиперфонографии (см. рис. 18А и врезку). На практике оказалось, что кости черепа плохо проницаемы для ультразвуковой волны, а потому метод не прижился [71].
Прорыв черепной обороны силами компьютерной и магнитно-резонансной томографии
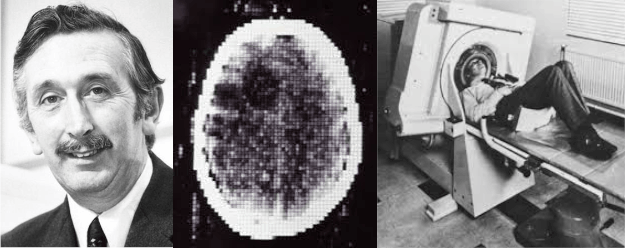
Когда с момента открытия рентгеновских лучей прошло почти сто лет, кости черепа так и не позволяли ученым получить изображение живого головного мозга: приходилось по-прежнему рассчитывать на анатомические атласы, топическую диагностику и собственный клинический опыт. В 1967 году один из неврологов, удрученный таким положением дел, пожаловался в отпуске своему знакомому Годфри Хаунсфилду, инженеру британской звукозаписывающей компании. А тот придумал, что можно объединить сотни рентгеновских снимков в один объемный срез!
Компьютерная томография (КТ)
В 1972 году был получен первый цифровой срез живого головного мозга методом компьютерной томографии (КТ) (рис. 19А). Этот метод воплотился в реальность благодаря совместным усилиям Годфри Хаунсфилда и физика Аллана Кормака, которые учли при разработке прибора все предыдущие попытки ученых математически обосновать и экспериментально доказать возможность послойного построения трехмерного изображения тела и подсчета плотности тканей с помощью множества рентгеновских снимков, полученных под разными углами при вращении рентгеновской трубки вокруг тела пациента. Первые компьютерные томографы имели разрешение лишь 80⨉80 3-миллиметровых пикселей, а реконструкция одного изображения занимала 15 минут. Сейчас КТ-сканирование головного мозга с разрешением 512⨉512 пикселей занимает секунды (рис. 19Б). В 1979 году Хаунсфилд и Кормак стали нобелевскими лауреатами. Их разработка произвела фурор в медицинском сообществе [72].
- Компьютерная томография —
- метод бесконтактного послойного исследования любой области тела с использованием рентгеновского излучения и компьютерной обработки данных с формированием трехмерного изображения.
Разработка альтернативных проектов по формированию цифровых изображений продолжалась. Дело в том, что компьютерная томография, основанная на рентгене, дает потенциально вредную лучевую нагрузку, а КТ-изображения мягких тканей, в том числе мозговых, неконтрастны, а потому мелкие структуры (например, подкорковые ядра, элементы ствола головного мозга, микроинсульты, очаги рассеянного склероза и т.д.) изучать сложно.
Магнитно-резонансная томография (МРТ)
Очень скоро в визуализацию мозга вмешались химики. В 1973 году американский химик Пол Лотербур предложил использовать явление ядерного магнитного резонанса (ЯМР), активно применяемого в расшифровке химической структуры молекул, для построения цифровых изображений. Ряд ученых, в том числе отечественных, уже высказывали эту идею ранее, но по иронии судьбы им всем, включая Лютербура, не выделяли государственного финансирования на разработку прибора, настолько фантастически-невозможным казалось воплощение идеи. Однако Лотербуру удалось впервые получить на своем приборе ЯМР-изображения (рис. 20А). Далее английский физик Питер Мэнсфилд усовершенствовал математические алгоритмы преобразования ЯМР-спектров в цифровое изображение. Мэнсфилд «не пощадил живота своего» — за полчаса он просканировал на приборе свою брюшную полость, чтобы убедить всех, что его метод эффективен и безопасен. С 1982 г. началось коммерческое производство ЯМР-томографов. После аварии на Чернобыльской атомной электростанции в 1986 г. ЯМР-томографы стали называть просто магнитно-резонансными томографами или МРТ, чтобы не пугать людей — ведь метод не дает лучевой нагрузки, в отличие от КТ (рис. 20Б). В 2003 году П. Лотербуру и П. Мэнсфилду была присуждена Нобелевская премия [73].
- Ядерный-магнитный резонанс (ЯМР) —
- физическое явление, при котором ядра атомов в сильном магнитном поле поглощают и излучают энергию на определенных частотах. Помимо нейровизуализации, ЯМР активно применяют для определения структуры биомолекул — подробнее об этом можно прочесть в статье «Структурная биология» [74] цикла «12 методов в картинках» и в заметке «Ядерный магнитный резонанс, или волшебная палочка для химиков и биологов» [75]. Также мы писали и о российских достижениях в этой области: «Сверхпроводящие магниты и рецепторы биомембран: Лаборатория биомолекулярной ЯМР-спектроскопии ИБХ РАН» [76].
- Магнитно-резонансная томография (МРТ) —
- метод бесконтактного послойного исследования любой области тела, основанный на регистрации электромагнитного сигнала от ядер водорода при их возбуждении радиочастотными импульсами в мощном постоянном магнитном поле.
С чистого энтузиазма нескольких людей начался новый виток развития нейротехнологий. МРТ как метод обеспечил не только качественную визуализацию живого головного мозга, но и оказался более многофункциональным, чем КТ. Картинка мягких тканей головного мозга получается невероятно четкой — мы видим структуру каждой извилины. Современные приборы позволяют получать тонкие цифровые срезы толщиной менее миллиметра на десятках специфических режимов, по уровню разрешающей способности приближающиеся к световой микроскопии! В совокупности с возможностью оценки химического состава среза по ЯМР-спектрам это позволяет оценивать микроструктуру мозговых тканей на самых ранних этапах заболеваний или в результате нейромодуляции и обучения, приближая современную нейровизуализацию к цифровой гистологии.
Тем не менее, компьютерная томография тоже не потеряла актуальности — она остается более быстрым (десятикратно) и доступным методом визуализации, позволяющим экстренно выявлять свежие очаги кровоизлияний, отложения кальция, эффективно оценивать плотность костных структур для планирования нейрохирургических операций, а также лучше визуализировать сеть мозговых сосудов с помощью йод-содержащего контраста из-за меньшей зависимости от артефактов (таких как движения пациента и турбулентный ток крови), по сравнению с МРТ.
Нейровизуализация со спецэффектами: функциональная МРТ (фМРТ)
Ученым и врачам хотелось большего: видеть сквозь череп не только структуру, но и работу живого мозга [77]. Первые предпосылки появились в конце 19-го века: итальянский врач Анджело Моссо наблюдал за головным мозгом пациента через дефект в черепе и заметил, что пульсация мозговых сосудов усиливалась в разных участках мозга, когда пациент слышал звон колоколов или читал молитву — активация мозга для обработки внешнего сигнала требует больше кислорода, что усиливает кровоток (рис. 21А) [78].
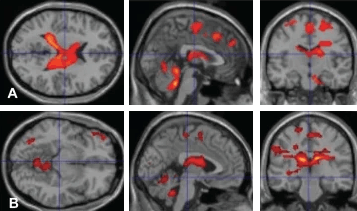
В 1936 году Л. Полинг, известный своим открытием вторичной структуры белка [79], установил, что гемоглобин, насыщенный и обедненный кислородом, по-разному взаимодействует с магнитным полем. Наконец, в 1990 году команда японского биофизика Сэйдзи Огавы объединила все эти знания и разработала принцип BOLD-контраста, то есть локального изменения МР-сигнала в зависимости от степени насыщения гемоглобина крови кислородом. Чем активнее нейроны, тем больше они забирают кислород у гемоглобина. На помощь японским ученым пришли животные и уже известные методы: они заставили крыс дышать воздухом с разным содержанием кислорода и сопоставляли изменения ЭЭГ-активности с МРТ-изображениями [80]. Так зародились основы функциональной МРТ — инструмента, который в реальном времени показывает, какие зоны «вспыхивают», когда мы читаем, лжем или решаем головоломки (рис. 21Б). В основе метода лежит оценка изменения активности нейронов по локальному изменению кровотока в покое и при выполнении различных задач. Разработка фМРТ очень пригодилась в нейрохирургии для индивидуального планирования операций, а также выявила ключевые нервные контуры, отвечающие за различные функциональные состояния головного мозга [77].
Функциональная МРТ (фМРТ) —
- разновидность магнитно-резонансной томографии, которая по изменению уровня оксигенации (насыщения кислородом) крови позволяет в режиме реального времени визуализировать активность нейронов головного мозга в ответ на внешние раздражители или выполнение задач.
Более подробно о современных возможностях нейровизуализации будет рассказано в следующей статье спецпроекта.
Нейрохирургия: семь раз отмерь, один раз отрежь
Нейрохирургия зародилась на рубеже 19–20 веков на «пяти китах»:
-
Топическая диагностика (накопленные знания о специфических функциях различных участков мозга);
-
Функциональная диагностика (достижения в области электрофизиологии и нейровизуализации, позволяющие мониторить функции мозговых тканей в режиме реального времени);
-
Анестезиология (введение пациента в управляемый наркоз и обезболивание);
-
Принципы асептики и антисептики (профилактика инфекционных осложнений);
-
Остановка кровотечения в операционной ране за счет «прижигания» сосудов.
Именно отцы-основатели нейрохирургии (такие как Х. Кушинг, У. Денди) стояли у истоков формирования современных принципов анестезиологического пособия, одними из первых в медицине внедряли методы рентгенографии и электростимуляции, электрокоагуляции сосудов при разрезе; а отец-основатель отечественной нейрохирургии Н. Н. Бурденко называл нейрохируров «неврологами с ножом», подчеркивая важность знаний о топической диагностике.
Философия нейрохирургии основана на компактном расположении большого количества мозговых структур небольших размеров, многослойно упакованных, обладающих чрезвычайной уязвимостью и низким регенеративным потенциалом в условиях стресса, покрытых утолщенной костной капсулой черепа. Если нейрохирург промахнется в своем действии на несколько миллиметров — человек может остаться инвалидом на всю жизнь или вовсе умереть [82]. Подробнее о буднях нейрохирургов читайте в научно-популярной книге Генри Марша «Не навреди. Истории о жизни, смерти и нейрохирургии».
Осторожной поступью по поверхности живого мозга
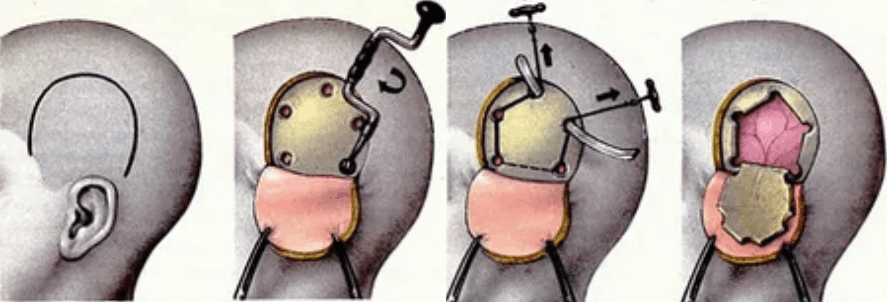
На рубеже 19–20 веков нейрохирурги удаляли только крупные и поверхностные образования мозга — опухоли, гематомы, фрагменты долей больших полушарий. Для планирования операции они использовали анатомические атласы, о которых мы говорили выше, для доступа к мозгу проводили трепанацию (создавали отверстие в черепе под наркозом, формируя костный лоскут в виде «крышки») (рис. 22А), если требовалось определить границы жизнеспособных тканей в этой области — будили пациента во время операции и просили его выполнять задания или стимулировали его мозговую ткань электродами, чтобы не вырезать лишнего.
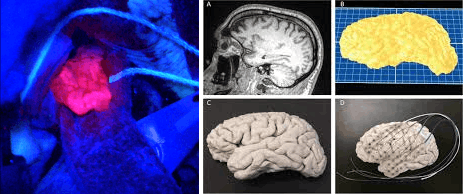
Традиционная нейрохирургия продолжает развиваться (рис. 22Г): используются операционные микроскопы, снимки МРТ/КТ показывают необходимое место и объем операции. Появились методы, позволяющие лучше ориентироваться в оперативном поле: флуоресцентная навигация, когда опухолевая ткань начинает «светиться» на фоне здоровой; 3D-навигация, учитывающая положение инструмента относительно тканей на основе инфракрасных датчиков и данных МРТ. Если раньше нейрохирурги отрабатывали оперативный доступ на мозгах животных, то теперь на основе индивидуальных МРТ-снимков и 3D-принтера они воссоздают точную 3D-копию черепа и мозга пациента, чтобы подготовиться к операции.
«Глубинная» нейрохирургия — стереотаксис и нейронавигация
На рубеже XIX–XX веков ученые предлагали решать проблему доступа к глубоким мозговым структурам с помощью стереотаксиса — системы внешнего проецирования зон мозга на поверхность головы, выполняющих роль «нейрохирургического навигатора» (рис. 23А). В 1947 году американские нейрохирурги Эрнст Шпигель и Генри Уайсис представили один из первых стереотаксических аппаратов для человека, рассчитывающий доступ к патологическому очагу с точностью до 1 миллиметра [84]. Такие устройства фиксировали голову в жесткой рамке и позволяли двигать инструмент в пространстве по трем осям, как по координатной сетке. Когда цель была определена, хирург рассчитывал траекторию и глубину введения инструмента и проводил электрод, зонд или канюлю по заданному «маршруту».
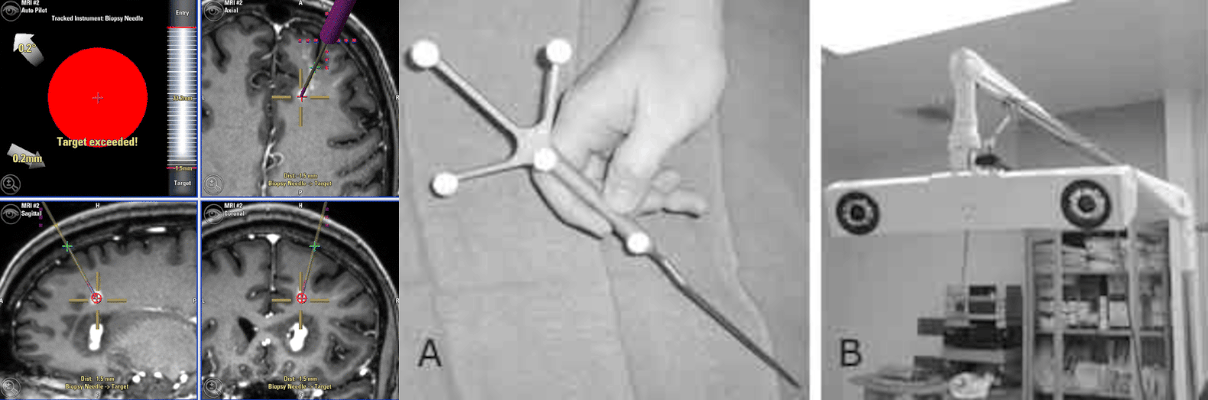
Стереотаксический подход сильно трансформировался с появлением МРТ- и КТ-снимков головного мозга высокого разрешения. Они позволяют быстро и с высокой точностью наметить оптимальный операционный доступ, выполнять операции на труднодоступных участках. Стереотаксис стал безрамочным: голова пациента также жестко фиксируется, однако определение нужных координат стало проводится не по атласам и рамочным конструкциям, а по МРТ-изображениям с помощью автоматики (рис. 23Б) [48].
Внедрение стереотаксиса стало важнейшим шагом на пути к малоинвазивной нейрохирургии, не требующей трепанации и большого оперативного поля. Это уменьшает риск воспаления и кровотечения после операции, пациент быстрее восстанавливается. В медицине этот метод начал активно применяться в середине XX века, когда неврологи столкнулись с заболеваниями, плохо поддающимися терапевтическому контролю: болезни движения (тремор, дистония, обедненные или избыточные движения, спастическое напряжение мышц), хроническая боль, тяжелая генерализованная эпилепсия. Появились стереотаксические атласы и функциональные карты подкорковых ядер (таламус, базальные ганглии), с помощью которых ученые выявили «глубинные мишени» регуляции движения и настроения, возбудимости корковых нейронов, восприятия боли. Начался поиск мягкого и управляемого способа влияния на эти мишени. Это стало основой для зарождения функциональной нейрохирургии, направленной не на удаление структурных повреждений и опухолей, а на коррекцию работы глубинных нервных контуров для управления нейропсихологическими, вегетативными и двигательными процессами при различных заболеваниях, не поддающихся лечению лекарствами [85].
Функциональная нейрохирургия
направлена на коррекцию нарушенных функций мозга (двигательных, болевых, психических) путем прицельного воздействия на конкретные нервные структуры без их физического разрушения.
Поразительный луч: от рентгенохирургии до фокусированного ультразвука
Еще в 1950-х годах нейрохирурги всерьез задумались: если мы научились диагностировать патологию с помощью рентгеновских лучей, почему бы не научиться их использовать для лечения, например разрушать патологические структуры на расстоянии, не открывая череп. Шведский нейрохирург Ларс Лекселл предложил использовать ионизирующее излучение для точечного воздействия на опухоли и другие глубинные мишени. Чтобы не повредить здоровые ткани, он придумал сфокусировать десятки слабых пучков в одной точке — по отдельности они безвредны, но в месте пересечения создают мощный «энергетический удар» (рис. 24А) [86]. Так появилась первая клиническая установка «гамма-ножа» и родилась радиохирургия — оперативное вмешательство без скальпеля, где роль инструмента выполняет сфокусированная энергия. «Гамма-нож» подходит для разрушения небольших глубоко расположенных опухолей и сосудистых патологий; более современной установкой является «кибер-нож», который умеет подстраивается под дыхание пациента, ювелирно направляя лучи даже в движущуюся мишень, благодаря компьютерным алгоритмам.
- Радиохирургия —
- метод лучевой терапии, основанный на однократном направленном облучении патологического очага с установленными координатами высокой дозой ионизирующего излучения.
- Гамма-нож —
- «золотой стандарт» радиохирургии для лечения патологий головного мозга с использованием стереотаксической фиксации головы и неподвижных источников радиоактивного изотопа кобальта-60.
- Кибер-нож —
- универсальная роботизированная система, которая используется для радиохирургического лечения опухолей в любых частях тела, при котором не требуется стереотаксической фиксации, а робот-манипулятор подстраивается под дыхание и движения пациента в режиме реальном времени.
Путешествие по сосудам
Еще одним важным применением рентгеновской визуализации стала эндоваскулярная нейрохирургия, «отцом» которой признан наш соотечественник Федор Андреевич Сербиенко (рис. 24Б) [87], доказавший, что до мозговых сосудов можно добраться изнутри. Под контролем рентгенографии врач вводит тончайший катетер через бедренную артерию и ведет его прямо к патологическому очагу в сосудах мозга. Сегодня этот метод позволяет «заклеивать» аневризмы специальными композитами или устанавливать спирали, предотвращая смертельно опасные кровоизлияния без единого разреза на голове. Эндоваскулярные методики особенно актуальны для сосудистых аномалий, локализованных на нижней поверхности мозга, т.е. труднодоступных и глубоких.
- Эндоваскулярная нейрохирургия —
- совокупность методов лечения заболеваний сосудов головного и спинного мозга изнутри под рентген-контролем с помощью катетеров, заведенных в патологическую область через прокол в крупной артерии.
Пульт управления: фокусированный ультразвук
Радиохирургия имеет принципиальный недостаток: эффект чаще отсрочен, клетки гибнут постепенно, поэтому метод хуже подходит там, где нужен немедленный результат. Поэтому в функциональной нейрохирургии особенно популярным стал метод фокусированного ультразвука (ФУЗ): множество ультразвуковых волн сходятся в одной точке и нагревают ткань. Еще в 1940–50-х американские исследователи Уильям и Фрэнк Фрай продемонстрировали на животных, что множество сфокусированных ультразвуковых пучков могут создавать точечные очаги разрушения в глубинных структурах мозга без грубого повреждения окружающих тканей [88]. Метод нашел эффективное применение в медицине, когда МРТ высокого разрешения позволила точно определять координаты для фокусировки пучка и измерять нагрев тканей в реальном времени (МР-термометрия). Сотни сфокусированных ультразвуковых волн точечно «выключают» зоны, ответственные за дрожание или боль (рис. 24В). Пациент при этом находится в сознании: во время процедуры он может поднять стакан воды и убедиться, что тремор исчез. Кроме того, ФУЗ умеет временно «открывать» гематоэнцефалический барьер, позволяя лекарствам проникать в мозг там, где раньше это было невозможно.
- Фокусированный ультразвук (ФУЗ) —
- технология дистанционного направленного воздействия ультразвуковыми волнами, которые фокусируются в одной точке внутри тела для точечного нагрева с целью разрушения тканей или изменения их функций.
- Гематоэнцефалический барьер (ГЭБ) —
- физиологический «фильтр» между кровью и мозговой тканью, который защищает нейроны от внешних факторов, таких как токсины и микробы, но одновременно ограничивает проникновение многих лекарств. За подробностями приглашаем в статьи «Сквозь тернии к нервам: особенности доставки лекарств в нервную систему» [89] и «Blood-brain barrier. Связующее между двумя мирами — кровеносной и центральной нервной системами» [90].
Более подробно о технологиях, применяемых в современной нейрохирургии, будет рассказано в отдельной статье спецпроекта по медицинским нейротехнологиям.
Эпилог. Мозговой штурм продолжается
Развитие медицинских нейротехнологий происходило параллельно с оформлением неврологии и нейрохирургии как отдельных клинических специальностей. Комбинация патоморфологических, электрофизиологических и нейровизуализационных методов позволили к 21 веку решить первостепенные задачи — систематизировать знания об устройстве и функциях нервной системы и разновидностях неврологических заболеваний, ускорить и детализировать их диагностику, значительно снизить смертность населения от инсультов, эпилепсии, инфекционных и опухолевых заболеваний головного мозга, а также повысить продолжительность и качество жизни пациентов с хроническими заболеваниями нервной системы, — такими как болезнь Паркинсона, рассеянный склероз или мигрень .
Читайте в «Биомолекуле» статьи о современных диагностике и лечении инсультов [91], опухолевых [92], аутоиммунных [32] и нейродегенеративных [93] заболеваний нервной системы.
Однако перед врачами, вооруженными современными нейротехнологиями, стоят колоссальные вызовы. Более трети населения планеты страдает от неврологических заболеваний — они являются ведущей причиной инвалидизации и второй причиной преждевременной смерти [94]. Такая тенденция связана с увеличившейся продолжительностью жизни и успехами в лечении инфекционных и онкологических заболеваний [95]. Современные нейротехнологии обеспечили многие заболевания быстрой диагностикой, позволяющей своевременно начать лечение, снизить риск инвалидизации и летального исхода. Однако для некоторых случаев установить достоверный диагноз не получается из-за отсутствия специфических инструментальных признаков. Например, современные методы нейровизуализации не позволяют напрямую оценить состояние мельчайших сосудов головного мозга. Некоторые заболевания мимикрируют друг с другом (например, злокачественная опухоль может иметь нейровизуализационные признаки воспалительного очага). При этом прямой доступ к мозговой ткани для установки диагноза нередко ограничен — из-за труднодоступности патологических очагов (например, в передних отделах спинного мозга, в стволе головного мозга) проведение прижизненной биопсии головного мозга существенно ограниченно риском повреждения значимых функциональных зон.
Отсутствие понимания причин многих неврологических заболеваний ограничивает их лечение. За последнее десятилетие расходы развитых стран на диагностику и лечение нейродегенеративных заболеваний, таких как болезнь Альцгеймера и болезнь Паркинсона, превысили расходы на лечение сахарного диабета, рака и сердечно-сосудистых заболеваний. Однако до сих пор (!) не разработано терапии, которая смогла бы остановить прогрессирование нейродегенерации [95].
Поэтому повышенное внимание в 21 веке уделяется совершенствованию и внедрению в клиническую практику методов лабораторной и молекулярно-генетической диагностики. Основная задача — это поиск циркулирующих по организму молекул, специфических для конкретного неврологического заболевания. Успехи в этом направлении (прежде всего, для аутоиммунных заболеваний нервной системы) способствуют разработке таргетной терапии — лекарственного воздействия на ключевые молекулярные мишени, задействованные в развитии заболевания [96]. Не стоит забывать, что для неврологических заболеваний существует проблема доставки лекарственных препаратов в мозговую ткань через гематоэнцефалический барьер [89]. Разработка новых лекарственных препаратов требует огромных финансовых вложений, а процедура испытаний нового лекарственного препарата перед использованием в клинической практике занимает десятилетия .
О проблемах разработки новых лекарств можно подробнее почитать в отдельных статьях [97] и спецпроектах «Биомолекулы»: «Генная и клеточная терапии», «Современные лекарства», «Терапевтические антитела», «Клинические исследования».
Подытожив, можно определить вектор развития современных нейротехнологий. Акцент ставится на усовершенствовании существующих методов: повышении разрешающей способности, доступности в повседневной клинической практике, использовании в режиме реального времени. Это позволяет сделать диагностику и лечение неврологических заболеваний более универсальными и в то же время персонализированными, т.е. все больше людей получают шанс на своевременную высокотехнологичную медицинскую помощь по международным стандартам, но с учетом индивидуальных особенностей организма. Проводятся крупные исследования эффективности различных нейротехнологий и их комбинаций на десятках тысяч пациентов в рамках доказательной медицины — таким образом, из каждого нового метода или его модификации извлекается максимум пользы, а риск навредить пациенту уменьшается.
Неврологи стремятся к внедрению принципов превентивной медицины. Создаются подробные шкалы прогнозирования развития неврологических заболеваний по совокупности факторов риска, разрабатываются методы диагностики хронических заболеваний на ранних стадиях. Это позволит в будущем сократить экономические издержки, связанные с необратимой нейродегенерацией и инвалидизацией пациента на более поздних стадиях неврологических заболеваний.
- Превентивная (профилактическая) медицина —
- направление, занимающееся выявлением факторов риска, ранней диагностикой и предупреждением хронических заболеваний еще до появления симптомов.
Расширяется спектр возможностей реабилитационно-восстановительного лечения для пациентов, перенесших инсульт, черепно-мозговую травму, сложную нейрохирургическую операцию. Ожидается, что в ближайшем будущем нейромодуляция и нейропротезирование станут более доступными и позволят повысить качество жизни большому количеству пациентов с утраченными функциями движения и восприятия. Ведутся проекты по когнитивному нейропротезированию с целью «совершенствования интеллекта» и приближения к универсальным формулам гениальности.
Многие нейротехнологии «перекочевывают» в операционные, позволяя нейрохирургам точнее и эффективнее устранять причину недуга. Из-за уменьшения инвазивности операций пациенты быстрее восстанавливаются после операций и реже страдают от последующих осложнений. Из ЭЭГ-ритмов и МРТ-изображений, данных секвенирования нуклеиновых кислот собираются цифровые хранилища больших данных, которые используются для обучения нейросетей. Нейросети позволяют предсказывать и моделировать течение неврологических заболеваний, генерировать новые концепции развития хронических заболеваний.
Все эти примеры указывают на большой скрытый потенциал уже разработанных методов. Однако в поисках способов борьбы со старением и другими современными вызовами (хронический стресс, информационная перегрузка, загрязнение окружающей среды) в руках неврологов и нейрохирургов непременно появятся новые инструменты для штурма мозговой крепости.
Литература
- MiguelA Faria. (2015). Neolithic trepanation decoded- A unifying hypothesis: Has the mystery as to why primitive surgeons performed cranial surgery been solved?. Surg Neurol Int. 6, 72;
- Enrico Crivellato, Domenico Ribatti. (2007). Soul, mind, brain: Greek philosophy and the birth of neuroscience. Brain Research Bulletin. 71, 327-336;
- Гален К. О назначении частей человеческого тела / пер. с древнегреч. проф. С. П. Кондратьева М.: Медицина, 1971. — 555 с.;
- Везалий А. О строении человеческого тела. Т. V, кн. VII: «Мозг» / пер. У. Ф. Ричардсона и Дж. Б. Кармана. San Francisco: Novato: Norman Publishing, 2009. — 413 с.;
- Кин С. Дуэль нейрохирургов : как открывали тайны мозга и почему смерть одного короля смогла перевернуть науку / пер. с англ. К. Савельева. М.: Издательство «Э», 2018. — 576 с.;
- Willis T. Cerebri Anatome, cui accessit nervorum descriptio et usus. London: James Flesher, Joseph Martyn and James Allestry, 1664. — 495 p.;
- Михаил Шифрин: 100 рассказов из истории медицины. Величайшие открытия, подвиги и преступления во имя вашего здоровья и долголетия. Рецензия;
- Ликбез по ЦНС;
- Arenn Faye Carlos, Tino Emanuele Poloni, Valentina Medici, Maia Chikhladze, Antonio Guaita, Mauro Ceroni. (2019). From brain collections to modern brain banks: A historical perspective. A&D Transl Res & Clin Interv. 5, 52-60;
- Шевченко Ю.Л., Карпов О.Э., Бронов О.Ю. (2020). Пироговские срезы, как предтеча современной компьютерной томографии. Вестник Национального медико-хирургического Центра им. Н.И. Пирогова. 15, 11–15;
- Модельные организмы: моллюски;
- Модельные организмы: данио рерио;
- Модельные организмы: ксенопус;
- Модельные организмы: грызуны;
- Модельные организмы: приматы;
- Peter Ratiu, Ion-Florin Talos. (2004). The Tale of Phineas Gage, Digitally Remastered. N Engl J Med. 351, e21;
- Коровски Ю. (2017). Знаменитые пациенты. №1: Финеас Гейдж. Издание «XX2 век»;
- Коровски Ю. (2017). Знаменитые пациенты. №2: Пациент Тан. Издание «XX2 век»;
- Pillmann F. (2007). Carl Wernicke and the neurobiological paradigm in psychiatry. Acta Neuropsychologica. 5, 246–260;
- Иллариошкин С.Н. (2016). Жан Мартен Шарко — основоположник современной клинической неврологии Анналы клинической и экспериментальной неврологии 10, 67–73;
- Kenneth L. Tyler, Rolf Malessa. (2000). The Goltz–Ferrier debates and the triumph of cerebral localizationalist theory. Neurology. 55, 1015-1024;
- Johannes Borgstein, Caroline Grootendorst. (2002). Half a brain. The Lancet. 359, 473;
- Окрасивший нейроны;
- 12 методов в картинках: микроскопия;
- Сотворивший нейробиологию: Сантьяго Рамон-и-Кахаль;
- 12 методов в картинках: нейробиология;
- Roy O. Weller, Michael Swash, D. Lindsay McLellan, Carl L. Scholtz. (1983). Development of Neurology and Neuropathology. Clinical Neuropathology. 1-6;
- Бунина Т.Л. (1962). О внутриклеточных включениях при семейном боковом амиотрофическом склерозе. Журнал невропатологии и психиатрии им. С. С. Корсакова. 62, 1293–1299;
- Tatyana S. Gulevskaya, Pavel L. Anufriev, Мarine М. Tanashyan. (2022). Morphology and pathogenesis of white matter changes in chronic cerebrovascular disease. Annals of Clinical and Experimental Neurology. 16, 78-88;
- Miloš Judaš, Maja Cepanec. (2010). Oskar Vogt: The first myeloarchitectonic map of the human frontal cortex. Translational Neuroscience. 1, 72-94;
- Иммунитет: борьба с чужими и… своими;
- Аутоиммунные заболевания нервной системы: как сдержать нечаянное зло?;
- 12 методов в картинках: иммунологические технологии;
- Vanda A. Lennon, Thomas J. Kryzer, Sean J. Pittock, A.S. Verkman, Shannon R. Hinson. (2005). IgG marker of optic-spinal multiple sclerosis binds to the aquaporin-4 water channel. The Journal of Experimental Medicine. 202, 473-477;
- Catherine Higgins, Jingyi Jessica Li, Michelle Carey. (2025). Spatial transcriptomics iterative hierarchical clustering (stIHC): A novel method for identifying spatial gene co‐expression modules. Quant. Biol. 13;
- Г.А. Корощенко, А.М. Суботялова, М.А. Суботялов. (2023). Development of Concepts on The Physiology of Excitable Tissues. Человеческий капитал. 89-97;
- Гальвани Л. Избранные работы о животном электричестве. — М.-Л.: Биомедгиз, 1937. — 430 с.;
- Формирование мембранного потенциала покоя;
- От искры к пожару: как рождается и путешествует нервный импульс;
- Gabriel Finkelstein. (2003). M. du Bois-Reymond goes to Paris. Br J Hist Sci. 36, 261-300;
- M. V. Aleksandrov. (2019). The roots of electroencephalography (to the 90th anniversary of the original editions of Hans Berger’s work). Medicinskij alfavit. 2, 6-8;
- Lauren Julius Harris, Jason B. Almerigi. (2009). Probing the human brain with stimulating electrodes: The story of Roberts Bartholow’s (1874) experiment on Mary Rafferty. Brain and Cognition. 70, 92-115;
- Все под контролем, или как сберечь нервную систему во время операции;
- Wilder Penfield, Edwin Boldrey. (1937). Somatic Motor and Sensory Representation in the Cerebral Cortex of Man as Studied by Electrical Stimulation. Brain. 60, 389-443;
- Пенфилд У. Мозг. Тайны разума. М.: Наука, 1975. — 124 с.;
- Бакулин И.С., Пойдашева А.Г., Лагода Д.Ю., Супонева А.А., Пирадов М.А. (2021). Перспективы развития терапевтической транскраниальной магнитной стимуляции. Нервные болезни. 4, 3–17;
- Инструкция к перезагрузке мозга: неинвазивная нейромодуляция для лечения резистентной депрессии;
- Maryam Rahman, Gregory J. A. Murad, J Mocco. (2009). Early history of the stereotactic apparatus in neurosurgery. FOC. 27, E12;
- Walter Rudolf Hess (2025). University of Zurich;
- James Olds, Peter Milner. (1954). Positive reinforcement produced by electrical stimulation of septal area and other regions of rat brain.. Journal of Comparative and Physiological Psychology. 47, 419-427;
- Marzullo T.C. (2017). The Missing Manuscript of Dr. Jose Delgado’s Radio Controlled Bulls Journal of Undergraduate Neuroscience Education. 15, R29–R35;
- Wiener N. Cybernetics: or Control and Communication in the Animal and the Machine. Paris: Hermann & Cie, 1948. — 194 p.;
- Что такое нейропротезирование? Это вредно?;
- Вижу цель: новые технологии для незрячих;
- Оптогенетика + голография = прозрение?;
- Восстановлению подлежит: как вернуть зрение?;
- Свет в конце туннеля: генная терапия болезней зрения;
- Когда зрение спит: мир на кончиках пальцев и как ему можно помочь;
- Д.В. Лунев, С.К. Полетыкин, Д. О. Кудрявцев. (2022). Brain-computer interfaces: technology overview and modern solutions. MIST. 2, 0117-0126;
- Naseem K., Basit A., Naseem F., Torshin I. (2023). Neuroprosthetics and Brain-Computer Interfaces: Revolutionizing Rehabilitation. ResearchGate;
- Нейроинтерфейсы: как наука ставит людей на ноги;
- Киборги сегодня: нейрокомпьютерные технологии становятся неотъемлемой частью нашей жизни;
- Нейроинтерфейсы и чтение мыслей. Способен ли «Призрак в доспехах» стать реальностью?;
- Редко, но метко: орфанные заболевания как вызов современной медицине;
- Левицкая О.С., Лебедев М.А. (2016). Интерфейс мозг–компьютер: будущее в настоящем Вестник РГМУ. 2, 4–16;
- Yuanrui Dong, Shirong Wang, Qiang Huang, Rune W. Berg, Guanghui Li, Jiping He. (2023). Neural Decoding for Intracortical Brain–Computer Interfaces. Cyborg Bionic Syst. 4;
- Нейротехнологии Илона Маска;
- Norman C. (2021). The history of neuro imaging. ResearchGate;
- Marco Artico, Marialuisa Spoletini, Lorenzo Fumagalli, Francesca Biagioni, Larisa Ryskalin, et. al. (2017). Egas Moniz: 90 Years (1927–2017) from Cerebral Angiography. Front. Neuroanat. 11;
- Эгаш Мониш: премия за убийство Макмерфи;
- Woo J. (2015). K. T. Dussik. History of Ultrasound in Obstetrics and Gynecology;
- Raymond A. Schulz, Jay A. Stein, Norbert J. Pelc. (2021). How CT happened: the early development of medical computed tomography. J. Med. Imag. 8;
- Robert R. Edelman. (2014). The History of MR Imaging as Seen through the Pages ofRadiology. Radiology. 273, S181-S200;
- 12 методов в картинках: структурная биология;
- Ядерный магнитный резонанс, или волшебная палочка для химиков и биологов;
- Сверхпроводящие магниты и рецепторы биомембран: Лаборатория биомолекулярной ЯМР-спектроскопии ИБХ РАН;
- Marcus E. Raichle. (2009). A brief history of human brain mapping. Trends in Neurosciences. 32, 118-126;
- Stefano Sandrone, Marco Bacigaluppi, Marco R. Galloni, Gianvito Martino. (2012). Angelo Mosso (1846–1910). J Neurol. 259, 2513-2514;
- На заре молекулярной графики;
- S Ogawa, T M Lee, A R Kay, D W Tank. (1990). Brain magnetic resonance imaging with contrast dependent on blood oxygenation.. Proc. Natl. Acad. Sci. U.S.A. 87, 9868-9872;
- Won Kim, Seungyeon Kim, Jaeseung Jeong, Kyung-Uk Lee, Kook-Jin Ahn, et. al. (2009). Temporal Changes in Functional Magnetic Resonance Imaging Activation of Heterosexual Couples for Visual Stimuli of Loved Partners. Psychiatry Investig. 6, 19;
- Лихтерман Л.Б. (2019). Философия клинической нейрохирургии. Kazakh Journal of Clinical Neuroscience. 1, 57–68;
- Коровски Ю. (2017). Знаменитые пациенты. №4: Пациент Г. М.. Издание «XX2 век»;
- E. A. SPIEGEL, H. T. WYCIS, M. MARKS, A. J. LEE. (1947). Stereotaxic Apparatus for Operations on the Human Brain. Science. 106, 349-350;
- P. L. Gildenberg, J. K. Krauss. (2009). History of Stereotactic Surgery. Textbook of Stereotactic and Functional Neurosurgery. 1-33;
- John M. Lasak, John P. Gorecki. (2009). The History of Stereotactic Radiosurgery and Radiotherapy. Otolaryngologic Clinics of North America. 42, 593-599;
- George P. Teitelbaum, Donald W. Larsen, Vladimir Zelman, Anatolii G. Lysachev, Leonid B. Likhterman. (2000). A Tribute to Dr. Fedor A. Serbinenko, Founder of Endovascular Neurosurgery. Neurosurgery. 46, 462-469;
- Maya Harary, David J. Segar, Kevin T. Huang, Ian J. Tafel, Pablo A. Valdes, G. Rees Cosgrove. (2018). Focused ultrasound in neurosurgery: a historical perspective. Neurosurgical Focus. 44, E2;
- Сквозь тернии к нервам: особенности доставки лекарств в нервную систему;
- Blood-brain barrier. Связующее между двумя мирами — кровеносной и центральной нервной системами;
- Сосудистые катастрофы и травмы ЦНС: можно ли спасти поврежденный мозг;
- Онкологические заболевания нервной системы;
- Нейродегенерации, или Массовые вымирания нейронов;
- Valery L Feigin, Theo Vos, Emma Nichols, Mayowa O Owolabi, William M Carroll, et. al. (2020). The global burden of neurological disorders: translating evidence into policy. The Lancet Neurology. 19, 255-265;
- Dirk M. Hermann, Marco Bacigaluppi, Claudio L. Bassetti, Gabrio Bassotti, Johannes Boltze, et. al. (2025). Most prominent challenges in translational neuroscience and strategic solutions to bridge the gaps: Perspectives from an editorial board interrogation. Explor Neurosci. 4;
- Таргетная терапия — прицельный удар по болезни;
- Путь лекарства.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚