
От яда до блокбастера: полная история создания первого инкретинового препарата
19 февраля 2026
От яда до блокбастера: полная история создания первого инкретинового препарата
- 386
- 0
- 0
Как токсин пустынной ящерицы привел к прорыву в лечении диабета и ожирения? На обложке — художественная версия превращения яда в терапевтическую молекулу. В реальности за этим путем стоят десятилетия исследований, упорная борьба за смелую идею и одна ядовитая рептилия.
Рисунок в полном размере.
картинка сгенерирована с помощью Gemini
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Мировой фармацевтический рынок захватили инкретиновые препараты, снижающие уровень сахара в крови, подавляющее аппетит и облегчающие процесс похудения. Сегодня такие лекарства — новая реальность, которая раньше казалась пугающей противоречивой идеей. Как изучение ядов в 1980-х позволило почти 30 лет спустя создать класс препаратов-блокбастеров? Что позволило пройти путь от экзотических животных до работающих инъекций для коррекции веса, и почему эти лекарства сейчас становятся ключевым направлением фармразработки?
Конкурс «Био/Мол/Текст»-2025/2026
 Эта работа заняла первое место в номинации «Академия & Бизнес» конкурса «Био/Мол/Текст»-2025/2026.
Эта работа заняла первое место в номинации «Академия & Бизнес» конкурса «Био/Мол/Текст»-2025/2026.

Генеральный партнер конкурса и партнер номинации — международная инновационная биотехнологическая компания BIOCAD.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
«Всё есть яд и всё есть лекарство»
В пустыне Аризоны, где камни раскаляются под обжигающим солнцем, а все живое замирает от жары, по песку медленно перебирает лапами пятнистая рептилия с крупным телом. Ее укус смертелен для мелких животных, а у человека может вызвать отравление и более тяжелые последствия. Это представитель вида Heloderma suspectum, он же аризонский ядозуб (рис. 1), жилатье или гила-монстр. И внимание к себе он привлек не экстравагантным образом или длинным хвостом, а составом слюны, который заинтересовал ученых и позволил сделать большой шаг к созданию новых лекарств. Чтобы понять, как это произошло, обратимся к истории.

Рисунок 1. Аризонский ядозуб (Heloderma suspectum) в естественной среде обитания. Длина его тела достигает 60 см, из них 15–17 см приходится на хвост. Вес особи — до 2 кг. Яркий окрас хищника предупреждает, что к нему лучше не подходить, но когда ученых это останавливало?

Рисунок 2. Доктор Джон Пизано усыпляет осу с помощью углекислого газа для обеспечения безопасного получения яда. В заметке указано, что семья Девентер из штата Мэриленд предоставила более 80 ос для проекта.
THE NIH RECORD. July 16, 1963
В 1980 году молодой гастроэнтеролог Жан-Пьер Рофман, совсем недавно окончивший медицинский колледж в Нью-Йорке и ординатуру в Бронксе, отправился в ведущий исследовательский центр в США — National Institutes of Health (NIH), — чтобы продолжить свою научную карьеру. Два года до этого он стажировался в Мичиганском университете и занимался классическими исследованиями в своей области. Его новая тема оказалась далека от врачебной практики. Жан-Пьер работал под наставничеством эксцентричного биохимика и кардиолога Джона Пизано, за которым закрепилась необычная слава: он собирал коллекцию ядов животных и делал это необычным, но действенным способом. Пизано писал объявления о приеме образцов в The Washington Post, а читатели газеты с радостью приносили к его дверям различных жалящих и кусающих существ — пчел, змей, лягушек и ящериц. В его лаборатории даже висело осиное гнездо (рис. 2): ученый разрабатывал установку для «доения» насекомых и выделял из их яда токсины для изучения синтеза пептидов в клетках животных.
Почему Пизано так привлекали яды? В их составе было множество коротких биологически активных пептидов, селективно взаимодействующих с рецепторами, что приводило к изменению проницаемости клеточных мембран и вызывало различные клеточные реакции. Токсины животных могут содержать тысячи компонентов разной химической природы [1] — все они сформировались в ходе эволюции и получили название «эволюционно отредактированная комбинаторная библиотека» [2]. Каждая из этих молекул специфично и с различной эффективностью взаимодействует с определенным рецептором. Комплекс токсинов бьет по множеству мишеней, но, если выделить из яда один пептид и использовать его в более низкой концентрации, можно получить обратный эффект. В каждом из таких соединений скрывается терапевтический потенциал.
Вероятно, Джон Пизано вдохновился успехом своих коллег или дословно воспринял главный принцип Парацельса: «Всё есть яд, ничто не лишено ядовитости, и всё есть лекарство. Одна только доза делает вещество ядом или лекарством». В любом случае, он выбрал верное направление для исследований. При этом самого Пизано больше интересовали осы, а новому ученику он передал часть коллекции с ядами рептилий. Рофман проводил эксперименты, помещая образцы в ацинарные клетки поджелудочной железы морских свинок, отвечающие за синтез, накопление и секрецию пищеварительных ферментов. Так он проверял гипотезу о том, что яд может стимулировать работу этих клеток.
Хотя Heloderma suspectum обитает далеко от Мэриленда, ее яд тоже попал в ту лабораторию. Более того, из всех образцов он показал лучшие результаты. В 1982 году Жан-Пьер Рофман опубликовал первую статью, где описал пептид, стимулирующий выработку ферментов поджелудочной железы лучше, чем известные ранее и вырабатываемые в организме вазоактивный интестинальный пептид (VIP), регулирующий множество функций в организме, включая кровяное давление, пищеварение и частоту сокращений сердца; и секретин — гормон, стимулирующий выработку бикарбонатов поджелудочной железой, секрецию желчи и желудочного сока [5]. Яд не разрушал клетки, а стимулировал синтез биоактивных соединений. Это означало, что из секрета гила-монстра можно было выделить аналог естественного лиганда рецептора (его агонист) и, возможно, научиться управлять метаболизмом так, как это получилось с артериальным давлением.
В следующем году ученый из Брюсселя выделяет из того же яда пептид, который получает название гелодермин (или эксендин-2) [6]. Он стимулировал секрецию пищеварительных ферментов, активировал аденилатциклазу и взаимодействовал со специфическими рецепторами: его эффект блокировался антагонистами рецепторов VIP и секретина. Гелодермин стал первым агонистом в этом семействе пептидов, а после его секвенирования в 1985 году ученые отметили эволюционную связь между ним и аналогичными гормонами у млекопитающих [7]. Это стало первым доказательством того, что яд рептилии содержит полноценный гормон, способный активировать рецепторы животных и человека и стимулировать секрецию клеток поджелудочной железы. Это открытие подстегнуло поиски других «полезных» пептидов в ядах.
Поиски продолжил Рофман: летом 1983 года он покинул лабораторию Джона Пизано и отправился в свободное плавание по научному миру. Его исследования в те годы были связаны с изучением регуляторных молекул желудочно-кишечного тракта.
В конце 1980-х Рофман познакомился с Джоном Энгом — молодым эндокринологом из Бронкса, который перенял экспертизу в работе с пептидами у своей наставницы, нобелевского лауреата Розалин Ялоу. В это время Энг уже почти десять лет работал с пациентами, больными сахарным диабетом (СД). Проблема контроля гликемии и недостатка инсулина была знакома ему с разных сторон, а ее решение он ищет в пептидах, которые продолжает изучать, выделяя их из крови и органов морских свинок и шиншилл. В ходе своих исследований Джон Энг познакомился с работой Рофмана и Пизано и оценил ее потенциал со стороны эндокринологии. Он посчитал, что пептиды из ядов помогут создать препарат для лечения диабета — и не ошибся.
Эндокринолог Энг и гастроэнтеролог Рофман образовали союз «охотников за гормонами»: один из них ищет и выделяет новые пептидные гормоны из крови и тканей, а другой продолжает изучать их влияние на клеточные модели. В 1990 году они опубликовали статью, в которой описали новый пептид, выделенный на этот раз из секрета не аризонского, а мексиканского ядозуба — эксендин-3. Спустя еще пару лет, в 1992 году, они получили эксендин-4 из яда Heloderma suspectum, с которого всё началось. Новый пептид является агонистом человеческого глюкагоноподобного пептида-1 (GLP-1) — имитирует его действие, но при этом обладает более длительным эффектом. Подробнее об инкретинах и GLP-1 рассказывается в статье «Аппетит как мишень: почему все попытки обуздать ожирение и диабет проваливались, пока не появились агонисты рецепторов инкретинов» [8] из цикла «Метаболизм, аппетит и инкретины».
Через тернии к патенту
Казалось бы, желание Джона Энга было исполнено: вместе с Жан-Пьером Рофманом они нашли пептид, который оказывает желаемый терапевтический эффект — эксендин-4 селективно активировал рецептор GLP-1 даже при низких концентрациях, стимулировал синтез инсулина и подавлял выработку глюкагона, что позволяло комплексно контролировать уровень глюкозы в крови. Однако применять вещество для лечения было нельзя: пептиду требовалось пройти долгий путь, чтобы попасть к пациенту. Но самым сложным было донести эту информацию до фармпроизводителей.
Так у амбициозного эндокринолога появилась новая цель: он решил получить патент на свое открытие. Ситуацию осложняло то, что Энг вел свои исследования в государственном учреждении — Медицинском центре Veterans Affairs (VA), а значит, и свидетельство о регистрации должно было осуществляться силами VA. Для организации этот процесс оказался неподъемным: для них это было сложно как с коммерческой стороны, так и для дальнейших этапов разработки. Они признали, что не смогут помочь в реализации задумки исследователя, и отказали в патентовании со своей стороны.
Энг старался не отчаиваться и нести свое открытие миру — для начала, его научной части. Он отправился в Копенгаген: там с 17 по 19 мая 1993 года проходил Первый международный симпозиум по агонистам GLP-1, который поддерживала датская компания Novo Nordisk [10]. Событие объединило более 40 ученых из 12 стран (рис. 3) [11]: исследователей, открывших глюканоподобный пептид, проводящих его клинические исследования и изучающих инкретиновую физиологию — раздел науки, посвященный гормонам кишечника и их помощи поджелудочной железе в управлении уровнем глюкозы после еды. Джон Энг совместно с Жан-Пьером Рофманом представили там результаты исследования эксендина-4 и получили признание открытия профессиональным обществом.

Рисунок 3. Первый международный симпозиум, посвященный агонистам GLP-1.
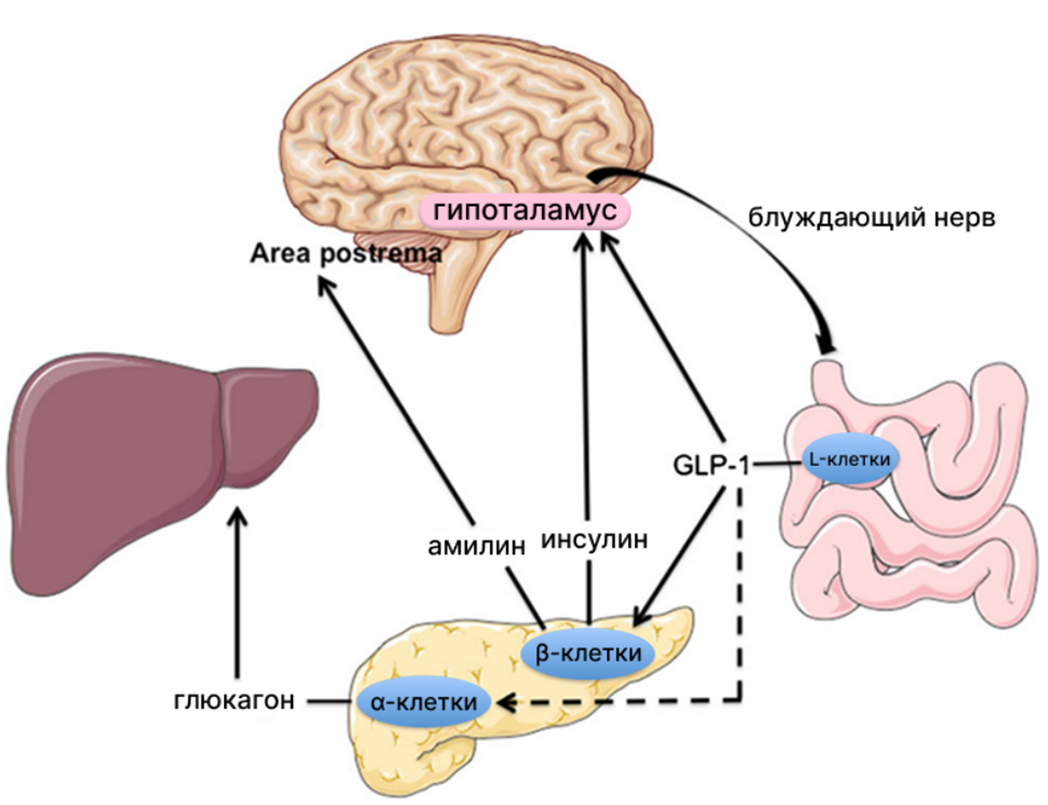
Рисунок 4. Схема работы амилина в организме. После приема пищи кишечные L-клетки выделяют GLP-1, который действует сразу по нескольким направлениям: стимулирует β-клетки поджелудочной железы к секреции инсулина и амилина, подавляет выделение глюкагона и передает сигналы насыщения в гипоталамус — напрямую и частично через блуждающий нерв. Амилин, открытый в начале 1980-х благодаря изучению амилоидных отложений в поджелудочной железе котов, страдающих диабетом, дополняет действие GLP-1: усиливает чувство сытости и снижает размер порций за счет влияния на рвотный центр (area postrema). Вместе GLP-1 и амилин ограничивают аппетит и подавляют глюконеогенез после еды (организм переходит в постпрандиальный режим). Сейчас Symlin на основе синтетического амилина остается единственным одобренным препаратом с этим действующим веществом для лечения СД1 и СД2 и применяется в комплексе с инъекциями инсулина.
адаптировано из [13]
Успешная презентация открытия и поддержка коллег сыграли свою роль: не прошло и недели с момента возвращения в США, как Энг подал личную заявку на получение патента. В 1995 году эксендин-3 и эксендин-4 официально были признаны изобретением Джона Энга, которое он предлагал использовать для лечения сахарного диабета.
Это было началом длинного доказательного пути: патент был получен, но это не прибавило представителям бизнеса доверия к потенциальному лекарству, полученному из яда. Энг продолжал бороться за свое детище: рассказывал об эксендине на конференциях, общался с представителями индустрии, но это не приводило к ожидаемым результатам. Все изменилось в 1996 году, когда «ядовитым» пептидом заинтересовался небольшой стартап из Сан-Диего. Группа ученых создала Amylin Pharmaceuticals в 1987 году с целью разработать лекарство от сахарного диабета на основе амилина, синтезируемого β-клетками поджелудочной железы и способного снижать аппетит и повышение глюкозы в крови после еды (рис. 4) [12], [13]. Препарат на основе этого пептида мог стать хорошим спутником для инсулина, как и эксендин, имеющий схожий эффект.
На момент знакомства Amylin Pharmaceuticals с Энгом у стартапа еще не было зарегистрированных препаратов: только в 1997 году они получили первый патент на прамлинтид, синтетический аналог амилина. Они поверили в будущее эксендина-4, купили эксклюзивные права на его использование и синтезировали пептид самостоятельно, чтобы окончательно уйти от историй с ящерицами. Amylin провели серию доклинических испытаний, которые подтвердили достоинства нового пептида: для того же действия, что оказывает GLP-1, требовалось в 5500 раз меньшее количество эксендина-4, а его эффект длился дольше, до 4–6 часов — в этом сыграла роль замена аминокислоты в позиции 3: она защищала пептид от фермента дипептидилпептидазы-4 (DPP-4), который разрушает человеческий GLP-1 (рис. 5) [14], [15].

Рисунок 5. Аминокислотная структура GLP-1 и эксендина-4. GLP-1 действует глюкозозависимым образом и после синтеза в течение нескольких минут разрушается под действием DPP-4. Эксендин-4 — природный аналог GLP-1 — не разрушается ферментом и сохраняет активность до 6 часов, что позволяет производить лекарства длительного действия для лечения метаболических заболеваний.
адаптировано из [15]
К 2000 году Amylin Pharmaceuticals имел полный пакет результатов, необходимых для следующего шага. Данные были убедительными, поэтому компания начала поиск индустриального партнера для проведения клинических исследований.
От разработки до пациента
В 2002 году Amylin Pharmaceuticals начали сотрудничество с Eli Lilly — первым в истории производителем инсулина, сосредоточенным на разработке лекарств для лечения диабета и ожирения. Инновационная молекула оказалась для них особо привлекательной. Eli Lilly купил лицензию и часть акций у стартапа, а также инвестировал в клинические исследования эксендина около 200 млн долларов. Оставались последние шаги до регистрации.
В ходе испытаний врачи отметили, что ожидаемое снижение уровня сахара в крови сопровождается потерей веса — редким эффектом для диабетологии. Эксенатид (такое МНН получил препарат) обещал стать дополнением к метформину и сульфонилмочевинам, традиционно применяемым для терапии СД. Результаты были убедительны: повышенный при диабете гликированный гемоглобин (HbA1c) у пациентов снижался на 0,8–1,0%, также они теряли 2–3 кг веса, и при всем этом риск гипогликемии был минимальным благодаря глюкозозависимому механизму и приемлемому профилю безопасности. Из побочных эффектов участники исследования часто отмечали тошноту, которая уменьшалась при продолжительном приеме.
В 2005 году FDA одобрила «Баета» — первый в мире препарат-агонист рецептора GLP-1 и гипогликемический препарат, который замедлял процесс опорожнения желудка, снижая скорость поступления глюкозы из пищи в кровоток. В отличие от сульфонилмочевин, эксенатид не истощал β-клетки, а стимулировал их регенерацию с помощью глюкозозависимого механизма действия [16]. Регистрация этого препарата и его позитивные клинические эффекты запустили импульс к разработке целого поколения GLP-1-агонистов — лираглутида, ликсисенатида, дулаглутида, семаглутида (рис. 6) и будущих, за первенство в создании которых борются современные фармкомпании.
В погоне за новыми инкретинами
Eli Lilly не так долго владела first-in-class препаратом: в 2011 году Amylin Pharmaceuticals расторгла сотрудничество, а стартап, выросший в полноценную самостоятельную организацию за годы работы с пептидами, купила Bristol-Myers Squibb. В 2014 году все доли диабетического альянса этой компании выкупила AstraZeneca, которая сейчас обладает регистрационным удостоверением на «Баета».

Рисунок 6. Эволюция основных инкретиновых препаратов от природных аналогов до модифицированных синтетических молекул. Человеческий GLP-1 (А) — короткий пептид, быстро разрушаемый DPP-4. Эксендин-4 (B) получен из яда Heloderma suspectum и представляет более длинный и устойчивый к воздействию DPP-4 пептид — прототип первого препарата эксенатида (C). Далее идет «второе поколение» аналогов GLP-1: лираглутид (D) и семаглутид (F) — к их последовательности присоединены жирные кислоты через линкеры, что позволяет им связываться с альбумином и циркулировать в организме значительно дольше. Строение дулаглутида (E) представляет слитый белок из двух копий модифицированного GLP-1 с Fc-фрагментом IgG4, что увеличивает продолжительность его действия до 5 дней. Нижняя часть картинки демонстрирует человеческий GIP (G) и тирзепатид (H) — мультиагонист, состоящий из модифицированного GIP-пептида с якорем из жирных кислот, активирующим рецепторы GIP и GLP-1.
адаптировано из [17]
Разработкой инкретиновых препаратов занялись и другие фармгиганты в разных точках мира: датская компания Novo Nordisk в 2014 зарегистрировала лираглутид, британская GlaxoSmithKline в 2014 году вывела на рынок албиглутид, американская Eli Lilly в тот же год расширила линейку, начатую с эксенатида, и получила удостоверение на дулаглутид, а французская Sanofi в 2016 представила ликсисенатид (рис. 6) [17]. Все эти лекарства вводились подкожно, имели схожий принцип действия и разное время полувыведения — от 2,4 часов до 5 дней.
Спустя год этот список пополнил семаглутид — знаменитый «Оземпик» от Novo Nordisk [18]. И если предыдущие препараты класса назначались только для лечения сахарного диабета 2 типа, то этот получил новое показание: его официально рекомендовали для терапии ожирения.
В 2022 году те же показания получил первый одобренный мультиагонист GLP-1 и глюкозозависимого инсулинотропного полипептида (ГИП, GIP) — тирзепатид (рис. 6) с торговым наименованием «Мунджаро» от Eli Lilly, рекомендованный для лечения СД 2 типа и избыточного веса. Спустя еще год в компании появляется еще один препарат с тем же действующим веществом, но с показанием к лечению исключительно ожирения — «Зепбаунд». Совмещение GLP-1 и GIP — инкретинового гормона, который синтезируется в клетках кишечника после приема пищи, особенно богатой углеводами и жирами, — позволил дополнить терапевтическое действие лекарства метаболическими функциями: регулировать липидный обмен и влиять на жировую ткань. Подробнее обо всех зарегистрированных инкретиновых препаратах написано в статье «Оземпик: больше, чем средство для похудения» [18].
Гонка продолжается?
Инкретины взорвали фармацевтический рынок: в США его емкость оценивается десятками миллиардов долларов (рис. 7). Ожидается, что к 2030 году рынок препаратов для лечения ожирения и сахарного диабета удвоится и достигнет 100–150 млрд долл.

Рисунок 7. С 2019 до 2023 года американский рынок агонистов GLP-1 вырос более, чем вдвое. Спрос на «Оземпик» лидирует, однако почетное второе место занимает «Трулисити» — препарат дулаглутида. Доля продаж тирзепатида («Мунджаро») также постепенно набирает обороты. Менее востребованы препараты предыдущего поколения: «Виктоза» и «Саксенда» с действующим веществом лираглутид, таблетированный семаглутид «Ребелсас» и «Будуреон» — еще один эксенатид от Amylin Pharmaceuticals с более продолжительным действием. В России ни один из этих препаратов не доступен, но у большинства существуют зарегистрированные аналоги.
адаптировано из Earnest Analytics
Тем не менее, рост продаж препаратов для лечения сахарного диабета и снижения веса коррелирует и с другой печальной статистикой: количество людей, страдающих ожирением и сахарным диабетом, ежегодно растет. Висцеральный жир становится причиной множества хронических заболеваний, включая развитие сахарного диабета 2 типа, а также опасных для здоровья кардиометаболических последствий [19]. Своевременное лечение действительно может сохранить годы активной жизни [20], но применение без наблюдения врача может и навредить — подробно об этом написано в статье «Две стороны инкретинов: спасение от ожирения и новые угрозы» [21].
Ученые не остановились на разработке двойного агониста, а продолжили искать новые мишени и синтезировать «чудо-пептиды». Например, компания Eli Lilly сейчас находится на заключительной стадии разработки агониста трех рецепторов: GLP-1, GIP и глюкагона. Ретатрутид — такое название получило действующее вещество препарата — проходит III фазу клинических исследований (рис. 9). Он сможет обеспечить пациентам более быстрое снижение массы тела за счет комплексного действия: препарат одновременно подавляет аппетит, замедляет опорожнение желудка, увеличивает интенсивность липолиза в печени за счет действия на рецептор глюкагона, а также, подобно предшественникам, повышает толерантность клеток к инсулину.

Рисунок 8. Названия лекарственных препаратов и соединений, имитирующих гормоны. Красная спираль представляет имитируемый гормон, который связан с цветными рецепторами: рецепторами GLP-1, GIP- и глюкагоновыми рецепторами. Рецепторы расположены на поверхности клеток, где происходит связывание гормонов.
адаптировано из The Conversation
Исследователи пробуют не только тройные, но и новые двойные комбинации инкретинов. Один из таких примеров — «Исида» с действующим веществом маздутид: препарат, разработанный Eli Lilly совместно с китайской компанией Innovent Biologics и зарегистрированный в июне 2025 года. Это рекомбинантный пептидный аналог оксинтомодулина (пептидного гормона, который секретируется кишечником вместе с GLP-1 после приема пищи), модифицированный для действия на рецепторы GLP-1 и глюкагона. Клинические исследования, проведенные на китайских пациентах, показали, что эффективность маздутида для коррекции веса сопоставима с аналогичным показателем у монопрепарата тирзепатида «Зепбаунд». В Innovent Biologics также подчеркнули, что при более высокой дозировке пациентам удавалось достичь снижения содержания жира в печени на 80%. Возможно, это лекарство станет новым блокбастером на мировом рынке и обгонит продажи семаглутида.
Почти все препараты, описанные выше, представлены в инъекционных лекарственных формах. Они выигрывают перед пероральными как минимум тем, что не требуют ежедневного приема, который бывает сложно контролировать и сочетать с применением другой терапии. Однако разработка более удобных и эффективных таблетированных вариантов для лечения диабета и ожирения активно продолжается. Из зарегистрированных препаратов на рынке представлены оральный семаглутид «Ребелсас» и низкомолекулярный непептидный агонист GLP-1 «Орфоглипрон». Многие разработки в этом направлении терпят неудачи: например, компания Pfizer на поздней стадии остановила исследования двух препаратов, схожих по действию с орфоглипроном, из-за повышенной выработки ферментов печени у участников клинических испытаний.
Еще одно направление исследований связано с увеличением длительности действия препаратов. Если первые представители класса действовали несколько часов, то сейчас ученые стремятся создать лекарство, которое нужно будет принимать раз в месяц. Например, стартап Metsera разрабатывает инъекционный агонист GLP-1, аналог амилина и таблетированный тройной агонист сверхдлительного действия. Некоторые из этих лекарств уже успешно прошли первые стадии клинических исследований, но о результатах мы сможем судить лишь спустя время.
Не конец, а начало чего-то большего
Путь к созданию первого инкретинового препарата занял более 20 лет. «Баета» долгое время оставалась востребованным средством для лечения сахарного диабета и помогла миллионам пациентов. За это время наука сделала шаг далеко вперед: оригинальный эксенатид практически не используется в клинике, но именно он открыл новое направление в терапии метаболических заболеваний. Спустя время это привело к созданию препаратов-блокбастеров, которые стимулируют рост мирового фармрынка.
История первого инкретинового препарата — история людей, увидевших в токсине не угрозу, а инструмент. Джон Пизано, собиравший яды ради фундаментальной науки, не дожил до клинического успеха своей идеи — его запомнили как человека с бескомпромиссными профессиональными стандартами и заразительным энтузиазмом. Жан-Пьер Рофман, разглядевший в секрете аризонского ядозуба перспективную молекулу, вернулся к клинической практике и продолжает изучать инкретины в Университете Мэриленда. Джон Энг, который заметил в молекуле эксендина потенциал для лечения диабета, донес ценность «ядовитого» пептида до бизнеса. За этот вклад ученый получил профессиональное признание и продолжил работу над модификациями инкретинов, включая мультиагонисты.
Аризонский ядозуб, с которого все началось, сегодня охраняется как редкий вид. Современная фармакология не собирает ядовитых животных у жителей округи, как это делал Пизано, но продолжает искать терапевтический потенциал там, где раньше видели лишь опасность, а инновационные технологии позволяют делать это более эффективно [22].
Не только доза делает вещество ядом или лекарством — решающим становится понимание того, как и для чего его применять. Будущее нередко рождается на границе риска и фундаментального знания. И, возможно, именно в самых пугающих веществах скрывается секрет новых препаратов-блокбастеров.
Литература
- Яды — высокоточное оружие: компьютерное исследование природных нейротоксинов;
- Великому комбинатору и не снилось: комбинаторика токсинов пауков;
- Juliana Mozer Sciani, Daniel Carvalho Pimenta. (2017). The modular nature of bradykinin-potentiating peptides isolated from snake venoms. J Venom Anim Toxins Incl Trop Dis. 23;
- Y.S. Bakhle. (2020). How ACE inhibitors transformed the renin–angiotensin system. British J Pharmacology. 177, 2657-2665;
- J. P. Raufman, R. T. Jensen, V. E. Sutliff, J. J. Pisano, J. D. Gardner. (1982). Actions of Gila monster venom on dispersed acini from guinea pig pancreas. American Journal of Physiology-Gastrointestinal and Liver Physiology. 242, G470-G474;
- Patrick Robberecht, Magali Waelbroeck, Jean-Paul Dehaye, Jacques Winand, André Vandermeers, et. al.. (1984). Evidence that helodermin, a newly extracted peptide from Gila monster venom, is a member of the secretin/VIP/PHI family of peptides with an original pattern of biological properties. FEBS Letters. 166, 277-282;
- Minoru Hoshino, Chizuko Yanaihara, Yeong-Man Hong, Satoshi Kishida, Yumiko Katsumaru, et. al.. (1984). Primary structure of helodermin, a VIP‐secretin‐like peptide isolated from Gila monster venom. FEBS Letters. 178, 233-239;
- Аппетит как мишень: почему все попытки обуздать ожирение и диабет проваливались, пока не появились агонисты рецепторов инкретинов;
- Daniel J. Drucker, Joel F. Habener, Jens Juul Holst. (2017). Discovery, characterization, and clinical development of the glucagon-like peptides. Journal of Clinical Investigation. 127, 4217-4227;
- International Symposium on Glucagon-Like Peptide-1. Copenhagen, Denmark, May 17-19, 1993. Abstracts. Digestion. 54, 337–397;
- Burkhard Göke, Rüdiger Göke, Jens Juul Holst, Cathrine Orskov. (1993). Glucagon-Like Peptide 1: On Its Way to Clinical Application. Digestion. 54, 339-340;
- Tahir Muhammad, Stephen F. Pastore, Katrina Good, Wai Haung Yu, John B. Vincent. (2025). The role of amylin, a gut–brain axis hormone, in metabolic and neurological disorders. FASEB BioAdvances. 7;
- T. Jorsal, J. Rungby, F. K. Knop, T. Vilsbøll. (2016). GLP-1 and Amylin in the Treatment of Obesity. Curr Diab Rep. 16;
- A A Young, B R Gedulin, S Bhavsar, N Bodkin, C Jodka, et. al.. (1999). Glucose-lowering and insulin-sensitizing actions of exendin-4: studies in obese diabetic (ob/ob, db/db) mice, diabetic fatty Zucker rats, and diabetic rhesus monkeys (Macaca mulatta).. Diabetes. 48, 1026-1034;
- Elliot J. Glotfelty, Lars Olson, Tobias E. Karlsson, Yazhou Li, Nigel H. Greig. (2020). Glucagon-like peptide-1 (GLP-1)-based receptor agonists as a treatment for Parkinson’s disease. Expert Opinion on Investigational Drugs. 29, 595-602;
- Alexander Sergeevich Ametov, Lyudmila Leonidovna Kamynina. (2011). Pharmalogical effects and results of clinical trials of the first incretinomimetic exenatide. Diabetes mellitus. 14, 63-68;
- Jee Sun Min, Seong Jun Jo, Sangyoung Lee, Duk Yeon Kim, Da Hyun Kim, et. al.. (2025). A Comprehensive Review on the Pharmacokinetics and Drug−Drug Interactions of Approved GLP-1 Receptor Agonists and a Dual GLP-1/GIP Receptor Agonist. DDDT. Volume 19, 3509-3537;
- Оземпик: больше, чем средство для похудения;
- Чумакова Г. А., Кузнецова Т. Ю., Дружилов М. А., Гриценко О. В. (2024). Метаболическое здоровье населения: современный взгляд на проблему и пути ее решения. Российский кардиологический журнал. 29, 7–15;
- Коварная стройность и безопасная полнота: метаболический синдром и сахарный диабет вне обычных границ индекса массы тела;
- Две стороны инкретинов: спасение от ожирения и новые угрозы;
- Changge Guan, Marcelo D. T. Torres, Sufen Li, Cesar de la Fuente-Nunez. (2025). Computational exploration of global venoms for antimicrobial discovery with Venomics artificial intelligence. Nat Commun. 16.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚





