Вижу цель, вижу препятствия: апатия, дофамин и не только
02 марта 2026
Вижу цель, вижу препятствия: апатия, дофамин и не только
- 2314
- 0
- 3
Рисунок в полном размере.
-
Авторы
-
Редакторы
-
Иллюстратор
Статья на конкурс «Био/Мол/Текст»: Состояние апатии знакомо многим: безразличие, подавленность и усталость иногда сопровождают человека в обычной жизни и становятся настоящей проблемой при многих заболеваниях и расстройствах. О том, что из себя представляют волевые усилия с биологической точки зрения, можно ли моделировать апатию на лабораторных грызунах и какие вещества потенциально могут улучшить нашу целенаправленную активность — в этой статье.
Конкурс «Био/Мол/Текст»-2025/2026
 Эта работа заняла первое место в номинации «Своя работа» конкурса «Био/Мол/Текст»-2025/2026.
Эта работа заняла первое место в номинации «Своя работа» конкурса «Био/Мол/Текст»-2025/2026.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Мотивация — это огонь изнутри. Если кто-то другой попытается зажечь этот огонь в вас, скорее всего, он будет гореть очень недолго
— Стивен Кови
Человек и целенаправленная активность
Жизнь — бесконечная работа невидимого механизма внутри мозга, определяющего, стоит начинаемое дело своих усилий или нет. Любое действие, перед совершением которого мы прикидываем соотношение усилий, которые необходимо совершить, и результатов, которые получим в итоге, называется целенаправленным [1]. В повседневности никто не обращает внимания на этот анализ (в англоязычной литературе — cost/benefit analysis), и нам сложно оценить его значение: все происходит автоматически и очень-очень быстро, буквально доли секунды. Но когда работа данного механизма нарушается, человеку становится очень тяжело жить полноценно. То, что раньше виделось нужным, интересным и желанным, кажется неподъемным и бессмысленным (например, хорошо подготовиться к экзамену по сложному предмету) [2].
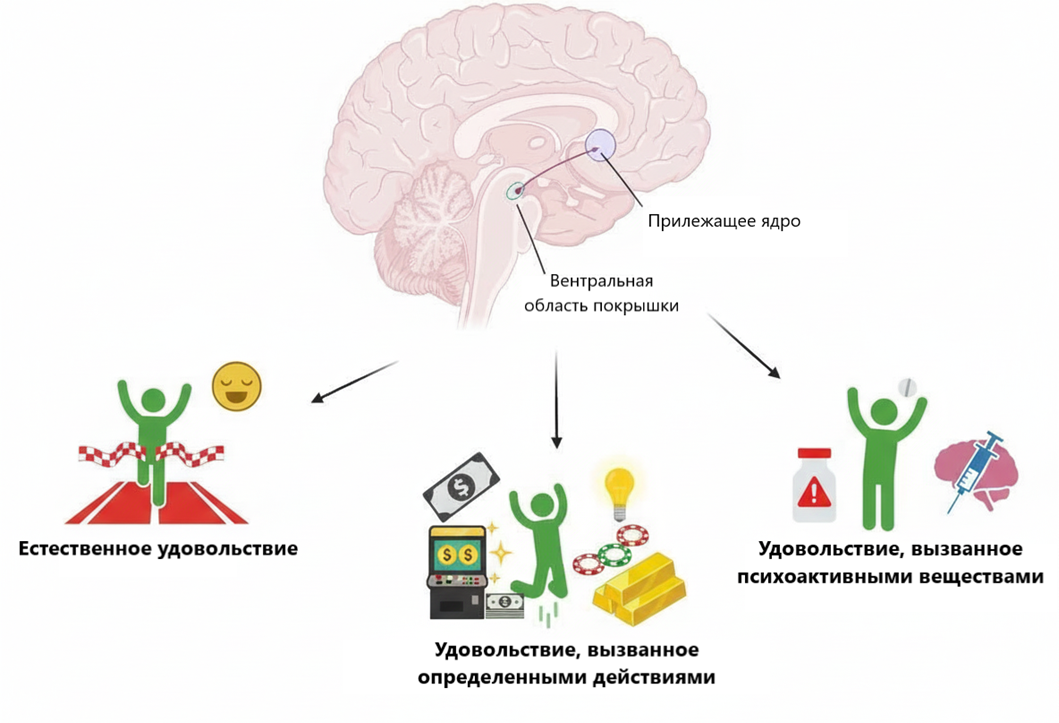
Рисунок 1. Система вознаграждения в общем виде.
адаптировано из [2]
Изменения контроля над целенаправленной деятельностью лежат в основе таких хорошо известных поведенческих нарушений, как апатия и компульсивность, которые как отдельные симптомы возникают при большом количестве психических и неврологических заболеваний. Да и не только их: так, например, апатия сопровождает множество соматических и даже инфекционных болезней, в том числе — является одной из важных составляющих постковидного синдрома [3]. Если говорить упрощенно, то апатию можно охарактеризовать как сдвиг целенаправленного поведения в сторону «минус»: репертуар целенаправленной деятельности обедняется, многие обычные виды активности становятся слишком «тяжелыми» для реализации [4]. Компульсивность немного сложнее: с одной стороны, это сдвиг в сторону плюс, с другой — нарушается способность переключаться от одной деятельности к другой [5], [6].
Ниже представлены основные заболевания, при которых нарушения целенаправленного поведения проявляются наиболее ярко.
Заболевания, при которых возникает апатия:
- Болезнь Альцгеймера (БА) [7];
- Лобно-височная деменция [7];
- Болезнь Гентингтона [7];
- Болезнь Паркинсона (БП) [7];
- Сосудистая деменция [7];
- Шизофрения [8];
- Шизофреноформное расстройство [8];
- Большое депрессивное расстройство (БДР) [8];
- Дистимическое расстройство [8];
- Шизотипическое расстройство личности [8];
- Расстройства пищевого поведения [8];
- Посттравматическое стрессовое расстройство (ПТСР) [8].
Заболевания, при которых возникает компульсивное поведение:
- Обсессивно-компульсивное расстройство (ОКР) [1];
- Генерализованное тревожное расстройство (ГТР) [1];
- Расстройства аутистического спектра [1];
- Расстройства пищевого поведения [1];
- Аддикции (от психоактивных веществ, в т.ч. алкоголя, игровая зависимость, гэмблинг) [1];
- Лобно-височная деменция [1];
- Трихотилломания [1];
- Синдром Туретта [1].
Хотя все эти болезни включают в себя множество нарушений, именно нарушения, связанные с целенаправленной активностью, часто выходят на первое место с практической точки зрения: они значительно усугубляют тяжесть заболеваний, повышают вероятность осложнений, снижают приверженность (или возможность достичь приверженности) лечению и, в конечном итоге, сильнее всего снижают качество жизни пациента [7], [8]. Наша работа посвящена вопросам изучения, моделирования и коррекции апатии, поэтому далее мы сосредоточимся именно на ней (но и другие нарушения тоже упомянем).
Дополнительной проблемой является вопрос определения апатии как клинического критерия: она бывает разной и встречается при разных расстройствах, которые иногда лечат разные врачи. Ее нельзя свести к прохождению одного опросника. Авторы по всему миру не сходятся во взглядах и применяют множество шкал для оценки апатии, и их можно понять [9].
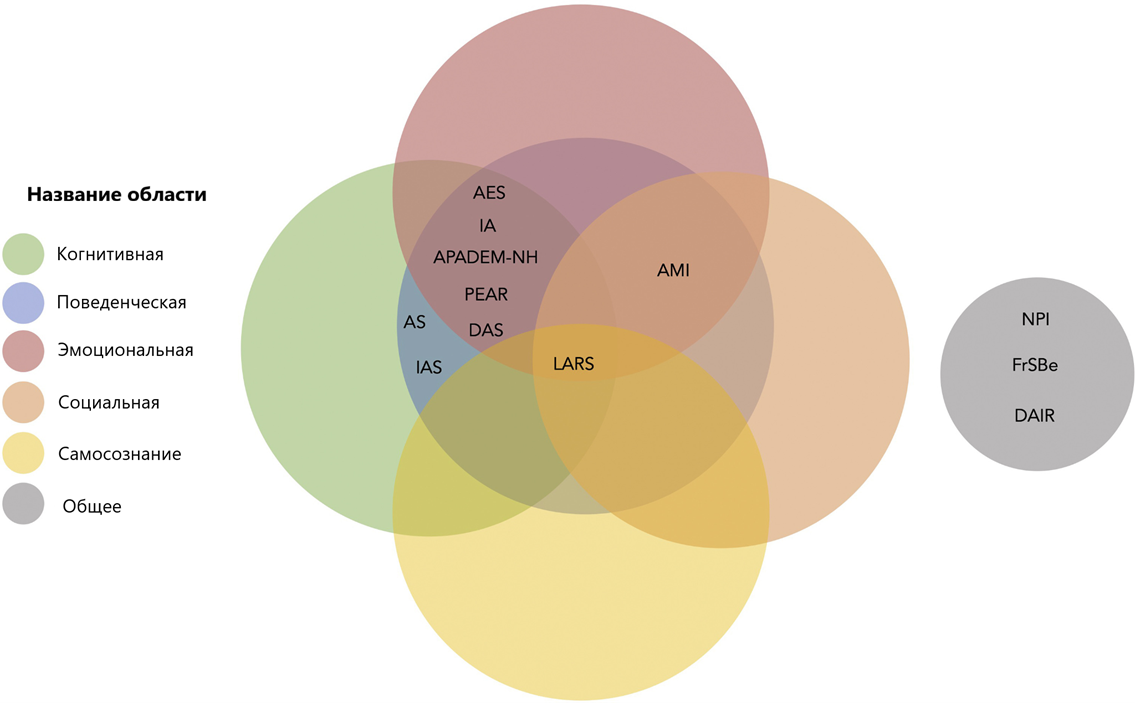
Рисунок 2. Основные шкалы для оценки апатии, применяемые в клинической практике. AS: apathy scale, IAS: irritability apathy scale, AES: apathy evaluation scale, IA: apathy inventory, APADEM-NH: apathy in institutionalised persons with dementia–nursing home, PEAR: Pearson environment apathy rating, LARS: Lille apathy rating scale, DAS: dimensional apathy scale, AMI: apathy motivation index, FrSBe: frontal system behaviour scale, DAS: dementia apathy rating scale, NPI: neuropsychiatric inventory.
адаптировано из [9]
Для того, чтобы прийти к какому-то общему знаменателю в этом море противоречий, в своей работе мы придерживаемся определения апатии, принятого Европейским конгрессом психиатров.
- Апатия —
- количественное снижение целенаправленной активности в поведенческом, когнитивном, эмоциональном или социальном измерениях по сравнению с предыдущим уровнем функционирования пациента в этих областях [4].
Рисунок 3. Нарушение cost-benefit анализа — основной субстрат апатии.
рисунок авторов
Это существенно меняет ситуацию: количественное снижение — то, что можно попробовать измерить, определить объективно и, в конечном итоге, смоделировать в эксперименте.
Так что же лежит в основе этих нарушений и можем ли мы помочь людям, столкнувшимся с ними? Для этого давайте на время отойдем от нозологий и попробуем посмотреть на целенаправленную активность с точки зрения фундаментальной нейробиологии.
Черный ящик для черных ящиков
Давайте сразу признаем одну неприятную вещь: поведение в целом и целенаправленная активность в частности до сих пор представляет собой своего рода «черный ящик» — мы можем наблюдать, как запускаются, изменяются, прекращаются поведенческие элементы, но какие процессы при этом происходят в головном мозге — загадка загадок и тайна тайн. Тем не менее, определенные успехи в понимании анатомических и нейрохимических коррелятов целенаправленного поведения все же есть. В этом мы и попробуем разобраться.
Как вы помните, целенаправленное поведение — процесс обмена усилий на награду, а основная задача нервных структур, участвующих в нем — определить, стоит ли награда необходимых усилий или нет [10]. На первый взгляд, процесс подготовки к целенаправленному действию прост и одномоментен: «о чем-то подумал, захотел и сделал». Внутри все немного сложнее и разнообразнее: от восприятия стимула до конечного действия следует несколько взаимосвязанных этапов, которые можно исследовать отдельно [11].
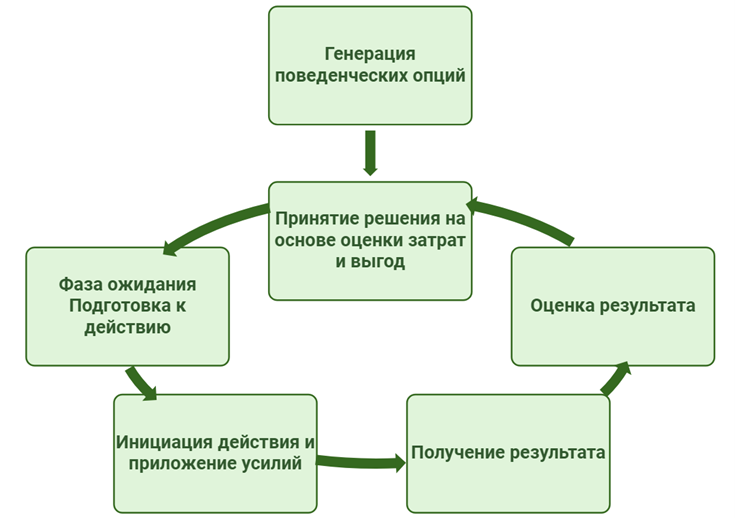
Рисунок 4. Общий план принятия решений, основанных на приложении усилий.
адаптировано из [7] с помощью Biorender
Вначале на основе «внутренней» и «внешней» информации генерируются возможные поведенческие опции. Затем они оцениваются и отбираются с учетом потенциальных выгод и затрат. Это и есть главный момент: здесь мозг оценивает и ценность награды, и затрачиваемые усилия, и вспоминает свой опыт похожих действий. Суммарно это и есть тот самый cost-benefit анализ. Во время фазы ожидания награды и подготовки к действию усиливается «мотивационное возбуждение», благодаря которому и происходит действие. Наконец, после получения результата происходит его оценка для корректировки поведения.
Как предполагают некоторые исследователи, разные участки мозга вовлечены в формирование разных элементов целенаправленного поведения и, соответственно, разных «типов» апатии. Дорсальная передняя поясная кора (dACC) и правый передний островок (AI) образуют особую «сеть выделения», которая контролирует переключение между вниманием и способствует мотивации и принятию решений (рис. 2, выделено зеленым) [12]. В каждом из этапов что-то может пойти не так, поэтому, несмотря на схожую внешнюю картину, с точки зрения нейробиологии апатия бывает разной. Более того, для некоторых заболеваний установлены наиболее характерные «места» поломки и соответствующие им виды апатии. Несложно догадаться, что это означает и возможность разных способов коррекции.
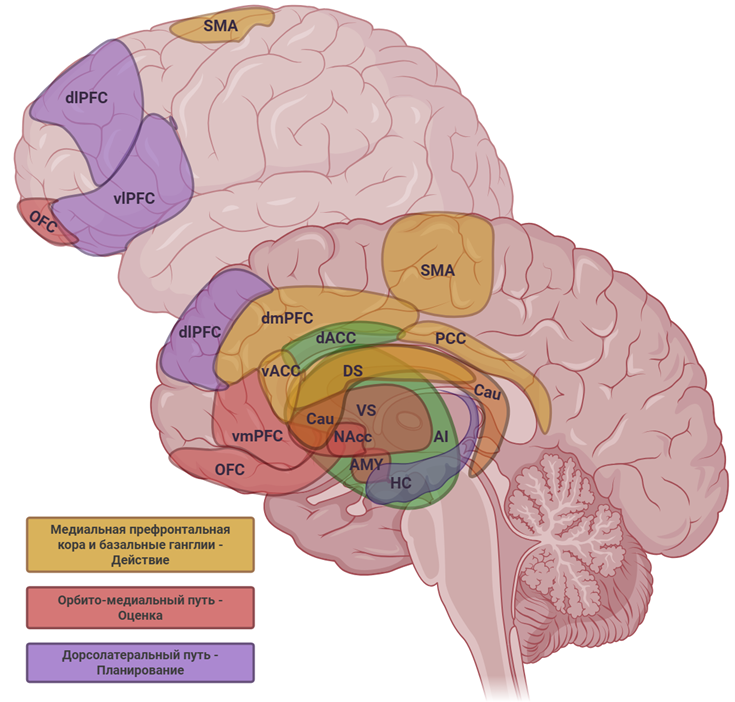
Рисунок 5. Основные области, задействованные в формировании апатии. SMA — дополнительная моторная область (supplementary motor area), dmPFC — дорсомедиальная префронтальная кора (dorsomedial prefrontal cortex), vACC — вентральная передняя поясная кора (ventral anterior cingulate cortex), DS — дорсальная часть полосатого тела (dorsal striatum), PCC — задняя поясная кора (posterior cingulate cortex), OFC — орбитофронтальная кора (orbitofrontal cortex), vmPFC — вентромедиальная префронтальная кора (ventromedial prefrontal cortex), NAcc — прилежащее ядро прозрачной перегородки (nucleus accumbens), AMY — миндалевидное тело (amygdala), VS — вентральная часть полосатого тела (ventral striatum), dlPFC — дорсолатеральная префронтальная кора (dorsolateral prefrontal cortex), vlPFC — вентролатеральная префронтальная кора (ventrolateral prefrontal cortex), HC — гиппокамп (hippocampus), dACC — дорсальная передняя поясная кора (dorsal anterior cingulate cortex), AI — передний островок (anterior insula).
адаптировано из [12] с помощью Biorender
Конечно же, все перечисленные структуры работают не в вакууме, они объединены друг с другом в сложную систему. И здесь мы можем чуть-чуть приоткрыть дофаминергическую составляющую [13] черного ящика целенаправленного поведения. Считается, что центральная роль в его регулировании лежит на аксонах от дофаминовых нейронов мезолимбического пути, тела которых расположены в вентральной области покрышки среднего мозга. Эти нейроны проецируются в прилежащее ядро прозрачной перегородки (на нее стоит обратить особое внимание), поясную извилину, энториальную кору, миндалину, обонятельный бугорок, прилежащее ядро, гиппокамп, парагиппокампальную извилину и другие структуры лимбической системы. Хорошо известно, что релиз дофамина может происходить в тоническом и фазовом режиме. Считается, что целенаправленное поведение, а вернее, cost/benefit анализ связан с фазовым выделением, при этом тонический релиз дофамина остается изученным не в полной мере [14].
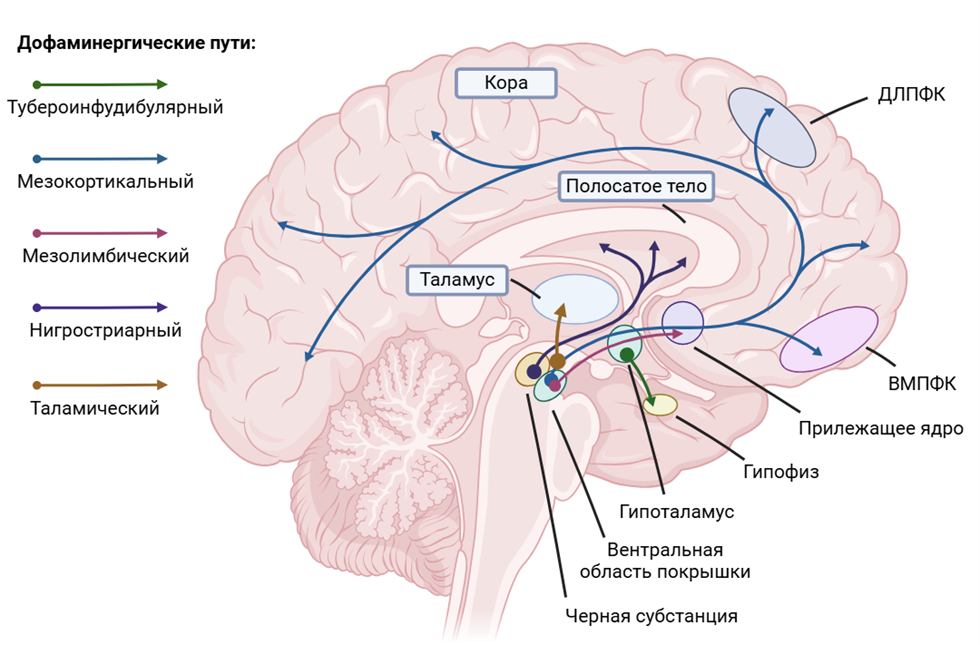
Рисунок 6. Дофаминергические проекции в головном мозге.
рисунок авторов, сделан с помощью Biorender
Впрочем, дофаминергическая составляющая в целом изучена недостаточно. Субпопуляции дофаминовых нейронов демонстрируют различные функциональные особенности [15], а значит, дофаминовая система может быть разбита на несколько субъединиц; точные границы между ними и полная характеристика разницы в их функциях требует дальнейшего уточнения. Также мало что понятно в подтипах дофаминовых рецепторах, ответственных за cost-benefit анализ.
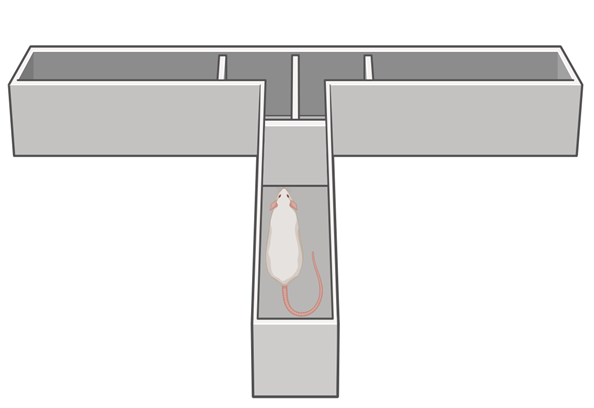
Лабиринты, педали и камеры
Для оценки целенаправленного поведения на лабораторных животных существует два основных подхода. Первый основан на выборе испытуемым между «низкозатратной» и «высокозатратной» поведенческими опциями, приводящими к получению разных по предпочтительности для животного подкреплений. Исторически первым методом данного типа является выбор между поеданием «обычного» корма, который находится в свободном доступе на полу оперантной камеры, и нажатиями на педаль за получение более предпочитаемой пищи [16]. Еще один метод, разработанный все той же группой исследователей, — модификация Т-образного лабиринта, где крысам необходимо выбирать между «низкозатратным» отсеком, содержащим «маленькое» подкрепление, и «высокозатратным», в котором для получения доступа к большему подкреплению необходимо преодолеть вертикальный барьер [17]. Другой пример — оперантная методика, основанная на выборе между двумя педалями: нажатие на первую («низкозатратную») позволяет получить 1 пищевую пеллету, на вторую («высокозатратную») — большее число пеллет, но за большее число нажатий [18].
Как нетрудно заметить, в данных методах «трудозатратные» поведенческие варианты связаны с большим количеством или лучшим качеством награды. Следовательно, влияние количества усилий не может быть исследовано отдельно от влияния характеристик подкрепления. Проще говоря, невозможно понять, почему животное начало выбирать более простой вариант реагирования: это может быть связано как со снижением способности прилагать усилия, так и с изменением восприятия (снижением ценности) награды.
Альтернативным подходом является использование режима подкрепления «возрастающее соотношение» (ВС), при котором число оперантных реакций, которое необходимо совершить испытуемому (соотношение реакции/подкрепление, далее — соотношение), увеличивается по той или иной закономерности. В отличие от методик выбора между высоко- и низкозатратными опциями, в данном случае количество и качество подкрепления остается одинаковым, а изменяется только количество необходимых усилий. По этой причине данный режим, вероятно, позволяет оценить влияние усилий наиболее прицельно и, соответственно, является более рациональным.
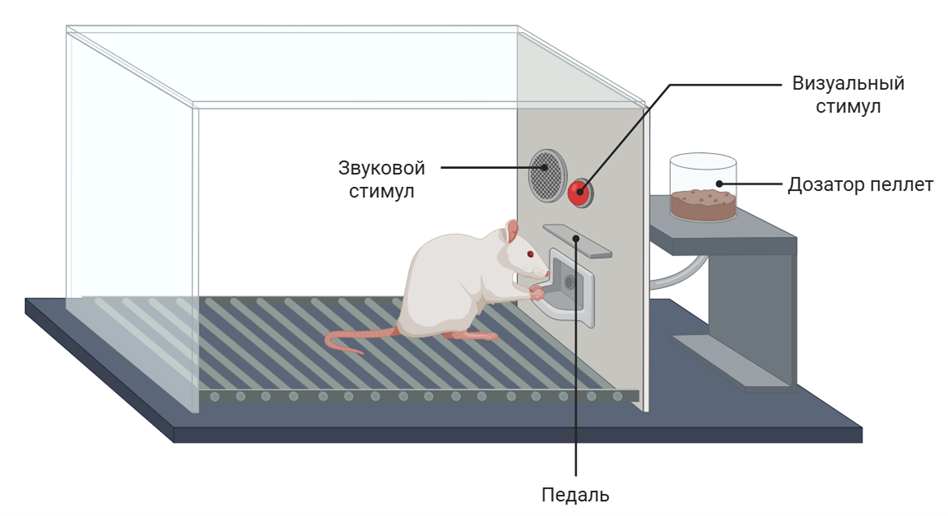
В своем исследовании мы используем именно режим «возрастающее соотношение» (ВС). Свои эксперименты мы проводим в оперантных камерах Скиннера для крыс. Это ящички, снабженные разными устройствами для предъявления животным различных стимулов и регистрации их поведения. В данном случае в качестве стимулов мы использовали автоматическую кормушку, каждый поворот приводил к тому, что в лотке появлялся маленький кусочек корма (пищевая пеллета), а также источник звука. Для регистрации поведения служит педалька, на которую крыса может нажимать, а также пара фотодатчиков, позволяющая фиксировать время, когда голова животного находится в лотке.
Обучение начинается с простого режима «Фиксированное соотношение» (ФС1): слегка голодная крыса, полная здорового энтузиазма относительно пищи, получает возможность нажимать на педаль и зарабатывать пищевые пеллеты. В этом режиме она получает пеллету за каждое нажатие. Когда животное обучилось навыку и получает 50 таких подкреплений за полчаса, задача становится чуть сложнее: за пеллету надо совершить не одно, а уже целых три нажатия (ФС3), а потом, аналогично, 5 (ФС5). Крысы сравнительно легко обучаются навыку нажатия, наши самцы «обычного» стока Wistar умудряются достичь критерия на ФС5 меньше, чем за неделю.
Настало время финального режима, «Возрастающее соотношение 3». На первый взгляд он мало чем отличается от ФС: чтобы получить пищу, крыса вновь должна жать на педаль. И вот животное нажало 3 раза, получило первую пеллету и собирается получить следующую. Жмет раз, другой, третий, но вместо ожидаемой пеллеты не получает ничего. Задача усложнилась: теперь для получения второй пеллеты надо нажать уже 6 раз, третьей — 9, четвертой — 12. Получается, задача усложняется в арифметической прогрессии, а вознаграждение остается таким же.

Рисунок 8. Общая схема экспериментов.
рисунок авторов
Можно провести аналогию с людьми: представим, что у нас нет денег, а за нажатие на кнопку большая машина дает нам 50 рублей. Если за эти 50 рублей нужно нажать на кнопку пару (или даже пару десятков) раз, большинство людей, вероятно, сделает это легко: по нужде, ради интереса или просто от скуки. Если же за эти пятьдесят рублей нужно нажать уже 500 раз, многие откажутся, а если несколько тысяч раз — нажимать будут единицы, а может быть, и никто. В какой-то момент испытуемый достигает «переломной точки», когда работать дальше на таких условиях он уже не готов. Это и есть основной (но не единственный) параметр, демонстрирующий работу cost-benefit анализа [19]. Примечательно, что аналогичный режим, хоть и в другом виде (и, конечно, без реальных денег) действительно используют на людях для исследования желания и способности прикладывать усилия, например, при психических расстройствах [20].
В экспериментах мы анализировали не только число подкреплений (количество полученных пеллет), но и более сложные аспекты, позволяющие оценить непосредственно «мотивацию» животного [21]. Основной из них — локальная частота оперантной реакции (ЛЧОР) — параметр, который рассчитывают по формуле (число необходимых нажатий/время, затраченные на получение подкрепления). Иными словами, это то, насколько быстро животное нажимает на педаль для получения каждого следующего подкрепления. Также мы анализировали параметры математической модели зависимости ЛЧОР от соотношений. Такие измерения позволяют взглянуть на поведение с разных сторон и лучше понять, на какие конкретно его элементы влияют те или иные условия и вещества [22].
| α | Оценка поощрительной силы подкрепления |
| δ | Оценка физической способности к совершению оперантных реакций |
| T0 | Информация о паузе после подкрепления (ППП) и ее динамике в зависимости от соотношения |
| k |
Как можно моделировать апатию?
Мы определились с методом, пора перейти от физиологического состояния к патологическому. Моделирование апатии [23] — достаточно сложный процесс. Нужно целенаправленно (простите за тавтологию) повлиять на целенаправленное поведение, при этом не подавить поведенческие реакции в целом. Как мы сможем оценить хоть какое-то поведение, если крыса будет неспособна нажимать на педаль или забрать корм из лотка?
Желательно не «выключать» какой-то из отделов мозга прицельно: все же мы хотим приблизиться к моделированию ситуации, происходящей в реальном мире, поэтому использование нейротоксинов [24] и хирургических операций, разрушающих нейроны, нам тоже не подходит. По схожей причине желательно не использовать генетически модифицированных животных: специальной модели апатии не существует, а линии, воспроизводящие различные болезни, помимо апато-подобных изменений имеют множество других нарушений и недостаточно универсальны [25]. Таким образом, для «синтетического» апато-подобного состояния нужно воздействие, с одной стороны, достаточно мощное, чтобы повлиять на волевые усилия, а с другой — достаточно тонкое, чтобы существенно не повлиять на остальные аспекты поведения. Как оказалось, средства такого воздействия существуют. Во-первых, это создание стрессовых условий [26]. Во-вторых, активация нейровоспаления [27], [28]. В-третьих, использование более современных избирательных препаратов, действующих на дофаминовую систему.
Наиболее чистым и популярным способом сдвинуть целенаправленное поведение в минус служит действие тетрабеназина, ингибитора везикулярного моноаминового транспортера 2-го типа (Vesicular Monoamine Transporter 2, VMAT2). Это трансмембранный белок, который перемещает моноаминовые нейромедиаторы (дофамин, норадреналин [29], серотонин [30] и гистамин) из цитозоля в везикулы. Таким образом, этот транспортер «обеспечивает» запас медиаторов для высвобождения в синаптическую щель. Если заблокировать VMAT2, их запас в везикулах начинает снижаться, а, следовательно, снижается и их релиз, а значит и действие на соответствующие рецепторы.
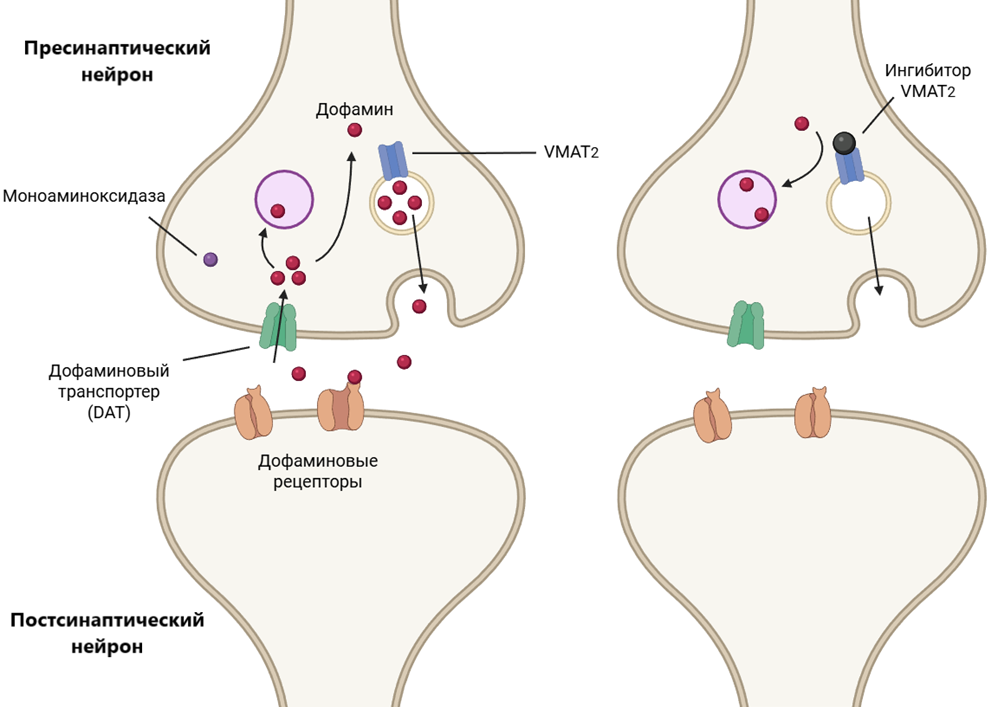
Рисунок 9. Влияние ингибиторов VMAT2 на нейротрансмиссию в дофаминовом синапсе.
адаптировано из [31] с помощью Biorender
- Тетрабеназин —
- лекарство, применяемое для лечения непроизвольных движений (гиперкинезов) при болезни Хантингтона [32], гемибаллизме, синдроме Туретта
Для начала мы хотели определить дозу тетрабеназина, которая будет специфически влиять на целенаправленное поведение. В малых дозах это вещество достаточно селективно подавляет целенаправленную деятельность и заставляет животных выбирать менее трудозатратные опции, практически не влияя на другие аспекты поведения [33], [34]. Помимо режима «Возрастающее соотношение», мы использовали ряд проверочных тестов (двигательная активность и оперантный режим фиксированное соотношение — фиксированный интервал) и выяснили, что в дозе 0,3 мг/кг тетрабеназин действительно угнетал активность только при увеличении количества требуемых усилий, не влияя на общую активность и способность выполнять действия. Это согласуется с общими представлениями об активности тетрабеназина: несмотря на влияние на транспорт моноаминов в целом, в низких концентрациях он селективен в отношении дофамина [35].
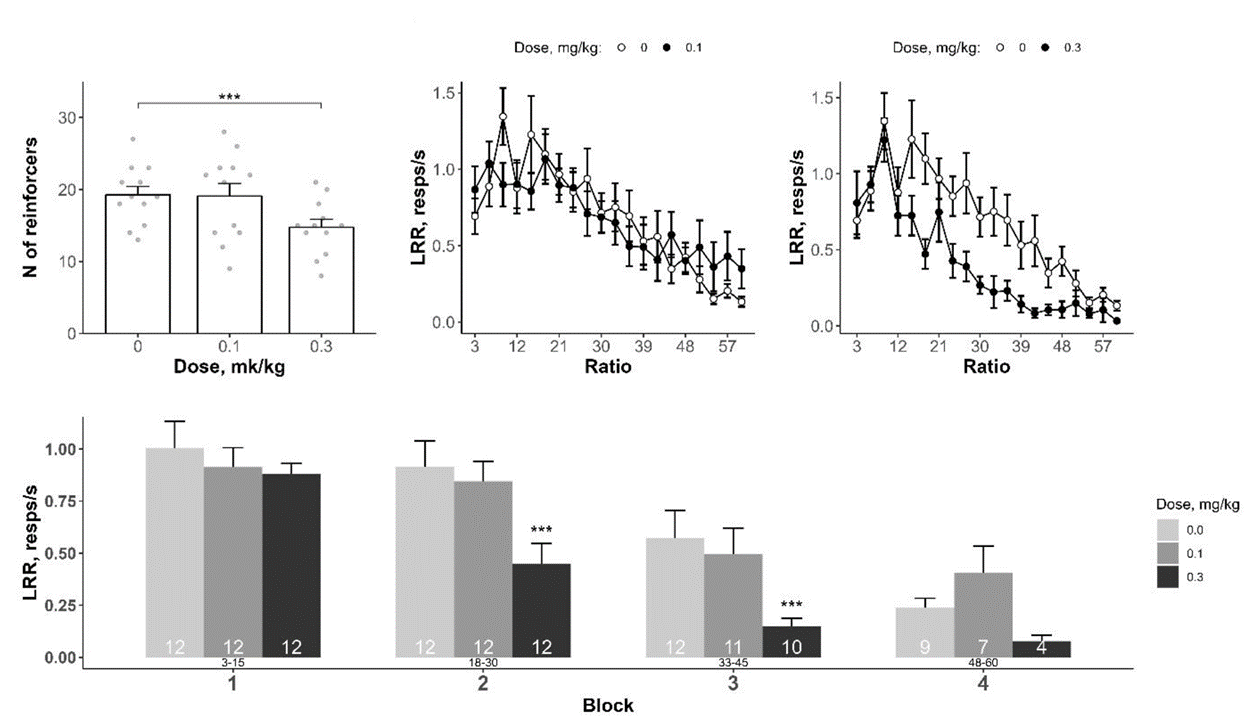
Рисунок 10. Подавление целенаправленного поведения тетрабеназином в режиме ВС3.
Дофамин и не только
Неважно, рассматриваем мы апатию как отдельный «трансдиагностический» феномен или как часть болезни, адекватного лечения для нее, несмотря на множество попыток, пока не разработано ни в каком виде [36], [37]. В клинической практике для снижения выраженности апатии используют препараты, применяемые для терапии основного заболевания: при болезни Паркинсона [38] — дофаминомиметики, при болезни Альцгеймера [39] — мемантин и ингибиторы ацетилхолинэстеразы, а при шизофрении — атипичные антипсихотики [40]. Но такой подход не учитывает особенности патогенеза апатии и имеет невысокую эффективность [41]. Особой проблемой являются депрессивные расстройства: во-первых, сами по себе они часто имеют апатические проявления, а во-вторых, некоторые часто используемые антидепрессанты, такие как селективные ингибиторы обратного захвата серотонина (СИОЗС), не только не устраняют, но и сами могут вызывать апатию у пациентов [42].
Выйти из нынешнего печального состояния можно, только лучше разобравшись в механизмах целенаправленного поведения, и таким образом выявить терапевтические мишени, на которые надо воздействовать, чтобы помочь пациентам.
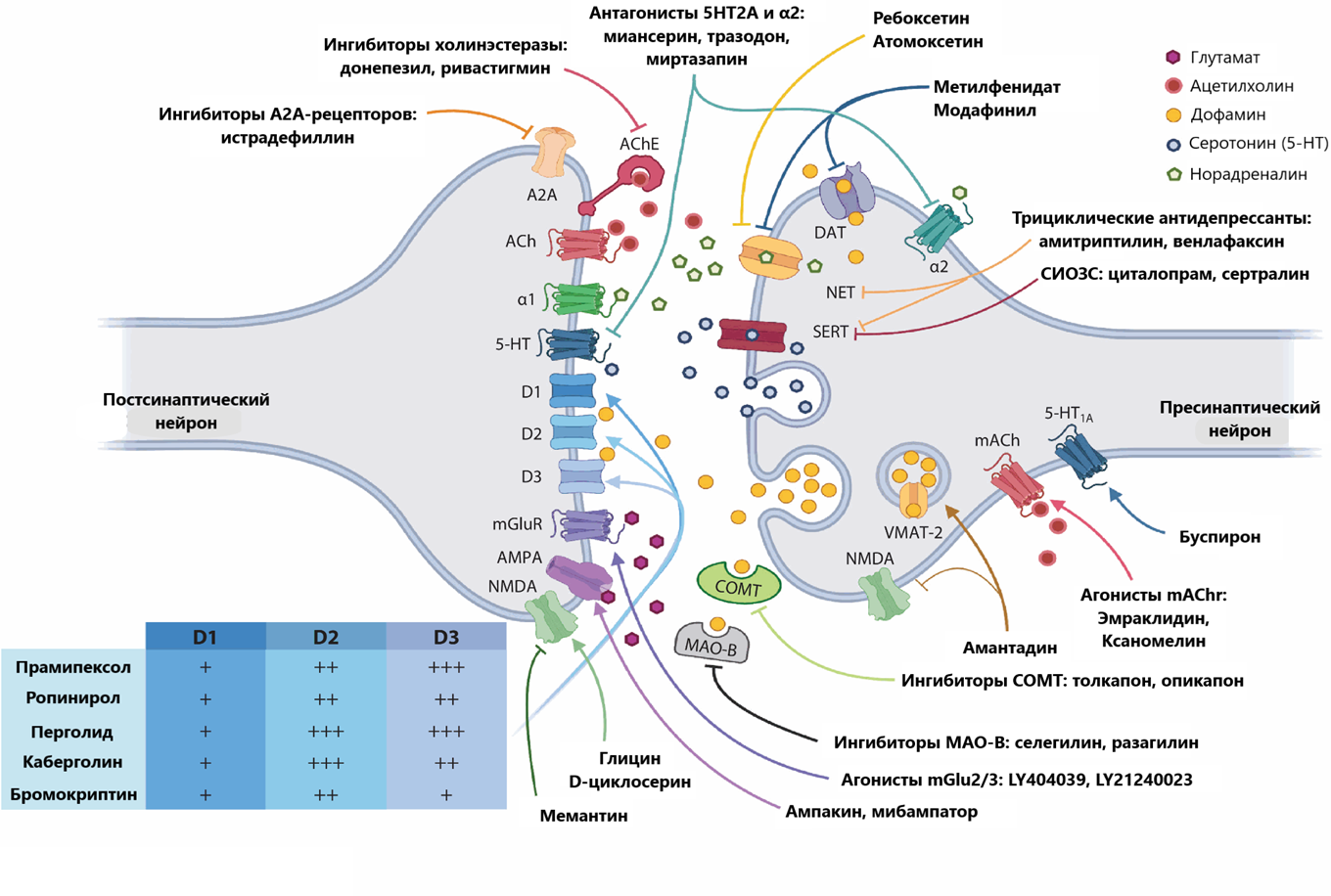
Рисунок 11. Препараты-кандидаты для лечения нарушений мотивации и мишени их действия. 5HT — серотонин, A2A — аденозиновый рецептор типа А2А, AChE — ацетилхолинэстераза, AMPA — ионотропный глутаматный рецептор типа AMPA (рецептор α-амино-3-гидрокси-5-метил-4-изоксазолпропионовой кислоты), COMT — катехол-О-метилтрансфераза, D (D1-D3) — дофаминовые рецепторы, DAT — дофаминовый транспортер, (m)ACh — мускариновый ацетилхолиновый рецептор (м-холинорецептор), MAO-B — моноаминоксидаза типа B, NET — норадреналиновый транспортер, mGluR — метаботропный глутаматный рецептор, SERT — серотониновый транспортер, SSRI — селективные ингибиторы обратного захвата серотонина (СИОЗС), SNRI — селективные ингибиторы обратного захвата серотонина и норадреналина (СИОЗСН), TCA — трициклические антидепрессанты, VMAT — везикулярный моноаминовый транспортер.
адаптировано из [37]
Как вы помните, дофаминовая нейропередача очень тесно связана с регулированием целенаправленного поведения. Среди многочисленных фармакологических мишеней в дофаминовом синапсе с нашей точки зрения наиболее интересным представляется дофаминовый транспортер (ДАТ). Это ключевой белок, который контролирует уровень внеклеточного дофамина за счет транспортировки его обратно в дофаминовый нейрон. Соответственно, выключение ДАТ приведет к пролонгации и повышению амплитуды физиологического дофаминового сигнала.
В фармакологии есть большая группа веществ, которые блокируют работу этого белка. Это вещества из группы психостимуляторов. Но не все так просто: во-первых, большинство из психостимуляторов запрещены из-за выраженного аддиктивного потенциала и других нежелательных, в первую очередь, кардиоваскулярных эффектов, связанных с ингибированием очень похожего на ДАТ норадреналинового транспортера. В последние годы в этом кажущемся безвыходным туннеле, однако, появился свет. Во-первых, уже созданы довольно селективные ингибиторы ДАТ [43], которые практически не влияют на работу норадреналинового транспортера, а, во-вторых, было показано, что ингибировать ДАТ можно по-разному. Выделяют группу «типичных» ингибиторов: такие вещества (амфетамин, кокаин) обладают высоким аддиктивным потенциалом и стабилизируют ДАТ в outward-facing (участок связывания дофамина находится снаружи клетки) «открытом» конформационном состоянии. Вторая группа — «атипичные» ингибиторы характеризуются низким или даже практически отсутствующим аддиктивным потенциалом. Вещества данной группы взаимодействуют с дофаминовым транспортером иными способами, например, преимущественно с inward-facing конформацией. К ним относится, в частности, модафинил, применяемый в США для стимулирования бодрствования и лечения чрезмерной дневной сонливости, связанной с нарколепсией, синдромом обструктивного апноэ сна или расстройством сна при сменной работе. В рамках этой парадигмы мы протестировали два атипичных ингибитора ДАТ: один из них, CE-123, пока не вышел за пределы экспериментальной фармакологии, а вот второй, фонтурацетам, активно и давно используют в клинической практике.
Мы попробовали «вылечить» апатию с помощью выбранных нами веществ. Мы обнаружили, что введение CE-123 способно восстанавливать целенаправленную активность, нарушенную из-за истощения запасов моноаминов. Под действием СЕ-123 увеличивалась количество получаемых подкреплений и повышалась локальная частота оперантных реакций. Получается, животные с апатоподобными нарушениями становились готовыми работать больше и усерднее, но при этом на интактных, «нормальных» крыс, которым не вводили тетрабеназин, этот эффект не распространялся [44].
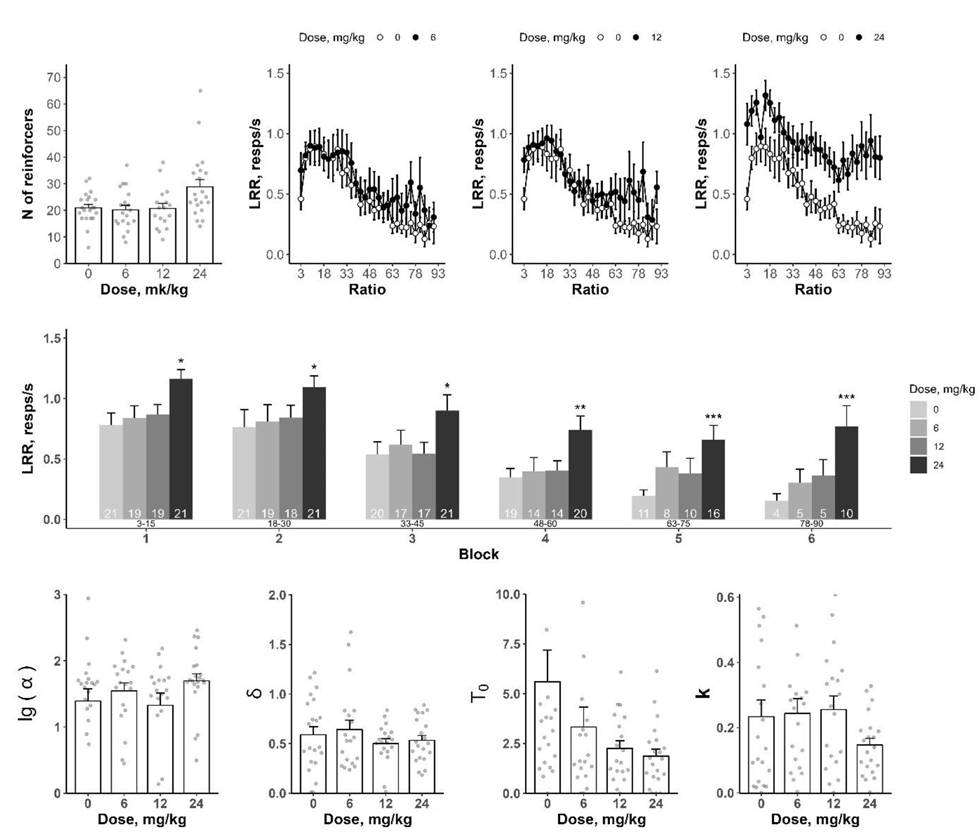
Рисунок 12. Эффекты CE-123 на поведение животных, находящихся под действием тетрабеназина.
Несмотря на то, что фонтурацетам действует аналогичным образом на ту же мишень, с ним ситуация обстоит по-другому. Он повышает количество реакций и параметры локальной чистоты как у интактных, так и у «апатичных» животных, при этом эффект на ЛЧОР проявляется не сразу: он возникает на большем числе подкреплений, то есть тогда, когда требуется приложить больше усилий. Параметры математической модели при этом меняются по-разному: альфа (α), основной мотивационный параметр, отражающий ценность награды, возрастает только при введении фонтурацетама интактным животным. Каппа (k), коэффициент возрастания паузы после получения подкрепления, дозозависимо снижается как у интактных крыс, так и у животных под действием тетрабеназина.
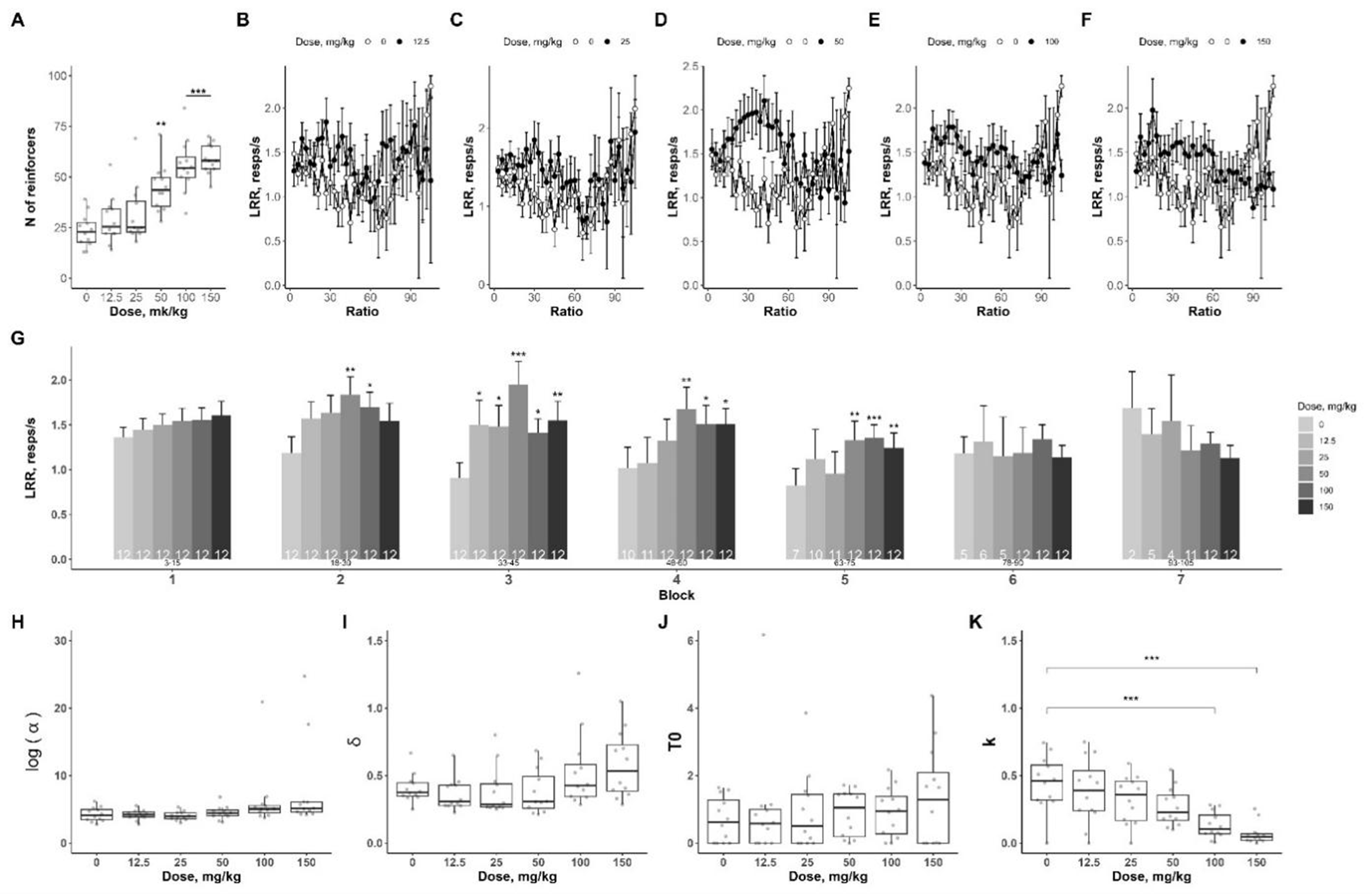
Рисунок 13. Эффекты фонтурацетама на поведение животных, находящихся под действием тетрабеназина.
рисунок авторов
Для воздействия на целенаправленное поведение можно использовать и другой подход, в чем-то может чуть более изощренный. Можно попробовать воздействовать на те же кортико-стриато-паллидо-таламо-кортикальные петли, на которые влияют ингибиторы ДАТ, но немного на другом уровне: попробовав убрать ингибирующее влияние глутаматного гиперпрямого пути (аксоны пирамидных нейронов) на уровне бледного шара. В рамках этого подхода мы протестировали влияние ингибитора глутаматных рецепторов NMDA-подтипа MK-801 [45]. NMDA-антагонисты, как и глутаматный сигналинг в целом, достаточно интересны. Например, кетамин, использующийся с 60-х годов прошлого века как общий анестетик, относительно недавно получил одобрение как антидепрессант и показан в США при терапевтически-резистентной депрессии [46].
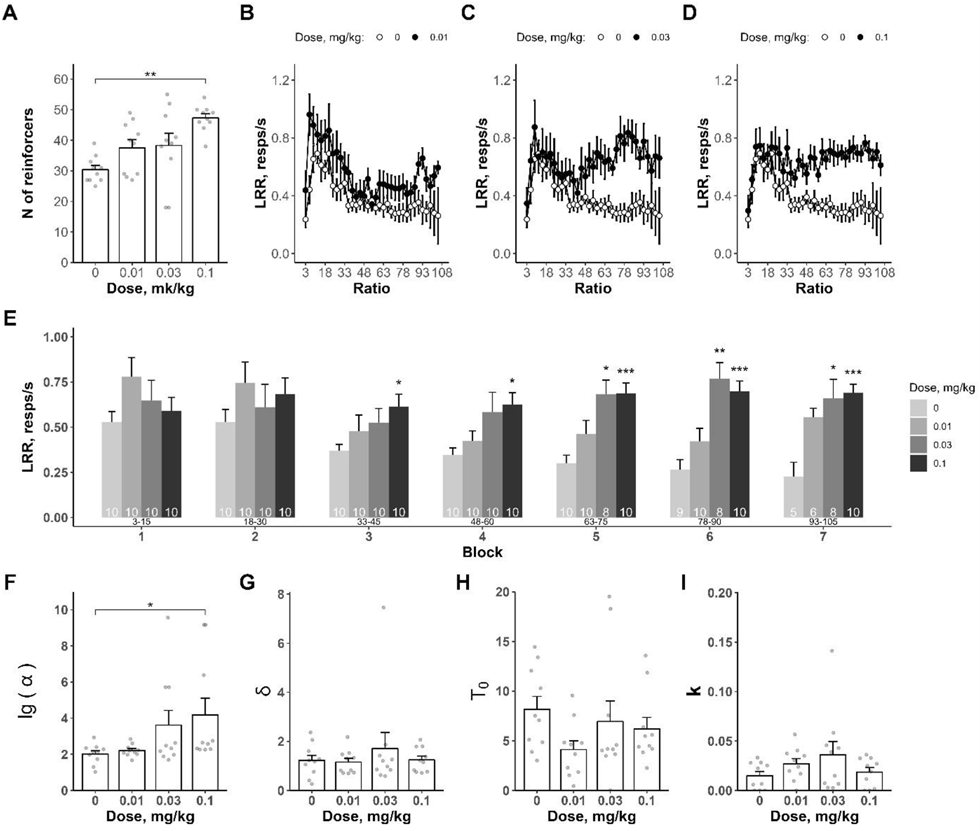
Рисунок 14. Эффекты MK-801 на поведение животных, находящихся под действием тетрабеназина.
Высокоаффинный канальный блокатор NMDA-рецепторов MK-801 показал результаты, частично похожие и на CE-123, и на фонтурацетам: у интактных животных он увеличивал число подкреплений и частоту реакции, а у «апатичных» — еще и параметр «специфической активации». При этом на мотивационное возбуждение все вещества действовали по-разному: CE-123 усиливал его только вначале, когда для вознаграждения требовалось немного нажатий, а MK-801 и фонтурацетам помогали выполнять более трудозатратные задачи. В зависимости от особенностей апатии и те, и другие улучшения могут быть более полезны.
Если с блокаторами ДАТ ситуация относительно более понятная, вмешательства в глутаматергический сигналинг выглядят более запутанными: NMDA рецепторы способны влиять непосредственно и на дофаминовую систему, а могут идти в обход нее. К предполагаемым вариантам не-дофаминергического влияния относятся влияние NMDA-рецепторы ГАМКергических интернейронов [47], а также подавление действия самих глутаматных путей, которые регулируют взаимодействие между корой и базальными ганглиями (например, гиперпрямого пути между лобной корой и субталамическим ядром) [48], [49].
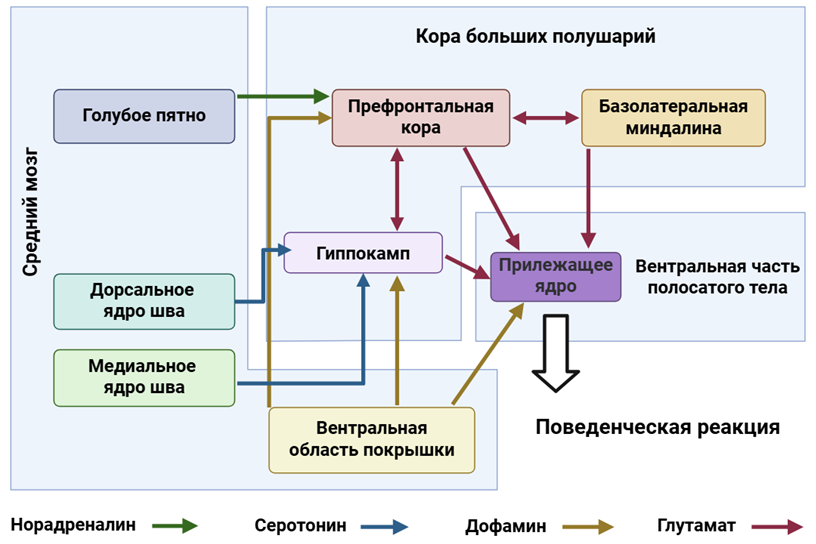
Рисунок 15. Взаимосвязь основных структур мозга, регулирующих поведение.
адаптировано по [49] с помощью BioRender
Перспективы и оставшиеся проблемы
Трудно сказать, можно ли будет однажды придумать «таблетку от апатии». Потенциальные антиапатические средства могут быть найдены среди новых молекул или получиться путем перепрофилирования уже имеющихся, могут иметь прямой или опосредованный дофаминергический или вообще не-дофаминергический механизм. Возможно, те вещества, которые использовали мы, смогут претендовать на роль «универсальных» агентов или же использоваться в терапии только некоторых отдельных заболеваний, а возможно — не дойдут до клиники в целом: переход «от лаборатории» к «постели больного» всегда сложен и неочевиден.
Конечно же, результаты, представленные в этой статье, являются лишь малой частью нашей работы с целенаправленной активностью. За годы экспериментов с обычными и генно-модифицированными животными накопилась большая «библиотека» веществ, которые не оказывают эффекта вообще, подавляют поведение целиком или парадоксальным образом меняют паттерны реагирования так, как от них не ждали. Здесь и ингибиторы фосфодиэстераз, и TAAR-агонисты, и селективные ингибиторы обратного захвата серотонина, и опиоидные антагонисты [50], и многие-многие другие.
С одной стороны, это прибавляет нам уверенности в положительных результатах: они обоснованы и не являются случайной находкой. С другой, это показывает, как мало человек пока еще знает о механизмах работы мозга. Сначала какие-то функции в нашем представлении укладывались в отдельные анатомические области, затем — в нервные пути, а что будет дальше — еще предстоит узнать.
Перед нейробиологией, трансляционной медициной и психофармакологией стоит еще много нерешенных задач.
Литература
- Trevor W. Robbins, Paula Banca, David Belin. (2024). From compulsivity to compulsion: the neural basis of compulsive disorders. Nat. Rev. Neurosci.. 25, 313-333;
- Стал С. М. Основы психофармакологии. Теория и практика. — М.: «ГЭОТАР-Медиа», 2023. — 656 с.;
- Marco Calabria, Carmen García-Sánchez, Nicholas Grunden, Catalina Pons, Juan Antonio Arroyo, et. al.. (2022). Post-COVID-19 fatigue: the contribution of cognitive and neuropsychiatric symptoms. J Neurol. 269, 3990-3999;
- P. Robert, K.L. Lanctôt, L. Agüera-Ortiz, P. Aalten, F. Bremond, et. al.. (2018). Is it time to revise the diagnostic criteria for apathy in brain disorders? The 2018 international consensus group. Eur. psychiatr.. 54, 71-76;
- Claire M. Gillan, Martina Papmeyer, Sharon Morein-Zamir, Barbara J. Sahakian, Naomi A. Fineberg, et. al.. (2011). Disruption in the Balance Between Goal-Directed Behavior and Habit Learning in Obsessive-Compulsive Disorder. AJP. 168, 718-726;
- Quanhao Yu, Feng Gao, Chuting Li, Jie Xia, Yanyuan Cao, et. al.. (2024). Compulsion is associated with impaired goal-directed and habitual learning and responding in obsessive-compulsive disorder. International Journal of Clinical and Health Psychology. 24, 100531;
- Masud Husain, Jonathan P. Roiser. (2018). Neuroscience of apathy and anhedonia: a transdiagnostic approach. Nat Rev Neurosci. 19, 470-484;
- Diana E. Clarke, Jean Y. Ko, Emily A. Kuhl, Robert van Reekum, Rocio Salvador, Robert S. Marin. (2011). Are the available apathy measures reliable and valid? A review of the psychometric evidence. Journal of Psychosomatic Research. 70, 73-97;
- Shannon S. Dickson, Masud Husain. (2022). Are there distinct dimensions of apathy? The argument for reappraisal. Cortex. 149, 246-256;
- John D. Salamone. (2009). Dopamine, Behavioral Economics, and Effort. Front. Behav. Neurosci.. 3;
- Andre Der-Avakian, Samuel A. Barnes, Athina Markou, Diego A. Pizzagalli. (2015). Translational Assessment of Reward and Motivational Deficits in Psychiatric Disorders. Current Topics in Behavioral Neurosciences. 231-262;
- David C. Steffens, Mario Fahed, Kevin J. Manning, Lihong Wang. (2022). The neurobiology of apathy in depression and neurocognitive impairment in older adults: a review of epidemiological, clinical, neuropsychological and biological research. Transl Psychiatry. 12;
- Дофаминовые болезни;
- Mark E. Walton, Sebastien Bouret. (2019). What Is the Relationship between Dopamine and Effort?. Trends in Neurosciences. 42, 79-91;
- Masayuki Matsumoto, Okihide Hikosaka. (2009). Two types of dopamine neuron distinctly convey positive and negative motivational signals. Nature. 459, 837-841;
- J. D. Salamone, R. E. Steinpreis, L. D. McCullough, P. Smith, D. Grebel, K. Mahan. (1991). Haloperidol and nucleus accumbens dopamine depletion suppress lever pressing for food but increase free food consumption in a novel food choice procedure. Psychopharmacology. 104, 515-521;
- John D. Salamone, Michael S. Cousins, Sherri Bucher. (1994). Anhedonia or anergia? Effects of haloperidol and nucleus accumbens dopamine depletion on instrumental response selection in a T-maze cost/benefit procedure. Behavioural Brain Research. 65, 221-229;
- Stan B Floresco, Maric T L Tse, Sarvin Ghods-Sharifi. (2008). Dopaminergic and Glutamatergic Regulation of Effort- and Delay-Based Decision Making. Neuropsychopharmacol. 33, 1966-1979;
- William Hodos. (1961). Progressive Ratio as a Measure of Reward Strength. Science. 134, 943-944;
- Gregory P. Strauss, Kayla M. Whearty, Lindsay F. Morra, Sara K. Sullivan, Kathryn L. Ossenfort, Katherine H. Frost. (2016). Avolition in schizophrenia is associated with reduced willingness to expend effort for reward on a Progressive Ratio task. Schizophrenia Research. 170, 198-204;
- Campbell Le Heron, Clay B Holroyd, John Salamone, Masud Husain. (2019). Brain mechanisms underlying apathy. J Neurol Neurosurg Psychiatry. 90, 302-312;
- C. M. Bradshaw, P. R. Killeen. (2012). A theory of behaviour on progressive ratio schedules, with applications in behavioural pharmacology. Psychopharmacology. 222, 549-564;
- Трансляционная психиатрия — как моделировать психические расстройства на животных?;
- John D. Salamone, Pamela A. Kurth, Louise D. McCullough, Jonathan D. Sokolowski, Michael S. Cousins. (1993). The role of brain dopamine in response initiation: effects of haloperidol and regionally specific dopamine depletions on the local rate of instrumental responding. Brain Research. 628, 218-226;
- Rachel Keszycki, Guadalupe Rodriguez, Jeffrey T. Dunn, Andrea Locci, Hector Orellana, et. al.. (2023). Characterization of apathy-like behaviors in the 5xFAD mouse model of Alzheimer’s disease. Neurobiology of Aging. 126, 113-122;
- Andrew Dieterich, Tonia Liu, Benjamin Adam Samuels. (2021). Chronic non-discriminatory social defeat stress reduces effort-related motivated behaviors in male and female mice. Transl Psychiatry. 11;
- Samantha E. Yohn, Yumna Arif, Allison Haley, Guiseppe Tripodi, Younis Baqi, et. al.. (2016). Effort-related motivational effects of the pro-inflammatory cytokine interleukin-6: pharmacological and neurochemical characterization. Psychopharmacology. 233, 3575-3586;
- Eric J. Nunes, Patrick A. Randall, Alexavier Estrada, Brian Epling, Evan E. Hart, et. al.. (2014). Effort-related motivational effects of the pro-inflammatory cytokine interleukin 1-beta: studies with the concurrent fixed ratio 5/ chow feeding choice task. Psychopharmacology. 231, 727-736;
- Тайны голубого пятна;
- Серотониновые сети;
- Joseph Jankovic. (2017). Progress in Parkinson disease and other movement disorders. Nat Rev Neurol. 13, 76-78;
- Как спасти Тринадцатую? (Перспективы лечения болезни Хантингтона);
- Patrick A. Randall, Christie A. Lee, Eric J. Nunes, Samantha E. Yohn, Victoria Nowak, et. al.. (2014). The VMAT-2 Inhibitor Tetrabenazine Affects Effort-Related Decision Making in a Progressive Ratio/Chow Feeding Choice Task: Reversal with Antidepressant Drugs. PLoS ONE. 9, e99320;
- Jen-Hau Yang, Rose E. Presby, Renee A. Rotolo, Taina Quiles, Kevin Okifo, et. al.. (2020). The dopamine depleting agent tetrabenazine alters effort-related decision making as assessed by mouse touchscreen procedures. Psychopharmacology. 237, 2845-2854;
- Douglas J. Pettibone, James A. Totaro, A.Barbara Pflueger. (1984). Tetrabenazine-induced depletion of brain monoamines: Characterization and interaction with selected antidepressants. European Journal of Pharmacology. 102, 425-430;
- Moyra E. Mortby, Lawrence Adler, Luis Agüera-Ortiz, Daniel R. Bateman, Henry Brodaty, et. al.. (2022). Apathy as a Treatment Target in Alzheimer's Disease: Implications for Clinical Trials. The American Journal of Geriatric Psychiatry. 30, 119-147;
- Harry Costello, Masud Husain, Jonathan P. Roiser. (2024). Apathy and Motivation: Biological Basis and Drug Treatment. Annu. Rev. Pharmacol. Toxicol.. 64, 313-338;
- Лечение болезни Паркинсона нейротрофическими факторами: есть ли свет в конце туннеля?;
- На руинах памяти: настоящее и будущее болезни Альцгеймера;
- Junko Ishizaki, Masaru Mimura. (2011). Dysthymia and Apathy: Diagnosis and Treatment. Depression Research and Treatment. 2011, 1-7;
- Аведисова А. С. (2018). Эффективность фармакологических подходов к терапии синдрома апатии при деменции. Журнал неврологии и психиатрии им. C.C. Корсакова. 118, 126–133;
- Vasilios G. Masdrakis, Manolis Markianos, David S. Baldwin. (2023). Apathy associated with antidepressant drugs: a systematic review. Acta Neuropsychiatr.. 35, 189-204;
- James R. Docherty, Hadeel A. Alsufyani. (2021). Pharmacology of Drugs Used as Stimulants. The Journal of Clinical Pharma. 61;
- Artem Savchenko, Salim Tarchokov, Olga Dravolina, Jana Lubec, Gert Lubec, Ilya Sukhanov. (2025). Reversal of the motivational effects of tetrabenazine by NMDA receptor blockade. Neuropharmacology. 266, 110277;
- Очень нервное возбуждение;
- John H. Krystal, Ege T. Kavalali, Lisa M. Monteggia. (2024). Ketamine and rapid antidepressant action: new treatments and novel synaptic signaling mechanisms. Neuropsychopharmacol.. 49, 41-50;
- Спокоен как GABA;
- Daisuke Koketsu, Satomi Chiken, Tatsuhiro Hisatsune, Shigehiro Miyachi, Atsushi Nambu. (2021). Elimination of the Cortico-Subthalamic Hyperdirect Pathway Induces Motor Hyperactivity in Mice. J. Neurosci.. 41, 5502-5510;
- Hiram Tendilla-Beltrán, Luis Enrique Arroyo-García, Gonzalo Flores. (2022). Amphetamine and the Biology of Neuronal Morphology. Handbook of Substance Misuse and Addictions. 1-24;
- Идеальный опиоид, или Как избавиться от Дамоклова меча.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚