
Хит-парад научных достижений. Биология и биомедицина в 2017 году
31 декабря 2017
Хит-парад научных достижений. Биология и биомедицина в 2017 году
- 4189
- 0
- 8
Эта по-ёлочному разноцветная картинка как бы говорит нам, что 2017 год был удивительно богат на прорывы в онко- и генотерапии.
-
Автор
-
Редакторы
Темы
В предпраздничной суете «Биомолекула» не может просто так взять и не подвести научные итоги уходящего года. В 2017-м завершил свою миссию легендарный зонд «Кассини», бушевали страсти вокруг глобального потепления и политических решений президента США, вздымались гравитационные волны... а также волна обвинений в домогательствах, которой, увы, не удалось избежать и ряду крупных университетов. Однако, разумеется, нас прежде всего интересуют биология и медицина — чем они впечатлили мир в этом году? С целью выделить самое важное, обратимся к экспертам крупнейших научных изданий — Nаture и Science, — а ради полноты картины учтем мнение мировой читательской публики, запечатленное в рейтинге «Альтметрики».
Почетные места в топах-2017 как Nature, так и Science, ожидаемо заняли достижения в области лечения рака, а также прорывы в генотерапии и генокоррекции, образно обозначенных авторами Nature как «золотое дно генетики» (genetics bonanza). Кстати, в этот вторник о научных итогах года уже говорили в «Науке на завтрак», которую мы также рекомендуем посмотреть.
Победы в онковойнах
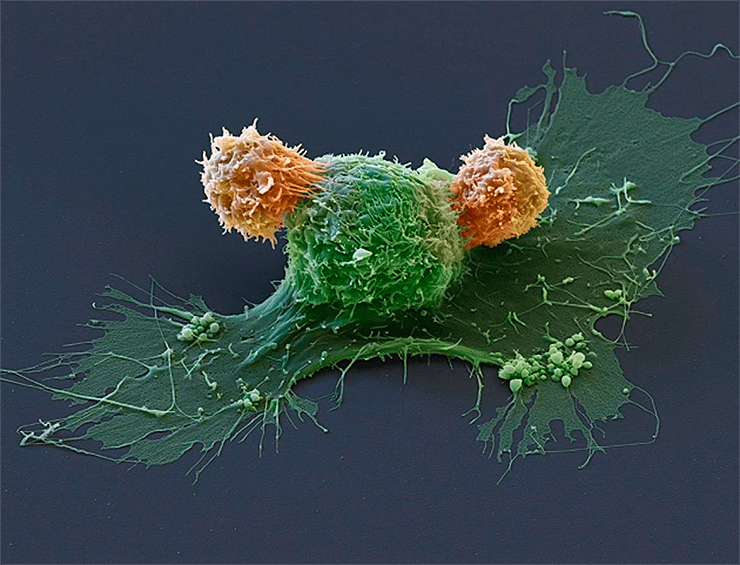
CAR-T лимфоциты (показаны оранжевым), видимо, в ближайшем будущем станут одним из самых продвинутых способов лечения рака.
В мае 2017 года Управление по контролю качества пищевых продуктов и лекарственных средств США (FDA) одобрило использование препарата пембролизумаб для лечения тех форм рака, которые вызваны нарушениями системы репарации неправильно спаренных оснований ДНК [1–3]. Как показали исследования, пембролизумаб особенно эффективен в отношении таких новообразований [4]. Это означает, что в основу терапии рака впервые легла не столько локализация опухоли, сколько ее генетическая природа.
Известно, что раковая опухоль способна обманывать иммунную систему, используя специальные молекулы, призванные подавлять иммунный ответ [5]. Один из способов такого подавления заключается в связывании этих молекул с рецептором PD-1 на поверхности цитотоксических T-лимфоцитов, что приводит к гибели последних. Пембролизумаб — это антитело к рецептору PD-1. Связываясь с ним, он защищает клетки-киллеры и позволяет им эффективно расправляться с опухолевыми клетками. Однако если рак вызван мутациями в системе репарации неправильно спаренных оснований ДНК, эффект лечения значительно возрастает. По-видимому, это связано с многочисленными мутациями в антигенах таких раковых клеток, в результате чего «пробужденный» пембролизумабом иммунитет уничтожает их гораздо активнее [6].
В этом году разрешение на клиническое использование получил и другой, более сложный и тонкий способ лечения рака [7]. Он основывается на генной инженерии с использованием собственных иммунных клеток пациента. Речь идет о создании химерных антигенных рецепторов Т-клеток (CAR-T) [8]. В основе этой технологии —модификация генов, кодирующих рецепторы клеток-киллеров, так, чтобы они распознавали раковые клетки конкретного пациента [9]. И хотя этот способ воздействия на организм чреват тяжелыми побочными эффектами [10], последние исследования сообщают о том, что польза терапии всё-таки превышает ее риски. Пока на рынок выведены два подобных препарата, предназначенные для лечения лимфопролиферативных заболеваний [11].
И снова CRISPR!
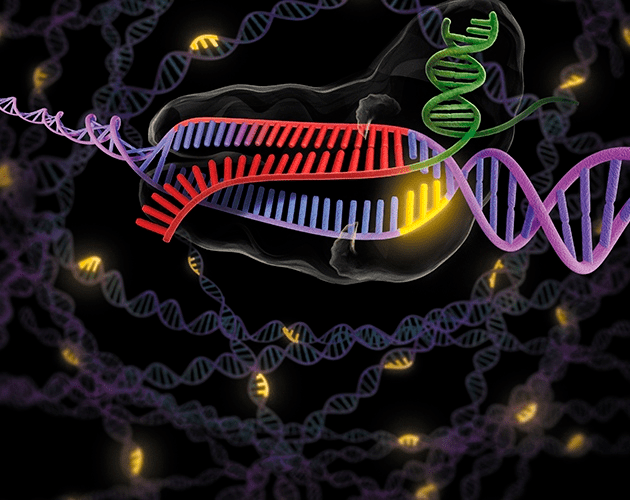
Исследователи во всем мире учатся использовать систему CRISPR-Cas9 как «генетические ножницы».
Прежде всего, если вам аббревиатура CRISPR-Cas9 знакома лишь смутно, почитайте соответствующий раздел на «Биомолекуле», в котором есть и подробные обзоры, и краткие новости, и инфографика, и захватывающие истории. Оно того стоит!
В этом году на горизонте отчетливо замаячили перспективы клинического применения популярной системы CRISPR-Cas9 во вспомогательных репродуктивных технологиях [12]. И если ранее эту систему обширно критиковали [13] за высокие риски возникновения мозаицизма эмбрионов и незапланированных изменений в геноме, то ее новые модификации позволили значительно снизить эти риски.
Группа ученых под руководством известного эмбриолога Шухрата Миталипова [14] провела успешные эксперименты по редактированию гена MYBPC3, ответственного за развитие аутосомно-доминантного генетического заболевания под названием гипертрофическая кардиомиопатия [15]. Оказалось, что лишних, незапланированных мутаций в геноме не возникало, при этом мозаицизм наблюдался только у одного эмбриона из 58. Такого блестящего результата им удалось добиться с помощью некоторых модификаций методики. В частности, вместо генов, кодирующих РНК-гид (нужен для распознавания ДНК-мишени) и «белок-ножницы» Cas9, в клетку вводили эти молекулы в готовом виде. Они делали свое дело, уничтожая мутантные копии гена, и вскоре утилизировались клеткой, а значит, больше не представляли опасности. В целях профилактики мозаицизма эмбрионов систему вводили непосредственно в момент оплодотворения яйцеклетки.
И пусть пока эксперименты проводили на эмбрионах, не подлежащих дальнейшей имплантации, в будущем с помощью этой технологии возможно будет излечить любую моногенную наследственную болезнь еще до того, как она проявит себя.
Весь 2017 год система CRISPR-Cas не выходила из фокуса внимания ученых и обывателей. Ученым из Гарварда удалось усовершенствовать комплекс таким образом, чтобы он не разрезал узнанный ген, как обычно, а заменял один нуклеотид на другой [16]. А исследователи из Кембриджского университета в Массачусетсе установили, что подобную замену можно производить не только в ДНК, но и в РНК. Для CRISPR-систем такая возможность показана впервые [17].
И даже более того, CRISPR-Cas9 открыла ученым перспективы по выращиванию химер, состоящих из клеток разных видов [18], [19]! Для этого необходимо «выключить» в зиготе конкретные гены, которые отвечают за развитие того или иного органа, а затем на стадии бластоцисты внедрить в эмбрион индуцированные стволовые клетки другого вида. Таким образом были получены химеры крысы и мыши, а также свиньи и человека. Тела одного вида, содержащие в себе органы другого вида. Успешные результаты этих экспериментов дают надежду на выращивание в будущем человеческих органов для трансплантации.
Разумеется, все эти прорывы вызывают тревогу у людей и становятся излюбленной темой в биоэтике [20].
Новые рубежи генотерапии

Милан и Елена Вилларреаль уже потеряли старшего ребенка из-за спинальной мышечной атрофии 1 типа к моменту, когда включили младшую дочь Эвелин в клинические испытания генной терапии.
Ученым из Национальной детской больницы в Колумбусе (Огайо) удалось с помощью генотерапии спасти жизни нескольких детей, рожденных с тяжелым наследственным недугом — спинальной мышечной атрофией 1 типа [21]. Заболевание вызывается мутацией в гене SMN1, которая ведет к поражению двигательных нейронов передних рогов спинного мозга. В результате нарушения работы мускулатуры ног, головы и шеи дети с этой мутацией умирают до достижения двухлетнего возраста, что делает эту болезнь самой частой генетической причиной гибели младенцев.
Ключом к лечению заболевания стал безвредный вирус AAV9, несущий нормальную копию гена SMN1. Как оказалось, он способен проникать через гематоэнцефалический барьер, ограждающий головной и спинной мозг от контакта с кровью. Следовательно, появляется шанс на лечение множества других наследственных нейродегенеративных заболеваний.
Удивительные результаты дали попытки коррекции с помощью генотерапии другого наследственного недуга — «синдрома бабочки», или буллезного эпидермолиза, вызванного повреждением гена LAMB3 [22–23]. Заболевание сопровождается образованием пузырей и эрозией кожи при малейшем воздействии на нее. Ребенку с тяжелой формой заболевания успешно трансплантировали трансгенный эпидермис. Его получали, выращивая культуры клеток эпидермиса пациента и обрабатывая их ретровирусами, несущими нормальную копию LAMB3. К радости исследователей, новая кожа прижилась, и вот уже два года прежних симптомов не наблюдается.
Успешной оказалась также генотерапия серповидноклеточной анемии [24] — наследственного заболевания крови, вызванного повреждением гена бета-глобина, HBB. Ранее этот подход тестировали на мышах, а в этом году впервые применили для лечения людей.
Человек и его братья меньшие

Pongo tapanuliensis, новый вид больших человекообразных обезьян.
Волей экспертов Science в категорию топовых достижений вместе с генетикой вошли вопросы эволюции приматов. Причем нашим собственным видом и его непосредственными предками дело не ограничилось.
Речь идет о выделении нового, седьмого вида ближайших родственников человека — больших человекообразных обезьян [25]. Популяция орангутанов в лесу Батанг-Тору была обнаружена еще в 1997 году, но выделена в отдельный вид только спустя 20 лет. И поскольку с момента описания последнего вида больших человекообразных обезьян прошло без малого 90 лет, это событие не могло не стать сенсацией.
Если же говорить о Homo sapiens, то в уходящем году он стал древнее на 100 000 лет [26]. Об этом говорят находки в марокканской пещере недалеко от Марракеша. Обнаруженные останки несут прогрессивные признаки, характерные уже для H. sapiens, но датируются примерно 300 000 лет.
На атомарном уровне
Кто бы спорил, что в нынешнее время развитие науки неразрывно связано с развитием научных методов (О том, как важны методы в биологии, читайте в материалах нашего спецпроекта «12 биологических методов в картинках».) Журнал Science назвал 2017 год знаковым для криоэлектронной микроскопии [27], [28], подчеркнув, что редко бывает, когда та или иная разработка заслуживает высокой чести в науке (Нобелевской премии по химии 2017 года [29]), еще не развернувшись в полную силу. С момента появления в 80-е годы XX века этот метод непрерывно совершенствовался, и сегодня мы имеем возможность наблюдать биомолекулы в атомарном разрешении! В уходящем году с помощью этой технологии ученые смогли глубже понять процессинг РНК, сборку клеточных мембран, развитие болезни Альцгеймера, работу CRISPR-комплекса и многие другие клеточные процессы.
Выбор читателей (и журналистов)
Эксперты-экспертами, а у читателя свое, особое мнение. Это мнение нашло воплощение в лайках и репостах под соответствующими публикациями и количестве их упоминаний во всевозможных СМИ. Если в прошлом году публика была всерьез обеспокоена вирусом Зика, особенностями системы здравоохранения и экзопланетами, то в 2017 году они предпочли озаботиться собственным здоровьем. Вопросам питания и здорового образа жизни посвящено около 20% (!) всех публикаций, вошедших в топ-100 «Альтметрики» за 2017 год.

В нынешнем году читателей научных новостей больше всего интересовала еда
Бесспорным лидером рейтинга оказалась статья-индульгенция для жиров в нашей диете [30]. Долгие годы диетологи всего мира рекомендовали ограничивать относительное потребление жиров, особенно насыщенных. Предполагалось, что это поможет снизить уровень «плохого» холестерина (ЛПНП) [31] и, следовательно, риск развития сердечно-сосудистых заболеваний. Однако данные обширного исследования, охватившего 135 000 человек, проживающих в 18 странах, в эту модель не уложились. Оказалось, что жиры на самом деле «хорошие» и, по-видимому, наоборот, снижают риски проблем с сердечно-сосудистой системой. Что касается углеводов, то их потребление всё-таки незначительно коррелирует с общей смертностью, но не со смертностью от сердечно-сосудистых заболеваний.
С другой стороны, публиковались сообщения о том, что употребление напитков, содержащих сахар и подсластители, повышает риск развития ишемического инсульта и различных форм слабоумия [32]. Досталось и шоколаду, который, несмотря на свое благотворное влияние на сердечно-сосудистую систему в целом, оказался фактором, повышающим риск фибрилляции предсердий [33]. На этом фоне значительно порадовал читателей кофе, который, оказывается, при регулярном употреблении способен снижать смертность от болезней печени, сердца, почек, от инсульта, диабета, респираторных заболеваний и даже рака [34], [35]. Впрочем, с раком не всё так однозначно, поскольку среди прочего обнаружили положительную корреляцию между употреблением кофе и раком яичников [34]. Неоднозначная история получилась и с алкоголем, который хоть и связан с риском когнитивных отклонений, но, вероятно, может препятствовать развитию диабета [36], [37]. Так что в преддверии новогодних застолий нелишне будет об этом вспомнить. Хотя, конечно, проблема здорового питания выходит далеко за рамки праздничного меню.
Другая топовая тема этого года касалась отмеченной тенденции роста ожирения людей по всему миру, в том числе в странах с низким подушевым доходом [38], [39]. Звучали прогнозы, что к 2022 году количество людей с ожирением в мире впервые превысит количество людей с нормальным и низким индексом массы тела.
Однако оставим вопросы диеты и здорового образа жизни. Разве могут они сравниться по яркости и сенсационности с другими крупными вехами, отмеченными пристальным вниманием публики? В их числе:
- Первое успешное выращивание животного в искусственной матке. Сильно недоношенного ягненка вырастили в специально разработанной системе с искусственной пуповиной и амниотической жидкостью [40]. Не исключено, что уже в ближайшем будущем можно будет спасти тех младенцев, которые рождаются на слишком ранних сроках.
- Первые успешные попытки использовать растительные клетки в тканевой инженерии. Сосудистую систему растений использовали при построении каркасов для биоинженерных тканей. После удаления целлюлозных стенок с растительных клеток систему жилок заселяли эндотелиоцитами и кардиоцитами человека. Последние сохраняли свою жизнеспособность в течение трех недель [41].
- Первый успешный случай создания протезов яичников для мышей с помощью 3D-печати. На основе 3D-печати пористого каркаса из гидрогеля и мышиных фолликулов были созданы искусственные яичники для мышей. После трансплантации они прекрасно прижились, а получившие их стерильные мыши снова обрели фертильность [42].
И это еще далеко не все свежие достижения науки. Согласитесь, 2017-й выдался удивительно «урожайным» для биологии и биомедицины. Есть что отпраздновать и о чем загадать желания на будущий год!
Литература
- Couzin-Frankel J. (2017). A cancer drug’s broad swipe. Science;
- Лечение Джимми Картера;
- Работа над ошибками;
- Dung T. Le, Jennifer N. Uram, Hao Wang, Bjarne R. Bartlett, Holly Kemberling, et. al.. (2015). PD-1 Blockade in Tumors with Mismatch-Repair Deficiency. N Engl J Med. 372, 2509-2520;
- Хороший, плохой, злой, или Как разозлить лимфоциты и уничтожить опухоль;
- Dung T. Le, Jennifer N. Durham, Kellie N. Smith, Hao Wang, Bjarne R. Bartlett, et. al.. (2017). Mismatch repair deficiency predicts response of solid tumors to PD-1 blockade. Science. 357, 409-413;
- Ledford H. (2017). Engineered cell therapy for cancer gets thumbs up from FDA advisers. Nature News;
- 12 методов в картинках: клеточные технологии;
- Успех в борьбе с лейкозом: на шаг ближе к клиническому применению геномного редактирования;
- Ledford H. (2016). Safety concerns blight promising cancer therapy. Nature News;
- 12 методов в картинках: генная инженерия. Часть I, историческая;
- Ledford H. (2017). CRISPR fixes disease gene in viable human embryos. Nature News;
- Ledford H. (2016). Enzyme tweak boosts precision of CRISPR genome edits. Nature News;
- Человек генно-модифицированный / Homo genere mutatio;
- Hong Ma, Nuria Marti-Gutierrez, Sang-Wook Park, Jun Wu, Yeonmi Lee, et. al.. (2017). Correction of a pathogenic gene mutation in human embryos. Nature. 548, 413-419;
- Nicole M. Gaudelli, Alexis C. Komor, Holly A. Rees, Michael S. Packer, Ahmed H. Badran, et. al.. (2017). Programmable base editing of A•T to G•C in genomic DNA without DNA cleavage. Nature. 551, 464-471;
- David B. T. Cox, Jonathan S. Gootenberg, Omar O. Abudayyeh, Brian Franklin, Max J. Kellner, et. al.. (2017). RNA editing with CRISPR-Cas13. Science. 358, 1019-1027;
- Jun Wu, Aida Platero-Luengo, Masahiro Sakurai, Atsushi Sugawara, Maria Antonia Gil, et. al.. (2017). Interspecies Chimerism with Mammalian Pluripotent Stem Cells. Cell. 168, 473-486.e15;
- Свинолюди, крысомыши и другие биотехнологические истории;
- Ledford H. (2016). UK bioethicists eye designer babies and CRISPR cows. Nature News;
- Kaiser J. (2017). Gene therapy’s new hope: a neuron-targeting virus is saving infant lives. Science;
- Tobias Hirsch, Tobias Rothoeft, Norbert Teig, Johann W. Bauer, Graziella Pellegrini, et. al.. (2017). Regeneration of the entire human epidermis using transgenic stem cells. Nature. 551, 327-332;
- Помочь тем, кого нельзя обнять;
- Jean-Antoine Ribeil, Salima Hacein-Bey-Abina, Emmanuel Payen, Alessandra Magnani, Michaela Semeraro, et. al.. (2017). Gene Therapy in a Patient with Sickle Cell Disease. N Engl J Med. 376, 848-855;
- Stokstad E. (2017). A new great ape species. Science;
- Gibbons A. (2017). Deeper roots for Homo sapiens. Science;
- Pennisi E. (2017). Life at the atomic level. Science;
- 12 методов в картинках: структурная биология;
- Крупные подробности микроскопического мира: Нобелевская премия по химии 2017;
- Mahshid Dehghan, Andrew Mente, Xiaohe Zhang, Sumathi Swaminathan, Wei Li, et. al.. (2017). Associations of fats and carbohydrate intake with cardiovascular disease and mortality in 18 countries from five continents (PURE): a prospective cohort study. The Lancet. 390, 2050-2062;
- Хороший, плохой, злой холестерин;
- Matthew P. Pase, Jayandra J. Himali, Alexa S. Beiser, Hugo J. Aparicio, Claudia L. Satizabal, et. al.. (2017). Sugar- and Artificially Sweetened Beverages and the Risks of Incident Stroke and Dementia. Stroke. 48, 1139-1146;
- Elizabeth Mostofsky, Martin Berg Johansen, Anne Tjønneland, Harpreet S Chahal, Murray A Mittleman, Kim Overvad. (2017). Chocolate intake and risk of clinically apparent atrial fibrillation: the Danish Diet, Cancer, and Health Study. Heart. 103, 1163-1167;
- Marc J. Gunter, Neil Murphy, Amanda J. Cross, Laure Dossus, Laureen Dartois, et. al.. (2017). Coffee Drinking and Mortality in 10 European Countries. Ann Intern Med. 167, 236;
- Song-Yi Park, Neal D. Freedman, Christopher A. Haiman, Loïc Le Marchand, Lynne R. Wilkens, Veronica Wendy Setiawan. (2017). Association of Coffee Consumption With Total and Cause-Specific Mortality Among Nonwhite Populations. Ann Intern Med. 167, 228;
- Anya Topiwala, Charlotte L Allan, Vyara Valkanova, Enikő Zsoldos, Nicola Filippini, et. al.. (2017). Moderate alcohol consumption as risk factor for adverse brain outcomes and cognitive decline: longitudinal cohort study. BMJ. j2353;
- Charlotte Holst, Ulrik Becker, Marit E. Jørgensen, Morten Grønbæk, Janne S. Tolstrup. (2017). Alcohol drinking patterns and risk of diabetes: a cohort study of 70,551 men and women from the general Danish population. Diabetologia. 60, 1941-1950;
- Leandra Abarca-Gómez, Ziad A Abdeen, Zargar Abdul Hamid, Niveen M Abu-Rmeileh, Benjamin Acosta-Cazares, et. al.. (2017). Worldwide trends in body-mass index, underweight, overweight, and obesity from 1975 to 2016: a pooled analysis of 2416 population-based measurement studies in 128·9 million children, adolescents, and adults. The Lancet. 390, 2627-2642;
- The GBD 2015 Obesity Collaborators. (2017). Health Effects of Overweight and Obesity in 195 Countries over 25 Years. N Engl J Med. 377, 13-27;
- Emily A. Partridge, Marcus G. Davey, Matthew A. Hornick, Patrick E. McGovern, Ali Y. Mejaddam, et. al.. (2017). An extra-uterine system to physiologically support the extreme premature lamb. Nat Comms. 8, 15112;
- Joshua R. Gershlak, Sarah Hernandez, Gianluca Fontana, Luke R. Perreault, Katrina J. Hansen, et. al.. (2017). Crossing kingdoms: Using decellularized plants as perfusable tissue engineering scaffolds. Biomaterials. 125, 13-22;
- Monica M. Laronda, Alexandra L. Rutz, Shuo Xiao, Kelly A. Whelan, Francesca E. Duncan, et. al.. (2017). A bioprosthetic ovary created using 3D printed microporous scaffolds restores ovarian function in sterilized mice. Nat Comms. 8, 15261.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚




