От подтипов к терапии: молекулярная логика гинекологических раков
24 апреля 2026
От подтипов к терапии: молекулярная логика гинекологических раков
- 950
- 0
- 3
Онкологические заболевания репродуктивных органов и молочных желез у женщин, несмотря на разное происхождение, обладают рядом общих молекулярных признаков, что важно для выработки эффективной стратегии лечения этой группы заболеваний.
Рисунок в оригинальном разрешении.
иллюстрация Анастасии Самоукиной
-
Автор
-
Редакторы
-
Иллюстратор
В современной онкологии наблюдается частичный отход от традиционной медицинской модели, когда основной характеристикой опухоли был орган происхождения («рак молочной железы», «рак легких» и так далее). Оказалось, что во многих случаях для выбора оптимальной схемы лечения гораздо важнее молекулярный подтип рака — характерный набор мутаций, который делает даже опухоли, происходящие из разных тканей, чувствительными к одним и тем же лекарствам. В продолжении спецпроекта «Онкология» мы рассмотрим перспективы и ограничения такого агностического подхода на примере гинекологических раков — злокачественных опухолей женской репродуктивной системы и молочных желез.
Онкология

Онкология — одно из самых динамично развивающихся направлений биомедицинских исследований. С одной стороны медицинское и практическое значение этой темы обеспечивает ей интерес общества и обширное финансирование; с другой — изучение раковой клетки и эволюции опухолей проливает свет на самые фундаментальные вопросы биологии, что делает данный спецпроект интересным для биологов самых разных специальностей.
Редактор спецпроекта — Мария Кондратова, к.б.н специалист в области молекулярной биологии рака и онкоиммунологии, автор научно-популярных книг «Кривое зеркало жизни» и «Невидимый страж», которые мы горячо рекомендуем всем интересующимся молекулярной онкологией и иммунологией.
Партнер спецпроекта — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Злокачественные новообразования репродуктивных органов и молочных желез — наиболее распространенная группа онкологических заболеваний у женщин во всем мире. Эти опухоли существенно снижают качество жизни пациенток и вносят значительный вклад в общую женскую смертность. По данным Международного агентства по изучению рака (МАИР), в 2022 году было зарегистрировано около 3 294 316 новых случаев рака молочной железы, рака шейки матки и рака яичников, что составило 16,5% от всех диагностированных онкологических заболеваний в мире. Кроме того, эти опухоли унесли жизни 1 220 712 человек, что соответствует 12,6% от общего числа смертей, обусловленных онкологическими причинами [1].
Опухоли, специфичные для женщин, объединяет ряд общих характеристик: органы, в которых они образуются, находятся под влиянием женских половых гормонов, а их лечение входит в компетенцию отдельной медицинской специальности — гинекологической онкологии, что, в свою очередь, находит свое отражение в организационной структуре медицинских учреждений. Нас же в этой статье будут интересовать прежде всего общие молекулярные паттерны этих заболеваний, которые позволяют лечить одними и теми же методами опухоли в разных органах, которые традиционная онкология считала разными болезнями.
Исторически наиболее хорошо изученным с молекулярной точки зрения является рак молочной железы (РМЖ) — именно на его примере мы рассмотрим принципы определения молекулярных подтипов рака и их связь с выбором стратегий профилактики и лечения. Кстати, это будет уже не первая статья о РМЖ на «Биомолекуле»: «Порочный цикл: от рака молочной железы до костных метастазов» [2]. Во второй части статьи мы более детально поговорим об агностическом подходе в онкологии и проанализируем параллели между подтипами РМЖ и других гинекологических раков и их значении для терапии этих онкологических заболеваний. Вкладка с экспертным мнением будет посвящена биоинформатическим методам определения чувствительности опухоли к PARP-ингибиторам, разработанным в институте Кюри (Франция) и уже внедряемым в клиническую практику.
Рак молочной железы — подтипы, прогнозы, стратегии лечения
Эпидемиология и факторы риска
РМЖ, который в быту часто называют «раком груди», — одна из древнейших болезней, известных человечеству: ее описание мы находим еще в древнеегипетских папирусах и античных медицинских текстах. Это также одно из наиболее изученных онкологических заболеваний. У мужчин тоже встречаются злокачественные опухоли в молочных железах, но очень редко. Почему же у женщин клетки этого органа столь подвержены злокачественному перерождению?
Видимо, основную роль в этом играет природная «отзывчивость» клеток молочных желез к сигналам, стимулирующим рост и деление. Во время беременности и в период грудного вскармливания под влиянием половых гормонов женская грудь увеличивается почти в два раза благодаря активному делению клеток. Однако такая «готовность делиться» оборачивается риском злокачественного перерождения 😔.
Среди многочисленных факторов риска болезни, обнаруженных эпидемиологами, значительная часть связана именно с балансом гормонов (рис. 1). Роды и продолжительное грудное вскармливание, напротив, снижают предрасположенность к заболеванию — вероятно, благодаря естественным изменениям, благотворно влияющим на дифференцировку тканей молочной железы. Наследственные мутации в генах BRCA1 и BRCA2 повышают риск заболевания в несколько раз. Меньший, но все равно заметный вклад в развитие РМЖ вносят также длительное воздействие эстрогенов, ожирение, курение, злоупотребление алкоголем и недостаточная физическая активность (рис. 1) [3].
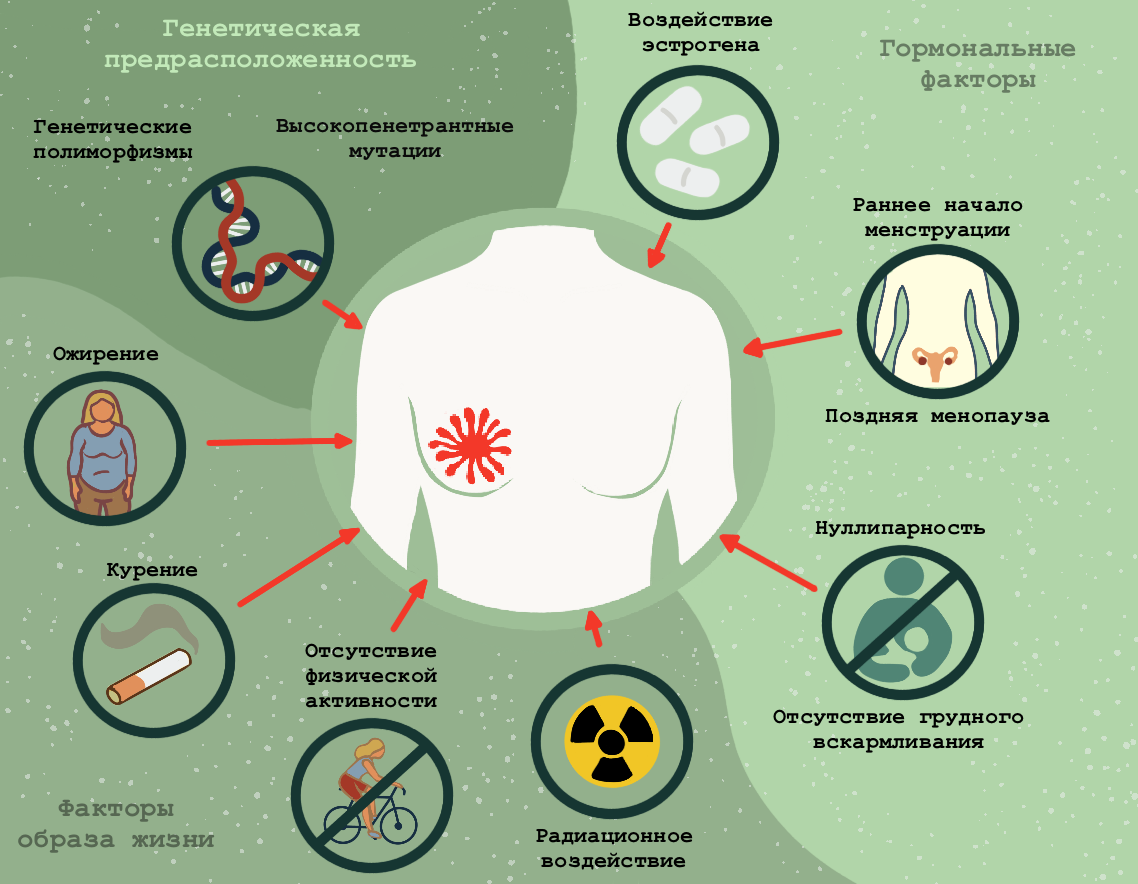
Рисунок 1. Факторы риска рака молочной железы. Для их измерения используют величину отношения рисков (hazard ratio; HR), которая показывает, насколько вероятнее развитие рака при наличии фактора риска в сравнении с тем, когда его нет. Гормональные факторы, такие как длительное воздействие эстрогенов (HR = 1,19), отсутствие родов (1,32) и грудного вскармливания (1,44), поздняя менопауза (1,03) или раннее менархе (1,05), повышают риск развития РМЖ, хотя и не очень сильно. Генетическая предрасположенность представляет серьезную угрозу для здоровья — тут соотношение рисков максимально. Пациенты с генетическими мутациями, такими как BRCA1 (7,62) и BRCA2 (5,23), а также лица, у которых у ближайших родственников был диагностирован РМЖ, более подвержены развитию этого злокачественного заболевания. Нездоровый образ жизни также может дать свой вклад. Чрезмерное воздействие радиации (1,54), злоупотребление алкоголем и курение (1,23), питание с высоким содержанием жиров или сахара, ожирение (1,44) и низкая физическая активность (1,16) — также относятся к основным факторам риска.
иллюстрация Анастасии Самоукиной по [3]
История вопроса: какие и когда выделяли типы РМЖ
Предыстория: до молекулярной эры
До конца 1990-х годов рак молочной железы классифицировали исключительно по морфологии клеток и рецепторному статусу. Иммуногистохимическое определение рецепторов эстрогена (ER) было внедрено в клиническую практику еще в 1970-х, определение HER2 — в конце 1980-х. Опухоли с высоким содержанием эстрогенового рецептора давали хороший ответ на терапию, связанную с блокировкой этого рецептора (тамоксифен), а трастузумаб стал прорывным препаратом для лечения опухолей с повышенной экспрессией рецептора HER2. Таким образом, именно для лечения рака груди были разработаны первые «таргетные» препараты .
Мы не раз уже писали о принципах таргетной терапии («Поиск лекарственных мишеней» [4], «Три поколения лекарств» [5]) и ее первых успехах, связанных с развитием технологии антител («Краткая история открытия и применения антител» [6], «От медицинской онкологии к молекулярной биологии рака» [7]). Отправляем к этим трудам интересующихся читателей.
В отличие от традиционной химиотерапии, которая воздействует на все активно делящиеся клетки, эти лекарства прицельно атакуют только клетки, в которых в значительном количестве присутствуют белки-мишени (targets), что делает их более эффективными и безопасными. Однако довольно скоро исследователи обнаружили, что опухоли одной ИГХ-группы зачастую ведут себя совершенно по-разному. Стало понятно, что для эффективного лечения болезни необходима более точная классификация подтипов РМЖ. Одновременно происходило развитие и удешевление методов молекулярно-биологических исследований, и стало возможным измерять активность множества генов в образце одновременно. Молекулярная онкология вышла на новый уровень.
2000-е: «Молекулярные портреты» — революция в понимании РМЖ
В 2001 году Тересе Соррли и соавторы опубликовали в PNAS работу, в которой впервые дали имена подтипам РМЖ: люминальный A, люминальный B, HER2-обогащенный и базальноподобный [9]. Авторы показали, что эти группы различаются не только транскриптомно, но и по клиническим исходам: базальноподобный и HER2-обогащенный подтипы показывали достоверно худшую выживаемость, чем люминальные.
Ими также была описана также группа «нормальноподобных» опухолей, однако ее в настоящий момент большинство исследователей склонны считать артефактом присутствия в образцах здоровых тканей.
Позже та же группа опубликовала подтверждение своих результатов на независимых наборах данных, продемонстрировав универсальность предложенного подхода [10]. Параллельно клиницисты собирали и систематизировали данные о прогностической и предиктивной ценности предложенных подтипов. Ключевые наблюдения этого периода:
- Люминальный A демонстрировал лучший прогноз и низкую чувствительность к химиотерапии — что предвосхитило современную концепцию деэскалации лечения. Так, исследования TAILORx и MINDACT показали, что пациентки с HR+/HER2−/N0 не получают выигрыша от добавления токсичной химиотерапии к более щадящей и легче переносимой эндокринной («гормональной») терапии. Это изменило стандарт лечения для сотен тысяч пациенток ежегодно [11].
- Люминальный B, несмотря на ER-позитивность, оказался более агрессивным и химиочувствительным, чем люминальный A.
- Базальноподобный подтип привлек внимание связью с BRCA1-мутациями. Оказалось, что спорадические базальноподобные опухоли функционально напоминают BRCA1-дефицитные — по геномной нестабильности, иммунной активности и чувствительности к ДНК-повреждающим агентам [12].
- HER2-обогащенный подтип оказался независимым предиктором ответа на антрациклины и, позднее, на неоадъювантные анти-HER2-режимы.
Однако внедрить эти научные наблюдения в регулярную клиническую практику было непросто — молекулярное типирование требовало замороженной ткани и анализа тысяч генов, что было недоступно большинству медицинских центров.
Ситуация изменилась в 2009 году, когда Паркер, Перу и соавторы опубликовали работу, описывающую PAM50 — предиктор на основе всего 50 генов [13]. PAM50 сохранял четыре клинических подтипа как основу классификации и добавлял количественную оценку риска рецидива (ROR-score). Такое упрощение подхода расширило возможности для его клинического применения.
Другим важнейшим практическим шагом стал клинический консенсус Сен-Галлена 2011 года. Эксперты в молекулярной онкологии не только признали четыре молекулярных подтипа клинически значимыми, но и предложили их ИГХ-эквиваленты для массового клинического использования [14]. Каждый подтип характеризовался с помощью уровня трех наиболее значимых рецепторов: эстрогенового (ER), прогестеронового (PR) и HER2; кроме того, для разделения люминальных подтипов использовался маркер клеточного деления белок Ki-67. Таким образом, получилась следующая картина:
- Люминальный A: ER+, PR+, HER2−, Ki-67 низкий;
- Люминальный B: ER+, PR± (или низкий), HER2±, Ki-67 высокий;
- HER2-обогащенный: ER−, PR−, HER2+;
- Тройной негативный / базальноподобный (ТНРМЖ): ER−, PR−, HER2−.
Это сделало классификацию доступной для любого патологоанатомического отделения в мире без молекулярного секвенирования. Однако при этом сформировался некоторый концептуальный разрыв, который важно осознавать — ИГХ- и PAM50-подтипы, несмотря на одинаковые названия, не полностью тождественны друг другу: несовпадение между ними может достигать 30% и быть особенно высоким для люминальных подтипов (рис. 2). Для различения люминальных подтипов А и В только ИГХ-анализа может оказаться недостаточно — в таких случаях обычно назначают дополнительные анализы (например, PAM50), позволяющие уточнить подтип.
На основе накопленных данных четыре подтипа были закреплены в международных руководствах по лечению РМЖ и определили подтип-специфические алгоритмы лечения этой группы заболеваний (табл. 1). В наши дни изучение подтипов продолжается, происходит уточнение более узких групп внутри каждого подтипа для дальнейшей персонализации лечения. Однако все эти уточнения «живут» внутри исходной четырехчастной системы (рис. 2) [16], не заменяя ее.
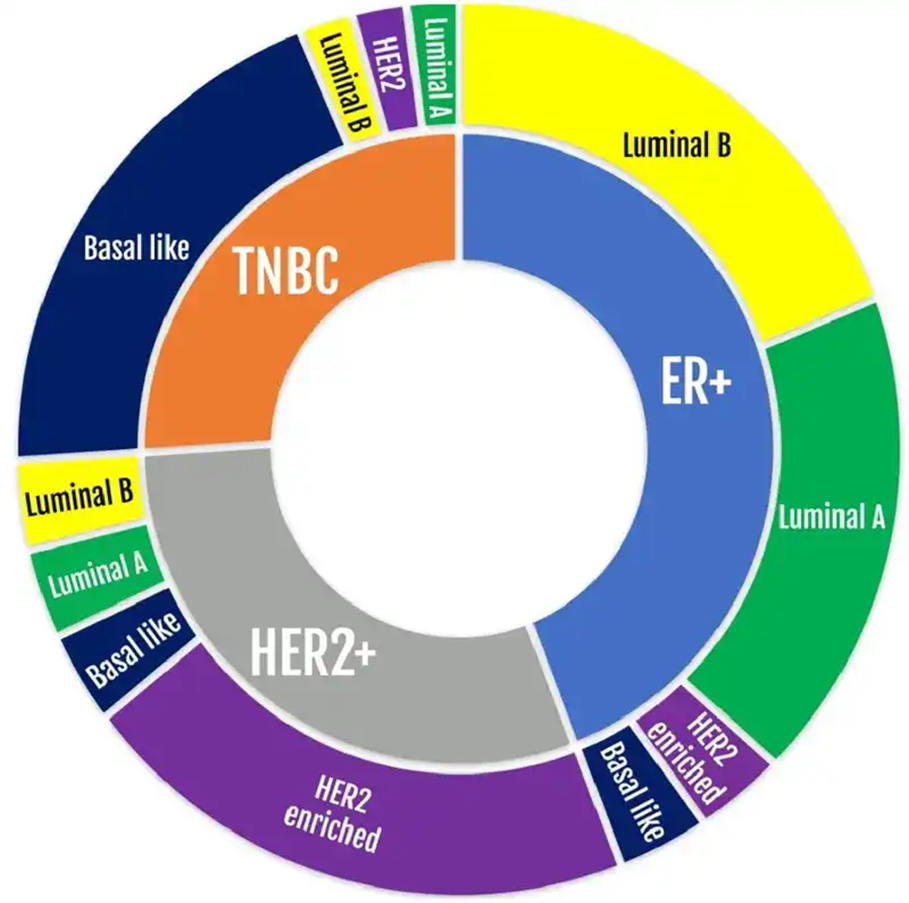
Рисунок 2. Молекулярная гетерогенность клинических подтипов рака молочной железы. Внутреннее кольцо представляет три клинических подтипа, определяемых иммуногистохимически (ER+, HER2+, ТНРМЖ — TNBC); внешнее — распределение молекулярных подтипов по PAM50 (люминальный A, люминальный B, HER2-обогащенный, базальноподобный — basal-like) внутри каждого клинического подтипа. Каждый клинический подтип включает опухоли нескольких молекулярных подтипов, что отражает неполную конкордантность между ИГХ- и транскриптомной классификацией.
Особенности протекания РМЖ и методы лечения
Основная информация о подтипах РМЖ, характерных мутациях, прогнозах и методах лечения собрана в Таблице 1.
| Подтип | Молекулярные особенности | Частота | Прогноз | Лекарственная терапия |
|---|---|---|---|---|
| Люминальный A HR+/HER2−/Ki-67<14% |
ESR1↑ Высокая активность эстрогенового рецептора. Относительно низкая активность генов клеточной пролиферации. Низкий уровень мутаций и геномной нестабильности |
~50–60% Наиболее частый подтип |
Благоприятный ★★★★★ Особенность: поздние рецидивы через 10–20 лет |
Основное лечение — эндокринная терапия: блокаторы эстрогенового рецептора (Тамоксифен), ингибиторы ароматазы (летрозол, анастрозол, эксеместан) |
| Люминальный B HR+/ HER2±/Ki-67>20% |
Геномная нестабильность выше, чем у A Высокая активность генов клеточной пролиферации (CCNB1↑, MKI67↑, AURKA↑, CDK1↑ и т.д.) |
~10–20% | Умеренный ★★★☆☆ Хуже Lum A Особенность: риск рецидива > 10 лет сохраняется |
Эндокринная терапия и химиотерапия применяются вместе. В эту схему часто добавляются еще ингибиторы CDK4/6 (абемациклиб), блокирующие деление клеток |
| HER2-обогащенный ER−/PR−/HER2+ |
ERBB2 — амплификация гена Очень высокий уровень хромосомной нестабильности |
~10–15% | Промежуточный ★★★☆☆ |
Таргетная терапия против HER2 (Трастузумаб, пертузумаб) в сочетании с химиотерапией |
| ТНРМЖ/Базальноподобный ER−/PR−/HER2−/Ki-67 высокий |
Очень высокий уровень хромосомной нестабильности Много мутаций в онкогенах (TP53, RB1, BRCA1, MYC и т.д.) HRD (Homologous Recombination Deficiency) — у >50% опухолей |
~15–20% | Неблагоприятный ★★☆☆☆ Особенность: ранние рецидивы (1–3 года) |
Основное лечение — разные варианты химиотерапии Дополнительно: иммунотерапия (пембролизумаб) При мутации в BRCA1/2 — PARP-ингибиторы (олапариб) |
В том, что касается протекания разных подтипов рака молочной железы, хочется акцентироваться на одном феномене, который получил название «парадокса трижды негативного рака молочной железы» (Triple negative paradox). Как правило, прогноз для люминальных раков гораздо более благоприятный, чем для трижды-негативных опухолей, однако при этом в случае успешного излечения первичной опухоли «тяжелые» трижды негативные раки имеют гораздо более низкую вероятность «возвращения» спустя несколько лет, чем «легкие» люминальные.
При трижды негативном РМЖ кривая рецидивов падает круто в первые 1–3 года, достигает «дна» примерно к 5 годам и затем выходит на плато. А вот при люминальном A — все наоборот: кривая снижается медленно, и риск рецидива продолжает оставаться ненулевым через 10, 15 и даже 20 лет [17]. Это и есть «феномен продленного риска» для люминальных опухолей (рис. 3).
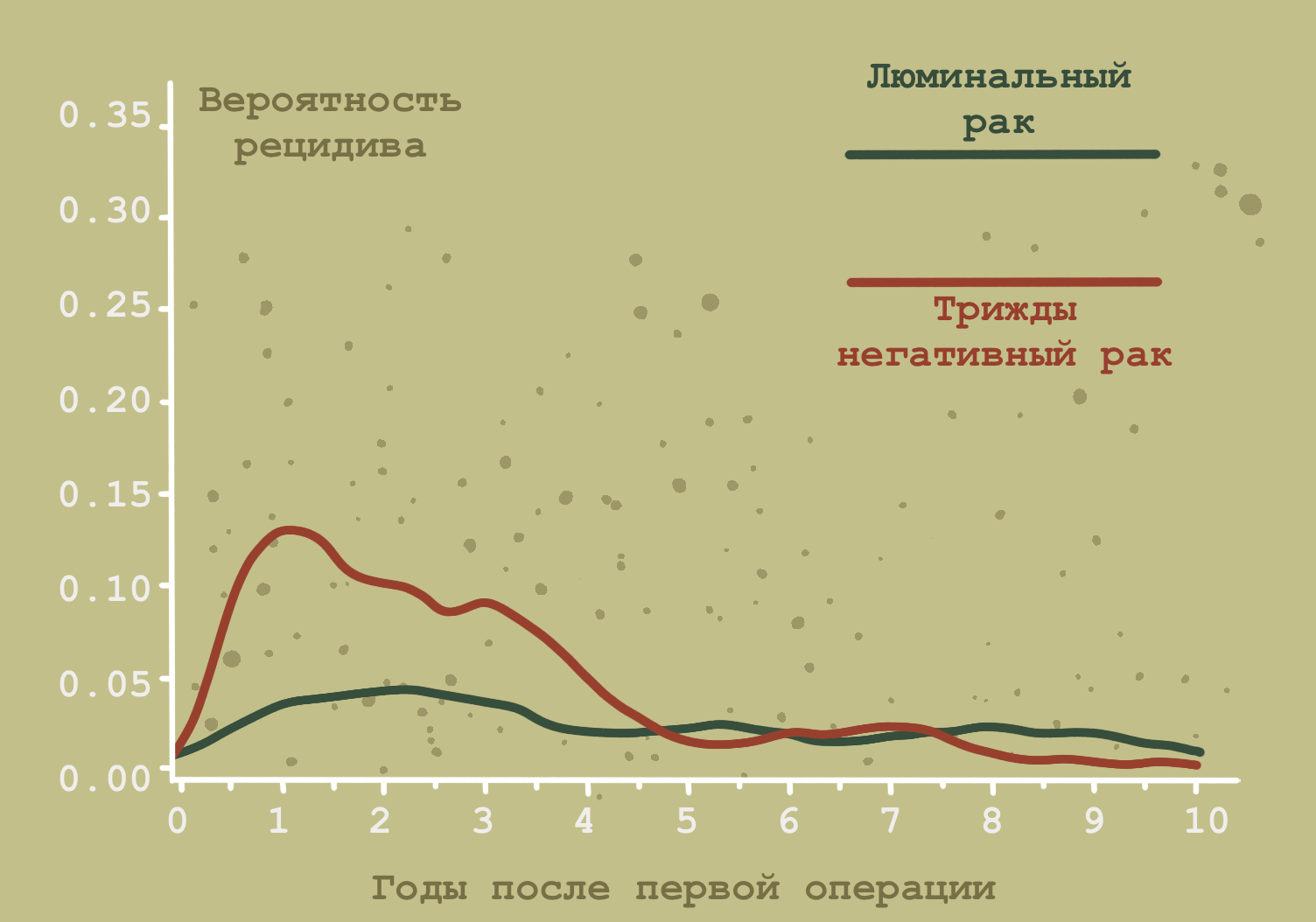
Рисунок 3. Парадокс «трижды негативного» РМЖ. Показана частота рецидивов для трижды негативных и люминальных раков. Трижды негативные раки имеют высокий уровень рецидивов в первые несколько лет, а затем он падает практически до нуля. Люминальные раки в целом имеют гораздо более низкий уровень рецидивов, но при этом возможно возвращение болезни и через 10–15 лет.
иллюстрация Анастасии Самоукиной по [17]
Этот феномен имеет биологическое объяснение. При ТНРМЖ нет гормонального сигнала, который мог бы поддерживать опухолевые клетки. Опухоль либо рецидивирует быстро — потому что агрессивна биологически, — либо иммунная система ее добивает. А вот при люминальном A ER-позитивные клетки, распространившиеся по организму (микрометастазы), могут десятилетиями находиться в «спящем» состоянии в костном мозге или других тканях — поддерживаемые эстрогеновым микроокружением [18]. Любое изменение гормонального статуса (менопауза, отмена тамоксифена после 5 лет и даже сильный стресс) способно «разбудить» их и побудить к активному делению. Именно это объясняет, почему эндокринная терапия для пациенток этой категории сейчас нередко продлевается до 7–10 лет.
Это явление имеет важные практические следствия, которые не всегда бывают очевидны женщинам, получающим лечение от РМЖ:
- При трижды негативном РМЖ: если пациентка прошла через 5 лет без рецидива — она статистически «вышла» из зоны высокого риска.
- При люминальном A: «5 лет без рецидива» — не финиш и не безопасная точка. Риск рецидива сохраняется еще долгие годы. Именно поэтому пациентки с Lum A должны наблюдаться дольше и получать продолжительную эндокринную терапию.
Агностический подход в современной онкологии. Общие молекулярные паттерны между РМЖ и другими гинекологическими раками
В последние годы в молекулярной онкологии все большее значение приобретает так называемый агностический подход, когда при подборе оптимальной схемы лечения внимание уделяется не столько органу происхождения опухоли («рак легких», «рак желудка»), сколько ее молекулярной характеристике и набору онкогенных мутаций. При агностическом подходе больные, имеющие первичные злокачественные опухоли в разных органах, могут получать одинаковое лечение, если эти опухоли имеют одни и те же молекулярные нарушения. Классическим примером такого подхода является одобренное FDA в 2017 году использование пембролизумаба (ингибитор PD-1) для опухолей, демонстрирующих микросателлитную нестабильность высокой степени (MSI-H) или дефицит системы репарации (dMMR). В настоящее время этот вариант иммунотерапии используется для лечения таких разных онкологических заболеваний как рак толстого кишечника, рак желудка и рак эндометрия [20].
Про это антитело «Биомолекула» уже не раз писала: «Лечение Джимми Картера» [21], «Хороший, плохой, злой, или Как разозлить лимфоциты и уничтожить опухоль» [22].
Другой пример агностического подхода — использование антител для блокады онкогенного рецептора HER2. Эта группа лекарств изначально была разработана для лечения одного из подтипов РМЖ, однако в настоящее время эти препараты используются также для лечения опухолей желудка с повышенным уровнем экспрессии этого рецептора (в сочетании с химиотерапией) и тестируются для других типов опухолей [23].
Пока еще рано говорить о том, что агностический подход способен полностью отменить «классические» орган-специфические методы лечения онкологических заболеваний, но это, безусловно, важный и убедительный шаг в направлении персонализированной медицины — одновременно и более эффективной, и более щадящей.
Молочная железа и репродуктивные органы женской половой системы имеют разное строение и эмбриональное происхождение, однако их объединяет общая чувствительность к одним и тем же молекулярным сигналам от женских половых гормонов — эстрогенов и прогестинов, регулирующих рост этих органов и деление клеток в них. Так что можно было ожидать, что и поломки нормальных механизмов регуляции клеточного цикла в этих опухолях могут быть похожи.
Уже давно было известно, что мутации в генах BRCA у женщин значительно повышают риск как рака молочной железы, так и рака яичников. Геномное и молекулярно-генетическое сравнение показало значительное сходство между базальным раком молочной железы (Basal-Like Breast Cancer) и серозным раком яичников высокой злокачественности (High-Grade Serous Ovarian Cancer). Профиль мутаций в этих типах рака очень похож — фактически, базальный рак молочной железы в молекулярном смысле ближе к серозной карциноме яичника, чем к другим подтипам РМЖ. В частности, ген TP53 имеет высокую частоту мутаций как при базальном раке молочной железы, так и при серозном раке яичника. Кроме того, для обеих опухолей характерны более частая инактивация BRCA1, потеря RB1, амплификация cyclin E1, высокая экспрессия AKT3 и амплификация MYC [24]. Эти общие молекулярные черты убедительно указывают на общие события, инициирующие опухолеобразование при обеих болезнях и, соответственно, поддерживают возможность сходных стратегий лечения базального РМЖ и серозных карцином яичника — например, при помощи PARP-ингибиторов (см. мнение эксперта).
В последние годы появляется все больше информации об общих признаках самых разных гинекологических раков. Еще в 2019 году была опубликована работа, в которой авторы проанализировали вместе данные по типичным «женским» ракам из базы данных TCGA и показали, что они группируются в несколько кластеров со схожими молекулярными характеристиками независимо от происхождения. При этом разные кластеры демонстрируют разные клинические характеристики (рис. 4) [25].
Позднее аналогичные работы были сделаны на других датасетах и других типах данных (протеомика, метиломика) [26]. Результаты этих исследований, хотя и не вошли еще в клиническую практику, намечают перспективу дальнейшего развития агностического подхода в лечении «женских» раков (и не только).
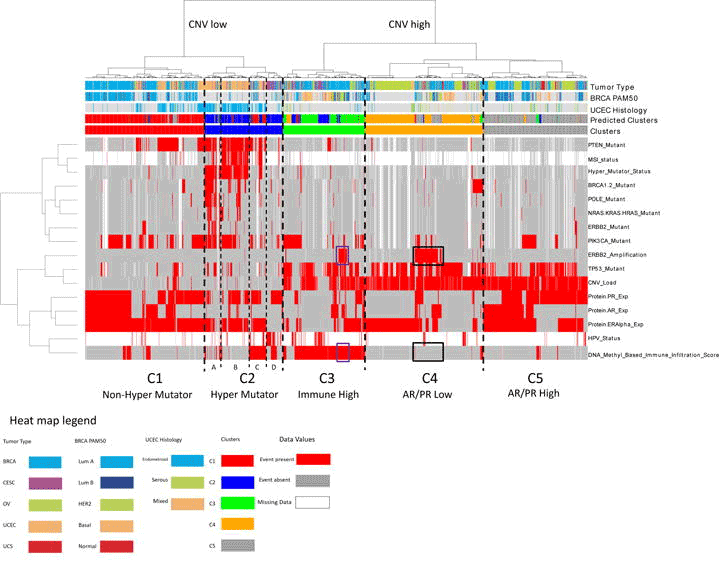
Рисунок 4. Молекулярные подтипы (кластеры) женских онкологических заболеваний. Опухоли из разных органов женской репродуктивной системы группируются вместе по молекулярным признакам, образуя стабильные кластеры.
BRCA — карцинома молочной железы («рак груди»); CESC — рак шейки матки; OV — рак яичников; UCEC — эндометриальная карцинома тела матки; UCS — карциносаркома матки.
Заключение
В заключение мы снова и снова повторяем, что, несмотря на огромный прогресс молекулярной онкологии, основным фактором успешного излечения продолжает оставаться ранняя диагностика. Своевременная маммография и регулярное посещение гинеколога — залог женского здоровья не только в юности, но и в зрелом возрасте. Особенно важно следить за своим здоровьем, если в семье в нескольких поколениях наблюдались случаи женских онкологических заболеваний. В таких случаях, помимо стандартного обследования, рекомендуется сделать генетические тесты на мутации в наиболее распространенных онкогенах.
К сожалению, в нашей культуре «женская медицина» все еще воспринимается преимущественно как сфера, «обслуживающая» детородную функцию. Пройдя через менопаузу и убедившись в том, что они больше не способны иметь детей, многие женщины перестают обращать внимание на свою репродуктивную систему, хотя на самом деле из-за возрастающего с возрастом риска онкологического перерождения тканей именно в зрелом возрасте она требует особого внимания. Если у вас есть родственницы или подруги, перешагнувшие порог 50–52 лет, которые годами не посещали маммолога и гинеколога, — покажите им эту статью и посоветуйте немедленно записаться к специалисту. Пусть это будет вашим личным вкладом в снижение смертности от гинекологических раков — болезней, которые продолжают убивать женщин, несмотря на все успехи медицины и фармакологии.
Литература
- Yingying Li, Wenfu Song, Ping Gao, Xutao Guan, Bing Wang, et. al.. (2025). Global, regional, and national burden of breast, cervical, uterine, and ovarian cancer and their risk factors among women from 1990 to 2021, and projections to 2050: findings from the global burden of disease study 2021. BMC Cancer. 25;
- Порочный цикл: от рака молочной железы до костных метастазов;
- Xin Xiong, Le-Wei Zheng, Yu Ding, Yu-Fei Chen, Yu-Wen Cai, et. al.. (2025). Breast cancer: pathogenesis and treatments. Sig Transduct Target Ther. 10;
- Поиск лекарственных мишеней;
- Три поколения лекарств;
- Краткая история открытия и применения антител;
- От медицинской онкологии к молекулярной биологии рака;
- Мáркеры для клеток: как ученые «раскрашивают» клетки, чтобы отличить одну от другой;
- Therese Sørlie, Charles M. Perou, Robert Tibshirani, Turid Aas, Stephanie Geisler, et. al.. (2001). Gene expression patterns of breast carcinomas distinguish tumor subclasses with clinical implications. Proc. Natl. Acad. Sci. U.S.A.. 98, 10869-10874;
- Therese Sørlie, Robert Tibshirani, Joel Parker, Trevor Hastie, J. S. Marron, et. al.. (2003). Repeated observation of breast tumor subtypes in independent gene expression data sets. Proc. Natl. Acad. Sci. U.S.A.. 100, 8418-8423;
- J.M.N. Lopes Cardozo, D. Byng, C.A. Drukker, M.K. Schmidt, M.A. Binuya, et. al.. (2022). Outcome without any adjuvant systemic treatment in stage I ER+/HER2− breast cancer patients included in the MINDACT trial. Annals of Oncology. 33, 310-320;
- Nicholas Turner, Andrew Tutt, Alan Ashworth. (2004). Hallmarks of 'BRCAness' in sporadic cancers. Nat Rev Cancer. 4, 814-819;
- Joel S. Parker, Michael Mullins, Maggie C.U. Cheang, Samuel Leung, David Voduc, et. al.. (2009). Supervised Risk Predictor of Breast Cancer Based on Intrinsic Subtypes. JCO. 27, 1160-1167;
- A. Goldhirsch, W.C. Wood, A.S. Coates, R.D. Gelber, B. Thürlimann, H.-J. Senn. (2011). Strategies for subtypes—dealing with the diversity of breast cancer: highlights of the St Gallen International Expert Consensus on the Primary Therapy of Early Breast Cancer 2011. Annals of Oncology. 22, 1736-1747;
- 12 методов в картинках: иммунологические технологии;
- Akshita Vyas, Sumeet Dwivedi, Sweta S. Koka, Gajanan Narayanrao Darwhekar. (2025). Triple-Negative Breast Cancer: Molecular Subtypes, Therapeutic Challenges, and Emerging Strategies—A Systematic Review. PJS;
- Rebecca Dent, Maureen Trudeau, Kathleen I. Pritchard, Wedad M. Hanna, Harriet K. Kahn, et. al.. (2007). Triple-Negative Breast Cancer: Clinical Features and Patterns of Recurrence. Clinical Cancer Research. 13, 4429-4434;
- Xiang H.-F. Zhang, Mario Giuliano, Meghana V. Trivedi, Rachel Schiff, C. Kent Osborne. (2013). Metastasis Dormancy in Estrogen Receptor–Positive Breast Cancer. Clinical Cancer Research. 19, 6389-6397;
- Цифровая ПЦР: измеряя истину;
- Vivek Subbiah, Mohamed A. Gouda, Bettina Ryll, Howard A. Burris, Razelle Kurzrock. (2024). The evolving landscape of tissue‐agnostic therapies in precision oncology. CA A Cancer J Clinicians. 74, 433-452;
- Лечение Джимми Картера;
- Хороший, плохой, злой, или Как разозлить лимфоциты и уничтожить опухоль;
- Funda Meric-Bernstam, Amber M. Johnson, Ecaterina E. Ileana Dumbrava, Kanwal Raghav, Kavitha Balaji, et. al.. (2019). Advances in HER2-Targeted Therapy: Novel Agents and Opportunities Beyond Breast and Gastric Cancer. Clinical Cancer Research. 25, 2033-2041;
- Melissa Burgess, Shannon Puhalla. (2014). BRCA 1/2-Mutation Related and Sporadic Breast and Ovarian Cancers: More Alike than Different. Front. Oncol.. 4;
- Ashton C. Berger, Anil Korkut, Rupa S. Kanchi, Apurva M. Hegde, Walter Lenoir, et. al.. (2018). A Comprehensive Pan-Cancer Molecular Study of Gynecologic and Breast Cancers. Cancer Cell. 33, 690-705.e9;
- Sara R. Savage, Xinpei Yi, Jonathan T. Lei, Bo Wen, Hongwei Zhao, et. al.. (2024). Pan-cancer proteogenomics expands the landscape of therapeutic targets. Cell. 187, 4389-4407.e15;
- Celine Callens, Manuel Rodrigues, Adrien Briaux, Eleonore Frouin, Alexandre Eeckhoutte, et. al.. (2023). Shallow whole genome sequencing approach to detect Homologous Recombination Deficiency in the PAOLA-1/ENGOT-OV25 phase-III trial. Oncogene. 42, 3556-3563.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚