-
Те, кто осмелился начать собственный биотехнологический бизнес, часто жалуются на недостаточное финансирование, однако крайне редко — на собственную недостаточную осведомленность о рынке, на который они планируют выводить продукт. Как медицинские стартапы могут получить поддержку от Большой фармы и почему это выгодно обеим сторонам процесса? Рассказываем об этом в продолжении спецпроекта «Открытые инновации».
-
Иммунология — одна из самых «прикладных» и «практичных» биологических дисциплин, и эпидемия COVID-19 позволила лишний раз в этом убедиться. Одновременно это, пожалуй, один из самых сложных разделов науки о живом. В реализации иммунного ответа задействованы десятки разных типов клеток; сотни белков-лигандов: цитокинов, хемокинов; тысячи генов. Приложение методов системной биологии к решению иммунологических задач породило самостоятельную дисциплину — системную иммунологию. В третьей статье цикла «Пятерка по системной биологии» мы увидим, как методы системной биологии помогают разобраться в фундаментальных и прикладных аспектах Т-клеточного ответа.
-
В XX веке медицина и фармацевтика совершили невероятный скачок. Были созданы и внедрены в широкую практику самые разные лекарства — от антибиотиков до первых терапевтических антител, — благодаря чему существенно улучшилось здоровье и самочувствие многих людей, а также выросла средняя продолжительность жизни. Однако прогресс не остановить: доставка нужных генов прямо в клетки и ткани организма или их направленное редактирование позволяют «починить» неисправные молекулярные процессы, что дает в сравнении с традиционной фармацевтикой принципиально новые возможности для терапии ранее неизлечимых болезней. А поскольку технологии не стоят на месте, в будущем генная терапия займет важнейшее место в арсенале медиков.
-
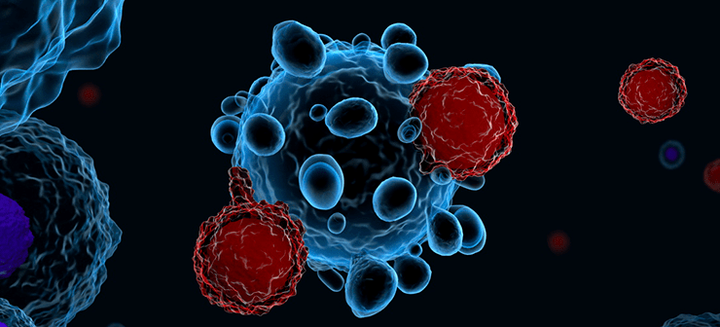
Статья на конкурс «био/мол/текст»: Способность использовать иммунные клетки, направленно изменять их и обучать нацеливаться на опухолевые клетки изменила парадигму лечения многих гематологических опухолевых заболеваний, в том числе неходжкинской лимфомы и острого лимфобластного лейкоза. Т-клеточная терапия химерным рецептором антигена (CAR) показала замечательную противоопухолевую активность против В-клеточных опухолей. В 2017 году Управление по санитарному надзору за качеством пищевых продуктов и лекарственных препаратов (FDA) одобрило две терапии CAR-T, что дало шанс на ремиссию и увеличение продолжительности жизни множеству пациентов. Наш обзор посвящен эволюции CAR-T-клеток, способам их производства, а также будущим перспективам использования.
-
1012Комикс на конкурс «био/мол/текст»: Давным-давно, в далекой-далекой Галактике... Нет, на самом деле, каждую секунду в каждом человеческом организме... Идет освободительная война. Космические корабли защитников Галактики одержали первую победу в битве со зловещими захватчиками. Во время сражения разведчикам защитников удалось заполучить образцы секретного оружия, способного уничтожить целую Галактику. Эти образцы помогут обнаружить вражеские корабли. Воодушевленные успехом, защитники собирают космический флот, чтобы дать захватчикам решительный отпор.
-
Этой статьей мы открываем спецпроект, который расскажет о состоянии сегодняшней фармацевтической индустрии, о том, как она складывалась исторически и о наиболее замечательных лекарствах прошлого, настоящего и будущего. Прогресс в естественных науках увлек за собой и фармацевтику, создав базу для рационального «конструирования» лекарств, в том числе на основе биологических молекул. Многие знают про случайное открытие и последующее выделение из плесневого гриба пеницилла первого антибиотика, революционизировавшего лечение инфекционных болезней и способствовавшего спасению миллионов человеческих жизней во всем мире. Однако далеко не всем известно о достижениях, позволивших синтезировать малые лекарственные молекулы, в промышленных масштабах получать продуцируемые живыми клетками биопрепараты, а также создавать лекарства самой прогрессивной на сегодняшний день передовой (advanced) терапии. Обо всем этом, а также об истории развития фарминдустрии, ее современном состоянии и будущих перспективах, и расскажет наша статья.
-
4307В начале марта 2019 года публикация в журнале Science Translational Medicine сообщила о том, что ученым удалось успешно применить CAR T-клеточную терапию для лечения системной красной волчанки в мышиной модели заболевания. Как работает новое лечение и что это значит для пациентов с системной красной волчанкой?
-
6644В начале 2019 года в Санкт-Петербурге состоится значимое для российской науки и медицины событие: 26–30 января пройдет очередная зимняя школа Future Biotech. Спикерами зимней школы в этом году станут ученые из ведущих научных центров мира: Гарварда, Йеля, Университетского колледжа в Лондоне и многих других. Также в школе примут участие именитые российские ученые, деятельные бизнесмены, руководители наукоемких стартапов и увлеченные наукой студенты, аспиранты и молодые исследователи. Ключевая тема в этом году неразрывно связана с медициной и посвящена технологиям редактирования генома и генной терапии.
-
Статья на конкурс «био/мол/текст»: Фундаментальные исследования молекулярной биологии создали предпосылки для разработки таргетных лекарств, прицельно воздействующих на биомолекулы-мишени в клетках. В статье описана история появления таких препаратов: от исследований Пауля Эрлиха, ставших прообразом рационального поиска лекарств, до первой таргетной терапии, — и к самым последним разработкам наших дней. Мы проследим, как после первых успехов в лечении химиотерапевтическими препаратами зародилось понимание молекулярных механизмов развития заболеваний и как понимание этих закономерностей помогло ученым создать таргетные лекарства. Рассмотрим и наиболее многообещающие направления современного лечения: иммунотерапию, генную терапию, и применение лекарств, созданных с помощью нанотехнологий. В конце затронем тему перспектив таргетного лечения.


- Лента
- Спецпроекты
- ▶Подкаст
-
Конкурс
- О конкурсе «Био/мол/текст»
- «Био/мол/текст»-2025/2026
- «Био/мол/текст»-2024/2025
- «Био/мол/текст»-2023/2024
- «Био/мол/текст»-2022/2023
- «Био/мол/текст»-2021/2022
- «Био/мол/текст»-2020/2021
- «Био/мол/текст»-2019
- «Био/мол/текст»-2018
- «Био/мол/текст»-2017
- «Био/мол/текст»-2016
- «Био/мол/текст»-2015
- «Био/мол/текст»-2014
- «Био/мол/текст»-2013
- «Био/мол/текст»-2012
- «Био/мол/текст»-2011
- Объявления
- Авторы
- Партнеры
- Поддержать
Публикации
—
Темы
—
Авторы
—
Комментарии
—
Поиск не дал результатов
По вашему запросу ничего не найдено
- Медицина
- SARS-CoV-2
- «Биомолекула» — Forbes
- Аллергия
- Антибиотики
- Атеросклероз
- Аутоиммунитет
- Боль
- ВИЧ/СПИД
- Вакцины
- Вирус Зика
- Вирус Эбола
- Генная терапия
- Грипп
- Депрессия
- Дерматология
- Диагностика
- Здравоохранение
- Нейродегенерация
- Никотин
- Онкология
- Персонализированная медицина
- Питание
- Сон
- Стволовые клетки
- Фармакология
- Эпилепсия
- Биология
- «Сухая» биология
- Антропология
- Бионика
- Биофизика
- Вирусология
- Вопросы пола
- ГМО
- Генетика
- Иммунология
- Микробиология
- Нейробиология
- Носимые технологии
- Психогенетика
- Синтетическая биология
- Старение
- Структурная биология
- Цитология
- Эволюционная биология
- Экология
- Эмбриология
- Эпигенетика
- Этология
- Биомолекулы
- GPCR
- АФК
- Амилоиды
- Биомембраны
- Гормоны растений
- ДНК
- Ионные каналы
- МГЭ
- Матрикс
- Нейромедиаторы
- РНК
- Рецепторы
- Хроматин