Сахарный диабет I типа, или Охота на поджелудочную железу
29 апреля 2017
Сахарный диабет I типа, или Охота на поджелудочную железу
- 36946
- 1
- 20
Сахарный диабет вызывает невыносимую жажду, превращая человека в «водный сифон».
рисунок Елены Беловой
-
Автор
-
Редакторы
-
Рецензенты
-
Иллюстратор
Сахарная болезнь — звучит загадочно и как будто несерьезно. Что же кроется за этим названием? К сожалению, сахарная болезнь (diabetes mellitus) — совсем «не сахар»: на фоне масштабной потери жидкости больных изнуряет постоянная жажда, а многие узнают о своем недуге лишь после выхода из диабетической комы. Среди осложнений неконтролируемого сахарного диабета нередки поражения глаз, почек, нервной и сердечно-сосудистой систем, в связи с чем это заболевание относят к одной из серьезнейших проблем нашего общества.
Аутоиммунные заболевания
Мы продолжаем цикл по аутоиммунным заболеваниям — болезням, при которых организм начинает бороться сам с собой, вырабатывая аутоантитела и/или аутоагрессивные клоны лимфоцитов. Мы рассказываем о том, как работает иммунитет и почему иногда он начинает «стрелять по своим». Некоторым самым распространенным заболеваниям будут посвящены отдельные публикации. Для соблюдения объективности мы пригласили стать куратором спецпроекта доктора биологических наук, чл.-корр. РАН, профессора кафедры иммунологии МГУ Дмитрия Владимировича Купраша. К тому же у каждой статьи есть свой рецензент, более детально вникающий во все нюансы.
Рецензентом этой статьи стал Павел Юрьевич Волчков — заведующий лабораторией геномной инженерии МФТИ.
Партнеры проекта — Михаил Батин и Алексей Маракулин (Open Longevity / «Объединенные Консультанты Финправо»).
О «болезни неутолимой жажды и потери жидкости» писали еще древнеиндийские, древнеегипетские и древнегреческие врачи. Конкретное же ее наименование — διαβαινω (что по-гречески означает «перехожу, пересекаю») — появилось в третьем веке до нашей эры, вероятнее всего, в трудах Аполлона из Мемфиса. Оно отражало представления тех времен об этом недуге: больной, вынужденный постоянно выводить и принимать жидкость, окружающим напоминал своеобразный сифон, через который постоянно «переходит» вода. Первое подробное описание того, что мы сейчас называем diabetes mellitus, то есть сахарный диабет, дал Аретей из Каппадокии.
Сегодня сахарным диабетом первого и второго типов страдает примерно 8,5% населения Земли, то есть каждый двенадцатый ее житель. Чаще всего диабет второго типа поражает жителей развитых стран, однако темпы роста заболеваемости сейчас выше в не столь благополучных регионах. Статистические данные, собранные в США, указывают и на расово-этническую неоднородность в предрасположенности к сахарной болезни: например, диабет находят чуть ли не у каждого шестого индейца или аляскинского эскимоса и лишь у каждого тринадцатого «белого» с неиспанскими корнями. При таких масштабах распространения заболевание приобретает помимо медицинской еще и социальную значимость. Только представьте себе, что будет, если у государств закончатся деньги на производство инсулина или на обучение врачей — специалистов по диабету! Поэтому развитые страны уделяют этой болезни особое внимание, создавая центры адаптации для заболевших и выделяя ученым деньги на исследования, посвященные diabetes mellitus.
Первый рецепт микстуры для лечения сахарной болезни (точнее, ее ведущего симптома — полиурии, или учащенного мочеиспускания) обнаружили в источнике 16 века до нашей эры — папирусе Эберса (рис. 1). Вероятно, в районе шестого века до нашей эры индийский врачеватель Сушрута изобрел метод диагностики диабета, суть которого остается неизменной и по сей день. Конечно, изменилось «оборудование»: в Древней Индии болезнь определяли по сладкому вкусу мочи пациента. Примерно тогда же были описаны и другие симптомы: склонность к ожирению, усиленная жажда, диабетическая гангрена. Самые блестящие доктора разных веков пытались справиться с этой болезнью, однако, несмотря на солидный «возраст» детального описания диабета, больших успехов не достигли.

Рисунок 1. Папирус Эберса.
сайт wikiwand.com
Что сулит нам инсулин?
Что же ломается в нашем таком тонко и изящно устроенном организме, что он начинает так тяжело болеть? Сахарный диабет может довести больного до комы и смерти, а значит, с ним шутки плохи, и надо обязательно разобраться, откуда что берется.
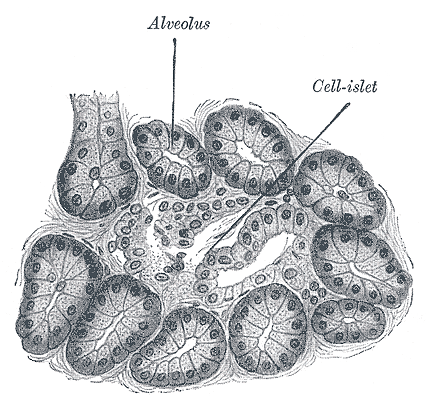
У всех на слуху некое вещество — инсулин, — но не все знают, что оно собой представляет. Инсулин — это пептид [1], а еще точнее — пептидный гормон. Он выделяется в кровь человека клетками островков Лангерганса поджелудочной железы. Эти островки в 1869 году открыл 22-летний студент-медик Лангерганс, впоследствии ставший известным немецким гистологом и анатомом (рис. 2а). Рассматривая в микроскоп срезы поджелудочной железы, он обнаружил необычные островки клеток (рис. 2б), которые, как выяснилось позже, выделяют важные для пищеварения субстанции. Островки Лангерганса состоят из трех видов клеток:
- α-клеток немного (около 20%), они выделяют гормон глюкагон — антагонист инсулина;
- β-клеток большинство, они секретируют инсулин — главный гормон переработки сахаров в организме человека;
- δ-клеток совсем мало (около 3%), они секретируют гормон соматостатин, который угнетает секрецию многих желез.
Непосредственная задача инсулина заключается в том, чтобы помочь потребляемым сахарам попасть в клетку, которая в них нуждается .
Инсулин связывается с двумя мономерами инсулинового рецептора, расположенного в мембране клетки, соединяя их в димер. Внутриклеточные домены инсулинового рецептора являются тирозиновыми киназами (то есть ферментами, присоединяющими фосфатный остаток к аминокислоте тирозину), которые запускают внутриклеточный каскад фосфорилирования. Фосфорилирование, в свою очередь, вызывает проникновение глюкозы в клетку, так как белки глюкозного канала перемещаются из внутриклеточного пространства на мембрану (рис. 3) [2]. Кстати, родственные инсулиновому рецептору тирозиновые киназы — обширное семейство сенсоров, реагирующих на ростовые факторы, гормоны и даже щелочной pH (!) [3].
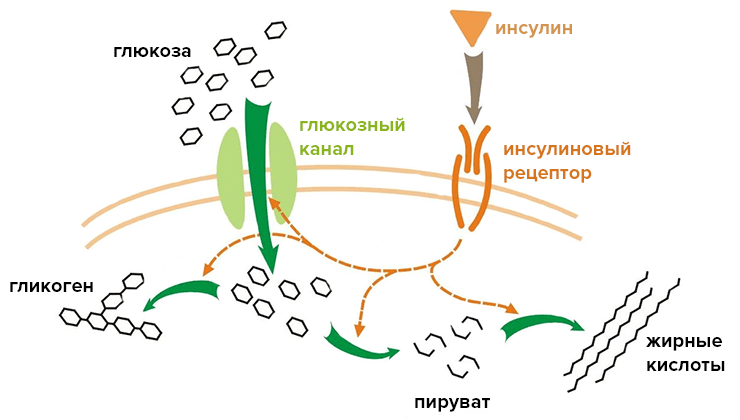
Рисунок 3. Механизм действия инсулина. Связывание инсулина запускает каскад фосфорилирования внутриклеточных белков, что приводит к сборке глюкозного транспортера на мембране и проникновению молекул глюкозы внутрь клетки.
[4], рисунок адаптирован
Сахар — жизненно необходимое для организма вещество. Именно благодаря сахару глюкозе функционирует наш сложный и умный мозг: при расщеплении глюкозы он получает энергию для своей работы [5]. Клетки других органов тоже очень нуждаются в глюкозе — это наиболее универсальный источник их жизненной энергии. Наша печень делает запасы сахара в виде гликогена — полимера глюкозы, — а на черный день ее можно переработать и хранить в виде жировых отложений. Однако чтобы проникнуть в клетки некоторых тканей, глюкозе нужен инсулин. Такие ткани называются инсулинзависимыми. В первую очередь к ним относятся печеночная, мышечная и жировая ткани. Есть и инсулиннезависимые ткани — нервная, например, — но это уже совсем другая история.
В случае инсулинзависимых тканей глюкоза самостоятельно не может проникнуть в клетки — ей обязательно нужен проводник, которым как раз и является инсулин. Глюкоза и инсулин независимо проникают к клеткам органов через «двери» кровеносного русла. Затем инсулин взаимодействует со своим рецептором на поверхности клетки и открывает проход для глюкозы.
Главным сигналом к поступлению инсулина в кровь служит повышение в ней уровня глюкозы. Но есть и иные стимулы: например, секрецию инсулина усиливают не только углеводы, но и некоторые другие вещества, поступающие с пищей — аминокислоты и свободные жирные кислоты. Нервная система тоже вносит свой вклад: при получении определенных сигналов она может давать команду к повышению или понижению уровня инсулина в крови.
Вас много, а я один
Казалось бы, недостаток такого важного гормона, как инсулин, — и так немалая беда для заболевших и врачей. Но нет, проблема диабета гораздо глубже. Дело в том, что существует два его типа , различающихся причинами недостаточной эффективности инсулина.
Если уж быть совсем точными, то даже не два, а больше, просто они не столь распространены. Например, LADA (latent autoimmune diabetes in adults) — латентный аутоиммунный диабет взрослых, или диабет 1,5 типа [6]. По симптоматике он схож с диабетом 2 типа, однако механизм развития у него совсем иной: в организме появляются антитела к β-клеткам поджелудочной железы и ферменту глутаматдекарбоксилазе. Еще один тип сахарного диабета — MODY (maturity onset diabetes of the young), диабет зрелого типа у молодых [7]. Название этого моногенного, наследуемого по аутосомно-доминантному типу, заболевания обусловлено тем, что начинается оно в юном возрасте, однако протекает мягко, подобно «взрослому» диабету 2 типа, при этом снижения чувствительности к инсулину может и не происходить.
Диабет 2 типа (его еще называют инсулинорезистентным) встречается гораздо чаще, чем все прочие формы болезни: его диагностируют примерно у 80% диабетиков. Главная его особенность в том, что чувствительность клеток к действию инсулина значительно снижается, то есть инсулин практически теряет способность запускать глюкозу в ткани. Поджелудочная железа при этом получает сигнал, что инсулина недостаточно, и начинает производить его с повышенной интенсивностью. Из-за постоянной перегрузки β-клетки со временем истощаются, и человеку приходится делать инсулиновые инъекции. Но у заболевших вторым типом диабета есть возможность свести его проявления к минимуму: при достаточной физической активности, соблюдении диеты и снижении массы тела количество глюкозы в крови уменьшается, углеводный обмен нормализуется.
Диабет 1 типа выявляется у 5–10% диабетиков, однако этот диагноз сулит менее радужные перспективы для больного. Это аутоиммунное заболевание, то есть организм по каким-то причинам атакует сам себя, в результате чего содержание инсулина в крови стремится к нулю. Нападкам подвергаются β-клетки островков Лангерганса поджелудочной железы (рис. 2б).
Хотя симптомы двух диабетов схожи, их биологическая сущность разнится. Диабет 1 типа является заболеванием иммунной системы, первопричина же диабета 2 типа кроется в метаболических нарушениях. Различаются они и «типажом» заболевших: диабетом первого типа чаще всего страдают молодые люди до 30 лет, а второго — люди среднего и старшего возраста.
Выживших нет. Механизм развития аутоиммунного диабета
Основные механизмы уничтожения нормальных тканей организма своими же иммунными клетками уже рассматривались в первой статье нашего спецпроекта по аутоиммунным заболеваниям («Иммунитет: борьба с чужими и... своими» [8]). Для того чтобы без затруднений изучать, что происходит с организмом во время сахарного диабета, очень рекомендуем ее прочесть.
Что же должно случиться, чтобы организм начал атаковать клетки собственной поджелудочной железы? Чаще всего это происходит из-за того, что иммунные клетки Т-хелперы пробиваются через гематоэнцефалический барьер — преграду между кровеносными сосудами и головным мозгом, не дающую некоторым веществам и иммунным клеткам взаимодействовать с нейронами. Когда эта преграда страдает, и эти два вида клеток встречаются, происходит иммунизация защитных клеток организма. По сходному механизму развивается еще одно заболевание — рассеянный склероз (РС), однако при РС происходит иммунизация другими антигенами нервных клеток. При помощи своего Т-клеточного рецептора и дополнительного рецептора CD4 Т-хелперы взаимодействуют с комплексом MHC-II—пептид на поверхности антигенпрезентирующих клеток мозга и обретают способность распознавать антигены, которые находятся в нервных клетках. Такие Т-хелперы уже знают, какое «оружие» им потребуется, если они столкнутся с такими же «врагами-антигенами», как в клетках мозга, и они уже полностью готовы вступить с ними в борьбу. По несчастью, MHC-комплекс у некоторых людей «слишком» эффективно презентирует антигены β-клеток поджелудочной железы, очень похожие на те, что существуют в нервных клетках , и этим вызывает сильный иммунный ответ.
Самый важный из нейронных антигенов, который экспрессируется на поверхности β-клеток, — молекула адгезии N-CAM. Нервным клеткам эта молекула необходима для роста и взаимодействия друг с другом. В поджелудочной железе N-CAM выполняет адгезивную функцию и играет важную роль в структурной организации органа [9], [10].
Т-хелперы в скором времени распознают антигены β-клеток, начинают их атаковать и, увы, чаще всего побеждают. Поэтому при диабете 1 типа инсулин у больных прекращает вырабатываться совсем, ведь все клетки, которые были способны его производить, уничтожаются иммуноцитами. Единственное, что можно посоветовать таким пациентам, — это вводить инсулин в кровь искусственно , в виде инъекций. Если этого не делать, то довольно быстро диабет приводит к масштабным «разрушениям» в организме .
Инсулин для этих целей получают генно-инженерным способом. Первым делом культивируют бактериальный штамм-продуцент гибридного белка, содержащего человеческий проинсулин, — Escherichia coli BL21/pPINS07(BL07) или Escherichia coli JM109/pPINS07. Затем клетки бактерий разрушают и отделяют тельца включения, содержащие гибридный белок. Далее проводят предварительную отмывку телец, одновременно растворяют белок и восстанавливают в нём дисульфидные связи, ренатурируют его и проводят очистку гибридного белка ионообменной хроматографией. Расщепление проинсулина проводят совместным гидролизом трипсином и карбоксипептидазой Б. Очистку конечного продукта — инсулина — проводят гидрофобной хроматографией или обращенно-фазовой высокоэффективной жидкостной хроматографией с последующей гель-фильтрацией. Чистый продукт выделяют кристаллизацией в присутствии солей цинка [11].
Сахарный диабет поражает большинство органов. Возникшая гипергликемия (избыток сахара в крови) влечет за собой глюкозурию (появление сахара в моче), полиурию (повышенное мочевыделение), полидипсию (сильную жажду), повышение аппетита и при этом значительное снижение массы тела, а кроме того, вызывает повышенную утомляемость и слабость. Также поражаются сосуды (микроангиопатия) и почки (нефропатия), нервная система (нейропатия) и соединительные ткани, может развиться синдром диабетической стопы.
Поскольку те ткани, которым инсулин для усвоения глюкозы нужен больше всего (печеночная, мышечная и жировая), перестают утилизировать этот сахар, его уровень в крови стремительно возрастает: начинается гипергликемия. Это состояние порождает другие проблемы, в числе которых активизация распада белков и жиров в мышечной и жировой тканях соответственно, а следовательно, выброс жирных кислот и аминокислот в кровеносное русло и усиление образования кетоновых тел. Эти тела мозг и некоторые другие ткани в условиях голодания (дефицита углеводов) вынуждены использовать для извлечения энергии. Из организма активно выводится жидкость, так как глюкоза в крови «оттягивает» на себя воду из тканей и заставляет ее превращаться в мочу. Последствия всех этих процессов очень неприятны: организм обезвожен, лишен большинства необходимых минералов и основного источника энергии, в нём начинают разрушаться мышечная и жировая ткани.
Образование кетоновых тел вследствие разрушения жировой ткани вызывает так называемый кетоацидоз. Это состояние опасно тем, что кетоновые тела (в частности, ацетон) в высоких концентрациях очень токсичны, и если его вовремя не купировать, может развиться диабетическая кома.
Так как при диабете начинается разрушение нервов и сосудов, больному грозят такие осложнения, как диабетическая нейропатия и энцефалопатия, нередко ведущие к парезам, параличам, психическим расстройствам.
Один из самых известных и пугающих симптомов — нарушение зрения, или диабетическая офтальмопатия, — развивается в результате разрушения сетчатки глаза. Кроме того, значительно нарушается работа почек, начинают сильно болеть и хрустеть суставы, в результате чего страдает подвижность пациента.
Эти проявления и осложнения болезни действительно ужасны, но научные достижения всё же способны корректировать ситуацию. Ученые и врачи уже очень много знают об этом заболевании и умеют управлять его течением. Однако чтобы найти ключ к излечению или предотвращению сахарного диабета, необходимо знать его причины.
Всех причин не перечислишь...
Причин и поводов для развития такого сложного заболевания, как diabetes mellitus, немало. Невозможно для всех заболевших выявить какую-то одну, универсальную первопричину, которую можно было бы устранить и тем самым окончательно избавить их от сахарной болезни.
До начала двадцатого столетия врачи даже не предполагали, что может вызывать диабет. Однако к тому времени у них накопилась огромная статистическая база, так что можно было сделать кое-какие выводы. После длительного анализа информации о заболевших людях стало понятно, что к диабету есть генетическая предрасположенность [12], [13]. Это совсем не означает, что при наличии определенных вариантов генов вы обязательно заболеете. Но риск точно повышается. Спокойно вздохнуть могут лишь те, у кого нет никаких генетических особенностей, способствующих развитию диабета.
Предрасположенность к диабету 1 типа связывают в первую очередь с генами главного комплекса гистосовместимости человека второго типа (HLA II) — молекулярного комплекса, играющего важнейшую роль в иммунном ответе. Это не вызывает удивления, ведь именно взаимодействие HLA с рецептором Т-клеток определяет силу иммунного ответа. У HLA-генов существует множество аллельных вариантов (различных форм гена). Одними из наиболее предрасполагающих к заболеванию считают аллели гена рецептора HLA-DQ с названиями DQ2, DQ2/DQ8 и DQ8 , а наименее — аллель DQ6 [14].
Анализ генома 1792 европейских пациентов показал, что относительный риск заболевания для моногаплотипов DQ2 или DQ8 и гетерогаплотипа DQ2/DQ8 составляет соответственно 4,5% и 12,9%. Относительный риск для людей, не несущих ни один из указанных вариантов локуса HLA, составляет 1,8% [15].
Хотя гены главного комплекса гистосовместимости составляют 50% всех «генов-предсказателей» [14], не только они определяют степень устойчивости человека к развитию диабета.
Несмотря на обширные поиски, в последнее время ученые успели открыть всего несколько интересных генов предрасположенности к сахарному диабету:
- генетические вариации молекулы CTLA4, в норме отвечающей за торможение активности Т-клеток, тоже влияют на развитие этой болезни. При некоторых точечных мутациях гена CTLA4 риск заболеть повышается [16], ведь чем хуже будет работать система, снижающая силу иммунной реакции, тем, увы, выше будет вероятность аутоиммунного ответа;
- мутация в гене МТТL1, который кодирует митохондриальную транспортную РНК, переносящую аминокислоту лейцин при синтезе белка в митохондриях, вызывает «синдром диабета и глухоты» и передается по материнской линии [17];
- мутации в гене GCK, кодирующем глюкокиназу (фермент, стимулирующий присоединение фосфора к глюкозе), и в генах гепатоцитарных ядерных факторов HNF-1α или HNF-4α (транскрипционных факторов, синтезирующихся преимущественно в клетках печени) — самые частые изменения, приводящие к диабету MODY.
Как мы видим, генетических причин возникновения диабета может быть довольно много. Но если мы будем знать, какие гены ответственны за заболевание, можно будет быстрее его диагностировать и подбирать самое эффективное лечение.
Однако помимо генетических факторов развития диабета 1 типа есть еще и другие, внешние факторы. Наиболее интересен вклад вирусов. Казалось бы, диабет не относится к вирусным заболеваниям в привычном для нас смысле. Но исследования показывают, что некоторые энтеровирусы вносят значительный вклад в патогенез этого заболевания [18]. Если задуматься, не так уж это и удивительно. Когда вирусы (например, коксакиевирус B1) поражают β-клетки поджелудочной железы, развивается ответ врожденного иммунитета — воспаление и выработка интерферона-α, которые в норме служат для защиты организма от инфекции. Но они же могут сыграть и против него: такая атака патогена организмом создает все условия для развития аутоиммунного ответа (рис. 4).
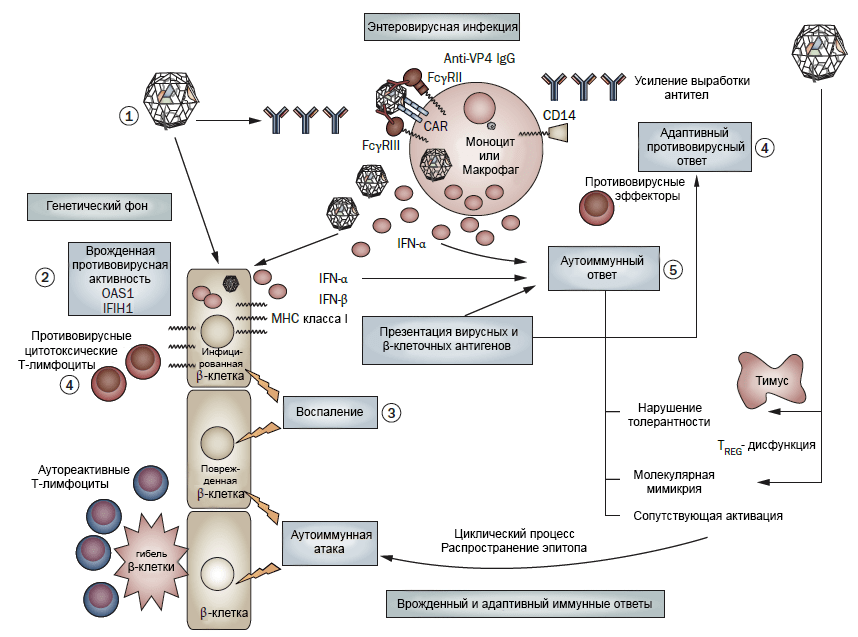
Рисунок 4. Развитие иммунного ответа при размножении коксакиевируса В1 в β-клетках поджелудочной железы. 1 — Организм реагирует на вторжение вируса выработкой антител. Вирус заражает лейкоциты и β-клетки, в результате чего вырабатывается интерферон-α, способный стимулировать аутоиммунные процессы. 2 — Генетическая вариабельность влияет на вероятность заболевания сахарным диабетом 1 типа. Варианты гена OAS1 повышают риск заболевания, а полиморфизм гена IFIH1 понижает. 3 — Энтеровирус вызывает выработку интерферона-α и интерферона-β, индуцирует апоптоз и экспрессию антигенов MHC класса I, а также стимулирует выработку хемокинов, которые привлекают Т-клетки, вырабатывающие провоспалительные цитокины. 4 — Энтеровирусная инфекция одновременно стимулирует приобретенный иммунитет: вырабатываются антитела и привлекаются Т-киллеры, поражающие β-клетки, что приводит к высвобождению их антигенов. 5 — Одновременная активация воспаления и презентация β-клеточного антигена становятся причиной повышенной стимуляции приобретенного иммунитета. Все эти процессы ведут к возникновению аутореактивных Т-клеток, поражающих β-клетки. Чтобы увидеть рисунок в полном размере, нажмите на него.
[18], рисунок адаптирован
Конечно, нельзя забывать и о более привычных для нас внешних факторах, влияющих на развитие болезни. Самые важные из них — стресс и малоподвижный образ жизни. Ожирение, возникающее из-за низкой физической активности и неправильного питания, играет бóльшую роль в развитии диабета 2 типа, однако и в случае 1 типа тоже вносит свой вклад. Люди, в организм которых поступает избыточное количество сахаров, находятся в группе риска, так как повышение уровня глюкозы в крови при низком уровне инсулина может стимулировать аутоиммунные процессы. Любителям сахара приходится несладко, ведь соблазны повсюду. При таких масштабах распространения сахарного диабета необходимо подходить к проблеме «перепотребления» сахара комплексно. В первую очередь ученые советуют убрать глюкозу из списка безопасных веществ. Заодно стόит научить людей определять углеводный состав продуктов и следить за тем, чтобы не превышать допустимые нормы потребления сахара [19].
Ученые выяснили, что существует связь между сахарным диабетом 1 типа и составом кишечной микробиоты [20], [21]. Эксперимент, в котором исследовали крыс, предрасположенных к заболеванию, показал, что у здоровых животных в кишечнике содержится меньше представителей типа Bacteroidetes. Тщательное обследование детей с диабетом 1 типа выявило существенную разницу в составе их кишечной микробиоты относительно здоровых детей. Причем у диабетиков было повышено соотношение Bacteroidetes/Firmicutes, и преобладали бактерии, утилизирующие молочную кислоту. У здоровых же детей в кишечнике было больше продуцентов масляной кислоты [22].
В третьем исследовании ученые «выключали» взаимодействие микробиоты с клетками хозяина, удаляя у экспериментальных животных ген MyD88 — один из главных генов-передатчиков сигналов. Оказалось, что нарушение общения кишечных микробов с хозяином довольно быстро ведет к развитию сахарного диабета 1 типа у мышей [23]. Такая зависимость не удивительна, ведь именно наши бактерии в первую очередь «тренируют» иммунную систему.
Источник многих бед человека — стресс — тоже вносит не последний вклад в развитие diabetes mellitus. Он усиливает воспалительные процессы в организме, что, как уже было описано, повышает вероятность развития сахарного диабета 1 типа. Кроме того, на данный момент достоверно известно, что из-за стресса может «пробиваться» гематоэнцефалический барьер, что ведет ко многим и многим неприятностям...
Что же делать? Как нам быть? Терапия сахарного диабета 1 типа
Казалось бы, ответ на вопрос «что делать?» лежит на поверхности. Если не хватает инсулина — значит, надо его добавить. Так оно и происходит. Инсулин заболевшим вводят внутримышечно на протяжении всей жизни. С того момента, как у человека выявляют diabetes mellitus первого типа, его жизнь кардинально меняется. Ведь даже если в организм поступает инсулин, метаболизм уже всё равно нарушен, и больному приходится следить за каждым своим шагом, чтобы не развалилась с таким трудом собранная заново хрупкая система.
Сейчас, с развитием современных технологий, ученые стараются максимально облегчить пациентам уход за собой. В 2016 году сотрудники компании Google разработали линзу с датчиками, измеряющими концентрацию глюкозы в слезной жидкости. При достижении порогового уровня сахара в линзе загораются миниатюрные светодиоды, тем самым оповещая своего хозяина о произошедших изменениях и о необходимости сделать очередную инъекцию.
Чтобы можно было автоматически вбрасывать инсулин в кровь по мере необходимости, ученые из Швейцарии придумали специальный прибор — инсулиновую помпу с набором функций, существенно облегчающих жизнь больного (рис. 5) [24], [25]. Пока что подобные приборы используют для химиотерапии онкологических заболеваний, но, возможно, в скором времени многие диабетики смогут обзавестись похожей медицинской машиной. Создаются и более комфортные приборы: например, уже разработали датчики, регистрирующие концентрацию глюкозы в поту, и на их основе создали специальный пластырь, определяющий и даже регулирующий уровень сахара в крови [26]. Для этого выстроили систему микроигл, которые впрыскивают лекарство, если концентрация сахара в поту высока. Пока что эту систему опробовали только на лабораторных мышах.
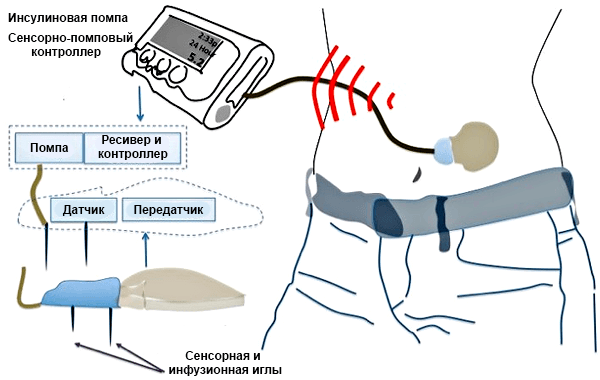
Рисунок 5. Имплантируемая помпа для людей, страдающих сахарным диабетом.
[25], рисунок адаптирован
Пока разнообразные девайсы находятся в разработке, врачи дают своим пациентам старые рекомендации. Впрочем, от больного не требуется ничего сверхъестественного: обычно рекомендуют соблюдать низкоуглеводную диету, заниматься легким спортом и тщательно следить за своим общим состоянием. Со стороны может показаться, что это довольно несложно. Но стόит только представить себя на месте заболевшего человека, как появляется очень неприятное ощущение, что теперь всю жизнь тебе придется во многом себя ограничивать и придерживаться строгого режима во всех сферах жизни — иначе последствия будут тяжелыми. Жить с настолько серьезной ответственностью за свое здоровье никому не хочется. Поэтому врачи и ученые продолжают искать иные способы терапии сахарного диабета, с помощью которых можно будет или полностью излечивать заболевших, или хотя бы существеннее облегчать их жизнь.
Одним из самых интересных и, похоже, работающих подходов оказалась иммунотерапия диабета [27]. Чтобы уменьшить разрушающее действие Т-хелперов, Т-киллеров и B-клеток, в организм вводят так называемую ДНК-вакцину [28]. Звучит загадочно, но на самом деле ДНК-вакцина представляет собой маленькую кольцевую молекулу ДНК, содержащую ген проинсулина (в случае с диабетом 1 типа) или другого белка, который нужен для предотвращения того или иного заболевания. Кроме гена белка, в такой вакцине содержатся все генетические элементы, необходимые для выработки этого белка в клетках организма. Более того, ДНК-вакцину научились конструировать таким образом, чтобы при ее взаимодействии с иммунными клетками врожденного иммунитета происходило ослабление, а не усиление их реакций. Такого эффекта добились благодаря замене нативных CpG-мотивов в ДНК проинсулина на GpG-мотивы, которые супрессируют антиген-специфический иммунный ответ.
Еще один вариант потенциального лечения сахарного диабета 1 типа — блокада рецепторных молекул на атакующих поджелудочную железу Т-клетках. Рядом с Т-клеточным рецептором находится функционально дополняющий его, то есть корецепторный, белковый комплекс. Называется он CD3 (от англ. cell differentiation — дифференцировка клетки). Несмотря на то, что этот молекулярный комплекс не является самостоятельным рецептором, он очень важен, поскольку без него Т-клеточный рецептор не будет полноценно распознавать и передавать внутрь клетки сигналы извне. Без CD3 Т-клеточный рецептор может даже отсоединиться от клеточной мембраны, поскольку корецептор помогает ему держаться на ней. Ученые быстро догадались, что если заблокировать CD3, то Т-клетки будут работать не очень хорошо. Хотя для здорового организма ослабленный таким образом иммунитет не принесет никакой радости, при аутоиммунных заболеваниях это может сослужить добрую службу [29].
Более радикальные подходы и вовсе предполагают замену «не оправдавшей надежды» поджелудочной железы на новую. В 2013 году группа японских ученых сообщила о разработке технологии выращивания человеческих органов в свиньях. Для того чтобы получить чужеродную поджелудочную железу, у эмбриона свиньи необходимо «выключить» гены, отвечающие за образование и развитие его собственного органа, а затем внедрить в этот эмбрион человеческую стволовую клетку, из которой разовьется нужная поджелудочная железа [30]. Идея отличная, однако налаживание массового производства органов таким способом вызывает много вопросов, в том числе и этических. Но возможен и вариант без использования животных: заранее изготавливаемые синтетические каркасы можно заселять клетками необходимых органов, которые впоследствии будут «разъедать» эти каркасы. Также разработаны технологии построения некоторых органов на основе каркасов природных, полученных из других животных [31]. И конечно, нельзя забывать об очень быстро распространяющемся методе 3D-печати. Принтер в таком случае вместо краски использует соответствующие клетки, выстраивая орган слой за слоем. Правда, эта технология еще не вошла в клиническую практику [32], и к тому же у пациента с подобной поджелудочной железой всё равно придется угнетать иммунитет, чтобы избежать нападок иммунных клеток на новый орган.
Предупрежден — почти спасен
Но всё-таки мало кто не согласится с тем, что болезнь лучше предотвратить, чем потом лечить. Или хотя бы заранее знать, к чему готовиться. И тут человечеству приходит на помощь генетическое тестирование. Генов, по которым можно судить о предрасположенности к сахарной болезни, немало. Как уже было сказано, сейчас наиболее перспективными в этом плане считают гены главного комплекса гистосовместимости человека [33]. Если проводить такие тесты в самом раннем возрасте или даже до рождения ребенка, можно будет заранее оценить, насколько велика вероятность когда-либо столкнуться с диабетом, и в дальнейшем избегать тех факторов, которые могут заставить болезнь развиться.
Диабетики всего мира — объединяйтесь!
Хотя диабет 1 типа уже не считается смертельно опасным заболеванием, пациенты сталкиваются с большим количеством неприятностей. Конечно, заболевшим очень нужна поддержка — как со стороны близких, так и со стороны общества в целом. Для таких целей и создаются сообщества диабетиков: благодаря им люди общаются с другими заболевшими, узнают об особенностях своей болезни и учатся новому образу жизни. Одна из лучших организаций подобного рода — Американское диабетическое общество. Портал общества наполнен статьями о разных типах диабета, а еще там работает форум и предоставляется информация о возможных проблемах для «новичков». Похожие сообщества есть во многих развитых странах, в том числе и в Англии. В России тоже есть такое общество, и это здорово, ведь без него российским диабетикам было бы гораздо сложнее адаптироваться к сложившейся ситуации.
* * *
Приятно мечтать о том, что сахарный диабет может исчезнуть с лица Земли. Как оспа, например. Ради осуществления такой мечты можно много чего придумать. Можно, например, пересаживать пациентам островки Лангерганса со всеми необходимыми клетками. Правда, к этому методу еще очень много вопросов: пока неизвестно, как они будут приживаться, будут ли адекватно воспринимать гормональные сигналы от нового хозяина, и так далее.
А еще лучше создать искусственную поджелудочную железу. Только представьте: кроме того что больным не придется постоянно вводить себе инсулин, можно будет еще и регулировать его уровень одним нажатием кнопки в мобильном приложении. Впрочем, пока это всё остается в мечтах. Но вполне вероятно, что когда-нибудь диагноз «сахарный диабет 1 типа» исчезнет из списка пожизненных тяжелых заболеваний, и люди с предрасположенностью к нему смогут вздохнуть спокойно!
Литература
- Неизвестные пептиды: «теневая» система биорегуляции;
- C R Kahn. (1985). The Molecular Mechanism of Insulin Action. Annu. Rev. Med.. 36, 429-451;
- Рецептор «нетрадиционной ориентации»;
- Alan R. Saltiel, C. Ronald Kahn. (2001). Insulin signalling and the regulation of glucose and lipid metabolism. Nature. 414, 799-806;
- Прожорливый мозг;
- P. Pozzilli, U. Di Mario. (2001). Autoimmune Diabetes Not Requiring Insulin at Diagnosis (Latent Autoimmune Diabetes of the Adult): Definition, characterization, and potential prevention. Diabetes Care. 24, 1460-1467;
- Kazuya Yamagata, Hiroto Furuta, Naohisa Oda, Pamela J. Kaisaki, Stephan Menzel, et. al.. (1996). Mutations in the hepatocyte nuclear factor-4α gene in maturity-onset diabetes of the young (MODY1). Nature. 384, 458-460;
- Иммунитет: борьба с чужими и… своими;
- Cirulli V., Baetens D., Rutishauser U., Halban P.A., Orci L., Rouiller D.G. (1994). Expression of neural cell adhesion molecule (N-CAM) in rat islets and its role in islet cell type segregation. J. Cell Sci. 107, 1429–1436;
- Esni F., Täljedal I.B., Perl A.K., Cremer H., Christofori G., Semb H. (1999). Neural cell adhesion molecule (N-CAM) is required for cell type segregation and normal ultrastructure in pancreatic islets. J. Cell Biol. 144, 325–337;
- Зинченко А.А., Мелихова Т.Д., Нокель Е.А., Гордеева Е.А., Толстов Д.Н., Михалев А.В. и др. (2002). Способ получения генно-инженерного инсулина человека. Патент № 2208637;
- Ilonen J., Herva E., Tiilikainen A., Akerblom H.K., Koivukangas T., Kouvalainen K. (1978). HLA-Dw2 as a marker of resistance against juvenile diabetes mellitus. Tissue Antigens. 11, 144–146;
- Bluestone J.A., Herold K., Eisenbarth G. (2010). Genetics, pathogenesis and clinical interventions in type 1 diabetes. Nature. 464, 1293–1300;
- F Pociot, M F McDermott. (2002). Genetics of type 1 diabetes mellitus. Genes Immun. 3, 235-249;
- Thomson G., Robinson W.P., Kuhner M.K., Joe S., MacDonald M.J., Gottschall J.L. et al. (1988). Genetic heterogeneity, modes of inheritance, and risk estimates for a joint study of Caucasians with insulin-dependent diabetes mellitus. Am. J. Hum. Genet. 43, 799–816;
- V M de Jong, A Zaldumbide, A R van der Slik, S Laban, B P C Koeleman, B O Roep. (2016). Variation in the CTLA4 3′UTR has phenotypic consequences for autoreactive T cells and associates with genetic risk for type 1 diabetes. Genes Immun. 17, 75-78;
- J. Finsterer. (2007). Genetic, pathogenetic, and phenotypic implications of the mitochondrial A3243G tRNALeu(UUR) mutation. Acta Neurol Scand. 116, 1-14;
- Didier Hober, Pierre Sauter. (2010). Pathogenesis of type 1 diabetes mellitus: interplay between enterovirus and host. Nat Rev Endocrinol. 6, 279-289;
- Сахар — сладкая смерть;
- Зоопарк в моем животе;
- Микробиом кишечника: мир внутри нас;
- Новые функции кишечной микрофлоры;
- Li Wen, Ruth E. Ley, Pavel Yu. Volchkov, Peter B. Stranges, Lia Avanesyan, et. al.. (2008). Innate immunity and intestinal microbiota in the development of Type 1 diabetes. Nature. 455, 1109-1113;
- Киборги среди нас;
- Ebrahim Ghafar-Zadeh. (2015). Wireless Integrated Biosensors for Point-of-Care Diagnostic Applications. Sensors. 15, 3236-3261;
- «Большой брат следит за тобой», или Как развитие технологий меняет нашу жизнь;
- Roep B.O., Solvason N., Gottlieb P.A., Abreu J.R., Harrison L.C., Eisenbarth G.S. et al. (2013). Plasmid-encoded proinsulin preserves
C-peptide while specifically reducing proinsulin-specific CD8⁺ T cells in type 1 diabetes. Sci. Transl. Med. 5, 191ra82; - Что такое ДНК-вакцины и с чем их едят?;
- Anastasia G. Daifotis, Scott Koenig, Lucienne Chatenoud, Kevan C. Herold. (2013). Anti-CD3 clinical trials in type 1 diabetes mellitus. Clinical Immunology. 149, 268-278;
- Желудок размером с горошину + человеческий кишечник, выращенный в мыши;
- Искусственные органы и тканевая инженерия;
- Органы из лаборатории;
- Steck A.K., Dong F., Wong R., Fouts A., Liu E., Romanos J. et al. (2014). Improving prediction of type 1 diabetes by testing non-HLA genetic variants in addition to HLA markers. Pediatr. Diabetes. 15, 355–362..
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚