-
376Разработан новый подход к предсказанию темпов роста численности бактерий, основанный на особенностях удвоения их генетического материала. Копирование кольцевого генома начинается с одной точки — ориджина репликации. Оказывается, отношение количества копий фрагментов ДНК рядом с ориждином к количеству копий максимально удаленных от него участков отлично коррелирует с темпами роста бактериальной популяции. Теперь можно предсказывать изменения численности представителей микробиоты человека, имея только одну пробу от донора и секвенатор.
-
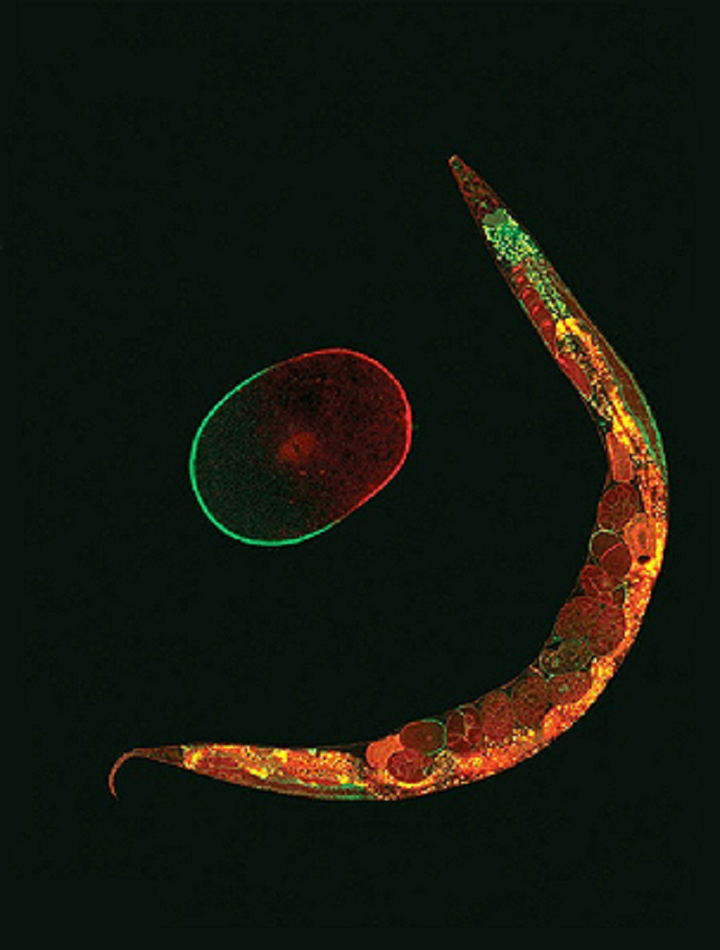
У самок млекопитающих две Х-хромосомы, а у самцов одна. У круглых червей C. elegans почти та же история, только представительницы их слабого пола на самом деле гермафродиты. И для того, чтобы у самок (гермафродитов) не было слишком много продуктов генов Х-хромосом, существует дозовая компенсация. На ее механизмы у червей и пролили свет ученые из США, исследуя структуру хроматина.
-
Любой организм развивается только из одной клетки, но рождается многоклеточным. Как же сложно и закономерно делится эта клетка, что в итоге все живые организмы не похожи друг на друга! Что за закономерности приводят к правильному развитию животных, уже изучено достаточно подробно, а какова логика в случае растений?
-
Генетический вариант, найденный у аборигенов Новой Гвинеи, в эксперименте помог защитить мышей от всех известных прионных заболеваний, в том числе от недавно обнаруженных особо опасных штаммов прионов, вызывающих неклассическую болезнь Крейтцфельдта-Якоба. Чем выше была доля мутантного белка, нарабатываемого у подопытных мышей, тем лучше была их защита. У мышей с двумя мутантными аллелями, то есть производящих только мутантный белок, вырабатывался полный иммунитет ко всем исследованным прионным болезням.
-
Хромотрипсис — недавно открытый тип комплексных геномных изменений, для которого характерны множественные случайные перестройки в хромосомах; чаще всего он встречается в раковых клетках. Механизм хромотрипсиса неизвестен, но полагают, что катастрофические изменения могут происходить в особой клеточной структуре — микроядре. С помощью комбинации методов — визуализации живых клеток и секвенирования геномов отдельных клеток — ученые продемонстрировали, что формирование микроядра может генерировать перестройки в геноме, которые воспроизводят все известные черты хромотрипсиса.
-
Ученые выяснили, почему регуляция экспрессии генов c помощью микроРНК так распространена и консервативна, хотя лишь слегка снижает количество продуктов большинства генов-мишеней. Оказывается, микроРНК помогают уменьшить экспрессионный «шум» — то есть вариабельность, возникающую при реализации генетической информации случайно.
-
Ученые сравнили геномы 10 видов пчел с различной социальностью — от видов, представители которых ведут одиночный образ жизни, до тех, что образуют сложные сообщества, иногда называемые «суперорганизмами». Оказалось, что генетический «рецепт» эусоциальности не единственный, и достичь ее можно изменением разных наборов генов. Однако у пчел, независимо развивших эусоциальность, обнаружили и общие принципы генетической трансформации: усложнение регуляторных сетей — многие гены попали под управление большего числа транскрипционных факторов — и уменьшение транспозонной нагрузки.
-
Первый вопрос, который задают знакомые, узнав, что женщина беременна: «У тебя девочка или мальчик?» Казалось бы, что такого сложного, ведь УЗИ покажет? Но не тут-то было. В одном организме могут мирно сосуществовать и клетки с Y-хромосомой, и их более «женственные» сестры с двумя X-хромосомами. Так что пол — это характеристика не качественная, а количественная.
-
Развитие биотехнологий открыло новые возможности использования живых организмов на благо человечества. Методы генетической инженерии позволяют производить различные вещества в живых объектах, следовательно, мы можем использовать эти объекты в качестве природных «фабрик». Центральная догма молекулярной биологии в общем случае гласит: ДНК → РНК → белок. Именно белок часто является конечным продуктом биотехнологического производства: это может быть инсулин, интерфероны, антитела, ферменты, вакцины... Нам лишь нужно задать программу и «записать» ее в ДНК, а живой объект всё сделает сам. В качестве «фабрик» используют клетки дрожжей, бактерий, растений, а также культуры клеток насекомых и млекопитающих. В этой статье речь пойдет о растительных биофабриках.


- Лента
- Спецпроекты
- ▶Подкаст
-
Конкурс
- О конкурсе «Био/мол/текст»
- «Био/мол/текст»-2025/2026
- «Био/мол/текст»-2024/2025
- «Био/мол/текст»-2023/2024
- «Био/мол/текст»-2022/2023
- «Био/мол/текст»-2021/2022
- «Био/мол/текст»-2020/2021
- «Био/мол/текст»-2019
- «Био/мол/текст»-2018
- «Био/мол/текст»-2017
- «Био/мол/текст»-2016
- «Био/мол/текст»-2015
- «Био/мол/текст»-2014
- «Био/мол/текст»-2013
- «Био/мол/текст»-2012
- «Био/мол/текст»-2011
- Объявления
- Авторы
- Партнеры
- Поддержать
Публикации
—
Темы
—
Авторы
—
Комментарии
—
Поиск не дал результатов
По вашему запросу ничего не найдено
- Медицина
- SARS-CoV-2
- «Биомолекула» — Forbes
- Аллергия
- Антибиотики
- Атеросклероз
- Аутоиммунитет
- Боль
- ВИЧ/СПИД
- Вакцины
- Вирус Зика
- Вирус Эбола
- Генная терапия
- Грипп
- Депрессия
- Дерматология
- Диагностика
- Здравоохранение
- Нейродегенерация
- Никотин
- Онкология
- Персонализированная медицина
- Питание
- Сон
- Стволовые клетки
- Фармакология
- Эпилепсия
- Биология
- «Сухая» биология
- Антропология
- Бионика
- Биофизика
- Вирусология
- Вопросы пола
- ГМО
- Генетика
- Иммунология
- Микробиология
- Нейробиология
- Носимые технологии
- Психогенетика
- Синтетическая биология
- Старение
- Структурная биология
- Цитология
- Эволюционная биология
- Экология
- Эмбриология
- Эпигенетика
- Этология
- Биомолекулы
- GPCR
- АФК
- Амилоиды
- Биомембраны
- Гормоны растений
- ДНК
- Ионные каналы
- МГЭ
- Матрикс
- Нейромедиаторы
- РНК
- Рецепторы
- Хроматин