-
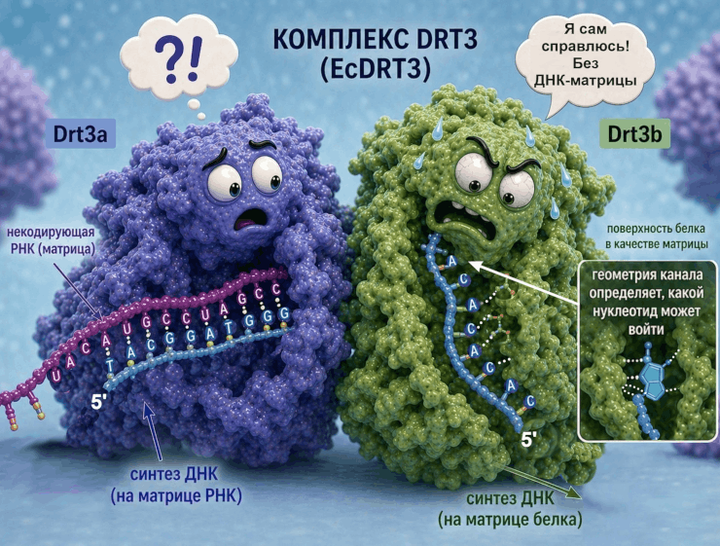
479Природа удивительна, а наука — важнейший инструмент ее познания. И особенно меня впечатляет, когда для чисто фундаментальных открытий люди начинают придумывать, как их можно было бы использовать на практике. На днях в журнале Science вышла статья американских исследователей [1], в которой они впервые показали, что длинные и специфичные последовательности ДНК могут синтезироваться без привычной нуклеотидной матрицы. Вместо этого используется матрица белка.
-
В современной онкологии наблюдается частичный отход от традиционной медицинской модели, когда основной характеристикой опухоли был орган происхождения («рак молочной железы», «рак легких» и так далее). Оказалось, что во многих случаях для выбора оптимальной схемы лечения гораздо важнее молекулярный подтип рака — характерный набор мутаций, который делает даже опухоли, происходящие из разных тканей, чувствительными к одним и тем же лекарствам. В продолжении спецпроекта «Онкология» мы рассмотрим перспективы и ограничения такого агностического подхода на примере гинекологических раков — злокачественных опухолей женской репродуктивной системы и молочных желез.
-
Статья на конкурс «Био/Мол/Текст»: Опухоль мозга — это не просто некое чужеродное для организма анатомическое образование. Такие опухоли тесно связаны с процессами с процессами, протекающими в нервной ткани. В этом тексте я предлагаю посмотреть на мозговые опухоли в трех приближениях. Сначала — на уровне одной спирали ДНК, где может происходить мутация в гистоне H3 или серотонилирование гистона. Потом — на уровне взаимодействия нейронов и опухоли: как сами нейроны могут ускорять или замедлять рост опухолевых клеток, а белок тромбоспондин-1 интегрирует глиобластомы в нейронную сеть. И наконец — на уровне ткани: как миелин, обеспечивающий быструю работу мозга, используется опухолью в качестве источника энергии и средства защиты.
-
Статья на конкурс «Био/Мол/Текст»: В мире животных мимикрия — искусный трюк, чтобы выжить. Оказывается, подобный принцип обмана существует и в наших хромосомах. Мимикрирующие транслокации — это редкие перестройки, при которых морфология хромосом под микроскопом выглядит как клинически значимая транслокация, но на генном уровне ожидаемая перестройка отсутствует, соответствующий химерный ген не образуется. Рассмотрим этот феномен на примере онкогематологических заболеваний.
-
Статья на конкурс «Био/Мол/Текст»: Я думаю, что у каждого есть знакомые, которые по-разному относятся к кофе. Первый с энтузиазмом наливает себе двойной эспрессо, потому что без него он просто не может начать свой день. Второй же не смотрит в сторону кофемашины, зная, что даже маленькая чашка обернется ему бессонной ночью и повышенным уровнем тревожности. Ну, и конечно же, третий тип — человек, который вообще не замечает никакого эффекта от этого напитка. Почему же так происходит? Ответ на этот вопрос вы узнаете в данной статье, погрузившись в удивительный мир генетики и биохимии.
-
101За последние пятнадцать лет поведенческая генетика пережила методологическую революцию: крупномасштабные GWAS-исследования и расчет полигенных индексов позволили количественно оценивать вклад тысяч вариантов ДНК в вариацию сложных признаков — от уровня образования до рисков психических расстройств. Тем не менее, у подобных исследований множество проблем, а полемика вокруг них иногда достигает невероятных масштабов. Кэтрин Пейдж Харден предлагает вынести эти данные из академической дискуссии в поле социальной теории, утверждая, что признание генетической вариативности не противоречит идее равенства, а задает более точные биологические рамки для разговора о неравенстве.
-
192Статья на конкурс «Био/Мол/Текст»: Поведение живых существ, особенно в рамках социума, представляет собой сложный сплав влияния окружающей среды и врожденных программ, зашифрованных в генах. Одним из наиболее интригующих вопросов современной биологии является поиск общих эволюционных путей, которые лежат в основе социального поведения у разных видов, например человека и медоносной пчелы. Исследование, проведенное научной группой из Университета Иллинойса (США), демонстрирует удивительное генетическое сходство в механизмах, регулирующих взаимодействия внутри пчелиной популяции и человеческого общества.
-
134Каждую династию объединяет фамилия, кровь и общая история, передающаяся на семейных встречах. Но семья — это и разные судьбы поколений, словно нити, переплетающиеся между собой в крепкие узлы, которые сложно разорвать. Одни проходят через репрессии и лагеря, сохраняя стойкость и передавая ее своим детям. Другие открывают двери в науку, даже когда они захлопываются под тяжестью клейма «сын врагов народа». Третьи, стоя на развилке, остаются на Родине ради близких и ближних. О твердости духа, желании разгадать тайны жизни и о детской мечте сделать из ласточки стрижа рассказывает София Георгиева, биолог и вирусолог, академик РАН, доктор биологических наук, директор Института молекулярной биологии РАН, дочь молекулярного биолога Георгия Георгиева. Интервью подготовлено в рамках мультимедийного проекта Российского научного фонда «Научные династии: гены открытий».


- Лента
- Спецпроекты
- ▶Подкаст
-
Конкурс
- О конкурсе «Био/мол/текст»
- «Био/мол/текст»-2025/2026
- «Био/мол/текст»-2024/2025
- «Био/мол/текст»-2023/2024
- «Био/мол/текст»-2022/2023
- «Био/мол/текст»-2021/2022
- «Био/мол/текст»-2020/2021
- «Био/мол/текст»-2019
- «Био/мол/текст»-2018
- «Био/мол/текст»-2017
- «Био/мол/текст»-2016
- «Био/мол/текст»-2015
- «Био/мол/текст»-2014
- «Био/мол/текст»-2013
- «Био/мол/текст»-2012
- «Био/мол/текст»-2011
- Объявления
- Авторы
- Партнеры
- Поддержать
Публикации
—
Темы
—
Авторы
—
Комментарии
—
Поиск не дал результатов
По вашему запросу ничего не найдено
- Медицина
- SARS-CoV-2
- «Биомолекула» — Forbes
- Аллергия
- Антибиотики
- Атеросклероз
- Аутоиммунитет
- Боль
- ВИЧ/СПИД
- Вакцины
- Вирус Зика
- Вирус Эбола
- Генная терапия
- Грипп
- Депрессия
- Дерматология
- Диагностика
- Здравоохранение
- Нейродегенерация
- Никотин
- Онкология
- Персонализированная медицина
- Питание
- Сон
- Стволовые клетки
- Фармакология
- Эпилепсия
- Биология
- «Сухая» биология
- Антропология
- Бионика
- Биофизика
- Вирусология
- Вопросы пола
- ГМО
- Генетика
- Иммунология
- Микробиология
- Нейробиология
- Носимые технологии
- Психогенетика
- Синтетическая биология
- Старение
- Структурная биология
- Цитология
- Эволюционная биология
- Экология
- Эмбриология
- Эпигенетика
- Этология
- Биомолекулы
- GPCR
- АФК
- Амилоиды
- Биомембраны
- Гормоны растений
- ДНК
- Ионные каналы
- МГЭ
- Матрикс
- Нейромедиаторы
- РНК
- Рецепторы
- Хроматин