-
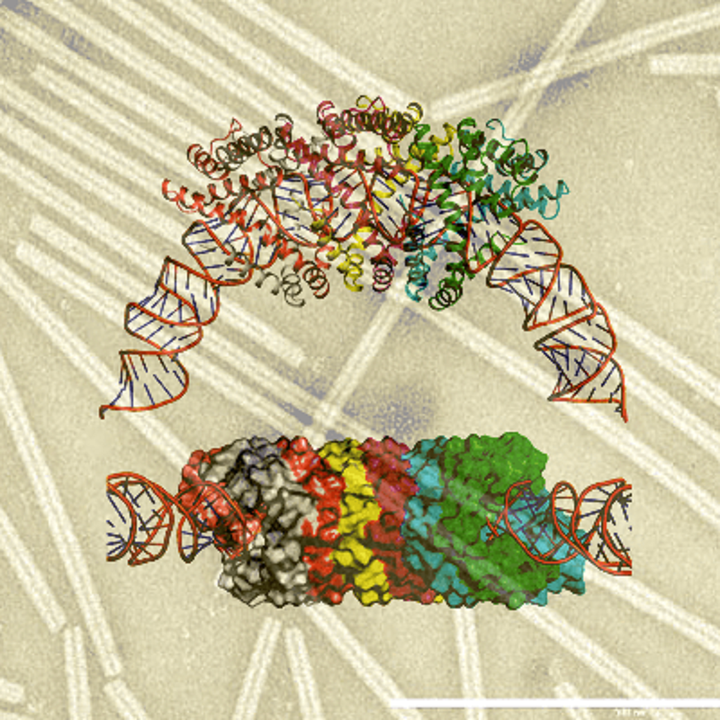
Как пережить перепады температур в 160 °C, встречу с кислотой и засуху? К ответу на этот вопрос приблизились ученые из США и Франции, изучая структуру вирусов. Вероятно, в экстремальных условиях совсем разные организмы используют принципиально одинаковые способы защиты. Важную роль в этих процессах играют особые белки, изолирующие геном от агрессивных сред и стабилизирующие А-форму ДНК.
-
Ученые сравнили геномы 10 видов пчел с различной социальностью — от видов, представители которых ведут одиночный образ жизни, до тех, что образуют сложные сообщества, иногда называемые «суперорганизмами». Оказалось, что генетический «рецепт» эусоциальности не единственный, и достичь ее можно изменением разных наборов генов. Однако у пчел, независимо развивших эусоциальность, обнаружили и общие принципы генетической трансформации: усложнение регуляторных сетей — многие гены попали под управление большего числа транскрипционных факторов — и уменьшение транспозонной нагрузки.
-
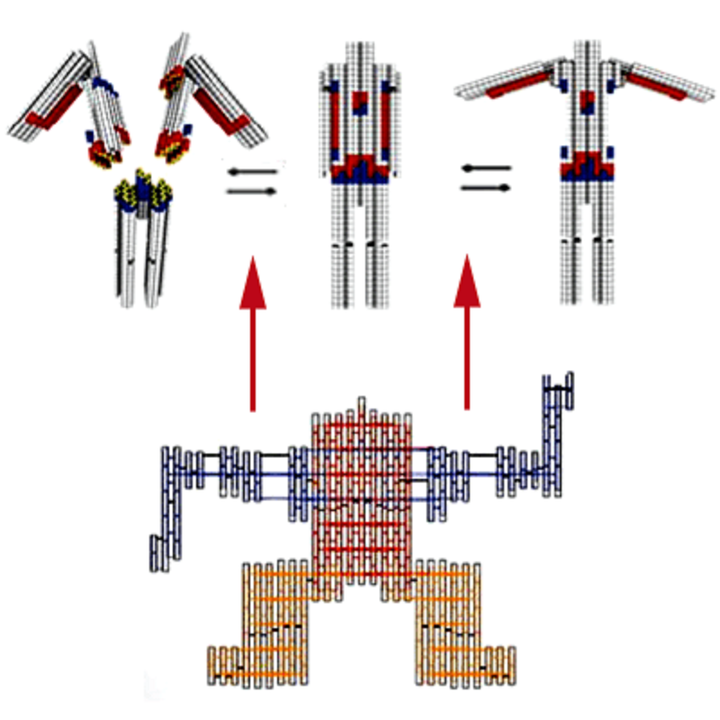
1246Немецкие ученые расширили возможности молекулярной инженерии, применив для сборки структур из ДНК стэкинг концов двойных спиралей. С помощью этих относительно слабых взаимодействий можно соединять отдельные блоки из ДНК, и, что важно, такие соединения будут обратимыми. Используя лабильные контакты для соединения отдельных блоков, можно управлять их сборкой и манипулировать формой конструкции.
-
Развитие биотехнологий открыло новые возможности использования живых организмов на благо человечества. Методы генетической инженерии позволяют производить различные вещества в живых объектах, следовательно, мы можем использовать эти объекты в качестве природных «фабрик». Центральная догма молекулярной биологии в общем случае гласит: ДНК → РНК → белок. Именно белок часто является конечным продуктом биотехнологического производства: это может быть инсулин, интерфероны, антитела, ферменты, вакцины... Нам лишь нужно задать программу и «записать» ее в ДНК, а живой объект всё сделает сам. В качестве «фабрик» используют клетки дрожжей, бактерий, растений, а также культуры клеток насекомых и млекопитающих. В этой статье речь пойдет о растительных биофабриках.
-
ДНК-вакцины относятся к типу принципиально новых биологических препаратов. С их разработкой связывают большие надежды на повышение эффективности профилактики не только заболеваний бактериальной, вирусной и паразитарной природы, но и аллергических, аутоиммунных и даже онкологических болезней. Более двадцати лет назад возникла идея использовать гены возбудителей заболеваний для активации защитных механизмов. Конструкция ДНК-вакцин гениально проста: главные компоненты в ней — вектор и целевой иммуноген. Но, несмотря на это, ДНК-вакцины не стоят на страже нашего здоровья: их не вводят пациентам в поликлиниках, они не продаются в аптеках...
-
Ученые установили связь между стресс-индуцируемым гемопоэзом, возникновением повреждений ДНК в стволовых клетках крови, истощением их запаса и нарушениями в их функционировании. Оказывается, если в организме постоянно возникают инфекции или травмы, то постепенно в ДНК стволовых клеток крови накапливаются повреждения. Они приводят к истощению запасов стволовых клеток и, следовательно, к «старению» кроветворной системы. А в случае, если в системах репарации повреждений ДНК есть дефекты (как, например, при редком заболевании — анемии Фанкони), то истощение запаса стволовых клеток наступает гораздо быстрее.
-
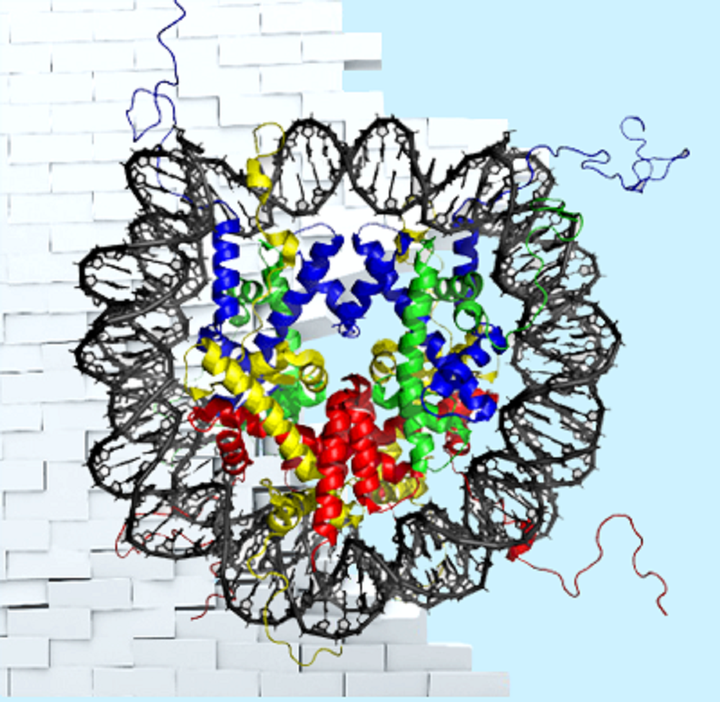
Перед РНК-полимеразой стоит сложная задача реализации генетической информации путем осуществления транскрипции. На своем пути фермент встречает массу препятствий. ДНК находится в комплексе с белками и плотно упакована, образуя нуклеосомы, которые создают барьер для полимераз, но несут важные регуляторные сигналы. Так как же транскрипционная машина проходит через нуклеосомы?
-
Давайте поговорим о роли слабых взаимодействий в биологических макромолекулах. Хотя они и слабые, их влияние на живые организмы отнюдь не ничтожно. Скромный набор видов слабых связей в биополимерах обусловливает всё многообразие биологических процессов, на первый взгляд никак не связанных между собой: передачу наследственной информации, ферментативный катализ, обеспечение целостности организма, работу природных молекулярных машин. А определение «слабые» не должно вводить в заблуждение — роль этих взаимодействий колоссальна.
-
Ученые получили трансгенные растения, в хлоропластах которых образуется двухцепочечная РНК, нарушающая работу жизненно важного гена колорадского жука — гена белка цитоскелета β-актина. Все личинки жуков, которые в эксперименте питались листьями таких растений, погибали в течение пяти дней. В то же время разработанный подход высокоселективен в отношении вредителя и безопасен для опылителей.
-
Словосочетание «генная инженерия» прочно вошло в лексикон нашего времени. Существуют тысячи генно-модифицированных организмов, идет речь о генной терапии наследственных заболеваний, «редактирование» геномов ведется в тысячах лабораторий по всему миру. Первый шаг на этом пути сделал человек, и поныне живущий на Земле. В следующем году создатель первой в мире рекомбинантной ДНК — Пол Берг — будет праздновать 90-летие, а в этом — 35-летие присуждения ему Нобелевской премии. Формулировка Нобелевского комитета: «за фундаментальные исследования биохимических свойств нуклеиновых кислот, в особенности рекомбинантных ДНК». Сама же генная инженерия постепенно приближается к своему полувековому юбилею, который мировая наука отметит в 2022 году.


- Лента
- Спецпроекты
- ▶Подкаст
-
Конкурс
- О конкурсе «Био/мол/текст»
- «Био/мол/текст»-2025/2026
- «Био/мол/текст»-2024/2025
- «Био/мол/текст»-2023/2024
- «Био/мол/текст»-2022/2023
- «Био/мол/текст»-2021/2022
- «Био/мол/текст»-2020/2021
- «Био/мол/текст»-2019
- «Био/мол/текст»-2018
- «Био/мол/текст»-2017
- «Био/мол/текст»-2016
- «Био/мол/текст»-2015
- «Био/мол/текст»-2014
- «Био/мол/текст»-2013
- «Био/мол/текст»-2012
- «Био/мол/текст»-2011
- Объявления
- Авторы
- Партнеры
- Поддержать
Публикации
—
Темы
—
Авторы
—
Комментарии
—
Поиск не дал результатов
По вашему запросу ничего не найдено
- Медицина
- SARS-CoV-2
- «Биомолекула» — Forbes
- Аллергия
- Антибиотики
- Атеросклероз
- Аутоиммунитет
- Боль
- ВИЧ/СПИД
- Вакцины
- Вирус Зика
- Вирус Эбола
- Генная терапия
- Грипп
- Депрессия
- Дерматология
- Диагностика
- Здравоохранение
- Нейродегенерация
- Никотин
- Онкология
- Персонализированная медицина
- Питание
- Сон
- Стволовые клетки
- Фармакология
- Эпилепсия
- Биология
- «Сухая» биология
- Антропология
- Бионика
- Биофизика
- Вирусология
- Вопросы пола
- ГМО
- Генетика
- Иммунология
- Микробиология
- Нейробиология
- Носимые технологии
- Психогенетика
- Синтетическая биология
- Старение
- Структурная биология
- Цитология
- Эволюционная биология
- Экология
- Эмбриология
- Эпигенетика
- Этология
- Биомолекулы
- GPCR
- АФК
- Амилоиды
- Биомембраны
- Гормоны растений
- ДНК
- Ионные каналы
- МГЭ
- Матрикс
- Нейромедиаторы
- РНК
- Рецепторы
- Хроматин