-
327Статья на конкурс «Био/Мол/Текст»: Глобальный кризис антибиотикорезистентности заставляет науку искать новые пути борьбы с бактериальными инфекциями. Оказалось, что самое совершенное оружие против бактерий создала сама природа — это бактериофаги. Но сегодня ученые берут на вооружение не целые вирусы, а их высокоспециализированные белки. В этой статье мы рассмотрим, как эти молекулярные «инструменты» — от «отмычек», вскрывающих бактериальную защиту, до «подрывных зарядов», разрушающих клетку изнутри, — становятся основой для лекарств нового поколения, систем целевой доставки и биотехнологических платформ, открывая новую эру в борьбе с инфекциями.
-
282Статья на конкурс «Био/Мол/Текст»: В современном мире все больше и больше интереса вызывает генная инженерия для лечения рака, то есть болезней, которые основаны на бесконтрольном делении клеток, приводящих к образованию опухолей [1]. Одно из последних решений — CAR-T терапия — генетическая модификация Т-лимфоцитов, превращающая их в метких «снайперов» для раковых клеток [2]. Но каждая опухоль индивидуальна и такая терапия не всегда может быть эффективной, а также имеет большие риски. Поэтому исследователи постоянно ищут новые пути, и один из них — создание нового варианта генной терапии — CAR-NK. В отличие от Т-лимфоцитов NK клеткам не нужно узнавать антиген через антигенпрезентирующие клетки, они реагируют на подозрительные молекулы в мембране клетки. Помимо этого, NK-клетки являются аллогенным продуктом — их можно забирать от здорового донора и вводить пациенту, в отличие от Т-лимфоцитов, которые аутологичны — забираются от пациента, модифицируются и возвращаются ему же. В данной статье рассматривается сравнение обеих терапий, идея CAR-NK и ее перспективы.
-
258Статья на конкурс «Био/Мол/Текст»: Слияние мозга с компьютером — заветная мечта футурологов и центральный образ киберпанка. Но на пути к ней стоит не технический, а биологический барьер: наш собственный мозг. Он воспринимает имплантаты как угрозу и изолирует их непроницаемым рубцом из глиальных клеток, обрекая интерфейсы на короткую жизнь. В этом обзоре мы покажем, что прорыв возможен только на острие нейробиологии, материаловедения и биоинженерии. Будущее — за «невидимыми» ультрамягкими имплантатами, щадящей хирургией и точечным контролем воспаления. Победим ли мы в этой войне с иммунитетом? От ответа зависит не только медицина будущего, но и сама возможность превратить человека в киборга.
-
128Статья на конкурс «Био/Мол/Текст»: Микрокапсулы — полые полимерные сферы размером от десятков нанометров до десятков микрометров — превратились из экзотической лабораторной технологии в универсальный инструмент для медицины, диагностики и биотехнологии. О том, что это за технология и как исследователям удалось превратить микрокапсулы в миниатюрные хранилища, лекарственные носители и элементы химического «мышления», читайте в этой статье.
-
217Статья на конкурс «Био/Мол/Текст»: Как человек запоминает важные встречи, лица и детали, так и бактерии хранят «память» о своих самых опасных врагах. Такой памятью служит система CRISPR-Cas, фиксирующая следы прошлых атак бактериофагов. Анализируя эти генетические «воспоминания», можно восстановить историю взаимодействий бактерии с фагами и понять, какие из них представляли для нее наибольшую угрозу. В этой статье мы расскажем о том, как по структуре CRISPR-Cas систем бактерии Clostridium botulinum можно реконструировать ее фаговое прошлое и почему это знание важно для развития более точных и безопасных подходов к фаготерапии в эпоху снижающейся эффективности антибиотиков.
-
402Статья на конкурс «Био/Мол/Текст»: Генетический код — это своего рода «язык», на котором записана информация о том, как устроены живые организмы. Почти у всех организмов этот язык устроен одинаково. В работе Escherichia coli with a 57-codon genetic code, опубликованной в журнале Science в 2025 году, о которой пойдет речь в этой статье, ученые показали, что этот язык можно существенно переписать. Генетический «язык» содержит много синонимов: одну и ту же аминокислоту могут кодировать разные кодоны. Авторы статьи задались вопросом: можно ли переписать геном так, чтобы часть этих синонимов исчезла? Для этого они создали бактерию Escherichia coli с полностью синтетическим геномом, в котором несколько кодонов были заменены синонимичными вариантами. В результате количество используемых кодонов сократилось с 64 до 57. Полученный организм назвали Syn57. С практической точки зрения такая перекодировка позволяет «освободить» часть кодонов и использовать их для задач биотехнологии и фармацевтики, например, для включения в белки новых, необычных аминокислот. Но не менее важно и фундаментальное значение этой работы: эксперимент показывает, что генетический код гораздо гибче, чем считалось раньше, и помогает лучше понять, как он мог возникнуть в ходе эволюции.
-
157В популярной культуре еда обычно остается чем-то очевидным и почти не требующим объяснений: хлеб выпекают, сыр созревает, овощи растут на грядках, а мясо появляется на полке супермаркета. Однако за этой кажущейся простотой скрывается огромная технологическая и научная история. Книга редактора «Биомолекулы» Анастасии Волчок предлагает заглянуть в эту скрытую часть пищевой индустрии — туда, где кухня встречается с лабораторией.
-
276Статья на конкурс «Био/Мол/Текст»: Попав в биологическую среду — например, в кровь — наночастица тут же покрывается белковой короной. Такая корона кардинально меняет поведение и характеристики частицы: у нее появляется новая идентичность. Ученые, работающие с наночастицами, попали в сложную ситуацию: то ли попытаться помешать формированию короны, то ли пойти другим путем — использовать корону в собственных целях. О том, какой путь они выбрали, мы расскажем в нашей статье.
-
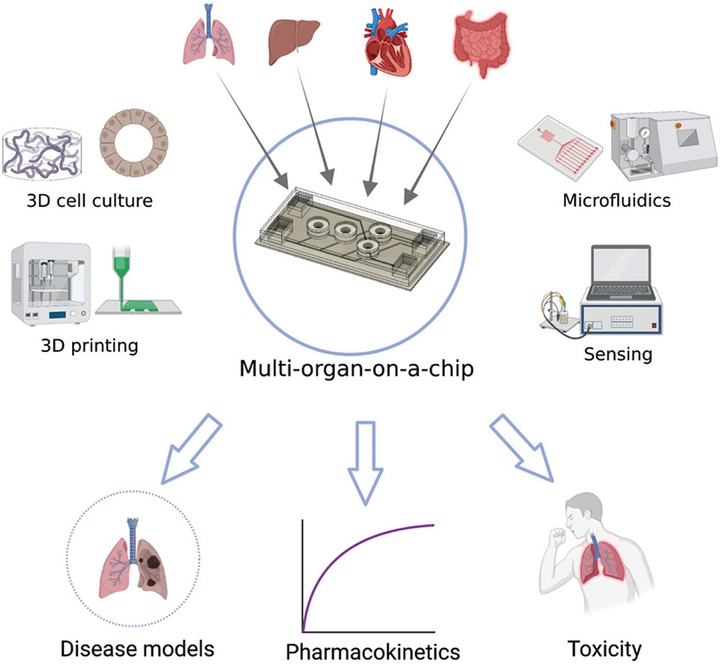
313Статья на конкурс «Био/Мол/Текст»: Микрофлюидика, наука о движении жидкостей в микроканалах, за последние десятилетия превратилась из академического эксперимента в одну из самых перспективных технологий современной биомедицины. «Лаборатория-на-чипе» позволяет объединять сложные процессы — от получения образца до обработки результата — на миниатюрных платформах, помещающихся на ладони. В данном обзоре рассматривается эволюция микрофлюидных систем от первых устройств 1970-х годов до современных моделей «орган-на-чипе», а также новые области применения в контексте 3D-печати и тканевой инженерии. Отдельное внимание уделено диагностическому направлению — микрофлюидные чипы уже используются для секвенирования, молекулярной детекции и экспресс-анализов. Микрофлюидика демонстрирует, как на стыке физики, химии и биологии рождается новая логика лабораторных исследований: от массивных приборов к автономным системам, где миллионы реакций могут происходить в капле жидкости одновременно.
-
Статья на конкурс «Био/Мол/Текст»: В статье описаны последние исследования в области восстановления зрения, результатом которых стала разработка лекарственного препарата на основе моноклональных антител к белку, предотвращающему регенерацию глиальных клеткок сетчатки — клеток Мюллера. Слепоту можно победить?


- Лента
- Спецпроекты
- ▶Подкаст
-
Конкурс
- О конкурсе «Био/мол/текст»
- «Био/мол/текст»-2025/2026
- «Био/мол/текст»-2024/2025
- «Био/мол/текст»-2023/2024
- «Био/мол/текст»-2022/2023
- «Био/мол/текст»-2021/2022
- «Био/мол/текст»-2020/2021
- «Био/мол/текст»-2019
- «Био/мол/текст»-2018
- «Био/мол/текст»-2017
- «Био/мол/текст»-2016
- «Био/мол/текст»-2015
- «Био/мол/текст»-2014
- «Био/мол/текст»-2013
- «Био/мол/текст»-2012
- «Био/мол/текст»-2011
- Объявления
- Авторы
- Партнеры
- Поддержать
Публикации
—
Темы
—
Авторы
—
Комментарии
—
Поиск не дал результатов
По вашему запросу ничего не найдено
- Медицина
- SARS-CoV-2
- «Биомолекула» — Forbes
- Аллергия
- Антибиотики
- Атеросклероз
- Аутоиммунитет
- Боль
- ВИЧ/СПИД
- Вакцины
- Вирус Зика
- Вирус Эбола
- Генная терапия
- Грипп
- Депрессия
- Дерматология
- Диагностика
- Здравоохранение
- Нейродегенерация
- Никотин
- Онкология
- Персонализированная медицина
- Питание
- Сон
- Стволовые клетки
- Фармакология
- Эпилепсия
- Биология
- «Сухая» биология
- Антропология
- Бионика
- Биофизика
- Вирусология
- Вопросы пола
- ГМО
- Генетика
- Иммунология
- Микробиология
- Нейробиология
- Носимые технологии
- Психогенетика
- Синтетическая биология
- Старение
- Структурная биология
- Цитология
- Эволюционная биология
- Экология
- Эмбриология
- Эпигенетика
- Этология
- Биомолекулы
- GPCR
- АФК
- Амилоиды
- Биомембраны
- Гормоны растений
- ДНК
- Ионные каналы
- МГЭ
- Матрикс
- Нейромедиаторы
- РНК
- Рецепторы
- Хроматин