-
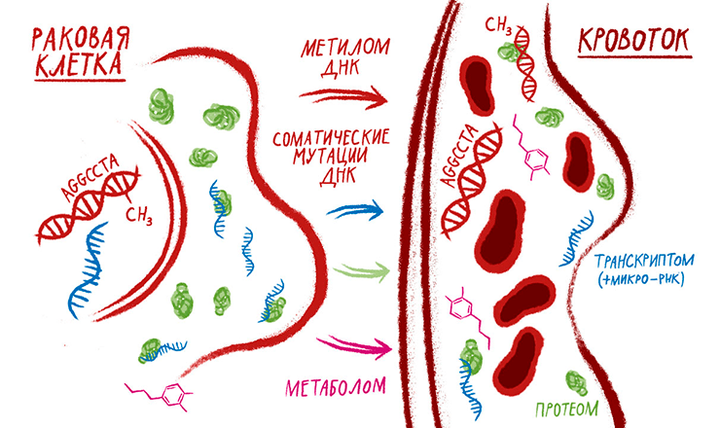
Одна из важных целей омикс-технологий (в том числе транскриптомики, протеомики, метаболомики) в медицине — это поиск биомаркеров для диагностики распространенных неинфекционных заболеваний, в основном злокачественных опухолей. Часто говорят о ранней диагностике, то есть о тех случаях, когда болезнь выявляют впервые и на ранней стадии. Но всегда ли имеет смысл использовать молекулярные технологии для поиска ранних маркеров? Я хочу поговорить о том, какие параметры характеризуют молекулярные биомаркеры и их сочетания, для каких случаев их следует разрабатывать, а также рассказать о десятилетии развития постгеномных технологий в медицине и о собственном опыте в протеомике рака. Этот материал адресован в основном биологам и физикам, которые занимаются омикс-технологиями, но не всегда вдаются в медицинские подробности. Он поможет им избежать бесполезной работы с точки зрения постановки клинической задачи.
-
287Свежие номера авторитетных научных журналов будут особенно интересны любителям древностей: в них можно прочесть об исследовании геномов древних жителей Исландии и Америки, о древнейшей чешуйчатой рептилии, о толерантности к уровню солености воды у девонских позвоночных и о восстановлении экосистем после падения метеорита на рубеже мелового и палеогенового периодов. А еще вы узнаете, как помочь мышам разлюбить сладкое, как заставить единичные клетки объединяться в многоклеточные агрегаты и почему у скатов электрическая чувствительность точнее, чем у акул, и позволяет им отличать других скатов от потенциальных жертв.
-
Современные технологии преображают жизнь ученых и работу в научной лаборатории. Приборы, реактивы, технологии меняются на глазах, и уже сейчас лаборатории 20-летней давности кажутся неимоверно устаревшими, а научная лаборатория середины XX века вполне может быть выставлена в экспозиции исторического музея наряду с мастерской алхимика. Технологии не стоят на месте, и на рынок научных приборов выходят небольшие, по сравнению с «монстрами-монополистами», компании, которые активно внедряют новые подходы к работе с научным оборудованием. Партнер этой публикации фирма «Аламед» как раз и работает с такими компаниями-инноваторами (ACEA Biosciences, Logos Biosystems, Sony Biotechnology и др.): мы постараемся на их примере показать, как новые технологии меняют работу ученых.
-
Биология — одна из самых быстро развивающихся наук современности. Ее успехи за последние десятилетия полностью изменили мир и даже позволили нам приблизиться к мечте о победе над смертельными заболеваниями. Однако за столь быстрыми изменениями в технологиях не всегда успевает система образования и подготовки новых специалистов. О том, чему нужно учиться современным биологам, чтобы найти и сохранить свое место в биотехе через пять–десять лет, мы поговорили с Хайнцем Шмидтом, директором российского отделения фармацевтической компании Merck.
-
Сегодня BIOCAD — одна из крупнейших российских фармацевтических компаний, специализирующаяся в том числе на разработке терапевтических моноклональных антител. Департамент вычислительной биологии (ДВБ) занимается биоинформатическим моделированием этих молекул, тем самым оптимизируя их разработку. Тому, как устроена компания в целом и ДВБ в частности, посвящена заключительная статья спецпроекта о терапевтических антителах.
-
Комикс на конкурс «био/мол/текст»: Давным-давно, в далекой-далекой Галактике... Нет, на самом деле, каждую секунду в каждом человеческом организме... Идет освободительная война. Космические корабли защитников Галактики одержали первую победу в битве со зловещими захватчиками. Во время сражения разведчикам защитников удалось заполучить образцы секретного оружия, способного уничтожить целую Галактику. Эти образцы помогут обнаружить вражеские корабли. Воодушевленные успехом, защитники собирают космический флот, чтобы дать захватчикам решительный отпор.
-
Иммунология — одна из самых «прикладных» и «практичных» биологических дисциплин, и эпидемия COVID-19 позволила лишний раз в этом убедиться. Одновременно это, пожалуй, один из самых сложных разделов науки о живом. В реализации иммунного ответа задействованы десятки разных типов клеток; сотни белков-лигандов: цитокинов, хемокинов; тысячи генов. Приложение методов системной биологии к решению иммунологических задач породило самостоятельную дисциплину — системную иммунологию. В третьей статье цикла «Пятерка по системной биологии» мы увидим, как методы системной биологии помогают разобраться в фундаментальных и прикладных аспектах Т-клеточного ответа.
-
Миллионы человек во всем мире живут в ожидании. Они знают, что множество ученых занято разработкой новых лекарств, которые должны помочь жить лучше, ярче и дольше... В третьей, заключительной статье спецпроекта «Открытые инновации» медицинский директор Bayer и руководитель Медицинского кластера стран СНГ Дмитрий Власов рассказывает, на чем сосредоточен фокус внимания исследователей сегодня и что делается для развития инновационной экосистемы в мире и в нашей стране.
-
Доклинические исследования (доКИ) лекарств нужны в первую очередь для подтверждения безопасности новых препаратов, чтобы в последующих клинических исследованиях не пострадали люди. Для этого ученые используют как животные модели, так и культуры клеток. И пусть пока доКИ не обходятся без экспериментов in vivo, работа с клеточными культурами уже сейчас является их неотъемлемой частью. В этой статье спецпроекта о будущем доклинических исследований мы совершим «путешествие к центру организма» — речь здесь пойдет именно о клетках.
-
305На этой неделе нас ждет погружение в полногеномный поиск ассоциаций с помощью метода GWAS: это поможет отслеживать мутации, связанные с аутоиммунными заболеваниями, а также изучать некодирующую часть генома. Также мы познакомимся с возможностями архитектурного моделирования растений, сравним способы навигации в городах и найдем корреляцию между названием статьи и ее цитированием.
-
1268Из новых номеров Nature и Science вы узнаете о том, откуда мы получаем свой первый в жизни иммунитет, благодаря чему мы чувствуем, что заболеваем, полезно ли голодать и о новом лекарстве против болезни Паркинсона. А еще заглянем одним глазом в процесс мейоза и немного поговорим о прививках против обезьяньей оспы, эволюции картофеля, приручении кур, грибах-паразитах и морских вирусах.
-
Книга врача-гематолога Марка Бугаертса из Нидерландов могла бы стать элегантной и увлекательной публикацией, прослеживающей историю человечества по крови в прямом смысле: через образы крови в искусстве, кровавые исторические события и до изучения крови в науке. Однако, несмотря на богатый материал и хорошую научную базу автора, эту книгу не хочется рекомендовать для чтения. Подробности в самой рецензии.


- Лента
- Спецпроекты
- ▶Подкаст
-
Конкурс
- О конкурсе «Био/мол/текст»
- «Био/мол/текст»-2025/2026
- «Био/мол/текст»-2024/2025
- «Био/мол/текст»-2023/2024
- «Био/мол/текст»-2022/2023
- «Био/мол/текст»-2021/2022
- «Био/мол/текст»-2020/2021
- «Био/мол/текст»-2019
- «Био/мол/текст»-2018
- «Био/мол/текст»-2017
- «Био/мол/текст»-2016
- «Био/мол/текст»-2015
- «Био/мол/текст»-2014
- «Био/мол/текст»-2013
- «Био/мол/текст»-2012
- «Био/мол/текст»-2011
- Объявления
- Авторы
- Партнеры
- Поддержать
Публикации
—
Темы
—
Авторы
—
Комментарии
—
Поиск не дал результатов
По вашему запросу ничего не найдено
- Медицина
- SARS-CoV-2
- «Биомолекула» — Forbes
- Аллергия
- Антибиотики
- Атеросклероз
- Аутоиммунитет
- Боль
- ВИЧ/СПИД
- Вакцины
- Вирус Зика
- Вирус Эбола
- Генная терапия
- Грипп
- Депрессия
- Дерматология
- Диагностика
- Здравоохранение
- Нейродегенерация
- Никотин
- Онкология
- Персонализированная медицина
- Питание
- Сон
- Стволовые клетки
- Фармакология
- Эпилепсия
- Биология
- «Сухая» биология
- Антропология
- Бионика
- Биофизика
- Вирусология
- Вопросы пола
- ГМО
- Генетика
- Иммунология
- Микробиология
- Нейробиология
- Носимые технологии
- Психогенетика
- Синтетическая биология
- Старение
- Структурная биология
- Цитология
- Эволюционная биология
- Экология
- Эмбриология
- Эпигенетика
- Этология
- Биомолекулы
- GPCR
- АФК
- Амилоиды
- Биомембраны
- Гормоны растений
- ДНК
- Ионные каналы
- МГЭ
- Матрикс
- Нейромедиаторы
- РНК
- Рецепторы
- Хроматин