Нанотехнологии — новый союзник в войне с болезнями
16 октября 2017
Нанотехнологии — новый союзник в войне с болезнями
- 5020
- 3
- 8
Нанотехнологии спешат на помощь
-
Автор
-
Редакторы
Статья на конкурс «био/мол/текст»: Наука XXI века развивается семимильными шагами. В недалеком будущем нанотехнологиям будет отводиться решающая роль. Наши нынешние методы лечения не всегда действенны: хирургия слишком груба, а лекарства зачастую слишком примитивны, неизбирательны и малоэффективны. Но наука не стоит на месте, и по всему миру ученые активно разрабатывают новые и эффективные подходы к прицельной доставке лекарств, чтобы улучшить результаты лечения и снизить побочные эффекты. Именно эти достижения и хотелось бы вынести из лабораторных кулуаров на всеобщее обозрение. Речь пойдет о нанотехнологиях в медицине. Это слово, в свете последних государственных инициатив, знакомо даже школьникам.
Конкурс «био/мол/текст»-2017
Эта работа опубликована в номинации «Биомедицина сегодня и завтра» конкурса «био/мол/текст»-2017.

Генеральный спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

Спонсором приза зрительских симпатий и партнером номинации «Биомедицина сегодня и завтра» выступила фирма «Инвитро».

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Нанотехнология принесет фундаментальный прорыв в медицине.
Эрик Дрекслер
С чем мы имеем дело?
Приставка «нано», добавляемая к названию описываемых объектов, означает, что они имеют размеры в пределах нескольких миллиардных долей метра (10–9 м), что соответствует молекулярному уровню организации жизни.
Нанотехнологии — это наука, инженерия и технологии, действующие на наноуровне (от 1 до 100 нанометров). По сути, это манипулирование и управление материалами на атомном и молекулярном уровнях. Под наночастицами же понимают конкретные молекулярные конструкции, которые можно разделить на несколько классов:
- Естественные наночастицы. Живой мир наводнен своеобразными наночастицами, выдуманными самой природой. В первую очередь, это молекулы белков, ДНК, вирусы и тому подобное. Яркий пример таких частиц — липосомы (липидные пузырьки, «подражающие» природным везикулам внутри клеток), которые могут формироваться при определенных условиях из раствора смеси липидов. Впервые на них обратил внимание англичанин Алек Бангем, в 1965 году заметивший, что они похожи на мембраны клеток . Тогда липосомы сразу же стали удобной экспериментальной моделью для их изучения. Так, они позволили исследовать проницаемость мембран и действие на них тех или иных веществ. Оказывается, липосомы хорошо переносят лекарства, а значит, могут найти применение в медицине [1], [2]. Пригодны для этого и созданные природой наночастицы — например, вирусы, часто используемые для геннетической модификации клеток. Аденовирусы с убранной функцией размножения могут быть использованы и для вакцинации [3], [4].
- Полимерные наночастицы создают из больших молекул (полимеров), которые имеют ряд преимуществ, определяющих эффективность их применения в прицельной доставке лекарств, — способность не вызывать ответ иммунной системы и разлагаться в организме. Ученые из Техаса предположили, что большую избирательность в борьбе с врагом показывают белки бактериофагов (вирусов, поражающих бактерий и безвредных для человека) [7]. Они получили три наночастицы, имитирующие строение фагов: сферу в 8 нанометров и два стержня длиной один 18, другой — 70 нм. Все три частицы испытали на активность по отношению к бактерии Escherichia coli (рис. 1) и на токсичность в отношении клеток крови. Оказалось, что наиболее эффективны «сферы» — чтобы убить почти все бактерии, нужно не более 32 мкг/мл таких частиц, — и что все три частицы безопасны для клеток крови. Такое лечение не будет вызывать у бактерий адаптации.
- Дендримеры — уникальный класс полимеров с сильно разветвленной структурой. При этом их размер и форма могут быть точно заданы при синтезе. Такие молекулы сейчас получают из меньших молекул, проводя их соединение, задавая характер ветвления. Контролируемые размеры и свойства такой большой молекулы, а также стабильность делают ее вполне пригодной для переноски лекарств [9], [10].
- Углеродные нанотрубки. Когда речь заходит о нанотехнологиях, их почти всегда упоминают в связи с необычными свойствами и прочностью, в триста раз превосходящей сталь (рис. 2). У нанотрубок есть огромный потенциал для диагностики и лечения рака, за разработку которого взялась компания CARBIO. Согласно их плану, лекарства будут надежно изолированы оболочкой, которая препятствует взаимодействию со здоровыми тканями, чтобы «всем весом» атаковать болезнь.
- Неорганические наночастицы. К ним относят структуры на основе оксида кремния или различных металлов, использование которых позволяет создавать переносчики, обладающие рядом уникальных свойств. Подробнее о том, как работают такие частицы, читайте здесь: «„Мал золотник, да дорог“, или об использовании золотых наночастиц в бионанотехнологиях» [11] и «Наномеханика для адресной доставки лекарств — насколько это реально?» [12]. А в моей статье мы остановимся на том, что нового прибавилось с момента написания той статьи в знаниях ученых.
- Нанороботы. Люди давно мечтали о крошечных роботах, которые перемещаются по обширной системе кровообращения организма, словно космические корабли. Потенциал, казалось, огромен: крошечные роботы могли бы, например, передавать радиоактивные препараты в раковые скопления, выполнять операции внутри тела или очищать сгустки крови, находящиеся глубоко внутри сердца или мозга, менять гены, погружаться прямо в кровоток, выжигать лазером все на своем пути, стирать воспоминания, добавлять навыки... Однако есть одно «но» — такие роботы по большей части являются фантазией писателей. Сейчас концепция переработана, и нынешние наниты уже не похожи на те «космические корабли», о которых велась речь в книгах. Они скорее напоминают обычные наночастицы.
О биологических мембранах и гидрофобном эффекте, лежащем в основе как самих мембран, так и везикул и липосом, читайте в статьях «Липидный фундамент жизни» [5] и «Физическая водобоязнь» [6]. — Ред.
Подробнее о применении вирусов в наномедицине читайте в статье «Вирусы-платформы: яд во благо» [8]. — Ред.

Рисунок 1. Микроскопические изображения E. coli. а — Контрольный образец. б—г — Образцы с наночастицами: длинным стержнем (б), коротким стержнем (в) и сферой (г). Нарушение целостности оболочки бактерий проявляется уже через 200 секунд после начала процедуры над E. coli с частицами в форме сферы и короткого стержня.
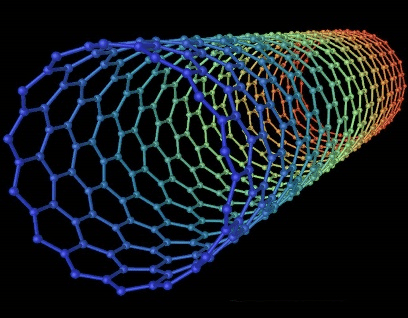
Рисунок 2. Структура углеродной нанотрубки
Что мы уже умеем делать в этой области?
Против газовых атак
Некоторые вещества очень вредны для здоровья, и злоумышленники с незапамятных времен используют их в качестве оружия. Они могут влиять на нервную, дыхательную и кровеносную системы, кожу, а также на психику жертвы.
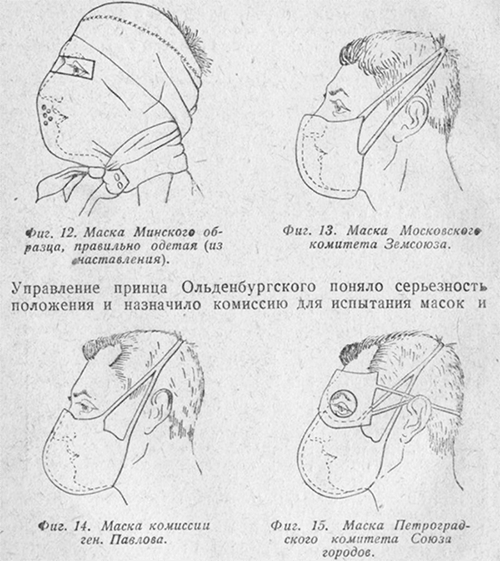
Первым химическим оружием стал хлор, использовавшийся немцами еще в Первой мировой войне (рис. 3). Его действие основано на образовании соляной кислоты при контакте с парами воды (которые всегда есть возле человека). При вдыхании кислота разъедает легкие, что ведет к смерти [14]. Для союзников газовые атаки были неожиданными. После первых атак началась лихорадочная разработка средств защиты. Никто не знал, как их шить, поэтому качество первых масок оставляло желать лучшего (рис. 4).
В 1938 году немцы синтезировали еще более токсичное вещество — зарин. В 1944-м открыли еще более токсичный и стойкий зоман. Эти вещества оказывают нервно-паралитическое действие и вызывают отравление при вдыхании и даже при попадании на кожу [15]. Объектом поражения зарина и других нервнопаралитических веществ является нервная система. При стимуляции нейронов в синапсе происходит выброс нейромедиатора ацетилхолина [16], благодаря чему производится передача импульса к мышце или органу. В норме после передачи импульса ацетилхолин расщепляется, и передача прекращается. Однако зарин уничтожает фермент, расщепляющий ацетилхолин, из-за чего его содержание растет, и возбуждающие сигналы непрерывно передаются, приводя органы к истощению [17].
Несмотря на то, что во Второй мировой у немцев были снаряды с зарином и зоманом, а также лаборатории по их созданию, это оружие Вермахт так и не применил. Такие вещества нашли военное применение лишь в середине XX столетия, когда создали самые опасные виды этих газов — британский VX (его создали как пестицид, но потом выяснилось, насколько он опасен, и передали на военные цели) и советский VR. Все запасы VX, VR, зарина и прочих боевых газов подлежат уничтожению в соответствии с Конвенцией 1997 года, но только две страны — Россия и США — признали наличие их у себя. Запасы этих газов есть, однако, и в ряде стран Ближнего Востока.
Поэтому проблема нейтрализации этих ядов по-прежнему важна. Российские химики предлагают использовать наночастицы, созданные группой Кабанова в 1990-х. Это пустые частицы, которые обычно в качестве «начинки» имеют лекарство, но команда Кабанова приспособила эти частицы для упаковки и доставки иной «начинки» — фермента, разработанного для нейтрализации зарина и прочих газов .
Об антидоте зомана и циклозарина читайте в статье «„Дизайнерские“ ферменты защищают от нервно-паралитических ядов» [18]. — Ред.
Это соединение и без наночастиц активно разрушает молекулы боевых газов, но при этом обладает одним недостатком — молекулы его быстро разрушаются иммунной системой, да и сам по себе он нестабилен и его запасы почти полностью распадаются всего за месяц.
«Загрузив» молекулы фермента в наночастицы, ученые замедлили процесс его разрушения, что позволило сделать фермент пригодным для защиты от химикатов. В таком виде противоядие можно хранить более трех лет, что лучше, чем у чистого фермента. Работу этих наночастиц проверили на крысах, в организм которых вводили смертельные количества яда VX. Введение наночастиц перед этим спасло 80% животных от яда, тогда как все особи из контрольной группы погибли [19].
Простота и технологичность подхода в сочетании с результатами дают надежду на то, что этот препарат может быть успешным и на людях. К примеру, наличие подобного лекарства у врачей во время терактов в Дамаске в 2013 году, когда боевики-исламисты применили зарин против мирного населения, могло спасти сотни людей.
Инновационное похудение
Сейчас ожирение сравнивают с глобальной эпидемией, ведь это заболевание может коснуться людей всех возрастов и рас. По статистике примерно 30% населения нашей страны страдают от той или иной степени ожирения .
Кстати, на стройность фигуры в большой степени влияет микробиом кишечника: «Почему так сложно похудеть, или Влияние кишечной микробиоты на метаболизм» [20]. — Ред.
Есть много методов борьбы с ожирением, но оптимального решения пока не найдено. Диеты и нагрузки малоэффективны, а расщепление жира при помощи специальных препаратов имеет побочные эффекты, так как действует на весь организм. Действие некоторых препаратов направлено на превращение белого жира в бурый, который намного быстрее переходит в энергию. Эта идея показалась перспективной ученым из США и Китая, которые придумали, как избавиться от побочных эффектов: медикаменты должны действовать локально, и если поместить их прямо на «проблемные зоны», они не принесут вреда.
Для этого разработали пластырь, содержащий наночастицы с «грузом» нужного препарата [21]. Это был препарат Rosi, стимулирующий рецепторы PPARγ (peroxisome proliferator activated receptor gamma), запускающие жиросжигание. Пластырь с десятками крошечных микроигл крепится на кожу, иглы проникают в ткани, разлагаются в течение трех дней и высвобождают препарат в кожу (рис. 5).
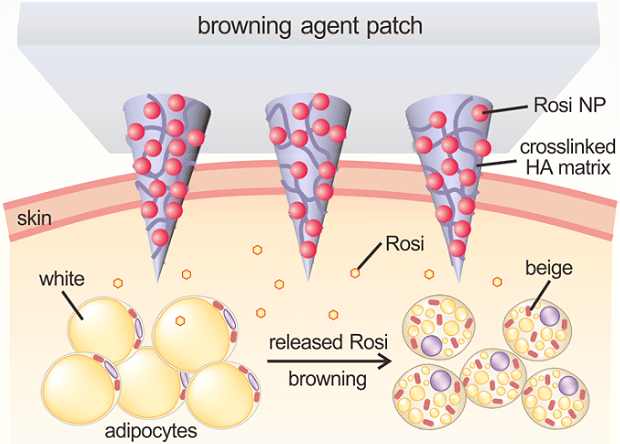
Рисунок 5. Схема действия нанопластыря. Иглы содержат частицы препарата (розовые шарики), связанные между собой матрицей. По мере разрушения игл, препарат высвобождается в ткани (желтые маленькие круги), действует на белые жировые клетки (слева внизу), способствуя их превращению в бурый жир (справа внизу).
Затем ученые протестировали пластырь на обычных и толстых мышах. Здоровых мышей разделили на три группы по шесть особей в каждой и прикрепили пластырь в паховой области. Пластырь либо содержал один из препаратов (совместно с Rosi использовали CL 316243, действующий по иному механизму), либо был пустым (в контрольной группе). У мышей с ожирением на каждую особь крепили по два пластыря, один из которых был пустым, а другой содержал препарат. Контрольная группа носила два пустых пластыря. За три дня пластырь высвобождал свое содержимое в ткани, и его меняли на новый. Это повторялось четыре недели.
Всё это время ученые следили за метаболизмом животных, оценивали их вес, аппетит, активность. После лечения проверили уровень глюкозы в крови и другие показатели. Сброс лишнего веса привел к положительным эффектам — уровень сахара в крови грызунов заметно снизился, их организм начал лучше реагировать на инсулин, они стали более активны.
Многие будут, несомненно, рады тому, что создали менее болезненную и более безопасную альтернативу липосакции. Что самое главное, эту методику можно применять не только для лечения ожирения, но и для борьбы с диабетом и другими расстройствами. Результаты показывают, что такая форма лечения более эффективна в борьбе с ожирением, так как его действие распространяется строго на обработанный участок. В будущем этот метод могут одобрить, а пока авторы ищут более эффективный препарат.
Кость на нанотрубке
Ученые всего мира занимаются поисками материала-основы, который может обеспечивать адекватное окружение для выращивания костной ткани. После того, как кость выращена, эта основа должна разлагаться, либо продолжать быть матрицей, на которой будет функционировать кость. После синтеза кость можно пересадить больному. Обычно для этих целей используют гидроксилапатит [22]. Однако некоторые исследователи считают, что в качестве материала-основы идеально подходят углеродные нанотрубки [23]. Плотность их намного ниже, чем у стали и титана, обычно применяемых в этих целях, — а значит, масса кости будет меньше. К тому же нанотрубки чрезвычайно прочны (и делают кость прочнее), а также гибки и эластичны. Таким образом, они демонстрируют все свойства кости. Работа показывает возможность использовать нанотрубки в качестве материала для роста кости. Это, безусловно, успех в области биоинженерии кости. Однако до внедрения материал должны проверить на биосовместимость и нетоксичность.
Церий против глаукомы
Наночастицы материала, используемого для полировки стекла — оксида церия — показывают большой потенциал при лечении глаукомы, которой подвержены люди по всему миру. Глаукома — это группа заболеваний глаз, которые объединяет то, что при них повышается внутриглазное давление со всеми вытекающими последствиями. Развитие глаукомы ведет к необратимому процессу потери зрения. Сначала ухудшается периферийное зрение, а затем меняется все поле зрения. Если давление продолжает расти, а больной не лечится, — зрение ухудшается вплоть до слепоты, так как отмирает нерв. Современное лечение способно лишь замедлить этот необратимый процесс.
Авторы новейшего исследования присоединили к наночастицам оксида церия вещество, блокирующее фермент, который играет главную роль при развитии одного из видов глаукомы. Высокое давление создается из-за образования диоксида углерода в глазе, а вещество, доставляемое при помощи оксида церия, ингибирует этот процесс [24].
Нанопластырь для забывчивых
Когда доктора выписывают больному лекарства, многое может пойти не так. Человек может просто забыть принять таблетку, у него может проявиться побочный эффект или случиться передозировка. Корейцы создали пластырь, который способен следить за состоянием пациента и поставлять при необходимости в его организм нужное количество выписанного врачом лекарства. Этот «умный» пластырь разработали именно для безопасности больных. Он может вводить лекарство в организм определенными порциями и прекратить подачу, если что-то пойдет не так или содержание препарата достигнет нужного уровня.
Пластырь — это прямоугольник из растягивающегося материала, который содержит наночастицы диоксида кремния. Эти частицы реагируют на мышечную активность и тепло тела и, управляемые этими сигналами, выпускают лекарство.
Прежде всего это идеально подходит людям с паркинсонизмом. При судорогах у больного пластырь начинает выпускать лекарство. Как только судороги прекращаются — подача останавливается. Такие пластыри поступят в продажу не раньше, чем через пять лет. Но то, что больше не нужно будет следить за часами, чтобы вовремя выпить таблетку, обрадует многих [25].
Наночастицами по раку
Нанотехнологии уверенно отвоевывают всё новые горизонты. Ученых привлекла для исследований онкология, а точнее — возможность воздействия на рак наночастицами.
Проблема рака, к сожалению, волнует нас только тогда, когда приходится с ней столкнуться. Загрязнение окружающей среды, неправильный образ жизни и стрессы приводят к тому, что показатели заболеваемости раком неуклонно возрастают. Многие раковые заболевания до сих пор практически неизлечимы, и ученые всего мира пытаются изменить ситуацию в лучшую сторону .
Однако молекулярная медицина делает серьезные успехи, и всё новые и новые виды рака оказывается возможным вылечить с помощью иммунотерапии, ингибирования ракового сигналинга и клеточных технологий на основе генетически модифицированных лимфоцитов: «Успех в борьбе с лейкозом: на шаг ближе к клиническому применению геномного редактирования» [26] и «Лечение Джимми Картера» [27]. — Ред.
Рак — это опухоль, свойства которой делают ее крайне опасной для жизни организма, что и дало основание называть ее «злокачественной». При этом заболевании из-за генетического нарушения появляется очаг бесконтрольно делящихся клеток, которые могут проникать в прилежащие ткани и метастазировать (то есть, образовывать новые очаги бесконтрольно делящихся клеток) в отдаленные органы [28]. Опухоли обычно прогрессируют вплоть до летального исхода. Это одна из основных причин смерти в развитых странах.
Ученые в экспериментах на мышах случайно обнаружили, что наночастицы железа, которые были созданы в качестве лекарства от анемии, заставляют макрофагов атаковать раковые клетки [29]. Это открытие, сделанное во время испытаний лекарства от анемии, натолкнуло ученых на мысль, что железные наночастицы можно использовать и для борьбы с раком. Они проверили свою идею на трех группах мышей с перевитыми опухолями. Первая популяция грызунов получала инъекции железных наночастиц с противораковым препаратом, вторая — «пустые» наночастицы, а третья служила контрольной группой.
Эксперимент показал, что и «полные», и «пустые» частицы одинаково хорошо подавляли рост опухолей и заставляли макрофагов атаковать раковые клетки и уничтожать их. В организме контрольных особей иммунная система просто игнорировала опухоль. Схожим образом наночастицы предотвращали появление метастазов.
Сегодня в биомедицине активно используют плазмонные наноматериалы на основе серебра и золота. Плазмонными называют наноструктуры, проявляющие необычные свойства, обусловленные колебанием свободных электронов внутри них. Само колебание зависит от формы и размера наночастиц. Такие частицы используются в иммуноанализе, терапии раковых клеток, адресной доставке лекарств и мониторинге клеток и тканей.
Приповерхностные молекулы наночастиц из золота значительно усиливают сигнал комбинационного рассеяния, то есть при свечении лазера наблюдается обратный яркий отблеск. Именно наночастицы из золота способны приумножить данный сигнал во много раз и ярко светиться при скоплении даже небольшого количества молекул, поэтому с их помощью можно диагностировать рак на самых ранних стадиях.
Однако у таких частиц есть большой недостаток: при введении в кровь они начинают слипаться под воздействием хлорида натрия крови, в результате чего сосуды засоряются. Ученые из МИСиСа смогли решить эту проблему, создав наночастицы на основе золота в форме звезд, которые не слипаются при введении в кровь и обладают высокой эффективностью [30].
Процесс терапии можно описать так. Когда наночастица добирается до пораженного участка, на нее начинают воздействовать лазером, она поглощает свет и преобразует его в тепло, которое концентрируется на кончике звезды. Тепловой поток разрывает мембрану раковой клетки и уничтожает ее, не действуя на здоровые клетки.
Стимулировать ваш мозг
Полина Аникеева из Массачусетского института и ее коллеги разработали метод, позволяющий специфическим образом стимулировать отдельные зоны мозга и обходиться при этом без электродов или имплантатов. В мозг вводят пустые наночастицы окиси железа (рис. 6). В магнитном поле они нагреваются и стимулируют в мембранах нейронов терморецепторы TRPV1, также реагирующие на капсаицин — алкалоид, обеспечивающий жгучий вкус красному перцу [31]. Рецепторные белки к нему есть у разных клеток, в том числе и у некоторых нейронов. Если рецепторов нет, то можно вмешательством в гены заставить клетку их синтезировать, что и было сделано. Далее рецепторы TRPV1 реагируют на нагретые частицы, и клетка возбуждается. Этот метод позволил достаточно точно стимулировать у мышей определенную область среднего мозга.

Рисунок 6. Наночастицы оксида железа на поверхности клетки.
В будущем наночастицы с магнитным полем можно использовать как беспроводной и «долгоиграющий» стимулятор нейронов, который позволял бы решать самые разные медицинские задачи — например, лечение болезней нервной системы. Разумеется, до практического применения еще далеко, но у нас есть доказательство того, что такой метод возможен и работает — а это уже немало [32].
Против налета на зубах
Стоматологи советуют ополаскиватели как лучшие вспомогательные средства при чистке зубов. Они позволяют удалить бактерии и частицы пищи оттуда, куда не добираются зубная щетка и нить. Ученые из МИСиСа создали ополаскиватель, который подавляет рост бактерий, снижая риск кариеса и других болезней ротовой полости. Высокой эффективности ученые добились, введя в его состав наночастицы металлов. Они способны быстро подавлять рост бактерий, образующих налет.
В ходе испытаний на людях, добровольцы месяц пользовались этим средством. Замеры проводились через 14 и 30 дней с момента начала использования. Оказывается, бактерии, образующие налет, очень чувствительны к растворам, содержащим наночастицы оксидов металлов. А это значит, что после таких процедур становится намного меньше налета на зубах [33].
Мечта гипертоника
Сибирские биологи впервые применили генную терапию для лечения крыс, страдающих от гипертонии [34]. Они использовали наночастицы, к которым были присоединены олигонуклеотиды, специфически ингибирующие мРНК фермента, участвующего в развитии гипертонии. Оказалось, что введение в брюшную полость или ингаляция этих препаратов понижает давление, причем надолго, в отличие от стандартных препаратов, которые надо принимать каждый день.
По статистике, болезни сердца и сосудов являются главной причиной смерти — каждый год от них умирает около 17 миллионов человек, и главной причиной развития этих болезней остается гипертония, развивающаяся из-за неправильного образа жизни. Экспериментируя c короткими цепочками ДНК (олигонуклеотидами), ученые создали препарат, позволяющий избавиться от высокого давления в сосудах на очень большой срок. Регуляторные олигонуклеотиды могут заметно менять работу генов, повышая или понижая их активность [35]. Это натолкнуло на мысль, что такие цепочки можно использовать для борьбы с гипертонией, меняя работу генов, управляющих расширением и сужением стенок сосудов, а конкретнее — гена ангиотензин-1-превращающего фермента.
Ученые проверили эту идею, присоединив нужные олигонуклеотидные цепочки к наночастицам из оксида титана, способным проникать внутрь клеток, и ввели их в организм нескольких крыс. У этих специально выведенных для эксперимента животных давление подскакивает даже при малейшем стрессе, что имитирует гипертонию пожилых людей. Частицы успешно справились с задачей и избавили грызунов от гипертонии на несколько недель [34]. Что интересно, наночастицы и цепочки ДНК можно вводить в организм не только при помощи уколов, но и через ингалятор, что делает лекарство удобнее. Появления подобных средств в аптеках стоит ожидать не раньше, чем через несколько лет, когда подобная терапия пройдет все клинические тесты.
Надежда крионики
Одной из главных проблем пересадки органов является то, что эти органы очень мало живут вне организма. Но все в ближайшее время может измениться, ведь в США медикам удалось разморозить кусочки замороженных органов, не повредив при этом их структуру.
Почему же нельзя просто так взять и заморозить органы? Все дело в том, что при заморозке в тканях образуются кристаллы льда, которые травмируют их. Но если заморозить орган еще как-то получается, то с разморозкой все куда сложнее: выживает лишь около 80% клеток, чего явно недостаточно.
Группе ученых из Миннесоты под руководством Джона Бишофа удалось решить эту проблему [36]. Ученые смогли разморозить и оживить при помощи лазера и особых наночастиц эмбрион рыбы-зебры (рис. 7), что открывает дорогу для сохранения вымирающих видов животных и создания новых методов борьбы с бесплодием. Несмотря на успехи в заморозке стволовых и половых клеток, ученые уже более 60 лет безуспешно бьются над проблемой заморозки позвоночных. Этому мешали и большие размеры эмбрионов, и то, что их клетки нужно заполнять токсичными «антифризами». Команда американских ученых, несколько лет работающая над технологией заморозки и разморозки живых клеток, установила, что замороженные органы можно возвращать к жизни с помощью особых наночастиц, способных нагреваться до высоких температур под воздействием облучения. Наночастицы поглощают микроволновое излучение, преобразуют его в тепло и равномерно распределяют по замороженному биоматериалу, не допуская трещин. Проверив технологию на образцах ткани, биологи пошли дальше и «воскресили» замороженные эмбрионы рыб-зебр. Эксперименты показали, что часть эмбрионов выжила и смогла развиться в нормальных мальков. Таким образом, выяснилось, что эмбрионы позвоночных существ реально можно замораживать и возвращать к жизни. Впоследствии ученые смогут использовать новый метод для ликвидации вымирания животных, начавшегося из-за истребления человеком.
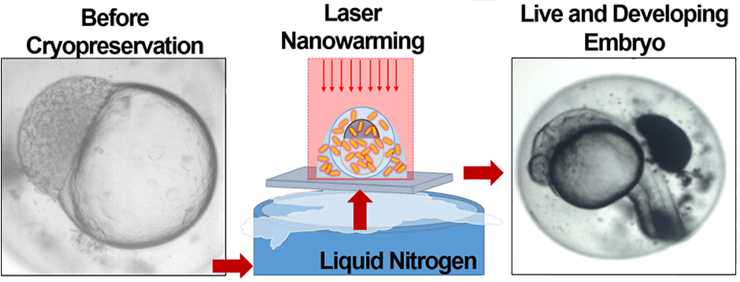
Рисунок 7. Эмбрионы до и после криоконсервации.
Против бактерий с резистентностью
Болезнетворные бактерии постепенно становятся невосприимчивыми к антибиотикам (про них говорят, что они выработали резистентность к антибиотикам), которые когда-то их истребляли, даже к таким лекарствам, которые некогда считались последней линией обороны. Теперь нам необходимо новое оружие в борьбе с инфекциями [37], [38].
Такие «супербактерии» убивают примерно один процент людей во всем мире. И если это оставить без внимания, они будут убивать в пять раз больше людей ежегодно. Многие вещи, которые мы считаем самими собой разумеющимися сейчас, вроде пересадки органов, без антибиотиков станут почти невозможны. И это тем ужаснее, что скоро антибиотики, возможно, уже не смогут нам помочь даже с мельчайшей царапиной.
Многие люди в этой области ищут альтернативные стратегии, которые можно было бы добавить в наш арсенал. Для борьбы с супербактериями мы обращаемся к новым союзникам, вроде бактериофагов или наночастиц. Каждый инструмент обладает своими преимуществами и недостатками, поэтому ученые изучают самые разные подходы.
Наногубка
Многие бактерии выделяют пороформирующие токсины, повреждающие мембраны клеток организма, в котором они живут. Лянфанг Чжан из Калифорнийского университета в Сан-Диего придумал, как защитить организм от этих «дырявящих клетки» токсинов. Он и его коллеги покрывают наночастицы «сладкой приманкой» — мембранами эритроцитов, которые «засасывают» токсин, как губка. Опасные молекулы просто «выводятся из оборота», не причиняя никакого вреда подопытным мышам [39].
«Нано-Пакман»
За последние годы биохимики сплели десятки различных машин из коротких цепочек ДНК, в том числе «щипцы», системы доставки лекарств и даже простейшие компьютеры [40–42]. Дальше этого разработка ДНК-оригами не продвинулась по нескольким причинам — сложные структуры из нитей ДНК собирать непросто, и еще сложнее — управлять ими.
Американцы создали из наночастиц миниатюрную версию старой видеоигры «Пакман» для практической цели — лечения от вирусов. В этой игре есть некое круглое существо с одним лишь ртом. Здесь надо «съесть» все белые точки, роль которых играют бактерии, вирусы и раковые клетки, избегая столкновений с привидениями (их роль исполняют клетки крови).
Эти ученые нашли новый, более простой способ сборки таких машин, который позволяет решать массу задач, используя не ДНК, а полимерные кубики, покрытые полосками кобальта. Намагничивая их, можно заставить кубы отталкиваться или собираться в конструкции. Его можно заставить открыть или закрыть «рот» (рис. 8).
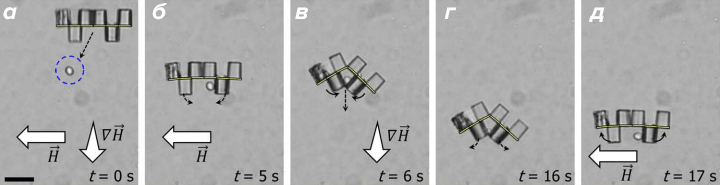
Рисунок 8. Снимки бота, содержащего шесть кубов для транспортировки дрожжевой клетки. а — Перемещение в открытом состоянии. б — Цепочка доводится до клетки путем притяжения магнитов. в — Бот самозакрывается при удалении магнитного поля, что приводит к захвату клетки. г — Бот переносится в место назначения с помощью магнита. д — Наконец клетка высвобождается.
Используя это устройство, ученые решили сложную и важную задачу: научили его плавать, периодически раскрывая и закрывая «рот», и заставили захватить и удерживать в себе клетку дрожжей, которую они запустили в раствор с наномашинами. Подобным образом эти устройства могут захватывать раковые клетки или бактерии и выводить их из организма (это будет своеобразной помощью иммунной системе) [43].
Широкий арсенал
Это не все оружие, которое мы добавляем в арсенал. Ученые изучают и другие варианты вроде отправки одних бактерий на борьбу с другими, поиска новых антибиотиков, доставки старых прямо к болезнетворным микробам (супербактерии с резистентностью не готовы к таким ударным дозам антибиотиков и будут умирать от них), использования бактериофагов (поскольку они не вызывают иммунного ответа у человека и не вредят ему, так как могут взаимодействовать только с бактериями [44]) и др. Не стоит полагаться на одну технологию, чтобы победить супербактерий. Их изучение, совмещение новых тактик и традиционных методов расширят арсенал.
Еще пара интересных разработок
Нанозолото из чая
Наночастицы золота все шире используют в разных областях, в том числе и в медицине для доставки лекарств против рака. Однако, хотя сами эти частицы нетоксичны, для их создания используют опасные вещества, которые ни в коем случае не должны попадать в организм. Не прореагировавшие частицы этих веществ перед введением в организм нужно удалять. Поэтому вопрос о так называемой «зеленой нанотехнологии», заключающейся в создании наноматериалов без ущерба природе и здоровью человека, стал очень актуален.
Такой безопасный способ получения нанозолота придумали американские ученые. Метод этот крайне прост — надо лишь заварить чай и подсыпать в него соль, которая содержит золото [45]. Не нужны никакие вещества, кроме NaAuCl4. Ученые поместили листья черного чая сорта «Дарджилинг» в десятимиллилитровый стаканчик, добавили воды и раствора NaAuCl4. Уже через полчаса были получены сферические золотые наночастицы, которые тут же отфильтровали от листьев чая (рис. 9).
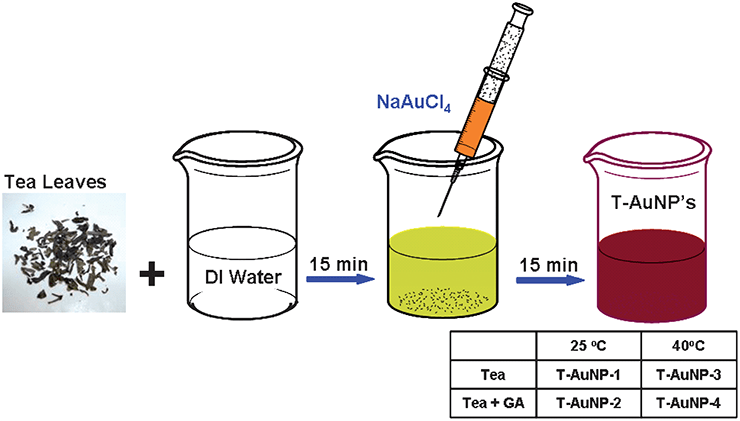
Рисунок 9. Выработка из чая наночастиц золота.
Вещества в чае оказались не только эффективными восстановителями золота из соли. Они также создали на частицах покрытие, препятствующее слипанию. Исследования показали прекрасную стабильность таких частиц в разных растворах и полную его безопасность. Такие наночастицы, усиленные веществами из листьев, смогут найти самое широкое применение.
Наночастицы высвобождают лекарство точно по расписанию
Часто бывает важно, чтобы какое-то вещество попало в организм в строго определенное время. Например, многие вакцины вводят несколькими порциями, соблюдая между ними интервалы — так иммунитет лучше запоминает особенности врага. Но для этого нужно регулярно ходить к врачу, что не всегда удобно или возможно.
Сегодня появляется много разработок, связанных с «грузовыми» наночастицами — их нагружают каким-то веществом и отправляют в организм. Наночастицы можно снабдить конкретным адресом назначения, или же их можно настроить, чтобы они освобождали свой груз постепенно, обеспечивая более длительное действие. Подобные наночастицы делали в Массачусетсе [46]. Однако если речь идет об описанной в статье схеме вакцинации, то вакцина должна выходить из частицы не медленно и непрерывно, а время от времени и сразу.
Чтобы обеспечить это, ученые использовали особый биоразлагаемый полимер PLGA, который применяют при создании материалов для протезов и хирургических инструментов. Полимер может распадаться с разной скоростью — в зависимости от модификации частицы полимера будут распадаться по очереди. Если мы хотим, чтобы вакцина выходила из частиц с перерывами, она должна быть в них заперта до того момента, пока частица не разрушится в свой срок. Ученые сделали что-то вроде чашки-параллелепипеда в несколько сотен мкм (рис. 10), куда можно было бы внести вакцину и плотно закрыть до поры до времени. Авторы работы сделали силиконовые формы для «чашек» и «крышек», в формы заливали PLGA, после чего на лист с «чашками» накладывали лист с «крышками» и нагревали — в итоге «крышка» запечатывала «чашку». Потом их решили испытать на мышах. В «чашки» добавили яичный белок, который используют, когда хотят спровоцировать иммунную реакцию. Материал модифицировали так, чтобы он разрушался через 9, через 20 и через 41 день после введения. Из наночастиц ничего преждевременно не вытекало, и иммунный ответ происходил строго по расписанию — как если бы его каждый раз вводили специально инъекцией. Между тем инъекция была только одна — в ней содержалась смесь наночастиц, которые должны были разрушиться в разное время.

Рисунок 10. «Наночашки» с «нанокрышками».
Исследователи также сконструировали наноконтейнеры, которые открываются еще позже — через несколько сотен дней, и сейчас эти долгоиграющие частицы испытывают с разными веществами. Новый метод позволяет делать частицы разной формы и из разных материалов, и, соответственно, применение им можно найти самое разное.
Миниатюрные двигатели
В любой клетке много моторных белков [47]. А что касается искусственных нанодвигателей? Принцип работы ферментативного нанодвигателя, созданного международной группой ученых, основан на реактивной тяге: выбрасываемые продукты задают движение в направлении, обратном выбрасываемому потоку. Это нанотрубка из диоксида кремния с диаметром отверстия 220 нанометров [48]. Стенки ее покрыты ферментом, расщепляющим мочевину на аммиак и углекислоты, — уреазой. Если ее поместить в жидкость с мочевиной (а в крови она есть), произойдет реакция и ее продукты создадут поток, придающий импульс: скорость при этом достигает 4 см/ч (рис. 11). Этот двигатель — самый маленький в мире. Кроме того, он полностью биосовместим. Аналоги используют катализаторы, на которых перекись водорода расщепляется на водород и кислород. И перекись, и пузырьки газа нежелательны в организме. Уреаза позволяет избежать этого — реакция не производит пузырьков, а фермент содержится в теле сам по себе.

Рисунок 11. Самоходный наноробот на ферментативном двигателе: нанотрубки, покрытые уреазой, движутся в жидкостях, содержащих мочевину. Реакция между ферментом и мочевиной приводит к реактивному движению наноробота.
Пузырьки газа не должны быть в жидкостях организма, но стали частью других ботов, которые изобрели немцы [49]. Здесь газ не опасен, так как помещен в специальные камеры и никак не может попасть в жидкости. Для передвижения используется ультразвук: он заставляет пузырьки вибрировать, приводя бота в движение вокруг своей оси. Частота звука зависит от размера пузырьков: чем меньше их размер, тем больше должна быть частота. Эта зависимость используется для задания направления вращения. Пузырьки разных размеров размещены на двух сторонах четырех граней параллелепипеда. Управляя частотой, ученые заставляют вибрировать нужную сторону, что приводит к вращению робота в нужном направлении (рис. 12). Пластинами с пузырьковыми камерами можно покрыть бота любой формы.
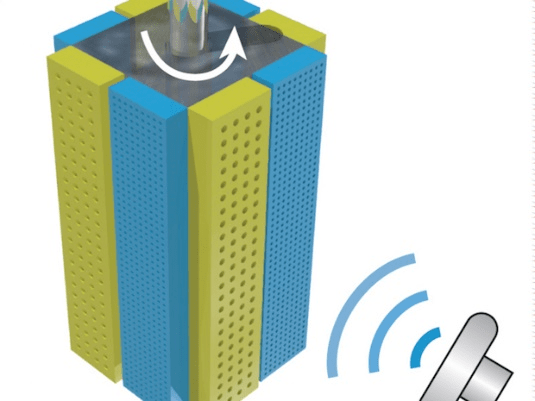
Рисунок 12. Управление ультразвуком: двигатель оборудован пузырьковыми камерами двух разных размеров (синие и желтые панели). Ультразвук заставляет пузырьки вибрировать, разница в силе толчков разных пузырьков заставляет систему вращаться.
Очень элегантное решение — использовать моторы, заимствованные у природы. Ведь все самое лучшее было придумано ей! Такие моторы в течение миллионов лет существуют в природе и буквально «проверены временем». Например, сперматозоиды снабжены бьющими хвостами наподобие хлыста, продвигающими клетку вперед.
Комбинируя механические и биологические средства передвижения, можно было бы заставить эти компоненты дополнять друг друга, когда один дает сбой. Примером может служить недавно разработанный спермбот (рис. 13, видео). Оливер Шмидт разработал крошечные металлические спирали, которые оборачиваются вокруг «ленивого» сперматозоида, давая ему мобильность, чтобы достичь яйцеклетки [50]. С помощью такого наноробота можно с успехом бороться против мужского бесплодия, причина которого — недостаточная подвижность сперматозоидов.
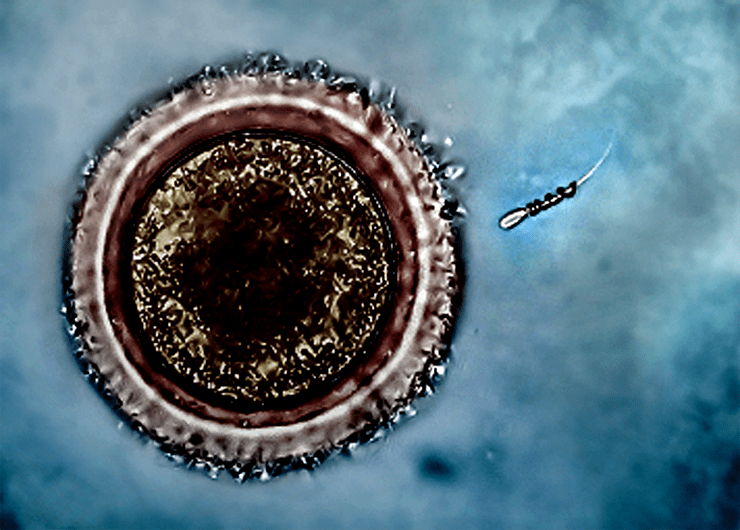
Рисунок 13. Спермбот направляет малоподвижный сперматозоид к яйцеклетке.
Видео. Спермбот в действии
Нанороботы
Ученые уже много лет мечтают о крошечных роботах, которые смогут работать внутри наших тел. Их еще в конце прошлого столетия описал известный американский ученый Эрик Дрекслер, который в своей книге «Машины создания» обозначил, что нанороботы смогут делать почти все — собирать любые предметы, чинить клетки на молекулярном уровне, внося изменения в геном, чем можно излечить любые болезни. В частности, эпиграфом к данной работе служит цитата именно из его книги. В те времена (1986 год) эта теория казалась правильной и абсолютно непротиворечивой, но потом ученые на практике показали, что в жизни (а не в мысленном эксперименте) такие вещи воплотить невозможно, и современные наниты совсем не похожи на то, о чем писали праотцы.
«ДНК-оригами»
Клетки некоторых раковых опухолей приобретают устойчивость к химиотерапии, активно выводя препарат через клеточную мембрану. Чтобы предотвратить этот процесс, ученые из Огайо использовали технологию, известную как «ДНК-оригами» [40–42].
Для этого они взяли фрагменты генома бактериофага и добавили к ним созданные искусственно цепочки генов, которые обеспечивают самостоятельную сборку ДНК в трубчатые структуры [51]. Поскольку большинство противоопухолевых препаратов действуют на геном раковых клеток, они легко проникают в полости «ДНК-оригами» и остаются там.
В эксперименте на мышах с лейкозом «упакованный» в ДНК препарат даунорубицин эффективно проникал в клетки. Под действием ферментов молекула ДНК разлагалась, высвобождая препарат прямо внутрь опухолевых клеток. Даунорубицин вызвал гибель большинства раковых клеток в течение 15 часов после введения.
Робот из принтера
Команда ученых из Иллинойса использовала 3D-принтер, чтобы создать гибкие гелевые площадки в несколько мм, на которые были посеяны сердечные клетки крысы [52]. Погруженная в питательную среду, мышечная ткань покрыла гель тонким слоем. Сокращающиеся клетки послужили хорошим мотором, и биоробот зашагал вперед. Впрочем, приз на спринтерской дистанции ему не взять — скорость передвижения составила всего 236 мкм/с. Ученые работают над тем, чтобы сделать биороботов быстрее, меньше и сильнее, а также снабдить их биологическими датчиками и системой реагирования.
Если заменить сердечные клетки на поперечнополосатую мышечную ткань, сокращения станет проще контролировать. Исследователи рассчитывают направить робота к источнику токсина, достигнув которого машина выпустит лекарство. Для этого они хотят добавить нейроны, которые обнаружат токсины и простимулируют сокращение.
И об остальных вопросах
Хотя ученые набросали кучу идей относительно движителей, огромной проблемой остается отслеживание устройств после внедрения в тело. На помощь должны прийти методы визуализации. Ультразвуковая, МРТ и инфракрасная визуализация слишком медленные, чтобы наблюдать за происходящим глубоко в организме. Но сочетая свет, звук и электромагнитные волны, мы могли бы увеличить разрешение и чувствительность.
В идеале метод визуализации должен иметь возможность отслеживать движущиеся частицы на глубине 10 см под кожей, в 3D и реальном времени. Сейчас этого сложно достичь, но ученые надеются, что методы, сочетающие инфракрасное и ультразвуковое изображение, подойдут для отслеживания наночастиц.
И тогда останется вопрос, что делать с роботами по завершении их миссии. Оставить их дрейфовать внутри тела — значит, допустить возникновение катастрофических побочных эффектов. Ученые рассматривают выведение их естественным путем или создание их из разлагаемых материалов.
Ну и конечно, никогда нельзя забывать о безопасности. Все свойства наночастиц надо еще тестировать и тестировать, чтобы убедиться, что они не причинят человеку вреда. Кое-какие испытания уже проводятся, причем довольно успешно.
Заключение
Итак, мы теперь можем небезосновательно придти к выводу, что использование нанотехнологий в медицине — реальность, подтвержденная в лабораториях. Были проведены реальные исследования, показавшие, что нанотехнологии могут сыграть в нашей войне против болезней роль союзника и перевести ее на новый уровень. Наночастицы могут быть получены довольно простыми методами, многие из них абсолютно безопасны и намного лучше справляются с теми или иными болезнями, чем те лекарства, которыми мы пользуемся сейчас. Эти средства уже прошли испытания на мышах, и готовятся их тесты уже на людях. И, возможно, когда-нибудь в больницах будут выписывать какие-то из этих препаратов от тех болезней, которые раньше считались неизлечимыми. Быть может, благодаря нанотехнологиям мы победим рак, ВИЧ и другие болезни с таким же успехом, как в свое время благодаря достижениям медицины побороли оспу, тиф и «черную смерть». Ведь недаром Эрик Дрекслер, один из праотцов нанотехнологий, сказал слова, выбранные мною в качестве эпиграфа к данной статье: «Нанотехнология принесет фундаментальный прорыв в медицине».
Литература
- Кобринский Г. (1988). Липосомы в медицине. «Наука и жизнь»;
- Наномедицина будущего: трансдермальная доставка с использованием наночастиц;
- Tae Kyung Kim, James H. Eberwine. (2010). Mammalian cell transfection: the present and the future. Anal Bioanal Chem. 397, 3173-3178;
- Что такое ДНК-вакцины и с чем их едят?;
- Липидный фундамент жизни;
- Физическая водобоязнь;
- Элементы: Полимерные наночастицы — новое оружие в борьбе с бактериями?;
- Вирусы-платформы: яд во благо;
- Семчиков Ю.Д. (1998). Дендримеры — новый класс полимеров. Соросовский образовательный журнал. 12;
- Hu Yang, Weiyuan John Kao. (2006). Dendrimers for pharmaceutical and biomedical applications. Journal of Biomaterials Science, Polymer Edition. 17, 3-19;
- «Мал золотник, да дорог», или об использовании золотых наночастиц в бионанотехнологиях;
- Наномеханика для адресной доставки лекарств – насколько это реально?;
- Невидимая граница: где сталкиваются «нано» и «био»;
- Romano J.A. Chemical warfare agents: chemistry, pharmacology, toxicology, and therapeutics. US: CRC Press, 2008. — 752 p.;
- Evans R.J. The Third Reich at war, 1939–1945. Penguin, 2009. — 944 p.;
- Как происходит выделение нейромедиатора;
- Charles B. Millard, Gitay Kryger, Arie Ordentlich, Harry M. Greenblatt, Michal Harel, et. al.. (1999). Crystal Structures of Aged Phosphonylated Acetylcholinesterase: Nerve Agent Reaction Products at the Atomic Level†,‡. Biochemistry. 38, 7032-7039;
- «Дизайнерские» ферменты защищают от нервно-паралитических ядов;
- Elena N. Efremenko, Ilya V. Lyagin, Natalia L. Klyachko, Tatiana Bronich, Natalia V. Zavyalova, et. al.. (2017). A simple and highly effective catalytic nanozyme scavenger for organophosphorus neurotoxins. Journal of Controlled Release. 247, 175-181;
- Почему так сложно похудеть, или Влияние кишечной микробиоты на метаболизм;
- Yuqi Zhang, Qiongming Liu, Jicheng Yu, Shuangjiang Yu, Jinqiang Wang, et. al.. (2017). Locally Induced Adipose Tissue Browning by Microneedle Patch for Obesity Treatment. ACS Nano. 11, 9223-9230;
- Гидроксилапатит — самый главный из фосфатов кальция;
- Laura P. Zanello, Bin Zhao, Hui Hu, Robert C. Haddon. (2006). Bone Cell Proliferation on Carbon Nanotubes. Nano Lett.. 6, 562-567;
- Swanand Patil, Serge Reshetnikov, Manas K. Haldar, Sudipta Seal, Sanku Mallik. (2007). Surface-Derivatized Nanoceria with Human Carbonic Anhydrase II Inhibitors and Fluorophores: A Potential Drug Delivery Device. J. Phys. Chem. C. 111, 8437-8442;
- Donghee Son, Jongha Lee, Shutao Qiao, Roozbeh Ghaffari, Jaemin Kim, et. al.. (2014). Multifunctional wearable devices for diagnosis and therapy of movement disorders. Nature Nanotech. 9, 397-404;
- Успех в борьбе с лейкозом: на шаг ближе к клиническому применению геномного редактирования;
- Лечение Джимми Картера;
- Метастазирование опухолей;
- Saeid Zanganeh, Gregor Hutter, Ryan Spitler, Olga Lenkov, Morteza Mahmoudi, et. al.. (2016). Iron oxide nanoparticles inhibit tumour growth by inducing pro-inflammatory macrophage polarization in tumour tissues. Nature Nanotech. 11, 986-994;
- M. Bhattacharya, V. Mazov, B. Satpati, P. Jena, S. Das Chakraborty, et. al.. (2017). Exploiting Le Chatelier's principle for a one-pot synthesis of nontoxic HHogGNPs with the sharpest nanoscopic features suitable for tunable plasmon spectroscopy and high throughput SERS sensing. Chem. Commun.. 53, 10402-10405;
- Жгучий перец облегчит боль;
- R. Chen, G. Romero, M. G. Christiansen, A. Mohr, P. Anikeeva. (2015). Wireless magnetothermal deep brain stimulation. Science. 347, 1477-1480;
- Russian scientists develop metal nanoparticles to kill oral bacteria. (2017). Sputnik;
- M. N. Repkova, A. S. Levina, A. A. Seryapina, N. V. Shikina, E. V. Bessudnova, et. al.. (2017). Toward gene therapy of hypertension: Experimental study on hypertensive ISIAH rats. Biochemistry Moscow. 82, 454-457;
- Обо всех РНК на свете, больших и малых;
- Kanav Khosla, Yiru Wang, Mary Hagedorn, Zhenpeng Qin, John Bischof. (2017). Gold Nanorod Induced Warming of Embryos from the Cryogenic State Enhances Viability. ACS Nano. 11, 7869-7878;
- Противостояние с резистентными бактериями: наши поражения, победы и планы на будущее;
- Антибиотики и антибиотикорезистентность: от древности до наших дней;
- Che-Ming J. Hu, Ronnie H. Fang, Jonathan Copp, Brian T. Luk, Liangfang Zhang. (2013). A biomimetic nanosponge that absorbs pore-forming toxins. Nature Nanotech. 8, 336-340;
- ДНК-оригами: путь от гравюры до нанороботов длиной в 30 лет;
- Биоинженеры научились получать ДНК-структуры, сборкой и разборкой которых можно управлять;
- Голактеко опасносте: ДНК-роботы в живом организме;
- Koohee Han, C. Wyatt Shields, Nidhi M. Diwakar, Bhuvnesh Bharti, Gabriel P. López, Orlin D. Velev. (2017). Sequence-encoded colloidal origami and microbot assemblies from patchy magnetic cubes. Sci. Adv.. 3, e1701108;
- Пожиратели бактерий: убийцы в роли спасителей;
- Satish K. Nune, Nripen Chanda, Ravi Shukla, Kavita Katti, Rajesh R. Kulkarni, et. al.. (2009). Green nanotechnology from tea: phytochemicals in tea as building blocks for production of biocompatible gold nanoparticles. J. Mater. Chem.. 19, 2912;
- Kevin J. McHugh, Thanh D. Nguyen, Allison R. Linehan, David Yang, Adam M. Behrens, et. al.. (2017). Fabrication of fillable microparticles and other complex 3D microstructures. Science. 357, 1138-1142;
- Белковые моторы: на службе у человека и нанотехнологий;
- Xing Ma, Ana C. Hortelao, Albert Miguel-López, Samuel Sánchez. (2016). Bubble-Free Propulsion of Ultrasmall Tubular Nanojets Powered by Biocatalytic Reactions. J. Am. Chem. Soc.. 138, 13782-13785;
- T. Qiu, S. Palagi, A. G. Mark, K. Melde, F. Adams, P. Fischer. (2016). Wireless actuation with functional acoustic surfaces. Appl. Phys. Lett.. 109, 191602;
- Mariana Medina-Sánchez, Lukas Schwarz, Anne K. Meyer, Franziska Hebenstreit, Oliver G. Schmidt. (2016). Cellular Cargo Delivery: Toward Assisted Fertilization by Sperm-Carrying Micromotors. Nano Lett.. 16, 555-561;
- Patrick D. Halley, Christopher R. Lucas, Emily M. McWilliams, Matthew J. Webber, Randy A. Patton, et. al.. (2016). Daunorubicin-Loaded DNA Origami Nanostructures Circumvent Drug-Resistance Mechanisms in a Leukemia Model. Small. 12, 308-320;
- Vincent Chan, Kidong Park, Mitchell B. Collens, Hyunjoon Kong, Taher A. Saif, Rashid Bashir. (2012). Development of Miniaturized Walking Biological Machines. Sci Rep. 2.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚