-
1478Статья на конкурс «био/мол/текст»: Научное сообщество начало познавать явление лизогении еще в 20-е годы XX века. Тогда заметили, что после многократных пассажей отдельных бактериальных колоний и их длительного размножения в антифаговой сыворотке в бактериальных культурах всё равно остаются фаги. Как можно охарактеризовать это явление спустя столетие, отбросив былые сомнения, задавшись новыми вопросами и следуя данным проведенных исследований? Предлагаем вашему вниманию биографию умеренного фага, после проникновения в бактерию ставшего внутриклеточным компонентом многих поколений ее потомков.
-
Статья на конкурс «био/мол/текст»: Ранее не осознаваемая нами ультрамикроскопическая жизнь генома с развитием науки оказывается все более важным фактором управления генетическим аппаратом клетки. Теперь весь геном можно рассматривать как сеть пространственных взаимодействий генетических элементов, что принципиально изменяет наше понимание событий внутри ядра. Биология трехмерности генома в тренде — в этой статье разберемся, почему это круто с точки зрения эволюции.
-
За последние несколько лет систему CRISPR/Cas9, казалось, попробовали применить во всех направлениях генной инженерии. С помощью этого мощнейшего инструмента редактировали геномы хозяйственно важных животных и растений, вредителей, переносчиков инфекций, модифицировали метаболические пути промышленно важных микроорганизмов. Разумеется, самые активные разработки ведутся в области применения CRISPR/Cas9 в медицине. Однако этот инструмент имеет не только прикладное значение, но и может пригодиться ученым, занимающимся фундаментальной наукой. В начале августа 2018 года Science опубликовал статью, авторы которой использовали CRISPR/Cas9 для отслеживания судьбы отдельных клеток в ходе развития организма мыши. О деталях этой замечательной работы мы сегодня и поговорим.
-
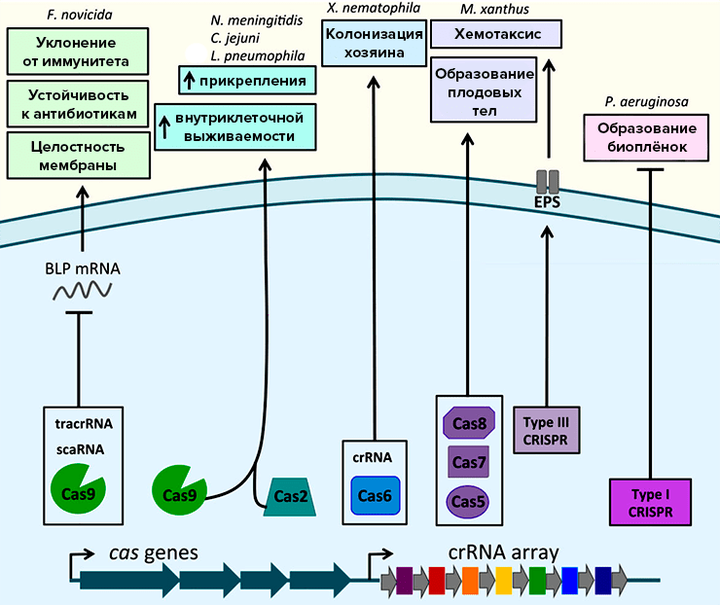
Как известно, система CRISPR/Cas служит мощнейшим средством защиты бактерий от мобильных генетических элементов (плазмид, транспозонов и, конечно, бактериофагов). За прошедшие несколько лет системы CRISPR/Cas обнаружены у большинства бактерий и архей. Однако накапливается все больше данных, свидетельствующих о том, что роль CRISPR/Cas не ограничивается адаптивным иммунитетом. Показано, что эти системы регулируют экспрессию многих бактериальных генов, влияя на вирулентность патогенных бактерий и групповое поведение, а также участвуют в репарации ДНК и ускоряют эволюцию геномов. Наш обзор посвящен неиммунным функциям систем CRISPR/Cas и их молекулярным механизмам.
-
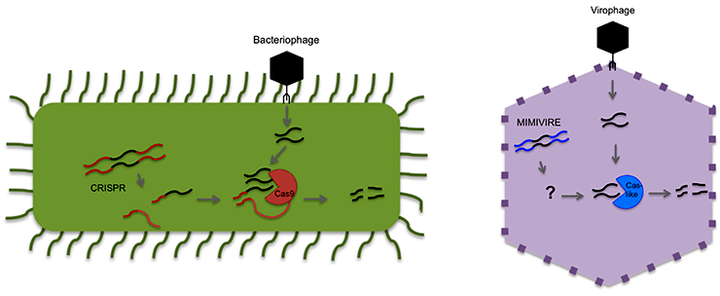
Вирофаги — это небольшая группа вирусов, которые могут размножаться в эукариотических клетках только вместе с другим вирусом-хозяином, используя его «фабрику» для производства собственных частиц. Известные на данный момент вирофаги паразитируют на гигантских вирусах, в частности мимивирусах, которые, в свою очередь, инфицируют клетки амёб. Используя ферменты вирусов-хозяев для образования своих частиц, вирофаги сильно портят им жизнь, мешая формированию вирионов и протеканию инфекционного цикла. Недавно было показано, что мимивирусы не так уж и беззащитны перед вирофагами: у них есть особая молекулярная машина, получившая название MIMIVIRE. Первоначально было заявлено, что по механизму работы MIMIVIRE очень напоминает систему CRISPR/Cas прокариот, направленную на защиту от вирусов и плазмид. Впрочем, история с MIMIVIRE куда более темная, чем кажется на первый взгляд...
-
В предпраздничной суете «Биомолекула» не может просто так взять и не подвести научные итоги уходящего года. В 2017-м завершил свою миссию легендарный зонд «Кассини», бушевали страсти вокруг глобального потепления и политических решений президента США, вздымались гравитационные волны... а также волна обвинений в домогательствах, которой, увы, не удалось избежать и ряду крупных университетов. Однако, разумеется, нас прежде всего интересуют биология и медицина — чем они впечатлили мир в этом году? С целью выделить самое важное, обратимся к экспертам крупнейших научных изданий — Nаture и Science, — а ради полноты картины учтем мнение мировой читательской публики, запечатленное в рейтинге «Альтметрики».
-
115351О том, что генная инженерия изменила мир, знают почти все, а вот каким образом — только специалисты. Об этом редко рассказывают в школе, а непонятное всегда подозрительно. Этим умело пользуются «говорящие головы», транслируя с телеэкранов альтернативную реальность. Чтобы не пугаться ГМО и не демонизировать генных инженеров, достаточно хоть немного представлять их работу и знать, что будущее их творений регулируется даже слишком строго. В первой части статьи мы вспомнили историю этой отрасли и затронули этические и коммерческие вопросы, с нею связанные. А сейчас предлагаем заглянуть в мастерскую генного инженера — пройти краткий курс кройки и шитья ДНК и познакомиться с методами, расширившими границы фундаментальных исследований, биотехнологии и медицины.
-
Системы CRISPR/Cas, обеспечивающие адаптивный иммунитет к вирусам и мобильным генетическим элементам у прокариот, обнаружены примерно у 50% бактерий и 90% архей. Однако некоторые бактериофаги могут нарушать работу системы CRISPR/Cas при помощи особых белков, получивших в совокупности название «анти-CRISPR» (англ. anti-CRISPR). На данный момент описано 22 семейства белков анти-CRISPR, которые действуют против систем CRISPR/Cas I и II типов. Предполагается, однако, что способность избегать действия систем CRISPR/Cas широко распространена среди фагов и других мобильных генетических элементов, так как, согласно новейшим данным, системы CRISPR/Cas минимально препятствуют горизонтальному переносу генов. Данная статья посвящена истории открытия, механизмам действия, а также эволюционному и биотехнологическому значениям известных на сегодняшний момент анти-CRISPR-белков.
-
Статья на конкурс «био/мол/текст»: Когда Олдос Хаксли писал «Дивный новый мир», думал ли он, что на самом деле может наступить эра детей, созданных по заказу? «Дети здесь не рождаются. Их выращивают в специальных инкубаторах и делят на альфы, беты, гаммы, дельты и эпсилоны в зависимости от умственных способностей». На сегодняшний день вряд ли найдется более рьяно обсуждаемая в СМИ тема биомедицины, чем CRISPR/Cas. СМИ готовят общество к появлению в будущем фабрик по производству детей на заказ, ученые — к возможности создания генетической панацеи. Исследования на человеческих эмбрионах с применением генетических модификаций лишь подливают масла в огонь. Общественность строит догадки, какие перспективы дает этот инструмент генного редактирования в руках ученых. Ждет ли мир появление «отредактированных» людей? Станет ли Homo genere mutatio в эволюционный ряд после Homo sapiens sapiens? К чему бы ни привела технология CRISPR/Cas, несомненно, что это шаг в бездну новых возможностей.


- Лента
- Спецпроекты
- ▶Подкаст
-
Конкурс
- О конкурсе «Био/мол/текст»
- «Био/мол/текст»-2025/2026
- «Био/мол/текст»-2024/2025
- «Био/мол/текст»-2023/2024
- «Био/мол/текст»-2022/2023
- «Био/мол/текст»-2021/2022
- «Био/мол/текст»-2020/2021
- «Био/мол/текст»-2019
- «Био/мол/текст»-2018
- «Био/мол/текст»-2017
- «Био/мол/текст»-2016
- «Био/мол/текст»-2015
- «Био/мол/текст»-2014
- «Био/мол/текст»-2013
- «Био/мол/текст»-2012
- «Био/мол/текст»-2011
- Объявления
- Авторы
- Партнеры
- Поддержать
Публикации
—
Темы
—
Авторы
—
Комментарии
—
Поиск не дал результатов
По вашему запросу ничего не найдено
- Медицина
- SARS-CoV-2
- «Биомолекула» — Forbes
- Аллергия
- Антибиотики
- Атеросклероз
- Аутоиммунитет
- Боль
- ВИЧ/СПИД
- Вакцины
- Вирус Зика
- Вирус Эбола
- Генная терапия
- Грипп
- Депрессия
- Дерматология
- Диагностика
- Здравоохранение
- Нейродегенерация
- Никотин
- Онкология
- Персонализированная медицина
- Питание
- Сон
- Стволовые клетки
- Фармакология
- Эпилепсия
- Биология
- «Сухая» биология
- Антропология
- Бионика
- Биофизика
- Вирусология
- Вопросы пола
- ГМО
- Генетика
- Иммунология
- Микробиология
- Нейробиология
- Носимые технологии
- Психогенетика
- Синтетическая биология
- Старение
- Структурная биология
- Цитология
- Эволюционная биология
- Экология
- Эмбриология
- Эпигенетика
- Этология
- Биомолекулы
- GPCR
- АФК
- Амилоиды
- Биомембраны
- Гормоны растений
- ДНК
- Ионные каналы
- МГЭ
- Матрикс
- Нейромедиаторы
- РНК
- Рецепторы
- Хроматин