От бизнеса ученых к законотворчеству
13 сентября 2024
От бизнеса ученых к законотворчеству
- 956
- 0
- 2
«Петровакс» — одна из немногих в России биотехнологических компаний полного цикла, производящая и препараты по лицензии, и собственные продукты.
Рисунок в полном размере.
иллюстрация Ирины Ефремовой
-
Автор
-
Редакторы
-
Иллюстратор
Компания «Петровакс» была основана российскими учеными в 1996 году. В мире, стране и в самой компании с тех пор многое изменилось. О производстве новых биотехнологических препаратов, о законодательном регулировании фармацевтической отрасли, о поиске новых молекул и обучении сотрудников «Биомолекула» пообщалась с президентом компании «Петровакс» Михаилом Цыферовым, руководителем направления развития биотехнологических продуктов Николаем Голубом и начальником департамента развития биотехнологических продуктов Андреем Болдыревым.
Современные лекарства
Спецпроект о современных лекарствах, истории их создания, методах разработки и тенденциях развития.
Партнер статьи — компания «Петровакс», которая более 25 лет успешно работает на фармацевтическом рынке и производит собственные оригинальные препараты и вакцины.
В спецпроекте «Современные лекарства» мы рассказываем о лекарствах на переднем крае науки и о процессе их разработки: о новых способах воздействия на мишени, прорывах в лечении ранее неизлечимых заболеваний, тенденциях в мире фармацевтики. Биофармацевтические компании в России стараются не отставать от мировых трендов и выводить на рынок новейшие препараты для терапии тяжелых заболеваний. Мы поговорили с представителями одной из таких компаний — «Петровакс» — и выяснили, как устроен поиск новых молекул; какова стратегия компании; и как в «Петровакс» решаются вопросы с поставками материалов, поиском сотрудников и расширением производства.
Сейчас компания активно инвестирует в расширение линейки продуктов и производственных мощностей. В ближайшее время ожидается регистрация антитела камрелизумаб (совместно с китайской Hengrui) против рецептора иммунного чекпойнта PD-1. Поскольку в компании уже существуют компетенции по производству низкомолекулярных веществ и биопрепаратов, мы начали с вопроса о различиях между этими классами веществ. Мы уже затрагивали эту тему в самой первой статье спецпроекта [1], и интересно было узнать мнение специалистов.
Молекулы
— В чем отличия между лекарствами, произведенными традиционным химическим синтезом, и биофармпрепаратами? Насколько их стоимость выше?

Вопрос простой, но ответить сложно. Химический синтез — это в какой-то степени математический расчет. Вы рассчитываете компоненты и можете предсказать выход, потери и другие параметры процесса. С биотехом сложнее — это использование живых систем, не всегда подчиняющихся прямой логике. Клетки-продуценты, которые производят антитела, ферменты и другие биотехнологические продукты — это сильно модифицированные живые системы, и поэтому предсказуемость результата сильно ниже. Хотя мы не действуем вслепую, вариативность результатов высока. Стоимость биофармацевтических препаратов обычно выше из-за сложности разработки и производства, а также необходимости соблюдения строгих регуляторных стандартов.
— А какова стратегия поиска новых разработок?

Мы развиваем вакцинально-госпитальную часть бизнеса и обращаем внимание на биосимиляры и оригинальные биотехнологические препараты, которые можно лицензировать в России. Вдобавок начинаем формировать кластер препаратов для терапии орфанных заболеваний, онкологии и вакцин. В каждом направлении чаще смотрим биосимиляры и редко дженерики.
Например, локализация агалсидазы бета (препарат «Фабагал»), которая применяется для лечения болезни Фабри , — первый в России проект по трансферу технологии производства субстанции для орфанного препарата, зарегистрированного за рубежом. Сейчас первые российские пациенты уже получают его. А до конца года мы ожидаем вывод на рынок полностью произведенного в России препарата.
Постепенно будем наполнять портфель другими препаратами для терапии орфанных заболеваний и надеемся в 2025 году представить еще два. В онкологии мы тоже начали с препарата для терапии костных метастазов — он выйдет в 2025 году. И еще один продукт в этом направлении — оригинальный иммуноонкологический препарат, блокирующий PD-1 рецептор .
— Сейчас вокруг PD1 много разных разработок ведется: иммунные чекпойнты [7] (рис. 1) — очень горячая тема [8]. Чем отличается ваш препарат от аналогов?
АБ: — У нашего препарата уникальные показания — там, например, где не сработал пембролизумаб. Например, для рака носоглотки, который распространен в Китае и в меньшей степени в России. Кроме того, у коллег из Китая уникальная специфика. Например, в раке печени — очень интересная комбинация их анти-PD1 с их же низкомолекулярным веществом, которая выглядит перспективной на фоне существующих терапий. В отличие от пембролизумаба, камрелизумаб обладает другим механизмом связывания с PD-1, что снижает вероятность развития пневмонита. И вот из-за этой интересной специфики будем осуществлять полный техтрансфер в РФ.
Аналогично смотрим вакцины. Наш следующий большой проект, надеюсь, — полный трансфер технологии производства конъюгированных вакцин.
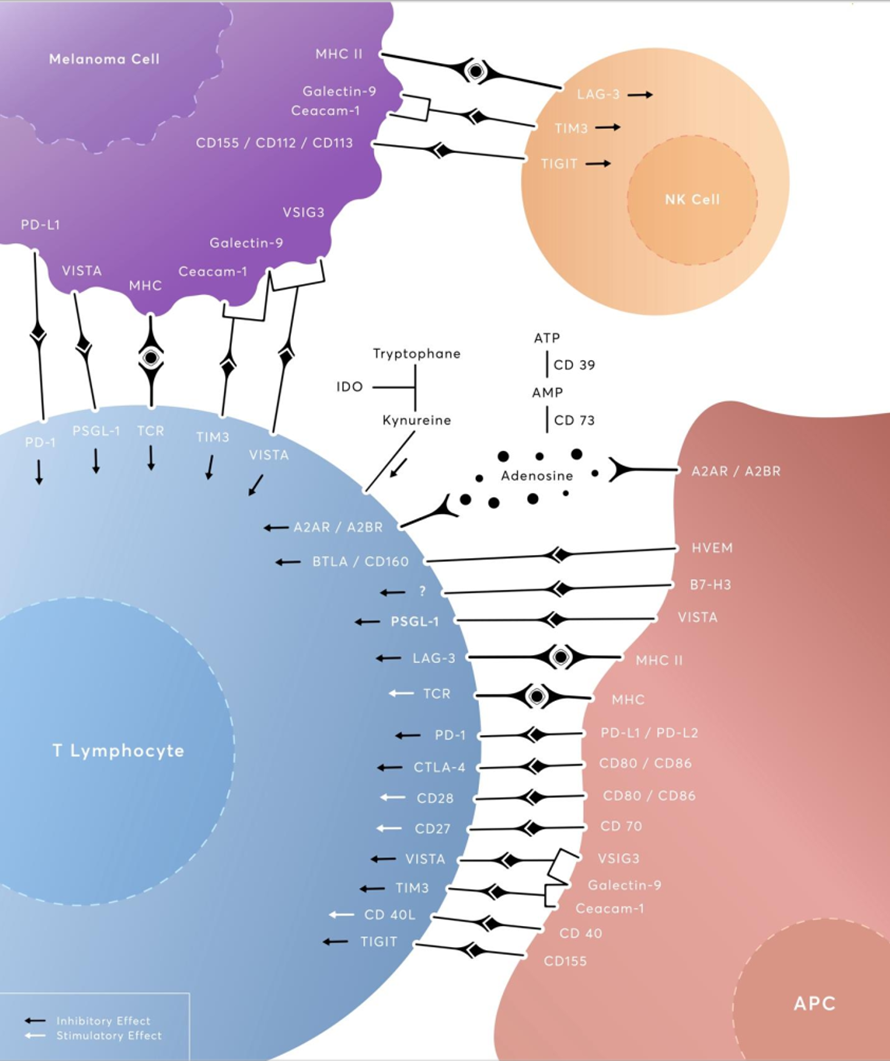
Рисунок 1. Разнообразные иммунные чекпойнты во взаимодействии не только между раковой (в данном случае — клеткой рака кожи, меланомы) и иммунными клетками, но также и с антигенпрезентирующей клеткой. APC (antigen presenting cell) может направлять действие Т-лимфоцитов против клеток, несущих определенные неоантигены или, наоборот, сыграть на стороне опухоли, ингибируя иммунный ответ.
— Экономические выгоды вакцин понятны. А орфанные заболевания*? Насколько этот рынок интересен сейчас фармкомпаниям? Ведь он довольно рискованный.

Несмотря на риски, и у нас, и в развитых странах это довольно раскачанный рынок. В России он, возможно, даже более динамичен по сравнению с масштабами экономики.
Бизнес идет в орфанные заболевания , потому что регуляторные барьеры привлекательны. Особенно ярко это выражено в России — возможно, доля орфанных заболеваний на рынке будет выше, чем во многих других странах, именно из-за позиции регулятора. Наша миссия здесь — сделать терапию еще доступнее. И сейчас уже можем за те же деньги вылечить больше пациентов. Например, наша агалсидаза бета на 40% дешевле референтного препарата с аналогичным действующим веществом и почти на 60% дешевле агалсидазы альфа . За те же средства можно вылечить почти в два раза больше пациентов или сэкономить половину. Мы с радостью пускаемся в такие проекты, потому что здесь важнее технологический аспект и экспертиза, чем финансовый ресурс. И это отличная возможность компании нашего размера за счет гибкости выигрывать в конкуренции с более крупными игроками. Это, кстати, первый пример трансфера клеточной линии ферментного препарата в Россию .
— Есть ли у вас какой-то систематический подход к поиску подходящих перспективных молекул?
МЦ: — Сегодня он довольно простой. Мы смотрим всё — и это не так уж много — всё, что более-менее регистрационно пригодно, что выделяется на общем фоне. Сортируем по годам готовности: ближайший горизонт — три года. То, что выпадает за этот горизонт — вне нашего интереса. И молекула должна быть перспективной для рынка, чтобы был финансовый смысл. Постепенно для нас становится важна кластеризация — если вчера было всё равно, то сейчас с вероятностью 90% это должна быть либо орфанка, либо онкология, потому что на все направления ресурсов не хватит, и нужно выбрать какую-то специализацию. Внутри орфанки для нас нет внутреннего деления — каждый раз это самостоятельная история, но ведет к тем же специалистам и лидерам мнений, на мнение которых мы ориентируемся.
— Аутоиммунные и метаболические заболевания вы исключили?
МЦ: — Мы смотрели и на те, и на другие. В сегменте аутоиммунных заболеваний мы проиграли борьбу за пару молекул и после этого решили, что не пойдем туда. А с метаболическими — сейчас все гоняются за Оземпиком [9] и похожими веществами, аналогами природных гормонов GLP-1 и GIP. Но это не наша специфика. Традиционное лечение диабета — точно нет, нам кажется, это уже изживает себя. А куда пойдут новые пути лечения — пока не понятно, и эта неопределенность отпугивает.
— Если в целом описать стратегию, то это вывод на российский рынок препаратов next-in-class , которые находятся на поздних стадиях испытаний — где? В Азии?
МЦ: — Там, откуда нам их готовы предоставить. Это преимущественно Азия, но не только. В настоящее время мы подписываем контракт с европейской компанией на орфанный препарат. Препараты next-in-class составляют 80% наших усилий — это долгосрочная, сложная и рискованная стратегия; остальные 20% — это биосимиляры. Нужен здоровый баланс — еще есть ниши биосимиляров, куда можно выйти с интересным препаратом, если вовремя его принести.
По степени инновационности препараты можно разделить на полностью инновационные — впервые одобренные против какой-то мишени [10]: их называют first-in-class. Если препарат направлен против известной мишени, но отличается по химической структуре, то его называют next-in-class (если препарат биологический, то используют также термин biobetter). Если различия дадут ему преимущество по эффективности или безопасности, он имеет шансы стать best-in-class. Дальше вниз по шкале инновационности идет me-too — препарат, хоть и отличающийся по структуре, но не претендующий на значительные отличия от оригинала. На нижней ступени находятся биосимиляры и дженерики.
— А свои препараты за рубежом вы регистрируете?
МЦ: — Основной рынок для нас — это ЕАЭС и ЕС, где зарегистрированы наши вакцины и оригинальные препараты. Мы успешно экспортируем противогриппозные вакцины, в том числе для национальных программ иммунизации нескольких стран уже около 10 лет. Если говорить о ритейле, Полиоксидоний активно поставляется в Словакию. Наш оригинальный продукт зарегистрирован в Евросоюзе и там пользуется высоким спросом. Наша компания одной из первых среди российских фармацевтических производителей получила сертификат GMP EU в 2012 году, что значительно расширило возможности для развития экспорта. В среднем доля экспорта в выручке составляет 15–20%, что очень неплохо для российской фармы.
В ковидную эпоху мы погнались за дальним экспортом, и сейчас у нас на финальных этапах регистрации находится несколько РУ (регистрационных удостоверений — прим. «Биомолекулы») на рынках Африки и Азии, но это очень непростой, и, что самое тяжелое — сложнопредсказуемый процесс. Я зарекся тут что-то прогнозировать. Завершим — расскажем.
— По модальностям вопрос — ферменты, антитела, вакцины — что еще?
— Есть ли аппетит к малым молекулам? К передовым терапиям? РНК, клетки [1]?
АБ: — Аппетит есть! Смотрим пептиды, малые молекулы, не дженерики — это скучно, и мы здесь далеко не самые быстрые. Мы всегда открыты для next-in-class препаратов, особенно если их можно добавить к существующим продуктам, в таком случае получается единая линия промоции.
— А биспецифики [12], конъюгаты антител c лекарствами [13]?
МЦ: — Тоже смотрим, но с ними всё не так просто, очень горячая тема. Бывает, смотришь на пайплайн партнеров, чувствуешь себя как в «Детском мире» — всё хочу. Но часто это особые продукты, которые готовят под глобальные сделки, и здесь мы неожиданно для себя опосредованно начинаем конкурировать с большой фармой. И партнеры часто не хотят делать какие-то изъятия из возможности продать глобальные права . И даже если мы говорим, что Россию никто не заметит в тех сделках, на которые они надеются, всё равно они боятся. Это очень дорогие сделки, и договориться о них тяжело. ADC (antibody-drug conjugate, рис. 2) сейчас много — у нас два на примете, но идет непросто.
Речь идет о том, что небольшая компания не хочет отдавать часть прав на Россию, потому что потом при продаже это может усложнить сделку.
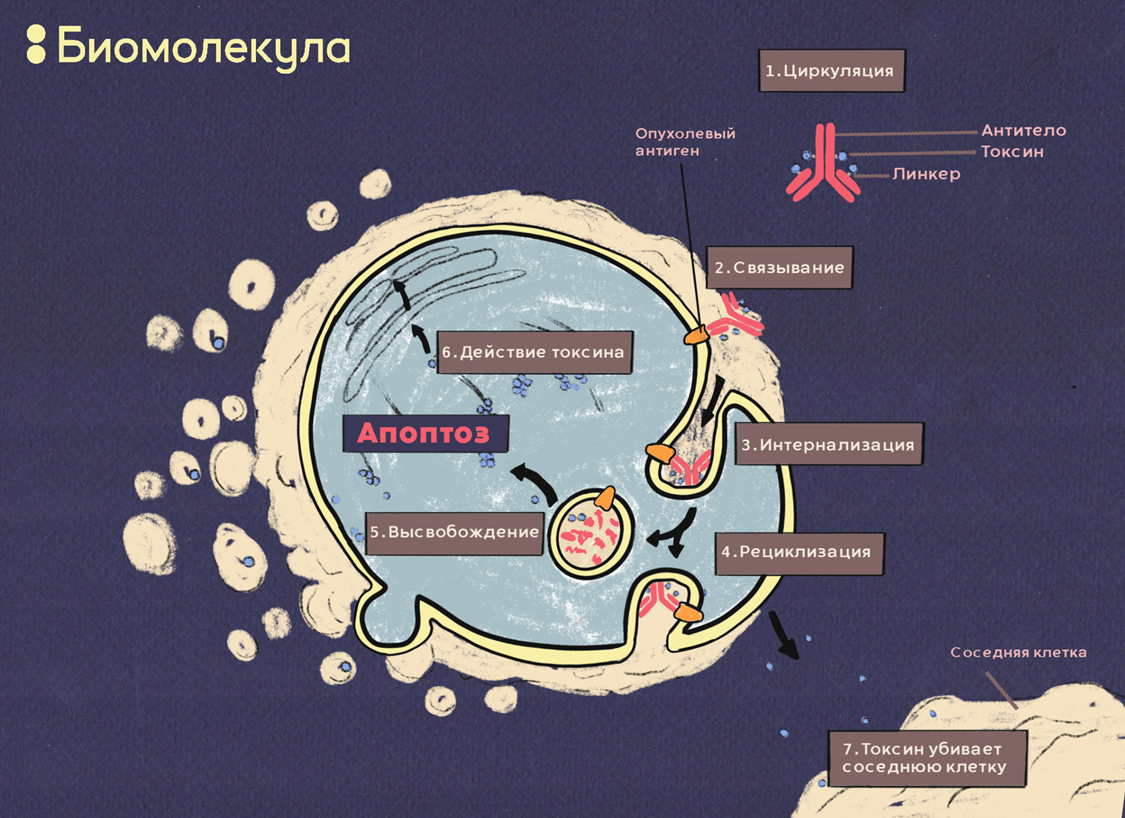
Рисунок 2. Структура и механизм действия обычных конъюгатов «антитело—лекарство» (ADC). (1) ADC состоят из трех ключевых элементов: фрагмента моноклонального антитела, который связывается с антигеном, обладающим высокой экспрессией на опухолевых клетках — этим обеспечивается адресная доставка; ковалентного линкера, необходимого для того, чтобы действующее вещество не высвобождалось в кровь; и цитотоксического действующего вещества (чаще всего — химиотерапевтического агента), которое будет вызывать гибель опухолевых клеток, воздействуя на ключевые компоненты (ДНК, микротрубочки, топоизомераза). ADC действуют последовательно в несколько этапов: (2) связывание с антигеном; (3) интернализация комплекса ADC-антиген; (4) часть ADC высвобождается обратно в циркуляцию; (5) лизосомная деградация и высвобождение цитотоксического агента в цитоплазме; и (6) взаимодействие с мишенью. Часть действующего вещества может быть высвобождена во внеклеточную среду, где она может быть поглощена соседними клетками (7).
— А локализуете вы всё на мощностях «Петровакс»?
МЦ: — Нет, не всё. У нас очень короткий горизонт выхода на рынок, и идти нужно как можно быстрее. Если есть готовые технические решения, то локализуем у себя, если нет — ищем контрактные площадки. Так было с нашим первым биосимиляром — Фабагал. C ним мы начали сотрудничество с институтом им. Гамалеи — у них достаточно мощный и современный производственный комплекс, который нам подходит для локализации производства субстанции. Готовую форму будем производить у себя.
— При поиске производственных мощностей есть какой-то чеклист, или это индивидуально?
НГ: — Индивидуально. Есть обязательный чеклист — соответствующие лицензии, качественное оборудование, успешный трек-рекорд — но, как правило, это регламентируется регуляторными требованиями к площадке. Мы открыты к сотрудничеству — готовы продолжать работать с институтом Гамалеи. Однако для специфических продуктов, которые в их стенах произвести невозможно, будем искать другие площадки.
— Я так понимаю, что по GMP вы их должны аудировать?
НГ: — Естественно. У нас есть внутренние процедуры для квалификации всех контрактных производителей. Наличие GMP — это минимальное требование. Мы также оцениваем логистику, производство, обеспечение качества и другие аспекты производства. И есть еще негласное требование — команда должна быть толковой. Производственный комплекс института Гамалеи выпускает препараты уже не первый год, и у них был толчок к развитию команды во времена ковида, когда они разрабатывали «Спутник V» [14], — это была очень новая и сложная технология. Мы тоже стараемся помогать партнерам в развитии компетенций команды: например, в рамках трансфера Фабагала мы получили достаточно консервативную технологию от наших корейских партнеров и выявили несколько точек для оптимизации — как снизить себестоимость, повысить производительность и уменьшить технологические риски.
— Институт Гамалеи как производственные мощности — это хорошо, но есть большое количество инновационных разработок на переднем крае науки. Вы как-то взаимодействуете с исследовательскими центрами, смотрите что-то интересное?
АБ: — Меньше. С коммерческой точки зрения интереснее me-too и next-in-class, когда мы выводим на рынок что-то, что уже сделано до нас и дополняем это всё клиническими данными и опытом.
— А собственные разработки вы продолжаете?
АБ, МЦ: — У нас есть свой R&D. Среди прочего, коллеги занимаются новыми интересными пролонгированными ферментами. Сейчас у нас есть два фермента, которые технически уже в доклинике.
Параллельно развиваем и делаем перепозиционирование своих оригинальных препаратов: по Лонгидазе завершилась третья фаза в long COVID — ждем публикацию, идет первая фаза испытаний Лонгидазы в новой ингаляционной форме в новом показании — при интерстициальном заболевании легких. Скоро планируем начать вторую фазу. Благодаря команде на базе R&D у нас еще «варится» рекомбинантная гиалуронидаза. Будем тестировать ее при мышечной спастичности. И так шаг за шагом мы развиваем что-то свое. Но всё это не может превратиться в одночасье в генотерапевтического единорога.
— Когда вы делаете техтрансфер, насколько часто приходится увеличивать производственные площадки — насколько это капиталоемкие вложения?
НГ: — Это зависит от технологии. Когда мы в ковидную эпоху начали переносить к себе технологию производства вакцин против коронавируса [17], [18], мы построили новый цех, который стоил примерно как четверть нашего предприятия. Если речь о том, чтобы поставить цех производства субстанций биопрепаратов, то по капиталовложениям это будет сопоставимо с половиной текущего предприятия. Для базовых технологий розлива и производства асептических препаратов потребуются небольшие модификации текущего оборудования, что будет измеряться десятками, сотнями тысяч евро. Это относительно небольшие инвестиции. Если мы говорим об ADC (antibody-drug conjugate, рис. 2), то это будет совершенно новое предприятие. Генная терапия [19] — опять же новый класс производства.
— И вы думаете о таком на будущее?
НГ: — Да, безусловно. Мы планируем расширять наше вакцинальное направление, а это требует полной локализации, и, следовательно, очень больших инвестиций в ближайшее время.
— А когда вы производите субстанции, сырье закупаете из-за рубежа или оно российского происхождения?
НГ: — В случае биопрепаратов всё сырье зарубежное. Более того, при трансфере технологии агалсидазы с корейской площадки наши партнеры (передающая сторона) использовали традиционные для индустрии материалы западных компаний. Сейчас эти зарубежные партнеры не поставляют в Россию свои материалы. Чтобы сохранить качество, нам необходимо перенести технологию один к одному. Тем не менее, выход нашелся, материалы мы смогли купить. Российское сырье мы тоже используем, но оно не ключевое, многое в России просто не производят. А такие товары, как питательные среды, мы не можем менять, потому что это повлияет на качество продукта, это будет уже не биосимиляр [2].
— Вы уже начали отвечать на следующий вопрос — от каждой бабушки: почему лекарства так дорого стоят?
НГ: — Стоимость [20] включает не только производство, но разработку ЛС [21], а также логистические издержки. Надо понимать, что технологии производства сами по себе дорогие. Когда выходит новый продукт, он будет стоить дорого, потому что объемы производства малы, и на препарат не сформирован полный спрос на рынке. Со временем объемы производства увеличиваются, и вместе с этим может снизиться себестоимость и конечная цена для потребителя. Но не всё зависит от конечного производителя лекарства: на изменение себестоимости может повлиять меняющаяся стоимость сырья и стоимость обслуживания оборудования. Можно изменить производителя материалов, но это повлияет на качество конечного продукта [2]. И на это мы не можем пойти ни с регуляторной точки зрения, ни с морально-этической позиции. Поэтому для высокотехнологичного производства, к которому относится биотех, мы выбираем качество, а это дорого. Но мы всегда ищем пути снизить себестоимость. Например, зарегистрировав и локализовав агалсидазу бета (препарат Фабагал), мы смогли существенно снизить стоимость препарата для российских потребителей.
Люди
— Как вы подходите к поиску сотрудников?
НГ: — Стратегия достаточно традиционная: объявляем вакансии, не исключаем сарафанное радио. Разумеется, смотрим на квалификацию, образование, опыт работы. Сейчас идет большой расцвет биотеха [22], и вакансий много, поэтому схватить хорошего специалиста вовремя бывает нелегко: большая конкуренция. Однако мы активно развиваем собственных сотрудников. Когда мы формировали наш биотехнологический отдел, около половины новых специалистов пришли из других подразделений.
Для мотивированных сотрудников у нас есть специализированные программы обучения, которые помогают развивать необходимые компетенции. Нередко мы направляем сотрудников к нашим международным партнерам для обмена опытом — с одной стороны, это желательно для процедуры техтрансфера, с другой — возможность увидеть работу других современных предприятий изнутри. Поскольку наши партнеры — это крупные фармкомпании с хорошей репутацией, такое обучение очень полезно.
— А стажировки и поиск молодых еще неопытных специалистов?
НГ: — В компании есть система стажировок. Принимаем студентов на практику, это отличная возможность для них погрузиться в нашу отрасль. Мы не просто обучаем, а ищем талантливых и инициативных людей, которым предоставляем возможность продолжить карьеру у нас после завершения учебы.
— А с кем у вас партнерства на этой почве?
НГ: — Уже не первый год к нам приезжают студенты Химического факультета МГУ, и мы получаем от них достаточно хорошие отзывы. Были студенты и из других стран — как правило, постсоветского пространства.
— Говорят, что в России дефицит фармацевтических инженеров на производстве, вы это чувствуете?
НГ: — Конкуренция за новых специалистов действительно очень высока, но у нас есть свои преимущества, которые позволяют оставаться привлекательным работодателем на рынке. Мы — предприятие полного цикла производства с современными технологиями и уникальной экспертизой в синтезе субстанций, есть устоявшиеся международные партнерства, интересные и масштабные проекты в разных сферах. Кроме того, у нас есть собственный R&D центр. Мы мотивируем не только зарплатой, но и возможностями для карьерного роста, развития компетенций, стажировок за рубежом.
— А на каких принципах вы формируете команду в R&D?
НГ: — Поскольку мы занимаемся разработкой новых препаратов, нам нужны научные мозги, талантливые исследователи. Многие сотрудники пришли к нам из научных институтов. Но в то же время нужны специалисты с понимаем того, что такое драг-девелопмент в индустрии. Поэтому часть сотрудников — это специалисты из фармкомпаний, из производственных департаментов и департаментов разработки. Так что наша стратегия — поиск и поддержание баланса между научными решениями и экономической целесообразностью.
— А откуда берутся задачи для R&D?
НГ: — У нас есть корпоративный чат, специально для новых идей — каждый сотрудник может предложить там свою идею, и мы ее обязательно рассмотрим. Это может быть не только что-то новое, с переднего края науки. Также коллеги из R&D ведут направленный поиск продуктов, которые будут комплементарны продуктам в текущем портфеле «Петровакс», а также работают над улучшением наших продуктов, то есть занимаются разработкой так называемых bio-betters.
— А чем вы мотивируете сотрудников предлагать идеи?
АБ: — У нас есть целая мотивационная программа «Предлагай» с внутренней корпоративной валютой. Есть и денежная мотивация.
Компания
— А как изменилась концепция за последние лет десять? Компания была основана в 1990-е, это был другой мир, плюс за последнее десятилетие произошло много важного.
НГ: — В целом концепция развития осталась традиционной для фармкомпании — мы выводим новые оригинальные продукты, инвестируем в R&D и фармпроизводство, расширяем доказательную базу для продуктов текущего портфеля. Компания была основана российскими учеными, у них было свое видение и препараты, которые они разработали и вывели на рынок, они до сих пор востребованы, но позже компания включила в свой портфель новые продукты и перестроила внутренние и внешние бизнес-процессы под обновленный портфель.
— А каковы отличия российского биотеха от мирового?
НГ: — По производственной части мы на уровне мировых стандартов: российский биотех способен воспроизводить все виды терапий (от рекомбинантных белков до генной терапии [19], а также клеточные технологии [25]). Несмотря на сложности с приобретением современного оборудования, мы поддерживаем высокий уровень производства. Однако, если сравнить количество разработанных препаратов в России и на западе, разница заметна. Есть компании, которые занимаются иммунными чекпойнтами, генной терапией, векторными вакцинами. Но все-таки объективная статистика говорит сама за себя.
Закон
— Нет ли турбулентности с регуляторными органами в последние годы?
НГ: — Нет. Законодательство живое, оно меняется, потому что появляются новые сведения о препаратах и об их действии, о том, как нужно проводить клинические исследования. У нас накопился опыт в части регуляции традиционных препаратов. Однако есть новые области — например, генная терапия. Был интересный период, когда в России стали появляться биомедицинские клеточные продукты, и в тот момент оказалось, что в принципе у нас очень большой пробел в законодательстве, которое не описывает, как работать с этими продуктами. Компании начинали разработку таких продуктов по каким-то тропкам, намеченным в западной фарме, и параллельно занимались законотворчеством вместе с регулятором. В результате появилось и законодательство, и первые продукты. Многое в регулировании отрасли основано на европейском законодательстве, но многое коллеги добавили исходя из внутреннего опыта. И сейчас, когда мы приносим препараты из-за рубежа, нам бывает нужно адаптировать европейские или американские требования к нашей специфике. Это один из ключевых рисков при выводе продуктов — в некоторых случаях российский регулятор проявляет большую строгость, чем зарубежный, и наша сила в том, что мы нашу специфику знаем.
— Насколько шаги, которые предпринимает государство, способствуют импортозамещению и существованию рынка?
АБ: — В импортозамещении мы участвуем на примере агалсидазы — это полная локализация. По поводу стимулов со стороны государства можно вспомнить прекрасную программу «Фарма-2020»: что-то смогли сделать, довели до рынка (развитие фарминдустрии в РФ в 2020–23 в цифрах: рис. 4 — «Биомолекула»). Хотят возродить этот формат в «Фарма-2030».
НГ: — Основные стимулы были направлены на разработку биосимиляров, дженериков и оригинальных препаратов, и это было сделано в предыдущем десятилетии, в «Фарме-2020». Мы находимся в этой парадигме — приносим биосимиляры. Планируем провести полную локализацию камрелизумаба — тоже своего рода импортозамещение. У нас есть успешный пример пневмококковой вакцины Превенар 13 — мы полностью перенесли технологию полного цикла готовой лекарственной формы: уже 10 лет как вакцина производится и предоставляется для национального календаря прививок и в целом на российский рынок. Это глобальный большой проект по трансферу технологий производства такой сложной высокотехнологичной вакцины. Сейчас поставлено более 40 млн доз на рынок.
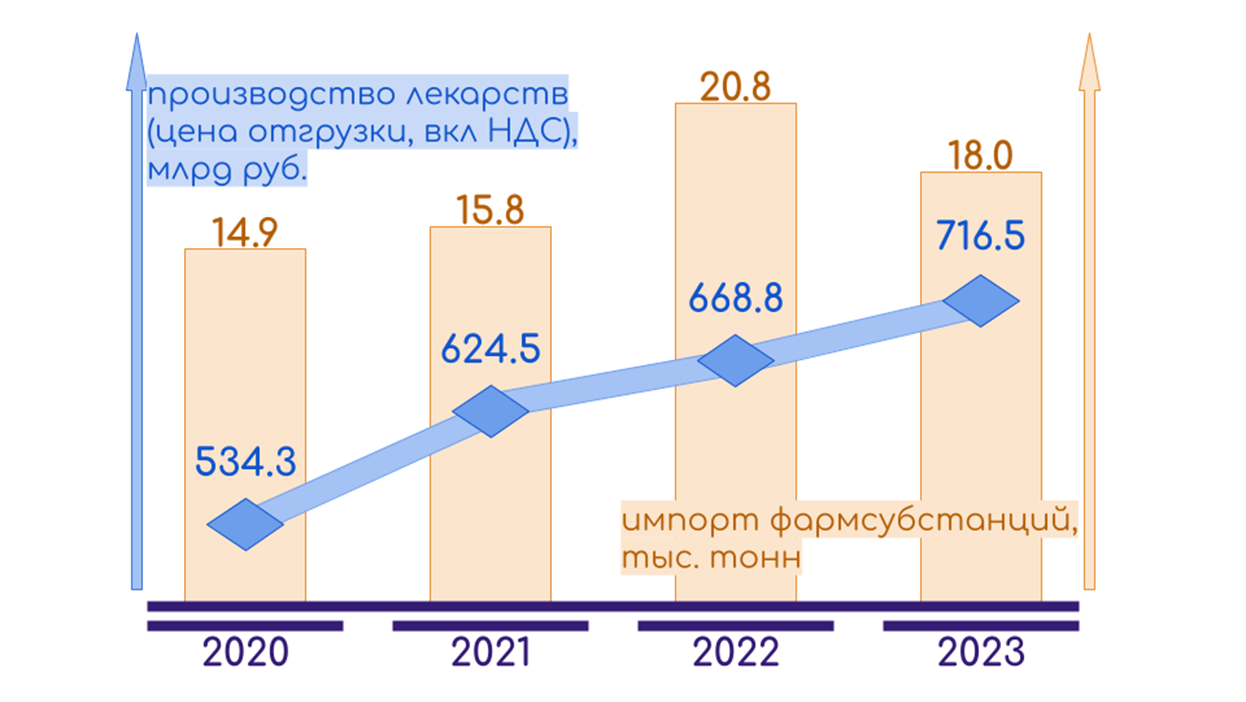
Рисунок 4. Развитие фарминдустрии в России за последние 4 года.
инфографика Камиля Айсина по RNC Pharma
— А как вы смотрите на нишевые стартапы в биотехе?
НГ: — Мы посматриваем — пока что это не фокус нашего внимания и не приоритет. Разработчики периодически приносят новые проекты, среди которых есть интересные продукты, но мы хотим нарастить свои компетенции в госпитальном рынке, чтобы потом более уверенно смотреть на что-то комплементарное, пусть и в ранней разработке. Нужна структура, на которую потом можно нанизывать биосимиляры, оригинальные молекулы на поздних этапах разработки, а уже потом и самые-самые передовые истории начнем брать в разработку.
Будущее
— Давайте в завершение о перспективах. Как вы считаете, какие ждут нас прорывы в ближайшие 10 лет?
НГ: — Бурное развитие генной терапии. Она себя хорошо показала на текущих примерах — может, не во всех случаях с точки зрения безопасности, но она продемонстрировала, что может существовать наряду с другими видами терапии. Сейчас по пальцам можно пересчитать, сколько в мире зарегистрировано препаратов генной терапии — а ее потенциал намного выше. Кроме того, биотеха в широком понимании станет больше. Финансирование и меры поддержки есть — в России биотех еще не вышел на максимальный уровень. Но химия, безусловно, останется.
— А в онкологии? PD1/PDL1 понятно — это сейчас горячая тема. Другие иммунные чекпойнты в меньшей степени, хотя по некоторым есть разработки. Будет ли расширяться пул иммунных чекпойнтов? Би- и триспецифические антитела?
АБ: — Со мной многие не согласятся, но я считаю, что иммунные чекпойнты — тупиковая ветвь: все эти таргеты весьма плохо сработали. В иммуноонкологии, как мне кажется, сейчас не всё так радужно [27]. А вот следующая большая история в онкологии будет связана с ядром клетки, с патогенезом. Будут вещества, которые могут влиять на фундаментальную проблему. В принципе, ингибиторы PARP уже начали этот тренд [28]. Возможно мишени, связанные с эпителиально-мезенхимальным переходом (ЭМП) [29]. Там было много провалов, но, если кто-то сможет найти валидированный таргет, это будет большая история.
— А что насчет применения искусственного интеллекта [30] в биотехе?
АБ: — В химии ИИ просто сокращает и оптимизирует времязатраты. А вот поиск мишени [10] — это в руках человека. Бигфарма может скрывать мишени, на которые идут разработки, чтобы избежать конкуренции. Что мы сейчас видим? Если у бигфармы есть что-то на третьей стадии клинических исследований (КИ) — значит, у китайцев на эту же мишень уже есть что-то на первой-второй стадии КИ. В биотехе ИИ используется на небольших отрезках как инструмент, который позволяет оптимизировать процессы.
Мы писали про перспективы ИИ в спецпроекте «Искусственный интеллект в биологии»: «История развития искусственного интеллекта и его пришествия в биологию» [31] и «Как языковые модели покорили мир белков» [32]. Если коротко, эти перспективы впечатляют, а вот реальные применения в индустрии пока что достаточно скромны.
НГ: — Если мы говорим о сложных вещах, таких как поиск мишени, ИИ может показать результат. Но как валидировать его решение, чтобы понимать степень достоверности? Если мы говорим об оптимизации оборудования, безусловно, это работает, и валидации не нужно, но куда это приведет, если мы доверимся ИИ? Он же учится на всем объеме данных, который содержит и ошибки тоже.
АБ: — В нашем исследовании по Лонгидазе мы использовали нейросетки. Был человек, который отсматривал гистологические срезы и искал фиброз легких. Ради интереса мы в параллель запустили программу. Был и третий — слепой проверяющий, и совпадений с человеком у него было гораздо больше. Пока что ИИ сильно не дотянул до человека. Он какие-то артефакты принимал за фиброз, а там было чистейшее легкое. Но это вопрос тренировки.
Литература
- Три поколения лекарств;
- Контроль качества биотехнологических продуктов;
- Болезнь Фабри: частая среди редких;
- Хороший, плохой, злой, или Как разозлить лимфоциты и уничтожить опухоль;
- Yunpeng Yang, Song Qu, Jingao Li, Chaosu Hu, Mingjun Xu, et. al.. (2021). Camrelizumab versus placebo in combination with gemcitabine and cisplatin as first-line treatment for recurrent or metastatic nasopharyngeal carcinoma (CAPTAIN-1st): a multicentre, randomised, double-blind, phase 3 trial. The Lancet Oncology. 22, 1162-1174;
- Dimitrios C. Ziogas, Charalampos Theocharopoulos, Panagiotis-Petros Lialios, Dimitra Foteinou, Ioannis-Alexios Koumprentziotis, et. al.. (2023). Beyond CTLA-4 and PD-1 Inhibition: Novel Immune Checkpoint Molecules for Melanoma Treatment. Cancers. 15, 2718;
- Иммунные войны: космическая онкологическая сага;
- Иммунитет без тормозов: Нобелевская премия за антитела против рака (2018);
- Оземпик: больше, чем средство для похудения;
- Поиск лекарственных мишеней;
- Неизвестные пептиды: «теневая» система биорегуляции;
- Биспецифические антитела, их мишени и перспективы применения в современной медицине;
- Что общего у боеголовок и антител? ADCs;
- «Спутник V» и не только: сказ об аденовирусных вакцинах;
- И царствуют, и правят: как регуляторы следят за допуском лекарств на рынок;
- Наукоемкий бизнес: как и почему фармацевтические компании сотрудничают с учеными и стартаперами?;
- Вакцины против коронавируса: перспективы;
- «Спутник V», «ЭпиВакКорону», «Модерну» делать будем? Ликбез по вакцинам против коронавируса;
- Генная терапия: познакомьтесь с лекарствами будущего;
- Путь лекарства;
- Фармакоэкономика: лечить или экономить?;
- «Бластим». Работа в биотехе? Да еще и в России?;
- Весь мир — большая лаборатория: что такое RWD и RWE, и как они помогают контролировать лекарства;
- Драг-дизайн: как в современном мире создаются новые лекарства;
- 12 методов в картинках: клеточные технологии;
- Постклиника: что осталось за кадром?;
- Иммунотерапия рака и молекулярная онкология — новинки на переднем крае науки;
- Сломать нельзя чинить;
- Метастазирование злокачественных опухолей: враг, который всегда впереди;
- От живого мозга к искусственному интеллекту;
- История развития искусственного интеллекта и его пришествия в биологию;
- Как языковые модели покорили мир белков.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚